La metástasis ósea , o enfermedad metastásica ósea , es una categoría de metástasis de cáncer que resulta de invasiones tumorales primarias en los huesos . Los tumores primarios de origen óseo, como el osteosarcoma , el condrosarcoma y el sarcoma de Ewing , son raros; el tumor óseo más común es una metástasis. [1] Las metástasis óseas se pueden clasificar como osteolíticas , osteoblásticas o ambas. A diferencia de las neoplasias hematológicas que se originan en la sangre y forman tumores no sólidos, las metástasis óseas generalmente surgen de tumores epiteliales y forman una masa sólida dentro del hueso. Los pacientes con cáncer de mama primario son particularmente vulnerables a desarrollar metástasis óseas. [2] Las metástasis óseas, especialmente en un estado de enfermedad avanzada, pueden causar dolor intenso, caracterizado por un dolor sordo y constante con picos periódicos de dolor incidente. [3]
En condiciones normales, el hueso sufre una remodelación continua a través de la resorción ósea mediada por osteoclastos y la deposición ósea mediada por osteoblastos . [4] Estos procesos normalmente están regulados de forma estricta dentro del hueso para mantener la estructura ósea y la homeostasis del calcio en el cuerpo. La desregulación de estos procesos por parte de las células tumorales conduce a lesiones osteoblásticas u osteolíticas , que reflejan el mecanismo subyacente de desarrollo. [4] Por lo general, las metástasis osteolíticas son más agresivas que las metástasis osteoblásticas, que tienen un curso más lento. Independientemente del fenotipo, las metástasis óseas suelen mostrar proliferación e hipertrofia de osteoclastos . [5]
Tumores primarios
Las metástasis óseas pueden causar dolor intenso, fracturas óseas , compresión de la médula espinal , hipercalcemia , anemia , inestabilidad espinal, disminución de la movilidad y rápida degradación en la calidad de vida de los pacientes. [7] [8] Los pacientes han descrito el dolor como un dolor sordo que empeora con el tiempo, con períodos intermitentes de dolor agudo e irregular. [3] Incluso con un tratamiento controlado del dolor, pueden ocurrir períodos de dolor irruptivo rápidamente, sin previo aviso, varias veces al día. [9] El dolor puede empeorar por la noche y aliviarse parcialmente con la actividad. [10] Las metástasis en los huesos que soportan peso pueden volverse sintomáticas al principio de la enfermedad, en comparación con las metástasis en los huesos planos de la costilla o el esternón. [10]
Las complicaciones mayores secundarias a metástasis óseas se denominan eventos relacionados con el esqueleto (ERE). [11]
Otros síntomas incluyen:
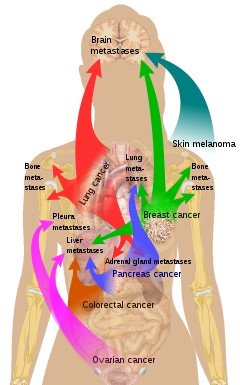

El hueso es la tercera ubicación más común de metástasis , después del pulmón y el hígado . [13] Si bien cualquier tipo de cáncer es capaz de formar tumores metastásicos dentro del hueso, el microambiente de la médula ósea tiende a favorecer tipos particulares de cáncer, incluidos los cánceres de próstata , mama y pulmón . [4] En el cáncer de próstata , las metástasis óseas tienden a ser el único sitio de metástasis. [3] Los sitios más comunes de metástasis óseas son la columna vertebral, la pelvis, las costillas, el cráneo y el fémur proximal. [10]
Tumores primarios comunes
Muchos cánceres se propagan a los huesos, pero no todos los huesos están implicados en la metástasis cancerosa. Se cree que el microambiente de los diferentes tipos de hueso desempeña un papel en su predisposición a la siembra de tumores. [14] Por ejemplo, el hueso trabecular rico en médula roja y el hueso sujeto a recambio frecuente tienen más probabilidades de ser sembrados [14] en nichos premetastásicos formados por interacciones entre células cancerosas y sustrato óseo [15] . Las células tumorales son atraídas entonces al nicho metastásico en el hueso. Sin embargo, las características de estos nichos aún deben dilucidarse por completo. [15] La siembra inicial puede ocurrir antes del descubrimiento del tumor primario. [15]
Se plantea la hipótesis de que la patogenia de la metástasis ósea a través de la vasculatura está relacionada con el plexo venoso vertebral de Batson , un sistema longitudinal sin válvulas conectado a la mama, el pulmón, el riñón, la tiroides y la próstata que se extiende desde el sacro hasta el cráneo. [16] Las ubicaciones más comunes de metástasis son la pelvis , los cuerpos vertebrales , las costillas y los extremos de los huesos largos. [16]
Una vez establecidas, las células tumorales pueden permanecer latentes en el microambiente óseo, radiológicamente indetectables, durante muchos años. [15] Los desencadenantes que finalmente despiertan a las células tumorales metastásicas son un campo de estudio activo, ya que podrían dilucidar los mecanismos de control de la latencia. [ 15 ]
Las células tumorales pueden tener efectos paraneoplásicos , como por ejemplo a través de la secreción de prostaglandina E , TGF-alfa , TGF-beta , TNF e interleucinas para aumentar la resorción ósea. La destrucción del hueso afectado por metástasis óseas es causada por la osteólisis mediada por osteoclastos . [16] La regulación desacoplada de osteoclastos y osteoblastos conduce a la malformación del hueso. [3] Las lesiones óseas líticas también pueden conducir a la patogénesis de la hipercalcemia en cánceres que se han propagado al hueso [17]
Una radiografía simple de todo el cuerpo puede identificar la metástasis ósea. Sin embargo, las lesiones escleróticas u osteolíticas deben tener al menos 1 cm de diámetro. [15] Una combinación de radiografías, tomografías computarizadas y resonancias magnéticas puede ser más sensible para el diagnóstico de metástasis óseas cancerosas. [15]
Una gammagrafía ósea o una gammagrafía con radionúclidos pueden identificar la metástasis ósea. El bisfosfonato marcado con tecnecio-99m se adhiere al calcio en los sitios de formación ósea activa. [15] Las gammagrafías óseas son más sensibles y pueden identificar lesiones antes que las radiografías simples. [15] Sin embargo, estos métodos son menos eficaces para identificar lesiones puramente osteolíticas y también resaltarán otras áreas de formación ósea, como las causadas por traumatismos o inflamaciones no relacionadas con el cáncer. [15] Además, la actividad de la vejiga puede enmascarar la detección de ciertas lesiones pélvicas. [15]
Una tomografía computarizada puede detectar metástasis óseas antes de que presenten síntomas en pacientes diagnosticados con tumores que tienen un alto riesgo de diseminación al hueso. Incluso las metástasis óseas escleróticas son generalmente menos radiodensas que las enostosis , y se ha sugerido que la metástasis ósea debería ser el diagnóstico preferido entre los dos para las lesiones óseas inferiores a un valor de corte de 1060 unidades Hounsfield (UH). [11] Si está indicada una biopsia, a menudo se utiliza una tomografía computarizada para localizar la lesión antes de la biopsia. [15]
La resonancia magnética se puede utilizar para detectar metástasis óseas con una sensibilidad del 82-100% y una especificidad del 73-100%.
La tomografía por emisión de positrones (PET) con fluorodesoxiglucosa marcada con flúor 18 ( 18 F-FDG) es una poderosa herramienta de diagnóstico para visualizar la actividad de la metástasis ósea. [15] Las metástasis óseas en la tomografía por emisión de positrones suelen ser focos múltiples, distribuidos de forma irregular, con una mayor captación del trazador sin relación con una única estructura anatómica. [15] Una tomografía por emisión de positrones puede identificar directamente células tumorales con una tasa metabólica significativa. Sin embargo, es un procedimiento costoso y la disponibilidad del dispositivo puede ser limitada. [15]
Debido a la alta tasa de recambio óseo, se cree que los metabolitos pueden detectar la metástasis ósea. [15] El uso de marcadores óseos para la detección y el cribado es un campo de investigación activo, aunque la evidencia radiográfica sigue siendo el estándar de oro. [15] Sin embargo, una vez que se ha establecido la presencia de una metástasis ósea, los marcadores metabólicos tumorales pueden proporcionar información útil para el diagnóstico y el pronóstico. [15]
Los objetivos del tratamiento de las metástasis óseas incluyen el control del dolor, la prevención y el tratamiento de las fracturas, el mantenimiento de la calidad de vida del paciente y el control local del tumor. [10] El tratamiento óptimo requiere un equipo multidisciplinario de médicos, incluidos oncólogos médicos y radioterapeutas, cirujanos ortopédicos, radiólogos, médicos de medicina nuclear, especialistas en medicina paliativa y más. [15] La evaluación del tratamiento está determinada por múltiples factores, incluido el estado funcional , la puntuación del dolor, el impacto en la calidad de vida y el estado general de la enfermedad clínica. [15] Las terapias importantes incluyen la radioterapia de haz externo , la terapia con radioisótopos dirigidos , la quimioterapia de ablación tumoral guiada por imágenes y los agentes quimioterapéuticos dirigidos al hueso, como los bifosfonatos y el denosumab . Las intervenciones ortopédicas como la fijación interna o la descompresión espinal pueden ser necesarias en el caso de pérdida de estabilidad estructural debido a la destrucción ósea. [15]
La escala del dolor de la Organización Mundial de la Salud fue diseñada para el manejo del dolor asociado al cáncer. La escala original detalla el manejo del dolor mediante una secuencia de medicamentos analgésicos, comenzando con medicamentos antiinflamatorios no esteroides y progresando a opioides débiles y fuertes [18]
Otros tratamientos incluyen corticosteroides , radioterapia y radionucleótidos . [3] La osteoplastia percutánea implica el uso de cemento óseo para reducir el dolor y mejorar la movilidad. [19] En la terapia paliativa , las principales opciones son la radiación externa y los radiofármacos . [20]
Las técnicas de ablación térmica se utilizan cada vez más en el tratamiento paliativo de la enfermedad ósea metastásica dolorosa. Aunque la mayoría de los pacientes experimentan un alivio completo o parcial del dolor después de la radioterapia externa, el efecto no es inmediato y se ha demostrado en algunos estudios que es transitorio en más de la mitad de los pacientes. [21] Para los pacientes que no son elegibles o no responden a las terapias tradicionales (es decir, radioterapia , quimioterapia , cirugía paliativa, bifosfonatos o medicamentos analgésicos), se han explorado técnicas de ablación térmica como alternativas para la reducción del dolor. Varios ensayos clínicos multicéntricos que estudian la eficacia de la ablación por radiofrecuencia en el tratamiento del dolor moderado a severo en pacientes con enfermedad ósea metastásica han demostrado disminuciones significativas en el dolor informado por el paciente después del tratamiento. [22] [23] Sin embargo, estos estudios se limitan a pacientes con uno o dos sitios metastásicos; el dolor de múltiples tumores puede ser difícil de localizar para la terapia dirigida. Más recientemente, también se ha explorado la crioablación como una alternativa potencialmente eficaz, ya que el área de destrucción creada por esta técnica se puede controlar de forma más efectiva mediante TC que la ablación por radiofrecuencia, una ventaja potencial al tratar tumores adyacentes a estructuras críticas. [24]
Una revisión Cochrane sobre la calcitonina para el tratamiento del dolor óseo metastásico sugiere que la calcitonina no produce ningún beneficio significativo en la reducción del dolor óseo ni en la mejora de la calidad de vida. [25]
Los agentes dirigidos a los huesos (BTAs), incluidos los bifosfonatos y el denosumab , pueden interrumpir la osteólisis mediada por osteoclastos . [15] Los inhibidores de osteoclastos, utilizados con mayor frecuencia en el tratamiento de la osteoporosis, pueden permitir la curación ósea y retrasar las complicaciones. [15] Se ha demostrado que los BTAs disminuyen la incidencia de eventos relacionados con el esqueleto (SREs) como fracturas patológicas, disminuyendo así la necesidad de intervención quirúrgica o medicación para el dolor. [15]
Muchos cánceres tienen predisposición a hacer metástasis en los huesos. [13] La siguiente lista detalla la probabilidad de que un cáncer, si se encuentra en una etapa de metástasis avanzada, se haya propagado a los huesos en el momento de la muerte: [26]
Dada la alta incidencia de cáncer de mama, pulmón y próstata, estos pacientes representan > 80% de los pacientes con metástasis óseas. [15]
En el caso de los pacientes con metástasis óseas avanzadas, la supervivencia media desde el momento del diagnóstico de una metástasis ósea varía según el tipo de tumor primario. A continuación se incluye una lista: [26]