La gingivitis es una enfermedad no destructiva que causa inflamación de las encías ; [1] gingivitis es un término alternativo. [2] La forma más común de gingivitis, y la forma más común de enfermedad periodontal en general, es en respuesta a biopelículas bacterianas (también llamadas placa ) que se adhieren a las superficies de los dientes, denominada gingivitis inducida por placa . La mayoría de las formas de gingivitis son inducidas por placa. [3]
Si bien algunos casos de gingivitis nunca progresan a periodontitis , [4] la periodontitis siempre está precedida por gingivitis. [5]
La gingivitis es reversible con una buena higiene bucal; sin embargo, sin tratamiento, la gingivitis puede progresar a periodontitis, en la que la inflamación de las encías produce destrucción de tejido y reabsorción ósea alrededor de los dientes. La periodontitis puede, en última instancia, provocar la pérdida de dientes . [6]
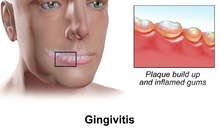
Los síntomas de la gingivitis son poco específicos y se manifiestan en el tejido de las encías como los signos clásicos de inflamación :
Además, el punteado que normalmente existe en el tejido de las encías de algunas personas suele desaparecer y las encías pueden lucir brillantes cuando el tejido de las encías se inflama y se estira sobre el tejido conectivo subyacente inflamado. La acumulación también puede emitir un olor desagradable. Cuando las encías están hinchadas, el revestimiento epitelial del surco gingival se ulcera y las encías sangrarán más fácilmente incluso con un cepillado suave, y especialmente al usar hilo dental.
Un estudio de 2018 encontró evidencia de que las bacterias de la gingivitis pueden estar relacionadas con la enfermedad de Alzheimer . Los científicos coinciden en que se necesita más investigación para demostrar un vínculo de causa y efecto. [8] "Los estudios también han descubierto que la bacteria P. gingivalis , responsable de muchas formas de enfermedad de las encías, puede migrar de la boca al cerebro en ratones. Y al ingresar al cerebro, P. gingivalis puede reproducir todos los rasgos característicos de la enfermedad de Alzheimer". [9]
La causa de la gingivitis inducida por placa es la placa bacteriana, que actúa para iniciar la respuesta del organismo al huésped . Esto, a su vez, puede conducir a la destrucción de los tejidos gingivales, que puede progresar a la destrucción del aparato de inserción periodontal. [10] La placa se acumula en los pequeños espacios entre los dientes, en los surcos gingivales y en áreas conocidas como trampas de placa : ubicaciones que sirven para acumular y mantener la placa. Los ejemplos de trampas de placa incluyen márgenes restaurativos voluminosos y salientes, broches de dentaduras postizas parciales removibles y cálculo (sarro) que se forma en los dientes. Aunque estas acumulaciones pueden ser diminutas, las bacterias en ellas producen sustancias químicas, como enzimas degradativas, y toxinas, como el lipopolisacárido (LPS, también conocido como endotoxina ) o el ácido lipoteicoico (LTA), que promueven una respuesta inflamatoria en el tejido de las encías. Esta inflamación puede causar un agrandamiento de la encía y su posterior formación. La placa temprana en la salud consiste en una comunidad bacteriana relativamente simple dominada por cocos y bacilos Gram-positivos . A medida que la placa madura y se desarrolla la gingivitis, las comunidades se vuelven cada vez más complejas con mayores proporciones de bacilos Gram-negativos , fusiformes, filamentos, espirilas y espiroquetas. Estudios experimentales posteriores sobre gingivitis, utilizando cultivos, proporcionaron más información sobre las especies bacterianas específicas presentes en la placa. Los taxones asociados con la gingivitis incluyeron Fusobacterium nucleatum subespecie polymorphum , Lachnospiraceae [G-2] especie HOT100, Lautropia especie HOTA94 y Prevotella oulorum (una especie de bacteria Prevotella ), mientras que Rothia dentocariosa se asoció con la salud periodontal. [11] Se justifica un estudio adicional de estos taxones y puede conducir a nuevos enfoques terapéuticos para prevenir la enfermedad periodontal, incluida la salud sistémica.
Los factores de riesgo asociados con la gingivitis incluyen los siguientes:
La gingivitis es una categoría de enfermedad periodontal en la que no hay pérdida de hueso pero sí inflamación y sangrado.
Cada diente se divide en cuatro unidades gingivales (mesial, distal, bucal y lingual) y se le asigna una puntuación de 0 a 3 según el índice gingival. A continuación, se promedian las cuatro puntuaciones para otorgar a cada diente una puntuación única.
El diagnóstico de la enfermedad periodontal gingivitis lo realiza un dentista. El diagnóstico se basa en los datos de la evaluación clínica obtenidos durante un examen periodontal completo. Tanto un higienista dental registrado como un dentista pueden realizar el examen periodontal completo, pero la interpretación de los datos y el diagnóstico los realiza el dentista. El examen periodontal completo consiste en un examen visual, una serie de radiografías, un sondaje de la encía, la determinación del grado de daño actual o pasado en el periodonto y una revisión completa de los antecedentes médicos y dentales.
Las investigaciones actuales muestran que los niveles de actividad de las siguientes enzimas en muestras de saliva están asociados con la destrucción periodontal: aspartato aminotransferasa (AST), alanina aminotransferasa (ALT), gamma glutamil transferasa (GGT), fosfatasa alcalina (ALP) y fosfatasa ácida (ACP). Por lo tanto, estos biomarcadores enzimáticos pueden utilizarse para ayudar en el diagnóstico y tratamiento de la gingivitis y la periodontitis.
Un higienista dental o dentista comprobará los síntomas de la gingivitis y también puede examinar la cantidad de placa en la cavidad bucal. Un higienista dental o dentista también buscará signos de periodontitis mediante radiografías o sondas periodontales, así como otros métodos.
Si la gingivitis no responde al tratamiento, puede ser necesaria la derivación a un periodoncista (un especialista en enfermedades de las encías y el hueso alrededor de los dientes y los implantes dentales) para un tratamiento adicional.
Según lo definido en el Taller Mundial sobre Periodoncia Clínica de 1999, existen dos categorías principales de enfermedades gingivales , cada una con numerosos subgrupos: [15]
Según lo definido en el Taller Mundial de 2017, la salud periodontal y las enfermedades/afecciones gingivales se han categorizado de la siguiente manera: [16]
La gingivitis se puede prevenir mediante una higiene bucal regular [17] que incluya el cepillado y el uso de hilo dental a diario . [18] También se pueden utilizar enjuagues bucales con peróxido de hidrógeno , solución salina , alcohol o clorhexidina . En un estudio clínico de 2004 se destacó el efecto beneficioso del peróxido de hidrógeno sobre la gingivitis. [19] El uso de cepillos de tipo oscilante podría reducir el riesgo de gingivitis en comparación con el cepillado manual. [20]
Los programas rigurosos de control de placa junto con el raspado y curetaje periodontal también han demostrado ser útiles, aunque según la Asociación Dental Americana , el raspado y alisado radicular periodontal se consideran un tratamiento para la enfermedad periodontal, no como un tratamiento preventivo para la enfermedad periodontal. [21] En una revisión de datos de efectividad de 1997, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) encontró evidencia clara que mostraba que la pasta de dientes que contenía triclosán era efectiva para prevenir la gingivitis. [22] En 2017, la FDA prohibió el triclosán en muchos productos de consumo, pero permitió que permaneciera en la pasta de dientes debido a su eficacia contra la gingivitis. [23] En 2019, Colgate, bajo presión de los defensores de la salud, eliminó el triclosán de la última pasta de dientes en el mercado que lo contenía, Colgate Total. [24]


El objetivo del tratamiento es eliminar la placa . La terapia está dirigida a la reducción de las bacterias bucales y puede adoptar la forma de visitas periódicas regulares a un profesional dental junto con un cuidado adecuado de la higiene bucal en el hogar. Por lo tanto, varios de los métodos utilizados en la prevención de la gingivitis también se pueden utilizar para el tratamiento de la gingivitis manifiesta, como el raspado, el alisado radicular, el curetaje , los enjuagues bucales que contienen clorhexidina o peróxido de hidrógeno y el uso de hilo dental. Los cepillos interdentales también ayudan a eliminar cualquier agente causal. [25]
Los cepillos de dientes eléctricos funcionan mejor que los cepillos de dientes manuales para reducir la enfermedad. [26]
Los ingredientes activos que "reducen la placa y demuestran una reducción eficaz de la inflamación gingival durante un período de tiempo" son el triclosán , el digluconato de clorhexidina y una combinación de timol , mentol , eucaliptol y salicilato de metilo . Estos ingredientes se encuentran en la pasta de dientes y el enjuague bucal. Durante mucho tiempo se consideró que el peróxido de hidrógeno era un agente de venta libre adecuado para tratar la gingivitis. Hay evidencia que muestra el efecto positivo en el control de la gingivitis en el uso a corto plazo. Un estudio indica que el enjuague bucal a base de peróxido de hidrógeno fluorado puede eliminar las manchas de los dientes y reducir la gingivitis. [19]
Según una evidencia limitada, los enjuagues bucales con aceites esenciales también pueden ser útiles, ya que contienen ingredientes con propiedades antiinflamatorias, como el timol, el mentol y el eucaliptol. [27]
Las bacterias que causan la gingivitis se pueden controlar mediante el uso diario de un irrigador bucal con un enjuague bucal que contenga un antibiótico. Una mezcla eficaz es amoxicilina , cefalexina o minociclina en 500 gramos de un enjuague bucal fluorado sin alcohol. [28]
En general, se ha demostrado que una higiene bucal intensiva mejora la salud gingival en personas con diabetes tipo 2 bien controlada. La destrucción periodontal también se ralentiza gracias a una higiene bucal exhaustiva. Una higiene bucal intensiva (educación sobre salud bucal más raspado supragingival) sin ningún tratamiento periodontal mejora la salud gingival y puede prevenir la progresión de la gingivitis en pacientes con diabetes bien controlada .
Aprobado por la Junta Directiva de la ADHA el 29 de abril de 1998