La reacción de Suzuki o acoplamiento de Suzuki es una reacción orgánica que utiliza un catalizador complejo de paladio para acoplar de forma cruzada un ácido borónico a un organohaluro . [1] [2] [3] Fue publicado por primera vez en 1979 por Akira Suzuki , y compartió el Premio Nobel de Química 2010 con Richard F. Heck y Ei-ichi Negishi por su contribución al descubrimiento y desarrollo de la catálisis de metales nobles. en síntesis orgánica . [4] Esta reacción a veces se combina con la borilación de Miyaura relacionada ; la combinación es la reacción de Suzuki-Miyaura . Se utiliza ampliamente para sintetizar poliolefinas , estirenos y bifenilos sustituidos .
El esquema general de la reacción de Suzuki se muestra a continuación, donde se forma un enlace simple carbono-carbono acoplando un haluro (R 1 -X) con una especie de organoboro (R 2 -BY 2 ) utilizando un catalizador de paladio y una base . La especie de organoboro generalmente se sintetiza mediante hidroboración o carboboración , lo que permite una rápida generación de complejidad molecular.

Se han publicado varias reseñas que describen los avances y el desarrollo de la reacción de Suzuki. [5] [6] [7]
El mecanismo de la reacción de Suzuki se ve mejor desde la perspectiva del catalizador de paladio. El ciclo catalítico se inicia mediante la formación de una especie catalítica activa de Pd 0 , A. Este participa en la adición oxidativa de paladio al reactivo de haluro 1 para formar el intermedio de organopaladio B. La reacción ( metátesis ) con la base da el intermedio C , que a través de la transmetalación [8] con el complejo de boronato D (producido por la reacción del reactivo de ácido borónico 2 con la base) forma la especie transitoria de organopaladio E. La etapa de eliminación reductora conduce a la formación del producto deseado 3 y restaura el catalizador de paladio A original que completa el ciclo catalítico .

El acoplamiento Suzuki se realiza en presencia de una base y durante mucho tiempo no se entendió completamente el papel de la base. Primero se creyó que la base formaba un borato de trialquilo (R 3 B-OR), en el caso de una reacción de un trialquilborano (BR 3 ) y alcóxido ( - OR); esta especie podría considerarse más nucleofílica y luego más reactiva hacia el complejo de paladio presente en el paso de transmetalación. [9] [10] [11] Duc y sus compañeros de trabajo investigaron el papel de la base en el mecanismo de reacción para el acoplamiento de Suzuki y encontraron que la base tiene tres funciones: Formación del complejo de paladio [ArPd(OR)L 2 ], formación del borato de trialquilo y aceleración de la etapa de eliminación reductora mediante reacción del alcóxido con el complejo de paladio. [9]
En la mayoría de los casos, la adición oxidativa es el paso determinante de la velocidad del ciclo catalítico. [12] Durante este paso, el catalizador de paladio se oxida de paladio (0) a paladio (II). La especie A de paladio catalíticamente activa se acopla con el sustrato 1 de haluro de arilo para producir un complejo B de organopaladio . Como se ve en el diagrama a continuación, el paso de adición oxidativa rompe el enlace carbono - halógeno donde el paladio ahora está unido tanto al grupo halógeno (X) como al grupo R 1 .

La adición oxidativa procede con la retención de la estereoquímica con haluros de vinilo , mientras que da inversión de la estereoquímica con haluros alílicos y bencílicos . [13] La adición oxidativa forma inicialmente el complejo cis -paladio, que rápidamente se isomeriza al complejo trans. [14]

El acoplamiento de Suzuki ocurre con retención de la configuración en los dobles enlaces tanto para el reactivo de organoboro como para el haluro. [15] Sin embargo, la configuración de ese doble enlace, cis o trans, está determinada por la isomerización cis a trans del complejo de paladio en el paso de adición oxidativa donde el complejo transpaladio es la forma predominante. Cuando el organoboro está unido a un doble enlace y está acoplado a un haluro de alquenilo, el producto es un dieno como se muestra a continuación.

La transmetalación es una reacción organometálica en la que los ligandos se transfieren de una especie a otra. En el caso del acoplamiento de Suzuki, los ligandos se transfieren de la especie de organoboro D al complejo C de paladio(II) , donde la base que se agregó en el paso anterior se intercambia con el sustituyente R 2 en la especie de organoboro para dar el nuevo paladio. (II) complejo E. El mecanismo exacto de transmetalación del acoplamiento Suzuki aún está por descubrir. Los compuestos de organoboro no sufren transmetalación en ausencia de una base y, por lo tanto, se cree ampliamente que la función de la base es activar el compuesto de organoboro y facilitar la formación del intermedio R 1 -Pd ll -O t Bu ( C ). del producto de adición oxidativa R 1 -Pd ll -X ( B ). [12]

El paso final es el paso de eliminación reductora donde el complejo de paladio (II) ( E ) elimina el producto ( 3 ) y regenera el catalizador de paladio (0) ( A ). Utilizando el marcaje con deuterio , Ridgway et al. han demostrado que la eliminación reductiva se produce con la retención de la estereoquímica. [dieciséis]

El ligando juega un papel importante en la reacción de Suzuki. Normalmente, el ligando fosfina se utiliza en la reacción de Suzuki. El ligando fosfina aumenta la densidad electrónica en el centro metálico del complejo y, por lo tanto, ayuda en el paso de adición oxidativa. Además, el volumen de la sustitución del ligando de fosfina ayuda en la etapa de eliminación reductora. Sin embargo, recientemente se han utilizado ligandos de carbeno N -heterocíclicos en este acoplamiento cruzado, debido a la inestabilidad del ligando de fosfina en las condiciones de reacción de Suzuki. [17] Los carbenos N -heterocíclicos son más ricos en electrones y más voluminosos que el ligando fosfina. Por lo tanto, tanto los factores estéricos como electrónicos del ligando carbeno N -heterocíclico ayudan a estabilizar el catalizador activo de Pd(0). [18]
Las ventajas del acoplamiento de Suzuki sobre otras reacciones similares incluyen la disponibilidad de ácidos borónicos comunes, condiciones de reacción suaves y su naturaleza menos tóxica. Los ácidos borónicos son menos tóxicos y más seguros para el medio ambiente que los compuestos organoestaño y organozinc . Es fácil eliminar los subproductos inorgánicos de la mezcla de reacción. Además, esta reacción es preferible porque utiliza reactivos relativamente baratos y fáciles de preparar. Poder utilizar agua como disolvente [19] hace que esta reacción sea más económica, ecológica y práctica de usar con una variedad de reactivos solubles en agua. Se puede utilizar una amplia variedad de reactivos para el acoplamiento de Suzuki, por ejemplo, ácidos aril o vinilborónicos y haluros de arilo o vinilo . El trabajo también ha ampliado el alcance de la reacción para incorporar bromuros de alquilo. [20] Además de que son posibles muchos tipos diferentes de haluros para la reacción de acoplamiento de Suzuki, la reacción también funciona con pseudohaluros como los triflatos (OTf), como reemplazos de los haluros . La reactividad relativa del compañero de acoplamiento con el haluro o pseudohaluro es: R 2 –I > R 2 –OTf > R 2 –Br >> R 2 –Cl. En lugar de ácidos borónicos se pueden utilizar ésteres borónicos y sales organotrifluoroborato . El catalizador también puede ser un catalizador basado en nanomateriales de paladio . [21] Con un nuevo ligando organofosfina ( SPhos ), se ha informado de una carga de catalizador de hasta 0,001% molar. [22] Estos avances y la flexibilidad general del proceso han hecho que el acoplamiento de Suzuki sea ampliamente aceptado para la síntesis química.
La reacción de acoplamiento de Suzuki es escalable y rentable para su uso en la síntesis de productos intermedios para productos farmacéuticos o productos químicos finos . [23] La reacción de Suzuki alguna vez estuvo limitada por altos niveles de catalizador y la disponibilidad limitada de ácidos borónicos . También se encontraron reemplazos para haluros, lo que aumentó también el número de parejas de acoplamiento para el haluro o pseudohaluro. Se han llevado a cabo reacciones a mayor escala en la síntesis de varios compuestos biológicos importantes, como el CI-1034, que utilizaba compañeros de acoplamiento de triflato y ácido borónico y que se ejecutaba en una escala de 80 kilogramos con un rendimiento del 95 %. [24]
Otro ejemplo es el acoplamiento de 3-piridilborano y 1-bromo-3-(metilsulfonil)benceno que formó un intermedio que se utilizó en la síntesis de un potencial agente del sistema nervioso central. La reacción de acoplamiento para formar el intermedio produjo 278 kilogramos con un rendimiento del 92,5%. [15] [23]
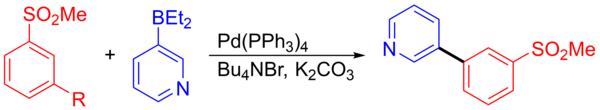
Se han puesto importantes esfuerzos en el desarrollo de catalizadores heterogéneos para la reacción CC de Suzuki, motivados por las ganancias de rendimiento en el proceso industrial (eliminando la separación del catalizador del sustrato), y recientemente se ha demostrado que un catalizador heterogéneo de un solo átomo de Pd supera al Catalizador de Pd(PPh 3 ) 4 homogéneo por defecto de la industria . [25]
El acoplamiento de Suzuki se ha utilizado frecuentemente en síntesis de compuestos complejos. [26] [27] El acoplamiento de Suzuki se ha utilizado sobre un derivado citronelal para la síntesis de caparratrieno, un producto natural altamente activo contra la leucemia: [28]

Se han desarrollado varios usos catalíticos de metales distintos del paladio (especialmente níquel). [29] Percec y sus colaboradores informaron de la primera reacción de acoplamiento cruzado catalizada por níquel en 1995 utilizando mesilatos de arilo y ácidos borónicos. [30] Aunque se necesitaba una mayor cantidad de catalizador de níquel para la reacción, alrededor del 5% en moles, el níquel no es un metal tan caro ni tan precioso como el paladio . La reacción de acoplamiento de Suzuki catalizada por níquel también permitió que se formaran una serie de compuestos que no funcionaron o funcionaron peor para el sistema catalizado por paladio que para el sistema catalizado por níquel. [29] El uso de catalizadores de níquel ha permitido a los electrófilos que resultaron desafiantes para el acoplamiento original de Suzuki usando paladio, incluidos sustratos como fenoles, éteres arílicos, ésteres, fosfatos y fluoruros. [29]
La investigación sobre el acoplamiento cruzado catalizado por níquel continuó y aumentó el alcance de la reacción después de que se mostraron estos primeros ejemplos y creció el interés en la investigación. Miyaura e Inada informaron en 2000 que se podría utilizar un catalizador de níquel más barato para el acoplamiento cruzado , utilizando trifenilfosfina (PPh 3 ) en lugar de los ligandos más caros utilizados anteriormente. [31] Sin embargo, el acoplamiento cruzado catalizado por níquel todavía requería altas cargas de catalizador (3-10%), requería un exceso de ligando (1-5 equivalentes) y seguía siendo sensible al aire y la humedad. [29] Los avances de Han y sus compañeros de trabajo han intentado abordar ese problema desarrollando un método que utiliza bajas cantidades de catalizador de níquel (<1 mol%) y ningún equivalente adicional de ligando. [32]
Wu y sus colaboradores también informaron en 2011 que se podría usar un catalizador de níquel altamente activo para el acoplamiento cruzado de cloruros de arilo que solo requería entre 0,01 y 0,1% en moles de catalizador de níquel. También demostraron que el catalizador podía reciclarse hasta seis veces sin prácticamente ninguna pérdida de actividad catalítica. [33] El catalizador era reciclable porque era un catalizador de nanopartículas de fosfina níquel (G 3 DenP-Ni) que estaba hecho de dendrímeros .
Las ventajas y desventajas se aplican a las reacciones de acoplamiento de Suzuki catalizadas tanto por paladio como por níquel. Además del sistema catalizador de Pd y Ni, en la reacción de acoplamiento de Suzuki se han utilizado fuentes metálicas baratas y no tóxicas como el hierro y el cobre [34] . El grupo de investigación de Bedford [35] y el grupo de investigación de Nakamura [36] han trabajado extensamente en el desarrollo de la metodología de la reacción de acoplamiento de Suzuki catalizada por hierro. El rutenio es otra fuente de metal que se ha utilizado en la reacción de acoplamiento de Suzuki. [37]
La catálisis de níquel puede construir enlaces CC a partir de amidas. A pesar de la naturaleza inherentemente inerte de las amidas como sintetizadores, se puede utilizar la siguiente metodología para preparar enlaces CC. El procedimiento de acoplamiento es suave y tolerante con innumerables grupos funcionales, incluidos: aminas, cetonas, heterociclos y grupos con protones ácidos. Esta técnica también se puede utilizar para preparar moléculas bioactivas y unir heterociclos de forma controlada mediante astutos acoplamientos cruzados secuenciales. A continuación se ofrece una revisión general del esquema de reacción. [38]

La síntesis de un compuesto de unión a tubulina (agente antiproliferativo ) se llevó a cabo utilizando una trimetoxi benzamida y un compañero de acoplamiento de indolil pinacol atoboro en una escala de gramos. [38]

Los ácidos arilborónicos son comparativamente más baratos que otros organoboranos y hay disponible comercialmente una amplia variedad de ácidos arilborónicos . Por lo tanto, se ha utilizado ampliamente en la reacción de Suzuki como socio organoborano. Las sales de ariltrifluoroborato son otra clase de organoboranos que se utilizan con frecuencia porque son menos propensos a la protodeboronación en comparación con los ácidos arilborónicos . Son fáciles de sintetizar y pueden purificarse fácilmente. [39] Las sales de ariltrifluoroborato se pueden formar a partir de ácidos borónicos mediante el tratamiento con fluoruro de hidrógeno y potasio , que luego se puede utilizar en la reacción de acoplamiento de Suzuki. [40]

La reacción de acoplamiento de Suzuki se diferencia de otras reacciones de acoplamiento en que puede realizarse en agua orgánica bifásica, [41] solo agua, [19] o sin disolvente. [42] Esto aumentó el alcance de las reacciones de acoplamiento, ya que se podía utilizar una variedad de bases, sistemas catalíticos y reactivos solubles en agua sin preocuparse por su solubilidad en disolventes orgánicos. El uso de agua como sistema disolvente también es atractivo debido a sus ventajas económicas y de seguridad. En los sistemas de disolventes para acoplamiento Suzuki se utilizan con frecuencia tolueno , [43] THF , [44] dioxano , [44] y DMF . [45] Las bases más utilizadas son K 2 CO 3 , [41] KO t Bu , [46] Cs 2 CO 3 , [47] K 3 PO 4 , [48] NaOH , [49] y NEt 3 . [50]
{{cite journal}}: Mantenimiento CS1: nombres numéricos: lista de autores ( enlace )