Neisseria gonorrhoeae , también conocida como gonococo (singular) o gonococo (plural), es una especie de bacteria diplococos gramnegativa aislada por Albert Neisser en 1879. [3] Causa lainfección genitourinaria de transmisión sexual gonorrea [4] , así como otras formas de enfermedad gonocócica que incluyen gonococemia diseminada, artritis séptica y oftalmía neonatal gonocócica.
Es oxidasa positiva y aeróbica, sobrevive a la fagocitosis y crece dentro de los neutrófilos . [4] Cultivarlo requiere suplementos de dióxido de carbono y agar enriquecido ( agar chocolate ) con varios antibióticos ( Thayer-Martin ). Exhibe variación antigénica a través de la recombinación genética de sus pili y proteínas de superficie que interactúan con el sistema inmunológico . [3]
La transmisión sexual se produce a través del sexo vaginal, anal u oral. [5] La transmisión sexual se puede prevenir mediante el uso de barreras de protección. [6] La transmisión perinatal puede ocurrir durante el parto y puede prevenirse mediante el tratamiento con antibióticos de la madre antes del nacimiento y la aplicación de gel antibiótico para los ojos del recién nacido. [6] Después de un episodio de infección gonocócica, las personas infectadas no desarrollan inmunidad a futuras infecciones. La reinfección es posible debido a la capacidad de N. gonorrhoeae para evadir el sistema inmunológico variando sus proteínas de superficie. [7]
N. gonorrhoeae puede causar infección de los genitales, la garganta y los ojos. [8] La infección asintomática es común en hombres y mujeres. [6] [9] La infección no tratada puede extenderse al resto del cuerpo (infección por gonorrea diseminada), especialmente a las articulaciones (artritis séptica). La infección no tratada en las mujeres puede causar enfermedad inflamatoria pélvica y posible infertilidad debido a las cicatrices resultantes. [8] El diagnóstico se realiza mediante cultivo , tinción de Gram o pruebas de ácido nucleico , como la reacción en cadena de la polimerasa , de una muestra de orina, un hisopo uretral o un hisopo cervical. [10] [11] Se recomienda realizar pruebas conjuntas de clamidia y otras ITS debido a las altas tasas de coinfección. [12]
La resistencia a los antibióticos en N. gonorrhoeae es un creciente problema de salud pública, especialmente dada su propensión a desarrollar resistencia fácilmente. [13]

Las especies de Neisseria soncocos gramnegativos fastidiosos que requieren suplementos de nutrientes para crecer en cultivos de laboratorio . Son facultativamente intracelulares y típicamente aparecen en pares (diplococos), asemejándose a la forma de los granos de café. Los miembros de este género no forman esporas, son capaces de moverse mediante motilidad espasmódica y son aerobios obligados (requieren oxígeno para crecer). De estas 11 especies que colonizan al hombre, sólo dos son patógenas. N. gonorrhoeae es el agente causante de la gonorrea y N. meningitidis es una causa de meningitis bacteriana. [14]
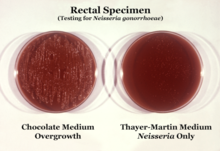

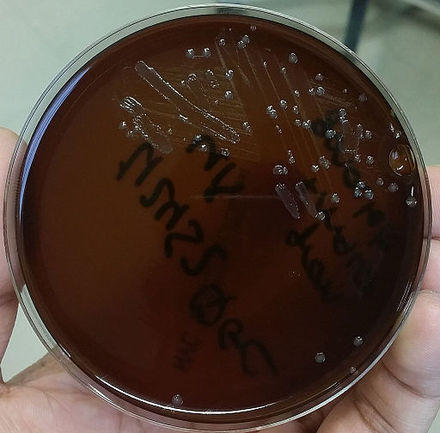
N. gonorrhoeae generalmente se aísla en agar Thayer-Martin (o VPN) en una atmósfera enriquecida con 3-7% de dióxido de carbono. [10] El agar Thayer-Martin es una placa de agar chocolate (agar sangre calentado) que contiene nutrientes y antimicrobianos ( vancomicina , colistina , nistatina y trimetoprima ). Esta preparación de agar facilita el crecimiento de especies de Neisseria al tiempo que inhibe el crecimiento de bacterias y hongos contaminantes. El agar Martin Lewis y el agar ciudad de Nueva York son otros tipos de agar chocolate selectivo que se utilizan comúnmente para el crecimiento de Neisseria . [10] N. gonorrhoeae es oxidasa positiva (posee citocromo c oxidasa) y catalasa positiva (capaz de convertir peróxido de hidrógeno en oxígeno). [10] Cuando se incuba con los carbohidratos lactosa, maltosa , sacarosa y glucosa , N. gonorrhoeae oxidará solo la glucosa. [10]
En su superficie, N. gonorrhoeae porta pelos parecidos a pelos , proteínas de superficie con diversas funciones y azúcares llamados lipooligosacáridos . Los pili median la adherencia, el movimiento y el intercambio de ADN. Las proteínas Opa interactúan con el sistema inmunológico, al igual que las porinas . El lipoligosacarido (LOS) es una endotoxina que provoca una respuesta inmune. Todos son antigénicos y todos exhiben variación antigénica (ver más abajo). Los pili exhiben la mayor variación. Los pili, las proteínas Opa, las porinas e incluso los LOS tienen mecanismos para inhibir la respuesta inmune, haciendo posible la infección asintomática. [15]
Los filamentos de proteínas poliméricas dinámicas llamados pili tipo IV permiten que N. gonorrhoeae se adhiera a las superficies y se mueva a lo largo de ellas. Para ingresar al huésped, la bacteria utiliza los pili para adherirse y penetrar las superficies mucosas. [4] Los pili son un factor de virulencia necesario para N. gonorrhoeae ; sin ellos, la bacteria no puede causar infección. [8] Para moverse, las bacterias individuales usan sus pili como un gancho de agarre: primero, se extienden desde la superficie celular y se adhieren a un sustrato . La retracción posterior del pilus arrastra la célula hacia adelante. El movimiento resultante se conoce como motilidad espasmódica. [16] N. gonorrhoeae es capaz de arrastrar 100.000 veces su propio peso, y los pili utilizados para hacerlo se encuentran entre los motores biológicos más fuertes conocidos hasta la fecha, ejerciendo un nanonewton . [17] Las proteínas PilF y PilT ATPasa son responsables de impulsar la extensión y retracción del pilus tipo IV, respectivamente. [18] [19] Las funciones adhesivas del pilus gonocócico desempeñan un papel en la agregación de microcolonias y la formación de biopelículas . [20] Las proteínas de superficie llamadas proteínas Opa se pueden usar para unirse a receptores en las células inmunes y prevenir una respuesta inmune. Se conocen al menos 12 proteínas Opa y las numerosas permutaciones de las proteínas de superficie dificultan el reconocimiento de N. gonorrhoeae y el montaje de una defensa por parte de las células inmunitarias. [21]
El lipopolisacárido (LOS) es una versión de bajo peso del lipopolisacárido presente en las superficies de la mayoría de las otras bacterias gramnegativas. Es una cadena lateral de azúcar (sacárido) unida al lípido A (por lo tanto, "lipo") en la membrana externa que recubre la pared celular de la bacteria. La raíz "oligo" se refiere al hecho de que es unos pocos azúcares más corto que el típico lipopolisacárido. [4] Como endotoxina, LOS provoca inflamación. La eliminación de LOS por parte de las bacterias es responsable de lesiones locales, por ejemplo, en la enfermedad inflamatoria pélvica. [4] Aunque su función principal es como endotoxina, LOS puede disfrazarse con ácido siálico del huésped y bloquear el inicio de la cascada del complemento . [4]
N. gonorrhoeae evade el sistema inmunológico mediante un proceso llamado variación antigénica . [22] Este proceso permite a N. gonorrhoeae recombinar sus genes y alterar los determinantes antigénicos (sitios donde se unen los anticuerpos), como los pili tipo IV, [23] que adornan su superficie. [4] En pocas palabras, la composición química de las moléculas cambia debido a cambios a nivel genético. [7] N. gonorrhoeae es capaz de variar la composición de sus pili y LOS; de estos, los pili exhiben la mayor variación antigénica debido al reordenamiento cromosómico. [8] [4] El gen PilS es un ejemplo de esta capacidad de reorganización, ya que se estima que su combinación con el gen PilE produce más de 100 variantes de la proteína PilE. [7] Estos cambios permiten el ajuste a las diferencias en el entorno local en el sitio de la infección, la evasión del reconocimiento por parte de los anticuerpos específicos y contribuyen a la falta de una vacuna eficaz. [7]
Además de la capacidad de reordenar los genes que ya tiene, también es naturalmente competente para adquirir ADN nuevo (a través de plásmidos ), a través de su pilus tipo IV, específicamente las proteínas Pil Q y Pil T. [24] Estos procesos permiten que N. gonorrhoeae adquirir/difundir nuevos genes, disfrazarse con diferentes proteínas de superficie e impedir el desarrollo de la memoria inmunológica , una capacidad que ha llevado a la resistencia a los antibióticos y también ha impedido el desarrollo de vacunas. [25]
La variación de fase es similar a la variación antigénica, pero en lugar de que los cambios a nivel genético alteren la composición de las moléculas, estos cambios genéticos dan como resultado la activación o desactivación de un gen. [7] La variación de fase surge con mayor frecuencia de un cambio de marco en el gen expresado. [7] Las proteínas Opacidad, u Opa, de N. gonorrhoeae dependen estrictamente de la variación de fase. [7] Cada vez que las bacterias se replican, pueden activar o desactivar múltiples proteínas Opa mediante un desemparejamiento de la hebra deslizada . Es decir, las bacterias introducen mutaciones de cambio de marco que hacen que los genes entren o salgan del marco. El resultado es que cada vez se traducen diferentes genes Opa. [4] Los pili varían según la variación antigénica, pero también según la variación de fase. [7] Se producen cambios de marco en los genes pilE y pilC , lo que desactiva efectivamente la expresión de pili en situaciones en las que no son necesarios, como después de la colonización, cuando N. gonorrhoeae sobrevive dentro de las células en lugar de en sus superficies. [7]
Después de que los gonococos invaden y transcitan las células epiteliales del huésped, aterrizan en la submucosa, donde los neutrófilos las consumen rápidamente. [4] Los pili y las proteínas Opa en la superficie pueden interferir con la fagocitosis, [8] pero la mayoría de los gonococos terminan en neutrófilos. Los exudados de individuos infectados contienen muchos neutrófilos con gonococos ingeridos. Los neutrófilos liberan una explosión oxidativa de especies reactivas de oxígeno en sus fagosomas para matar a los gonococos. [26] Sin embargo, una fracción significativa de los gonococos puede resistir la muerte mediante la acción de su catalasa [4] , que descompone las especies reactivas de oxígeno y es capaz de reproducirse dentro de los fagosomas de los neutrófilos. [27]
Stohl y Seifert demostraron que la proteína bacteriana RecA, que media en la reparación del daño del ADN, desempeña un papel importante en la supervivencia gonocócica. [28] Michod et al. han sugerido que N. gonorrhoeae puede reemplazar el ADN dañado en los fagosomas de neutrófilos con ADN de gonococos vecinos. [29] El proceso por el cual los gonococos receptores integran el ADN de los gonococos vecinos en su genoma se llama transformación. [30]
Los genomas de varias cepas de N . gonorrhoeae han sido secuenciados. La mayoría de ellos tienen un tamaño aproximado de 2,1 Mb y codifican entre 2.100 y 2.600 proteínas (aunque la mayoría parece estar en el rango inferior). [31] Por ejemplo, la cepa NCCP11945 consta de un cromosoma circular (2.232.025 pb) que codifica 2.662 marcos de lectura abiertos (ORF) predichos y un plásmido (4.153 pb) que codifica 12 ORF predichos. La densidad de codificación estimada en todo el genoma es del 87% y el contenido medio de G+C es del 52,4%, valores similares a los de la cepa FA1090. El genoma NCCP11945 codifica 54 ARNt y cuatro copias de los operones de ARNr 16S-23S-5S. [32]
En 2011, investigadores de la Universidad Northwestern encontraron evidencia de un fragmento de ADN humano en un genoma de N. gonorrhoeae , el primer ejemplo de transferencia horizontal de genes de humanos a un patógeno bacteriano. [33] [34]
Los síntomas de la infección por N. gonorrhoeae difieren según el sitio de la infección y muchas infecciones son asintomáticas independientemente del sexo. [35] [15] [5] Es importante tener en cuenta que, según la ruta de transmisión, N. gonorrhoeae puede causar infección de la garganta ( faringitis ) o infección del ano/recto ( proctitis ). [36] [8]
Las infecciones gonocócicas diseminadas pueden ocurrir cuando N. gonorrhoeae ingresa al torrente sanguíneo, a menudo diseminándose a las articulaciones y causando una erupción (síndrome de dermatitis-artritis). [36] El síndrome de dermatitis-artritis provoca dolor en las articulaciones ( artritis ), inflamación de los tendones ( tenosinovitis ) y dermatitis indolora, no pruriginosa (sin picazón) . [8] La infección diseminada y la enfermedad inflamatoria pélvica en las mujeres tienden a comenzar después de la menstruación debido al reflujo durante la menstruación, lo que facilita la propagación. [36] En casos raros, la infección diseminada puede causar infección de las meninges del cerebro y la médula espinal ( meningitis ) o infección de las válvulas cardíacas ( endocarditis ). [36] [37]
En los hombres sintomáticos, el síntoma principal de la infección genitourinaria es la uretritis: ardor al orinar ( disuria ), aumento de la necesidad de orinar y secreción pus (purulenta) del pene. La secreción puede tener mal olor. [36] Si no se trata, la cicatrización de la uretra puede provocar dificultad para orinar. La infección puede propagarse desde la uretra en el pene a estructuras cercanas, incluidos los testículos ( epididimitis / orquitis ) o a la próstata ( prostatitis ). [36] [8] [38] Los hombres que han tenido una infección por gonorrea tienen un riesgo significativamente mayor de tener cáncer de próstata. [39]
.jpg/440px-Neisseria_gonorrhoeae_and_pus_cells_in_a_vaginal_swab_(Gram_stain).jpg)
En las mujeres sintomáticas, los síntomas principales de la infección genitourinaria son aumento del flujo vaginal, ardor al orinar ( disuria ), aumento de la necesidad de orinar, dolor durante las relaciones sexuales o anomalías menstruales. La enfermedad inflamatoria pélvica se produce si N. gonorrhoeae asciende al peritoneo pélvico (a través del cuello uterino , el endometrio y las trompas de Falopio ). La inflamación y cicatrización resultantes de las trompas de Falopio pueden provocar infertilidad y un mayor riesgo de embarazo ectópico. [36] La enfermedad inflamatoria pélvica se desarrolla en 10 a 20% de las mujeres infectadas con N. gonorrhoeae . [36]
En la infección perinatal , la manifestación principal es la infección del ojo (conjuntivitis neonatal u oftalmía neonatorum ) cuando el recién nacido está expuesto a N. gonorrhoeae en el canal del parto. La infección ocular puede provocar cicatrices o perforación de la córnea y, en última instancia, provocar ceguera. Si el recién nacido está expuesto durante el parto, la conjuntivitis se produce entre 2 y 5 días después del nacimiento y es grave. [36] [37] La oftalmía neonatal gonocócica, que alguna vez fue común en los recién nacidos, se previene mediante la aplicación de gel de eritromicina (antibiótico) en los ojos de los bebés al nacer como medida de salud pública. El nitrato de plata ya no se utiliza en los Estados Unidos. [37] [36]
N. gonorrhoeae se transmite a través del sexo vaginal, oral o anal; La transmisión no sexual es poco probable en la infección en adultos. [5] También se puede transmitir al recién nacido durante el paso por el canal del parto si la madre tiene una infección genitourinaria no tratada. Dada la alta tasa de infección asintomática, todas las mujeres embarazadas deben hacerse pruebas para detectar infección por gonorrea. [5] Sin embargo, los baños comunitarios, las toallas o telas, los termómetros rectales y las manos de los cuidadores se han visto implicados como medios de transmisión en el entorno pediátrico. [40] Los besos también han sido implicados como un medio teórico de transmisión en la población masculina gay, según estudios más recientes. [41] [42] [43]
Tradicionalmente, se pensaba que la bacteria se movía adherida a los espermatozoides, pero esta hipótesis no explicaba la transmisión de la enfermedad de mujer a hombre. Un estudio reciente sugiere que en lugar de "navegar" sobre los espermatozoides que se mueven , la bacteria N. gonorrhoeae utiliza pili para anclarse a las proteínas del esperma y moverse a través del líquido coital. [44]
Para N. gonorrhoeae , el primer paso después de una transmisión exitosa es la adherencia a las células epiteliales que se encuentran en el sitio de la mucosa que está infectado. [45] La bacteria depende de pili tipo IV que se adhieren y retraen, tirando de N. gonorrhoeae hacia la membrana epitelial donde sus proteínas de superficie, como las proteínas de opacidad, pueden interactuar directamente. [45] Después de la adherencia, N. gonorrhoeae se replica y forma microcolonias . [46] Mientras coloniza, N. gonorrhoeae tiene el potencial de transcitorse a través de la barrera epitelial y abrirse camino hacia el torrente sanguíneo. [13] Durante el crecimiento y la colonización, N. gonorrhoeae estimula la liberación de citocinas y quimiocinas de las células inmunitarias del huésped que son proinflamatorias . [13] Estas moléculas proinflamatorias dan como resultado el reclutamiento de macrófagos y neutrófilos . [7] Estas células fagocíticas normalmente absorben patógenos extraños y los destruyen, pero N. gonorrhoeae ha desarrollado muchos mecanismos que le permiten sobrevivir dentro de estas células inmunes y frustrar los intentos de eliminación. [7]
La transmisión se reduce mediante el uso de barreras de látex (por ejemplo, condones o protectores dentales ) durante las relaciones sexuales y limitando las parejas sexuales. [6] También se deben utilizar condones y protectores dentales durante el sexo oral y anal. Los espermicidas, las espumas vaginales y las duchas vaginales no son eficaces para prevenir la transmisión. [4]
El tratamiento actual recomendado por los CDC es una dosis única inyectada de ceftriaxona (una cefalosporina de tercera generación ). [47] Las parejas sexuales (definidas por los CDC como contactos sexuales dentro de los últimos 60 días) [11] también deben ser notificadas, examinadas y tratadas. [6] [47] Es importante que si los síntomas persisten después de recibir tratamiento para la infección por N. gonorrhoeae , se debe realizar una reevaluación. [47]
La resistencia a los antibióticos en la gonorrea se ha observado a partir de la década de 1940. La gonorrea se trataba con penicilina, pero las dosis debían aumentarse progresivamente para que siguiera siendo eficaz. En la década de 1970, surgió en la cuenca del Pacífico la gonorrea resistente a la penicilina y la tetraciclina. Estas cepas resistentes luego se extendieron a Hawaii, California, el resto de Estados Unidos, Australia y Europa. Las fluoroquinolonas fueron la siguiente línea de defensa, pero pronto también surgió resistencia a este antibiótico. Desde 2007, el tratamiento estándar son las cefalosporinas de tercera generación, como la ceftriaxona, que se consideran nuestra "última línea de defensa". [48] [49] Recientemente, se descubrió en Japón una cepa de gonorrea de alto nivel resistente a la ceftriaxona llamada H041. Las pruebas de laboratorio encontraron que era resistente a altas concentraciones de ceftriaxona, así como a la mayoría de los demás antibióticos probados. Dentro de N. gonorrhoeae , existen genes que confieren resistencia a todos los antibióticos utilizados para curar la gonorrea, pero hasta ahora no coexisten dentro de un solo gonococo. Sin embargo, debido a la alta afinidad de N. gonorrhoeae por la transferencia horizontal de genes, la gonorrea resistente a los antibióticos se considera una amenaza emergente para la salud pública. [49]
Como bacteria Gram negativa, N. gonorrhoeae requiere mecanismos de defensa para protegerse contra el sistema del complemento (o cascada del complemento), cuyos componentes se encuentran en el suero humano . [15] Hay tres vías diferentes que activan este sistema; sin embargo, todas dan como resultado la activación de la proteína del complemento 3 (C3). [50] Una porción escindida de esta proteína, C3b , se deposita en superficies patógenas y da como resultado la opsonización , así como la activación posterior del complejo de ataque a la membrana . [50] N. gonorrhoeae tiene varios mecanismos para evitar esta acción. [13] En conjunto, estos mecanismos se denominan resistencia sérica. [13]
Neisseria gonorrhoeae lleva el nombre de Albert Neisser, quien la aisló como el agente causante de la enfermedad gonorrea en 1878. [13] [3] Galeno (130 d.C.) acuñó el término "gonorrea" del griego gonos , que significa "semilla" y rhoe. que significa "fluir". [51] [7] Por lo tanto, gonorrea significa "flujo de semilla", una descripción que se refiere a la secreción blanca del pene, que se supone que es semen, que se observa en la infección masculina. [13]
En 1878, Albert Neisser aisló y visualizó diplococos de N. gonorrhoeae en muestras de pus de 35 hombres y mujeres con los síntomas clásicos de infección genitourinaria por gonorrea, dos de los cuales también tenían infecciones oculares. [7] En 1882, Leistikow y Loeffler pudieron hacer crecer el organismo en cultivo. [13] Luego, en 1883, Max Bockhart demostró de manera concluyente que la bacteria aislada por Albert Neisser era el agente causante de la enfermedad conocida como gonorrea al inocular el pene de un hombre sano con la bacteria. [7] El hombre desarrolló los síntomas clásicos de gonorrea días después, satisfaciendo el último de los postulados de Koch . Hasta ese momento, los investigadores debatían si la sífilis y la gonorrea eran manifestaciones de la misma enfermedad o dos entidades distintas. [52] [7] Uno de esos investigadores del siglo XVIII, John Hunter, intentó resolver el debate en 1767 [7] inoculando a un hombre pus extraído de un paciente con gonorrea. Llegó a la conclusión errónea de que tanto la sífilis como la gonorrea eran en realidad la misma enfermedad cuando el hombre desarrolló la erupción de color cobrizo que es clásica de la sífilis. [50] [52] Aunque muchas fuentes repiten que Hunter se vacunó él mismo, [50] [13] otros han argumentado que en realidad fue otro hombre. [53] Después del experimento de Hunter, otros científicos intentaron refutar sus conclusiones inoculando pus gonorreico a otros médicos varones, estudiantes de medicina [13] y hombres encarcelados, quienes desarrollaron ardor y secreción de gonorrea. Un investigador, Ricord, tomó la iniciativa de realizar 667 inoculaciones de pus gonorreico a pacientes de un hospital psiquiátrico, sin ningún caso de sífilis. [7] [13] En particular, la llegada de la penicilina en la década de 1940 hizo que estuvieran disponibles tratamientos eficaces para la gonorrea. [ cita necesaria ]