La hipercolesterolemia familiar ( HF ) es un trastorno genético que se caracteriza por niveles elevados de colesterol , específicamente niveles muy elevados de colesterol de lipoproteínas de baja densidad (colesterol LDL), en la sangre y enfermedades cardiovasculares tempranas . Las mutaciones más comunes disminuyen la cantidad de receptores LDL funcionales en el hígado o producen receptores LDL anormales que nunca llegan a la superficie celular para funcionar correctamente (tráfico anormal). [ cita requerida ] Dado que la bioquímica corporal subyacente es ligeramente diferente en las personas con HF, sus niveles elevados de colesterol responden menos a los tipos de métodos de control del colesterol que suelen ser más eficaces en las personas sin HF (como la modificación de la dieta y las tabletas de estatinas ). Sin embargo, el tratamiento (incluidas dosis más altas de estatinas) suele ser eficaz.
La HF se clasifica como una dislipidemia familiar de tipo 2. [1] Existen cinco tipos de dislipidemia familiar (sin incluir los subtipos), y cada uno se clasifica tanto por el perfil lipídico alterado como por la anomalía genética. Por ejemplo, el LDL alto (a menudo debido a un defecto del receptor de LDL) es de tipo 2. Otros incluyen defectos en el metabolismo de los quilomicrones , el metabolismo de los triglicéridos y el metabolismo de otras partículas que contienen colesterol, como VLDL e IDL.
Aproximadamente 1 de cada 100 a 200 personas tienen mutaciones en el gen LDLR que codifica la proteína receptora de LDL , que normalmente elimina LDL de la circulación, o el gen APOB que codifica la apolipoproteína B (ApoB), la parte de las partículas LDL que se une a los receptores de LDL. Las mutaciones en otros genes son raras pero importantes de conocer, incluidas las mutaciones de ganancia de función en el gen PCSK9 que codifica la enzima PCSK9 (que degrada los receptores de LDL), lo que resulta en menos receptores de LDL disponibles. Las mutaciones de PCSK9 causan menos del 5% de los casos de HF según la mayoría de los estudios epidemiológicos. [2] Las personas que tienen una copia anormal (son heterocigotas ) del gen LDLR pueden desarrollar enfermedad cardiovascular prematuramente a la edad de 30 a 40 años. Tener dos copias anormales (ser homocigoto ) puede causar enfermedad cardiovascular grave en la infancia. La HF heterocigótica es un trastorno genético común, heredado con un patrón autosómico dominante , que se presenta en 1:250 personas en la mayoría de los países; [3] la HF homocigótica es mucho más rara y se presenta en 1 de cada 300.000 personas. [ cita requerida ]
La HF heterocigótica se trata normalmente con estatinas , secuestradores de ácidos biliares u otros agentes reductores de lípidos que reducen los niveles de colesterol. A los casos nuevos generalmente se les ofrece asesoramiento genético . La HF homocigótica a menudo no responde a la terapia médica y puede requerir otros tratamientos, incluida la aféresis de LDL (eliminación de LDL en un método similar a la diálisis ) y, ocasionalmente , trasplante de hígado . [4]
Los niveles altos de colesterol normalmente no causan ningún síntoma. Se pueden observar depósitos amarillentos de grasa rica en colesterol en varios lugares del cuerpo, como alrededor de los párpados (conocido como xantelasma palpebral ), el borde exterior del iris (conocido como arco senil de la córnea ) y en los tendones de las manos, los codos, las rodillas y los pies, particularmente el tendón de Aquiles (conocido como xantoma tendinoso ). [4] [5]
La deposición acelerada de colesterol en las paredes de las arterias conduce a la aterosclerosis , la causa subyacente de la enfermedad cardiovascular. El problema más común en la HF es el desarrollo de la enfermedad de la arteria coronaria (ateroesclerosis de las arterias coronarias que irrigan el corazón ) a una edad mucho más temprana de lo que se esperaría en la población general. Esto puede conducir a angina de pecho (dolor o presión en el pecho al hacer ejercicio) o ataques cardíacos . Con menor frecuencia, se afectan las arterias del cerebro ; esto puede conducir a ataques isquémicos transitorios (breves episodios de debilidad en un lado del cuerpo o incapacidad para hablar) o, ocasionalmente, accidente cerebrovascular . La enfermedad oclusiva de la arteria periférica (obstrucción de las arterias de las piernas) se presenta principalmente en personas con HF que fuman ; esto puede causar dolor en los músculos de la pantorrilla al caminar que se resuelve con el descanso ( claudicación intermitente ) y problemas debido a una disminución del suministro de sangre a los pies (como gangrena ). [6] El riesgo de aterosclerosis aumenta aún más con la edad y en quienes fuman, tienen diabetes , presión arterial alta y antecedentes familiares de enfermedad cardiovascular. [4] [7]
Aproximadamente el 85% de las personas con este trastorno no han sido diagnosticadas y, en consecuencia, no reciben tratamientos para reducir los lípidos. [9] Los hallazgos del examen físico pueden ayudar al médico a realizar el diagnóstico de HF. Los xantomas tendinosos se observan en el 20-40% de las personas con HF y son patognomónicos de la afección. [9] También se puede observar un xantelasma o un arco corneal. Estos signos comunes respaldan el diagnóstico, pero son hallazgos no específicos. [9]
Los niveles de colesterol se pueden determinar como parte de la evaluación de salud para el seguro médico o la salud ocupacional , cuando se notan signos físicos externos como xantelasma, xantoma, arco, se desarrollan síntomas de enfermedad cardiovascular o se ha encontrado que un miembro de la familia tiene HF. Por lo general, se encuentra un patrón compatible con la hiperlipoproteinemia tipo IIa en la clasificación de Fredrickson : nivel elevado de colesterol total, nivel marcadamente elevado de lipoproteína de baja densidad (LDL), nivel normal de lipoproteína de alta densidad (HDL) y nivel normal de triglicéridos . Los niveles de colesterol total de 350-550 mg/dL son típicos de la HF heterocigótica, mientras que los niveles de colesterol total de 650-1000 mg/dL son típicos de la HF homocigótica. [9] El LDL suele estar por encima del percentil 75 , es decir, el 75% de la población sana tendría un nivel de LDL más bajo. [4] Los niveles de colesterol pueden ser drásticamente más altos en personas con HF que también son obesas . [6]
En función de los valores aislados de LDL elevados y de los criterios clínicos (que difieren según el país), se pueden realizar pruebas genéticas para detectar mutaciones del receptor de LDL, mutaciones de ApoB y PCSK9 . Las mutaciones se detectan en entre el 50 y el 80% de los casos; aquellos que no presentan una mutación suelen tener niveles más altos de triglicéridos y, de hecho, pueden tener otras causas para su colesterol alto, como una hiperlipidemia combinada debida al síndrome metabólico . [10]
La HF debe distinguirse de la hiperlipidemia combinada familiar y la hipercolesterolemia poligénica . Los niveles de lípidos y la presencia de xantomas pueden confirmar el diagnóstico. La sitosterolemia y la xantomatosis cerebrotendinosa son dos afecciones raras que también pueden presentarse con aterosclerosis prematura y xantomas. Generalmente, la medición del colesterol no diferenciará a los pacientes con HF y sitosterolemia, en la que se acumula el estanol vegetal en lugar del colesterol de origen animal. El tratamiento de la afección es muy eficaz con una clase de agente reductor de lípidos: Ezetimiba. La hipercolesterolemia poligénica también puede implicar manifestaciones neurológicas o psiquiátricas, cataratas , diarrea y anomalías esqueléticas. [11] Esta afección no tiene un aumento del colesterol en sangre, pero la acumulación de derivados del colesterol en el tendón puede imitar la HF.
Los defectos genéticos más comunes en la HF son las mutaciones de pérdida de función de LDLR ( prevalencia de 1 en 250, dependiendo de la población), [3] las mutaciones de pérdida de función de ApoB (prevalencia de 1 en 1000), las mutaciones de ganancia de función de PCSK9 (menos de 1 en 2500) y LDLRAP1 . La enfermedad relacionada sitosterolemia , que tiene muchas similitudes con la HF y también presenta acumulación de colesterol en los tejidos, se debe a las mutaciones ABCG5 y ABCG8 . [4]


El gen del receptor de LDL se encuentra en el brazo corto del cromosoma 19 (19p13.1-13.3). [9] Comprende 18 exones y abarca 45 kb , y el producto del gen proteico contiene 839 aminoácidos en forma madura. Una sola copia anormal (heterocigoto) de FH causa enfermedad cardiovascular a la edad de 50 años en aproximadamente el 40% de los casos. Tener dos copias anormales (homocigoto) causa aterosclerosis acelerada en la infancia, incluidas sus complicaciones. Los niveles plasmáticos de LDL están inversamente relacionados con la actividad del receptor de LDL (LDLR). Los homocigotos tienen una actividad de LDLR de menos del 2%, mientras que los heterocigotos tienen un procesamiento defectuoso de LDL con una actividad del receptor de 2-25%, dependiendo de la naturaleza de la mutación. Se conocen más de 1000 mutaciones diferentes. [4]
Hay cinco clases principales de FH debido a mutaciones de LDLR : [12]
La apolipoproteína B , en su forma ApoB100, es la principal apolipoproteína o parte proteica de la partícula lipoproteica. Su gen se encuentra en el segundo cromosoma (2p24-p23) y tiene una longitud de 46,2 kb . La hipercolesterolemia familiar suele estar asociada a la mutación de R3500Q, que provoca la sustitución de la arginina por glutamina en la posición 3500. La mutación se encuentra en una parte de la proteína que normalmente se une al receptor de LDL, y la unión se reduce como resultado de la mutación. Al igual que el LDLR , el número de copias anormales determina la gravedad de la hipercolesterolemia. [4] [13]
En un informe de 2003, las mutaciones en el gen de la proproteína convertasa subtilisina/kexina tipo 9 ( PCSK9 ) se relacionaron con la hiperplasia folicular autosómica dominante (es decir, que requiere solo una copia anormal). [4] [14] El gen está ubicado en el primer cromosoma (1p34.1-p32) y codifica una proteína de 666 aminoácidos que se expresa en el hígado. Se ha sugerido que la PCSK9 causa hiperplasia folicular principalmente al reducir la cantidad de receptores de LDL en las células hepáticas. [15]
Las anomalías en el gen ARH , también conocido como LDLRAP1 , se informaron por primera vez en una familia en 1973. [16] A diferencia de las otras causas, se requieren dos copias anormales del gen para que se desarrolle la HF (autosómica recesiva). Las mutaciones en la proteína tienden a causar la producción de una proteína acortada. Su función real no está clara, pero parece desempeñar un papel en la relación entre el receptor de LDL y las fosas recubiertas de clatrina. Las personas con hipercolesterolemia autosómica recesiva tienden a tener una enfermedad más grave que los heterocigotos LDLR , pero menos grave que los homocigotos LDLR . [4]
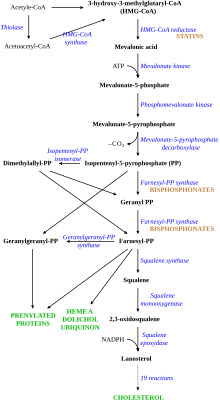
El colesterol LDL normalmente circula en el cuerpo durante 2,5 días y, posteriormente, la porción de apolipoproteína B del colesterol LDL se une al receptor de LDL en las células del hígado , lo que desencadena su captación y digestión . [9] Este proceso da como resultado la eliminación de LDL del sistema circulatorio. La síntesis de colesterol por el hígado se suprime en la vía de la HMG-CoA reductasa . [17] En la HF, la función del receptor de LDL se reduce o está ausente, [9] y la LDL circula durante una duración media de 4,5 días, lo que da como resultado un nivel significativamente mayor de colesterol LDL en la sangre con niveles normales de otras lipoproteínas. [6] En las mutaciones de ApoB , la unión reducida de partículas LDL al receptor provoca el aumento del nivel de colesterol LDL. No se sabe cómo la mutación causa la disfunción del receptor de LDL en las mutaciones de PCSK9 y ARH . [4]
Aunque la aterosclerosis se presenta en cierta medida en todas las personas, las personas con HF pueden desarrollar una aterosclerosis acelerada debido al exceso de niveles de LDL. El grado de aterosclerosis depende aproximadamente del número de receptores de LDL que aún se expresen y de la funcionalidad de estos receptores. En muchas formas heterocigóticas de HF, la función del receptor solo se ve levemente afectada y los niveles de LDL se mantendrán relativamente bajos. En las formas homocigóticas más graves, el receptor no se expresa en absoluto. [4]
Algunos estudios de cohortes de HF sugieren que, por lo general, hay factores de riesgo adicionales en juego cuando una persona desarrolla aterosclerosis. [18] [19] Además de los factores de riesgo clásicos, como el tabaquismo, la hipertensión arterial y la diabetes, los estudios genéticos han demostrado que una anomalía común en el gen de la protrombina (G20210A) aumenta el riesgo de eventos cardiovasculares en personas con HF. [20] Varios estudios encontraron que un alto nivel de lipoproteína (a) era un factor de riesgo adicional para la enfermedad cardíaca isquémica. [21] [22] También se encontró que el riesgo era mayor en personas con un genotipo específico de la enzima convertidora de angiotensina (ECA). [23]
La detección del colesterol y las pruebas genéticas entre los miembros de la familia de personas con HF conocida son rentables . [24] En 2001 se sugirieron otras estrategias, como la detección universal a la edad de 16 años . [25] [26] Sin embargo, este último enfoque puede ser menos rentable a corto plazo. [27] Se pensaba que la detección a una edad inferior a los 16 años probablemente conduciría a una tasa inaceptablemente alta de falsos positivos . [6]
Un metaanálisis de 2007 concluyó que "la estrategia propuesta de detección de hipercolesterolemia familiar en niños y padres podría tener un impacto considerable en la prevención de las consecuencias médicas de este trastorno en dos generaciones simultáneamente". [28] "El uso del colesterol total por sí solo puede ser el mejor método para discriminar entre personas con y sin hipercolesterolemia familiar entre 1 y 9 años de edad". [29] [28]
Se ha sugerido la realización de pruebas de detección en niños pequeños y en 2016 se publicaron los resultados de un ensayo con 10 000 niños de un año. Era necesario investigar para determinar si las pruebas de detección eran rentables y aceptables para las familias. [30] [31] El asesoramiento genético puede ayudar en las pruebas genéticas después de un análisis de colesterol positivo para HF. [32]
La hipercolesterolemia familiar heterocigótica (HeFH) se trata habitualmente con estatinas . [9] Las estatinas actúan inhibiendo la enzima hidroximetilglutaril CoA reductasa (HMG-CoA-reductasa) en el hígado. En respuesta, el hígado produce más receptores de LDL, que eliminan las LDL circulantes de la sangre. Las estatinas reducen eficazmente los niveles de colesterol y LDL, aunque a veces se requiere una terapia complementaria con otros fármacos, como secuestradores de ácidos biliares ( colestiramina o colestipol ), preparaciones de ácido nicotínico o fibratos. [33] [4] Es necesario controlar otros factores de riesgo de enfermedad cardiovascular, ya que el riesgo sigue siendo algo elevado incluso cuando se controlan los niveles de colesterol. Las directrices profesionales recomiendan que la decisión de tratar a una persona con HF con estatinas no se base en las herramientas habituales de predicción del riesgo (como las derivadas del Framingham Heart Study ), ya que es probable que subestimen el riesgo de enfermedad cardiovascular; A diferencia del resto de la población, los HF han tenido niveles altos de colesterol desde el nacimiento, lo que probablemente aumenta su riesgo relativo. [34] Antes de la introducción de las estatinas, se utilizaban clofibrato (un fibrato más antiguo que a menudo causaba cálculos biliares ), probucol (especialmente en xantomas grandes) y tiroxina para reducir los niveles de colesterol LDL.
Más controvertida es la adición de ezetimiba , que inhibe la absorción de colesterol en el intestino. Si bien reduce el colesterol LDL, no parece mejorar un marcador de aterosclerosis llamado espesor de la íntima-media . Se desconoce si esto significa que la ezetimiba no tiene ningún beneficio general en la HF. [35]
No existen estudios de intervención que demuestren directamente un beneficio en la mortalidad de la reducción del colesterol en la hipercolesterolemia familiar. Más bien, la evidencia del beneficio se deriva de una serie de ensayos realizados en personas con hipercolesterolemia poligénica (en la que la herencia desempeña un papel menor). Sin embargo, un estudio observacional de 1999 de un gran registro británico mostró que la mortalidad en personas con hipercolesterolemia familiar había comenzado a mejorar a principios de los años 1990 cuando se introdujeron las estatinas. [36]
Un estudio de cohorte sugirió que el tratamiento de la hiperplasia falciforme con estatinas conduce a una reducción del 48% en la mortalidad por enfermedad coronaria hasta un punto en el que las personas no tienen más probabilidades de morir de enfermedad coronaria que la población general. Sin embargo, si la persona ya tenía enfermedad coronaria, la reducción fue del 25%. Los resultados enfatizan la importancia de la identificación temprana de la hiperplasia falciforme y el tratamiento con estatinas. [37]
Alirocumab y evolocumab , ambos anticuerpos monoclonales contra PCSK9 , están específicamente indicados como complemento de la dieta y la terapia con estatinas máximamente tolerada para el tratamiento de adultos con hipercolesterolemia familiar heterocigótica que requieren una reducción adicional del colesterol LDL. [38]
Más recientemente, se ha aprobado el Inclisiran para el tratamiento de la HFHe.
Aunque los anticuerpos monoclonales contra PCSK9 son muy eficaces para los pacientes con hipercolesterolemia familiar, la administración parenteral hace que sea menos aceptable para el paciente. Hay muchos PCSK9 orales estudiados en ensayos clínicos (fase 2 y fase 3) y pronto se adoptarán como tratamiento de la hipercolesterolemia.
La hipercolesterolemia familiar homocigótica (HoFH) es más difícil de tratar. Los receptores de LDL (lipoproteína de baja densidad) son mínimamente funcionales, si es que lo son. Solo las dosis altas de estatinas, a menudo en combinación con otros medicamentos, son modestamente efectivas para mejorar los niveles de lípidos. [39] Si la terapia médica no tiene éxito en la reducción de los niveles de colesterol, se puede utilizar la aféresis de LDL ; esto filtra las LDL del torrente sanguíneo en un proceso que recuerda a la diálisis . [4] Los casos muy graves pueden considerarse para un trasplante de hígado ; esto proporciona un hígado con receptores de LDL normalmente funcionales y conduce a una rápida mejora de los niveles de colesterol, pero con el riesgo de complicaciones de cualquier trasplante de órgano sólido (como rechazo , infecciones o efectos secundarios de la medicación necesaria para suprimir el rechazo). [40] [41] Otras técnicas quirúrgicas incluyen la cirugía de derivación ileal parcial , en la que se desvía parte del intestino delgado para disminuir la absorción de nutrientes y, por lo tanto, el colesterol, y la cirugía de derivación portocava , en la que la vena porta se conecta a la vena cava para permitir que la sangre con nutrientes del intestino evite el hígado. [42] [43] [44]
La lomitapida , un inhibidor de la proteína de transferencia de triglicéridos microsomales , [45] fue aprobada por la FDA de EE. UU. en diciembre de 2012 como un fármaco huérfano para el tratamiento de la hipercolesterolemia familiar homocigótica. [46] En enero de 2013, la FDA de EE. UU. también aprobó mipomersen , que inhibe la acción del gen de la apolipoproteína B , para el tratamiento de la hipercolesterolemia familiar homocigótica. [47] [48] [49] La terapia génica es una posible alternativa futura. [50]
Evinacumab , un anticuerpo monoclonal que inhibe la proteína similar a la angiopoyetina 3 , fue aprobado en 2021 como terapia complementaria . [51]
Dado que la HF está presente desde el nacimiento y los cambios ateroscleróticos pueden comenzar temprano en la vida, [52] a veces es necesario tratar a los adolescentes o incluso a los jóvenes con agentes que fueron desarrollados originalmente para adultos. Debido a las preocupaciones de seguridad, muchos médicos prefieren usar secuestradores de ácidos biliares y fenofibrato , ya que están autorizados en niños. [53] Sin embargo, las estatinas parecen seguras y efectivas, [54] [55] y en niños mayores pueden usarse como en adultos. [6] [53]
En 2006, un panel de expertos recomendó una terapia de combinación temprana con aféresis de LDL, estatinas e inhibidores de la absorción de colesterol en niños con HF homocigótica con mayor riesgo. [56]
La prevalencia mundial de la HF es de aproximadamente 10 millones de personas. [9] En la mayoría de las poblaciones estudiadas, la HF heterocigótica se presenta en aproximadamente 1:250 personas, pero no todas desarrollan síntomas. [3] La HF homocigótica se presenta en aproximadamente 1:1.000.000. [4] [6]
Las mutaciones de LDLR son más comunes en ciertas poblaciones, presumiblemente debido a un fenómeno genético conocido como el efecto fundador : fueron fundadas por un pequeño grupo de individuos, uno o varios de los cuales eran portadores de la mutación. Los afrikáneres , los francocanadienses , los cristianos libaneses y los finlandeses tienen altas tasas de mutaciones específicas que hacen que la HF sea particularmente común en estos grupos. Las mutaciones de APOB son más comunes en Europa Central. [4]
El médico noruego Dr. Carl Müller fue el primero en asociar los signos físicos, los niveles altos de colesterol y la herencia autosómica dominante en 1938. [57] A principios de los años 1970 y 1980, el Dr. Joseph L. Goldstein y el Dr. Michael S. Brown de Dallas, Texas, describieron la causa genética de la HF . Inicialmente, encontraron una mayor actividad de la HMG-CoA reductasa, pero los estudios demostraron que esto no explicaba los niveles de colesterol muy anormales en las personas con HF. [58] El enfoque se desplazó a la unión de LDL a su receptor y los efectos de la unión alterada en el metabolismo; este resultó ser el mecanismo subyacente de la HF. [59] Posteriormente, se identificaron directamente numerosas mutaciones en la proteína mediante secuenciación. [12] Más tarde ganaron el Premio Nobel de Medicina de 1985 por su descubrimiento del receptor de LDL y su impacto en el metabolismo de las lipoproteínas. [60]
{{cite journal}}: CS1 maint: varios nombres: lista de autores ( enlace )