La gluconeogénesis ( GNG ) es una vía metabólica que da como resultado la biosíntesis de glucosa a partir de ciertos sustratos de carbono distintos de los carbohidratos . Es un proceso ubicuo, presente en plantas, animales, hongos, bacterias y otros microorganismos. [1] En los vertebrados, la gluconeogénesis se produce principalmente en el hígado y, en menor medida, en la corteza de los riñones . Es uno de los dos mecanismos principales (el otro es la degradación del glucógeno ( glucogenólisis )) utilizados por los humanos y muchos otros animales para mantener los niveles de azúcar en sangre , evitando niveles bajos ( hipoglucemia ). [2] En los rumiantes , debido a que los carbohidratos de la dieta tienden a ser metabolizados por los organismos del rumen , la gluconeogénesis ocurre independientemente del ayuno, las dietas bajas en carbohidratos, el ejercicio, etc. [3] En muchos otros animales, el proceso ocurre durante períodos de ayuno , inanición , dietas bajas en carbohidratos o ejercicio intenso .
En los seres humanos, los sustratos para la gluconeogénesis pueden provenir de cualquier fuente distinta de los carbohidratos que pueda convertirse en piruvato o intermediarios de la glucólisis (ver figura). Para la descomposición de las proteínas , estos sustratos incluyen aminoácidos glucogénicos (aunque no aminoácidos cetogénicos ); de la descomposición de los lípidos (como los triglicéridos ), incluyen glicerol , ácidos grasos de cadena impar (aunque no ácidos grasos de cadena par, ver más abajo); y de otras partes del metabolismo que incluyen el lactato del ciclo de Cori . En condiciones de ayuno prolongado, la acetona derivada de cuerpos cetónicos también puede servir como sustrato, proporcionando una vía desde los ácidos grasos hasta la glucosa. [4] Aunque la mayor parte de la gluconeogénesis ocurre en el hígado, la contribución relativa de la gluconeogénesis por parte del riñón aumenta en la diabetes y el ayuno prolongado. [5]
La vía de la gluconeogénesis es altamente endergónica hasta que se acopla a la hidrólisis de ATP o GTP , haciendo efectivamente el proceso exergónico . Por ejemplo, la vía que va del piruvato a la glucosa-6-fosfato requiere 4 moléculas de ATP y 2 moléculas de GTP para avanzar espontáneamente. Estos ATP se suministran a partir del catabolismo de los ácidos grasos mediante la oxidación beta . [6]

En los seres humanos, los principales precursores gluconeogénicos son el lactato , el glicerol (que forma parte de la molécula de triglicéridos ), la alanina y la glutamina . En conjunto, representan más del 90% de la gluconeogénesis total. [8] Otros aminoácidos glucogénicos y todos los intermedios del ciclo del ácido cítrico (mediante conversión a oxaloacetato ) también pueden funcionar como sustratos para la gluconeogénesis. [9] Generalmente, el consumo humano de sustratos gluconeogénicos en los alimentos no produce un aumento de la gluconeogénesis. [10]
En rumiantes , el propionato es el principal sustrato gluconeogénico. [3] [11] En los no rumiantes, incluidos los seres humanos, el propionato surge de la β-oxidación de ácidos grasos de cadena impar y ramificada, y es un sustrato (relativamente menor) para la gluconeogénesis. [12] [13]
El lactato se transporta de regreso al hígado, donde se convierte en piruvato mediante el ciclo de Cori utilizando la enzima lactato deshidrogenasa . El piruvato, el primer sustrato designado de la vía gluconeogénica, puede utilizarse entonces para generar glucosa. [9] La transaminación o desaminación de aminoácidos facilita la entrada de su esqueleto carbonado en el ciclo directamente (como piruvato u oxalacetato), o indirectamente a través del ciclo del ácido cítrico. La contribución del lactato del ciclo de Cori a la producción general de glucosa aumenta con la duración del ayuno . [14] Específicamente, después de 12, 20 y 40 horas de ayuno por parte de voluntarios humanos, la contribución del lactato del ciclo de Cori a la gluconeogénesis fue del 41%, 71% y 92%, respectivamente. [14]
La cuestión de si los ácidos grasos de cadena par pueden convertirse en glucosa en los animales ha sido una cuestión de larga data en bioquímica. [15] Los ácidos grasos de cadena impar se pueden oxidar para producir acetil-CoA y propionil-CoA , sirviendo este último como precursor de la succinil-CoA , que se puede convertir en oxaloacetato y entrar en la gluconeogénesis. Por el contrario, los ácidos grasos de cadena uniforme se oxidan para producir sólo acetil-CoA, cuya entrada en la gluconeogénesis requiere la presencia de un ciclo de glioxilato (también conocido como derivación de glioxilato) para producir precursores de ácidos dicarboxílicos de cuatro carbonos. [9] La derivación de glioxilato comprende dos enzimas, malato sintasa e isocitrato liasa, y está presente en hongos, plantas y bacterias. A pesar de algunos informes sobre actividades enzimáticas de derivación de glioxilato detectadas en tejidos animales, los genes que codifican ambas funciones enzimáticas solo se han encontrado en nematodos , en los que existen como una única enzima bifuncional. [16] [17] Se han identificado genes que codifican la malato sintasa sola (pero no la isocitrato liasa) en otros animales , incluidos artrópodos , equinodermos e incluso algunos vertebrados . Los mamíferos que poseen el gen de la malato sintasa incluyen monotremas ( ornitorrinco ) y marsupiales ( zarigüeya ), pero no mamíferos placentarios . [17]
No se ha establecido la existencia del ciclo del glioxilato en humanos y se sostiene ampliamente que los ácidos grasos no pueden convertirse directamente en glucosa en humanos. Se ha demostrado que el carbono-14 termina en la glucosa cuando se suministra en ácidos grasos, [18] pero esto se puede esperar de la incorporación de átomos marcados derivados del acetil-CoA en los intermedios del ciclo del ácido cítrico que son intercambiables con los derivados del otras fuentes fisiológicas, como los aminoácidos glucogénicos. [15] En ausencia de otras fuentes glucogénicas, la acetil-CoA de 2 carbonos derivada de la oxidación de ácidos grasos no puede producir un rendimiento neto de glucosa a través del ciclo del ácido cítrico , ya que dos átomos de carbono equivalentes se liberan como dióxido de carbono durante el ciclo. Sin embargo, durante la cetosis , la acetil-CoA de los ácidos grasos produce cuerpos cetónicos , incluida la acetona , y hasta ~60% de la acetona puede oxidarse en el hígado a los precursores del piruvato, acetol y metilglioxal . [19] [4] Por lo tanto, los cuerpos cetónicos derivados de ácidos grasos podrían representar hasta el 11% de la gluconeogénesis durante la inanición. El catabolismo de los ácidos grasos también produce energía en forma de ATP que es necesaria para la vía de la gluconeogénesis.
En los mamíferos, se cree que la gluconeogénesis está restringida al hígado, [20] el riñón, [20] el intestino, [21] y el músculo, [22] pero evidencia reciente indica que la gluconeogénesis ocurre en los astrocitos del cerebro. [23] Estos órganos utilizan precursores gluconeogénicos algo diferentes. El hígado utiliza preferentemente lactato, glicerol y aminoácidos glucógenos (especialmente alanina ), mientras que el riñón utiliza preferentemente lactato, glutamina y glicerol. [24] [8] El lactato del ciclo de Cori es cuantitativamente la mayor fuente de sustrato para la gluconeogénesis, especialmente para el riñón. [8] El hígado utiliza tanto la glucogenólisis como la gluconeogénesis para producir glucosa, mientras que el riñón solo utiliza la gluconeogénesis. [8] Después de una comida, el hígado pasa a la síntesis de glucógeno , mientras que el riñón aumenta la gluconeogénesis. [10] El intestino utiliza principalmente glutamina y glicerol. [21]
El propionato es el sustrato principal para la gluconeogénesis en el hígado de rumiantes, y el hígado de rumiantes puede hacer un mayor uso de aminoácidos gluconeogénicos (p. ej., alanina) cuando aumenta la demanda de glucosa. [25] La capacidad de las células hepáticas para utilizar el lactato para la gluconeogénesis disminuye desde la etapa prerumiante hasta la etapa rumiante en terneros y corderos. [26] En el tejido renal de oveja, se han observado tasas muy altas de gluconeogénesis a partir del propionato. [26]
En todas las especies, la formación de oxaloacetato a partir de piruvato y intermediarios del ciclo del TCA está restringida a la mitocondria, y las enzimas que convierten el ácido fosfoenolpirúvico (PEP) en glucosa-6-fosfato se encuentran en el citosol. [27] La ubicación de la enzima que une estas dos partes de la gluconeogénesis al convertir el oxalacetato en PEP ( PEP carboxiquinasa (PEPCK)) es variable según la especie: puede encontrarse completamente dentro de las mitocondrias , completamente dentro del citosol o dispersada uniformemente entre los dos, como ocurre en los humanos. [27] El transporte de PEP a través de la membrana mitocondrial se logra mediante proteínas de transporte dedicadas; sin embargo, no existen tales proteínas para el oxalacetato . [27] Por lo tanto, en especies que carecen de PEPCK intramitocondrial, el oxaloacetato debe convertirse en malato o aspartato , exportarse desde la mitocondria y convertirse nuevamente en oxaloacetato para permitir que continúe la gluconeogénesis. [27]
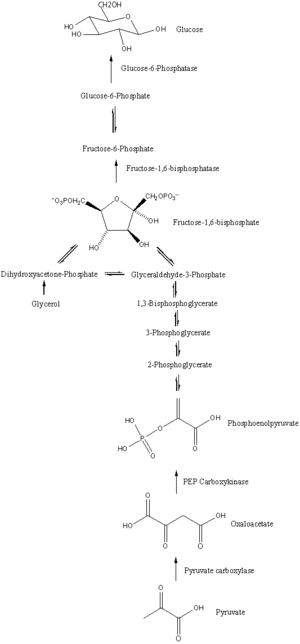
La gluconeogénesis es una vía que consta de una serie de once reacciones catalizadas por enzimas. La vía comenzará en el hígado o el riñón, en las mitocondrias o el citoplasma de esas células, dependiendo del sustrato que se utilice. Muchas de las reacciones son inversas a los pasos que se encuentran en la glucólisis . [ cita necesaria ]
Si bien la mayoría de los pasos en la gluconeogénesis son inversos a los que se encuentran en la glucólisis , tres reacciones reguladas y fuertemente endergónicas se reemplazan por reacciones cinéticamente más favorables. Las enzimas de la glucólisis hexoquinasa / glucocinasa , fosfofructoquinasa y piruvato quinasa se reemplazan por glucosa-6-fosfatasa , fructosa-1,6-bisfosfatasa y PEP carboxiquinasa /piruvato carboxilasa. Estas enzimas suelen estar reguladas por moléculas similares, pero con resultados opuestos. Por ejemplo, el acetil CoA y el citrato activan las enzimas de la gluconeogénesis (piruvato carboxilasa y fructosa-1,6-bisfosfatasa, respectivamente), al mismo tiempo que inhiben la enzima glicolítica piruvato quinasa . Este sistema de control recíproco permite que la glucólisis y la gluconeogénesis se inhiban mutuamente y evita un ciclo inútil de síntesis de glucosa para solo descomponerla. La piruvato quinasa también puede evitarse mediante 86 vías [28] no relacionadas con la gluconeogénesis, con el fin de formar piruvato y posteriormente lactato; Algunas de estas vías utilizan átomos de carbono originados a partir de la glucosa.
La mayoría de las enzimas responsables de la gluconeogénesis se encuentran en el citosol ; las excepciones son la piruvato carboxilasa mitocondrial y, en animales, la fosfoenolpiruvato carboxiquinasa . Este último existe como una isoenzima ubicada tanto en la mitocondria como en el citosol . [29] La tasa de gluconeogénesis está controlada en última instancia por la acción de una enzima clave, la fructosa-1,6-bisfosfatasa , que también está regulada mediante la transducción de señales por el AMPc y su fosforilación.
El control global de la gluconeogénesis está mediado por el glucagón ( liberado cuando la glucosa en sangre es baja ); desencadena la fosforilación de enzimas y proteínas reguladoras por la proteína quinasa A (una quinasa regulada por AMP cíclico), lo que da como resultado la inhibición de la glucólisis y la estimulación de la gluconeogénesis. La insulina contrarresta el glucagón inhibiendo la gluconeogénesis. La diabetes tipo 2 se caracteriza por un exceso de glucagón y resistencia a la insulina en el cuerpo. [30] La insulina ya no puede inhibir la expresión genética de enzimas como PEPCK, lo que conduce a mayores niveles de hiperglucemia en el cuerpo. [31] El fármaco antidiabético metformina reduce la glucosa en sangre principalmente mediante la inhibición de la gluconeogénesis, superando la incapacidad de la insulina para inhibir la gluconeogénesis debido a la resistencia a la insulina. [32]
Los estudios han demostrado que la ausencia de producción hepática de glucosa no tiene un efecto importante sobre el control de la concentración de glucosa plasmática en ayunas. La inducción compensatoria de la gluconeogénesis ocurre en los riñones y el intestino, impulsada por el glucagón , los glucocorticoides y la acidosis. [33]
En el hígado, la proteína FOX FOXO6 normalmente promueve la gluconeogénesis en ayunas, pero la insulina bloquea FOXO6 durante la alimentación. [34] En una condición de resistencia a la insulina , la insulina no logra bloquear FOXO6, lo que resulta en una gluconeogénesis continua incluso después de la alimentación, lo que resulta en un nivel alto de glucosa en sangre ( hiperglucemia ). [34]
La resistencia a la insulina es una característica común del síndrome metabólico y la diabetes tipo 2 . Por esta razón, la gluconeogénesis es un objetivo de la terapia para la diabetes tipo 2, como el fármaco antidiabético metformina , que inhibe la formación de glucosa gluconeogénica y estimula la absorción de glucosa por las células. [35]
La gluconeogénesis se considera una de las vías anabólicas más antiguas y es probable que se haya exhibido en el último ancestro común universal . [36] Rafael F. Say y Georg Fuchs declararon en 2010 que "todos los grupos de arqueas, así como los linajes bacterianos profundamente ramificados, contienen una fructosa 1,6-bisfosfato (FBP) aldolasa/fosfatasa bifuncional con actividad tanto de FBP aldolasa como de FBP fosfatasa. Esta enzima falta en la mayoría de las demás bacterias y en eucariotas, y es termoestable incluso en Crenarchaeota marina mesófila". Se propone que la fructosa 1,6-bifosfato aldolasa/fosfatasa era una enzima gluconeogénica ancestral y había precedido a la glucólisis. [37] Pero los mecanismos químicos entre la gluconeogénesis y la glucólisis, ya sea anabólica o catabólica, son similares, lo que sugiere que ambos se originaron al mismo tiempo. Se ha demostrado que la fructosa 1,6-bifosfato se sintetiza continuamente de forma no enzimática dentro de una solución congelada. La síntesis se acelera en presencia de aminoácidos como la glicina y la lisina, lo que implica que las primeras enzimas anabólicas fueron los aminoácidos. Las reacciones prebióticas en la gluconeogénesis también pueden desarrollarse de forma no enzimática en ciclos de deshidratación-desecación. Esta química podría haber ocurrido en ambientes hidrotermales, incluidos los gradientes de temperatura y los ciclos de congelación y descongelación. Las superficies minerales podrían haber desempeñado un papel en la fosforilación de intermediarios metabólicos de la gluconeogénesis y se ha demostrado que producen tetrosa, hexosas fosfatos y pentosas a partir de formaldehído, gliceraldehído y glicolaldehído. [38] [39] [40]