
Un biomaterial es una sustancia que ha sido diseñada para interactuar con sistemas biológicos con un propósito médico, ya sea terapéutico (tratar, aumentar, reparar o reemplazar una función tisular del cuerpo) o de diagnóstico . El campo de estudio correspondiente, llamado ciencia de los biomateriales o ingeniería de biomateriales , tiene unos cincuenta años. [ necesita actualización ] Ha experimentado un crecimiento constante a lo largo de su historia, y muchas empresas han invertido grandes cantidades de dinero en el desarrollo de nuevos productos. La ciencia de los biomateriales abarca elementos de la medicina , la biología , la química , la ingeniería de tejidos y la ciencia de los materiales .
Un biomaterial es diferente de un material biológico, como el hueso , que es producido por un sistema biológico . Sin embargo, "biomaterial" y "material biológico" suelen utilizarse indistintamente. Además, la palabra "bioterial" se ha propuesto como una posible palabra alternativa para materiales producidos biológicamente como huesos o biocompuestos fúngicos. [ cita necesaria ] Además, se debe tener cuidado al definir un biomaterial como biocompatible , ya que es específico de la aplicación. Un biomaterial que es biocompatible o adecuado para una aplicación puede no serlo en otra. [1]
Material explotado en contacto con tejidos, organismos o microorganismos vivos. [2] [a] [b] [c]
Los biomateriales pueden derivarse de la naturaleza o sintetizarse en el laboratorio utilizando una variedad de enfoques químicos utilizando componentes metálicos, polímeros , cerámicas o materiales compuestos . A menudo se usan y/o adaptan para una aplicación médica y, por lo tanto, comprenden la totalidad o parte de una estructura viva o dispositivo biomédico que realiza, aumenta o reemplaza una función natural. Dichas funciones pueden ser relativamente pasivas, como su uso para una válvula cardíaca , o tal vez bioactivas con una funcionalidad más interactiva, como los implantes de cadera recubiertos de hidroxiapatita . Los biomateriales también se utilizan habitualmente en aplicaciones dentales, cirugía y administración de fármacos. Por ejemplo, se puede colocar en el cuerpo una construcción con productos farmacéuticos impregnados, lo que permite la liberación prolongada de un fármaco durante un período de tiempo prolongado. Un biomaterial también puede ser un autoinjerto , aloinjerto o xenoinjerto utilizado como material de trasplante . [ cita necesaria ]
La capacidad de un biomaterial diseñado para inducir una respuesta fisiológica que respalde la función y el rendimiento del biomaterial se conoce como bioactividad. Más comúnmente, en vidrios bioactivos y cerámicas bioactivas, este término se refiere a la capacidad de los materiales implantados para unirse bien con el tejido circundante en funciones osteoconductoras u osteoproductivas. [4] Los materiales de implantes óseos a menudo están diseñados para promover el crecimiento óseo mientras se disuelven en el líquido corporal circundante. [5] Por lo tanto, para muchos biomateriales es deseable una buena biocompatibilidad junto con una buena resistencia y tasas de disolución. Comúnmente, la bioactividad de los biomateriales se mide por la biomineralización de la superficie en la que se forma una capa nativa de hidroxiapatita en la superficie. Hoy en día, el desarrollo de biomateriales clínicamente útiles se ve muy favorecido por la llegada de rutinas computacionales que pueden predecir los efectos moleculares de los biomateriales en un entorno terapéutico basado en una experimentación in vitro limitada . [6]
Autoensamblaje es el término más común en uso en la comunidad científica moderna para describir la agregación espontánea de partículas (átomos, moléculas, coloides , micelas , etc.) sin la influencia de fuerzas externas. Se sabe que grandes grupos de tales partículas se ensamblan en conjuntos termodinámicamente estables y estructuralmente bien definidos, que recuerdan bastante a uno de los siete sistemas cristalinos que se encuentran en la metalurgia y la mineralogía (por ejemplo, cúbico centrado en las caras, cúbico centrado en el cuerpo, etc.). . La diferencia fundamental en la estructura de equilibrio está en la escala espacial de la celda unitaria (parámetro de red) en cada caso particular.
El autoensamblaje molecular se encuentra ampliamente en los sistemas biológicos y proporciona la base de una amplia variedad de estructuras biológicas complejas. Esto incluye una clase emergente de biomateriales mecánicamente superiores basados en características y diseños microestructurales que se encuentran en la naturaleza. Así, el autoensamblaje también se perfila como una nueva estrategia en la síntesis química y la nanotecnología . Los cristales moleculares, los cristales líquidos, los coloides, las micelas, las emulsiones , los polímeros de fases separadas, las películas delgadas y las monocapas autoensambladas representan ejemplos de los tipos de estructuras altamente ordenadas que se obtienen utilizando estas técnicas. La característica distintiva de estos métodos es la autoorganización. [7] [8] [9]
Casi todos los materiales podrían considerarse estructurados jerárquicamente, ya que los cambios en la escala espacial provocan diferentes mecanismos de deformación y daño. [10] Sin embargo, en materiales biológicos, esta organización jerárquica es inherente a la microestructura. Uno de los primeros ejemplos de esto, en la historia de la biología estructural, es el temprano trabajo de dispersión de rayos X sobre la estructura jerárquica del cabello y la lana realizado por Astbury y Woods. [11] En el hueso, por ejemplo, el colágeno es el componente básico de la matriz orgánica , una triple hélice con un diámetro de 1,5 nm. Estas moléculas de tropocolágeno se intercalan con la fase mineral ( hidroxiapatita , fosfato cálcico) formando fibrillas que se enrollan en helicoides de direcciones alternas. Estas " osteones " son los componentes básicos de los huesos, siendo la distribución de la fracción de volumen entre la fase orgánica y la mineral aproximadamente 60/40.
En otro nivel de complejidad, los cristales de hidroxiapatita son plaquetas minerales que tienen un diámetro de aproximadamente 70 a 100 nm y un espesor de 1 nm. Originalmente se nuclean en los espacios entre las fibrillas de colágeno. [12]
De manera similar, la jerarquía de la concha de abulón comienza en el nivel nanométrico, con una capa orgánica que tiene un espesor de 20 a 30 nm. Esta capa está formada por monocristales de aragonito (un polimorfo de CaCO 3 ) que consisten en "ladrillos" de dimensiones 0,5 y rematados en capas de aproximadamente 0,3 mm (mesoestructura). [13]
Los cangrejos son artrópodos, cuyo caparazón está hecho de un componente duro mineralizado (muestra fractura frágil) y un componente orgánico más blando compuesto principalmente de quitina . El componente frágil está dispuesto en forma de hélice. Cada una de estas "barras" minerales (1 μm de diámetro) contiene fibrillas de proteína de quitina con aproximadamente 60 nm de diámetro. Estas fibrillas están formadas por canales de 3 nm de diámetro que unen el interior y el exterior del caparazón.
Los biomateriales se utilizan en:
Los biomateriales deben ser compatibles con el cuerpo y, a menudo, existen problemas de biocompatibilidad que deben resolverse antes de que un producto pueda comercializarse y utilizarse en un entorno clínico . Por esta razón, los biomateriales suelen estar sujetos a los mismos requisitos que los que se aplican a las nuevas terapias farmacológicas . [19] [20] Todas las empresas fabricantes también deben garantizar la trazabilidad de todos sus productos, de modo que si se descubre un producto defectuoso, se puedan rastrear otros en el mismo lote.
El sulfato de calcio (sus α y β hemihidratos) es un material biocompatible bien conocido que se usa ampliamente como sustituto de injertos óseos en odontología o como aglutinante. [21] [22]
En Estados Unidos, el 49% de los 250.000 procedimientos de reemplazo valvular realizados anualmente implican un implante valvular mecánico. La válvula más utilizada es una válvula cardíaca de disco bivalva o válvula St. Jude. La mecánica implica dos discos semicirculares que se mueven hacia adelante y hacia atrás, y ambos permiten el flujo de sangre y la capacidad de formar un sello contra el reflujo. La válvula está recubierta con carbón pirolítico y fijada al tejido circundante con una malla de tela tejida llamada Dacron (el nombre comercial de Du Pont para el tereftalato de polietileno ). La malla permite que el tejido del cuerpo crezca, al mismo tiempo que incorpora la válvula. [23] [ verificación necesaria ]
La mayoría de las veces, el tejido artificial se cultiva a partir de las propias células del paciente. Sin embargo, cuando el daño es tan extremo que es imposible utilizar las células del propio paciente, se cultivan células de tejido artificial. La dificultad está en encontrar un andamiaje sobre el que las células puedan crecer y organizarse. Las características del andamio deben ser que sea biocompatible, que las células puedan adherirse al andamio, mecánicamente fuerte y biodegradable . Un andamio exitoso es un copolímero de ácido láctico y ácido glicólico . [23]
Como se analizó anteriormente, los biomateriales se utilizan en dispositivos médicos para tratar, ayudar o reemplazar una función dentro del cuerpo humano. La aplicación de un biomaterial específico debe combinar la composición, las propiedades del material, la estructura y la reacción in vivo deseada para realizar la función deseada. Se definen categorizaciones de diferentes propiedades deseadas para maximizar los resultados funcionales. [24] [25]
La respuesta del huésped se define como la "respuesta del organismo huésped (local y sistémica) al material o dispositivo implantado". La mayoría de los materiales tendrán una reacción cuando entren en contacto con el cuerpo humano. El éxito de un biomaterial depende de la reacción del tejido huésped con el material extraño. Se pueden generar reacciones específicas entre el tejido huésped y el biomaterial mediante la biocompatibilidad del material. [25] [26]
La funcionalidad in vivo y la longevidad de cualquier dispositivo médico implantable se ven afectadas por la respuesta del cuerpo al material extraño. [27] El cuerpo sufre una cascada de procesos definidos bajo la respuesta al cuerpo extraño (FBR) para proteger al huésped del material extraño. Se deben comprender las interacciones entre el dispositivo sobre el tejido/sangre huésped así como entre el tejido/sangre huésped sobre el dispositivo para evitar complicaciones y fallos del dispositivo.
La lesión tisular causada por la implantación del dispositivo provoca respuestas inflamatorias y curativas durante la RBA. La respuesta inflamatoria se produce en dos periodos de tiempo: la fase aguda y la fase crónica. La fase aguda ocurre durante las primeras horas o días de la implantación y se identifica por una exudación de líquido y proteínas [28] junto con una reacción neutrofílica. [29] Durante la fase aguda, el cuerpo intenta limpiar y curar la herida suministrando exceso de sangre, proteínas y monocitos al sitio. [30] La inflamación continua conduce a la fase crónica, que puede clasificarse por la presencia de monocitos, macrófagos y linfocitos. [29] Además, se forman vasos sanguíneos y tejido conectivo para curar el área herida. [31]
La biocompatibilidad está relacionada con el comportamiento de los biomateriales en diversos entornos bajo diversas condiciones químicas y físicas. El término puede referirse a propiedades específicas de un material sin especificar dónde o cómo se utilizará el material. Por ejemplo, un material puede provocar poca o ninguna respuesta inmune en un organismo determinado, y puede o no integrarse con un tipo de célula o tejido en particular . Los biomateriales inmunoinformados que dirigen la respuesta inmune en lugar de intentar eludir el proceso son un enfoque prometedor. [32] La ambigüedad del término refleja el desarrollo continuo de conocimientos sobre "cómo interactúan los biomateriales con el cuerpo humano " y, eventualmente, "cómo esas interacciones determinan el éxito clínico de un dispositivo médico (como un marcapasos o un reemplazo de cadera )". Los dispositivos médicos y las prótesis modernos suelen estar fabricados con más de un material, por lo que puede que no siempre sea suficiente hablar de la biocompatibilidad de un material específico. [33] La implantación quirúrgica de un biomaterial en el cuerpo desencadena una reacción inflamatoria del organismo con la consiguiente curación del tejido dañado. Dependiendo de la composición del material implantado, la superficie del implante, el mecanismo de fatiga y la descomposición química, existen otras reacciones posibles. Estos pueden ser tanto locales como sistémicos. Estos incluyen la respuesta inmune, la reacción a un cuerpo extraño al aislar el implante del tejido conectivo vascular, una posible infección y el impacto en la vida útil del implante. La enfermedad de injerto contra huésped es un trastorno autoinmune y aloinmune que presenta un curso clínico variable. Puede manifestarse de forma aguda o crónica, afectando a múltiples órganos y tejidos y provocando graves complicaciones en la práctica clínica, tanto durante el trasplante como durante la implantación de materiales biocompatibles. [34]
Un biomaterial debe realizar la función prevista dentro del cuerpo vivo sin afectar negativamente a otros tejidos y órganos corporales. Para evitar interacciones no deseadas entre órganos y tejidos, los biomateriales no deben ser tóxicos . La toxicidad de un biomaterial se refiere a las sustancias que el biomaterial emite mientras está in vivo . Un biomaterial no debería emitir nada a su entorno a menos que así lo pretenda. No toxicidad significa que el biomaterial es: no cancerígeno, no pirogénico , no alergénico , compatible con la sangre y no inflamatorio . [35] Sin embargo, un biomaterial puede diseñarse para incluir toxicidad para un propósito previsto. Por ejemplo, la aplicación de biomateriales tóxicos se estudia durante las pruebas de inmunoterapia contra el cáncer in vivo e in vitro . Los biomateriales tóxicos ofrecen la oportunidad de manipular y controlar las células cancerosas. [36] Un estudio reciente afirma: "Los nanobiomateriales avanzados, incluidos liposomas , polímeros y sílice , desempeñan un papel vital en la administración conjunta de fármacos e inmunomoduladores . Estos sistemas de administración basados en nanobiomateriales podrían promover eficazmente respuestas inmunes antitumorales y reducir simultáneamente los efectos adversos tóxicos. ". [37] Este es un excelente ejemplo de cómo la biocompatibilidad de un biomaterial se puede alterar para producir cualquier función deseada.
Los biomateriales biodegradables se refieren a materiales que son degradables mediante reacciones enzimáticas naturales . La aplicación de polímeros sintéticos biodegradables comenzó a finales de los años 1960. [38] Los materiales biodegradables tienen una ventaja sobre otros materiales, ya que tienen un menor riesgo de efectos nocivos a largo plazo. Además de los avances éticos que utilizan materiales biodegradables, también mejoran la biocompatibilidad de los materiales utilizados para la implantación. [38] Varias propiedades, incluida la biocompatibilidad, son importantes al considerar diferentes biomateriales biodegradables. Los biomateriales biodegradables pueden ser sintéticos o naturales según su fuente y tipo de matriz extracelular (MEC). [39]
Algunos de los materiales biocompatibles (o biomateriales) más utilizados son polímeros debido a su flexibilidad inherente y propiedades mecánicas ajustables . Los dispositivos médicos hechos de plástico a menudo están hechos de unos pocos selectos que incluyen: copolímero de olefina cíclica (COC), policarbonato (PC), polieterimida (PEI), policloruro de vinilo (PVC) de grado médico , polietersulfona (PES), polietileno (PE), polieteretercetona ( PEEK) e incluso polipropileno (PP). Para garantizar la biocompatibilidad , existen una serie de pruebas reguladas que el material debe superar para estar certificado para su uso. Estos incluyen la prueba de reactividad biológica de la Farmacopea de los Estados Unidos IV (USP Clase IV) y la evaluación biológica de dispositivos médicos 10993 (ISO 10993) de la Organización Internacional de Estándares. El principal objetivo de las pruebas de biocompatibilidad es cuantificar la toxicidad aguda y crónica del material y determinar cualquier posible efecto adverso durante las condiciones de uso, por lo que las pruebas requeridas para un material determinado dependen de su uso final (es decir, sangre, sistema nervioso central, etc.). .). [40]
Dos propiedades que tienen un gran efecto en la funcionalidad de un biomaterial son las propiedades de superficie y de volumen . [41]
Las propiedades a granel se refieren a las propiedades físicas y químicas que componen el biomaterial durante toda su vida. Se pueden generar específicamente para imitar las propiedades fisicoquímicas del tejido que reemplaza el material. Son propiedades mecánicas que se generan a partir de la construcción atómica y molecular de un material.
Propiedades importantes a granel: [42]
Las propiedades de la superficie se refieren a las características químicas y topográficas de la superficie del biomaterial que tendrán interacción directa con la sangre/tejido del huésped. [43] La ingeniería y modificación de superficies permite a los médicos controlar mejor las interacciones de un biomaterial con el sistema vivo huésped.
Propiedades superficiales importantes: [44]
Además de que un material esté certificado como biocompatible , los biomateriales deben diseñarse específicamente para su aplicación objetivo dentro de un dispositivo médico . Esto es especialmente importante en términos de propiedades mecánicas que gobiernan la forma en que se comporta un biomaterial determinado. Uno de los parámetros de los materiales más relevantes es el módulo de Young, E , que describe la respuesta elástica de un material a las tensiones . Los módulos de Young del tejido y el dispositivo que se le acopla deben coincidir estrechamente para lograr una compatibilidad óptima entre el dispositivo y el cuerpo, ya sea que el dispositivo esté implantado o montado externamente. Hacer coincidir el módulo elástico permite limitar el movimiento y la delaminación en la biointerfaz entre el implante y el tejido, además de evitar la concentración de tensiones que pueden provocar fallos mecánicos . Otras propiedades importantes son las resistencias a la tracción y a la compresión que cuantifican las tensiones máximas que un material puede soportar antes de romperse y pueden usarse para establecer límites de tensión a los que puede estar sujeto un dispositivo dentro o fuera del cuerpo. Dependiendo de la aplicación, puede ser deseable que un biomaterial tenga una alta resistencia para que sea resistente a fallas cuando se somete a una carga; sin embargo, en otras aplicaciones puede ser beneficioso que el material tenga una resistencia baja. Existe un cuidadoso equilibrio entre resistencia y rigidez que determina qué tan resistente al fallo es el dispositivo de biomaterial. Normalmente, a medida que aumenta la elasticidad del biomaterial, la resistencia última a la tracción disminuirá y viceversa. Una aplicación en la que no se desea un material de alta resistencia es en sondas neuronales ; Si se utiliza un material de alta resistencia en estas aplicaciones, el tejido siempre fallará antes que el dispositivo (bajo carga aplicada ) porque el módulo de Young de la duramadre y el tejido cerebral es del orden de 500 Pa . Cuando esto sucede, puede ocurrir daño irreversible al cerebro, por lo que el biomaterial debe tener un módulo elástico menor o igual al tejido cerebral y una baja resistencia a la tracción si se espera una carga aplicada. [46] [47]
Para los biomateriales implantados que pueden experimentar fluctuaciones de temperatura , por ejemplo, implantes dentales , la ductilidad es importante. El material debe ser dúctil por una razón similar: la resistencia a la tracción no puede ser demasiado alta, la ductilidad permite que el material se doble sin fracturarse y también evita la concentración de tensiones en el tejido cuando cambia la temperatura. La propiedad del material de dureza también es importante para los implantes dentales, así como para cualquier otro implante rígido que soporte carga, como una articulación de cadera de reemplazo . La dureza describe la capacidad del material para deformarse bajo tensión aplicada sin fracturarse y tener una alta dureza permite que los implantes de biomaterial duren más dentro del cuerpo, especialmente cuando se someten a grandes tensiones o tensiones cargadas cíclicamente , como las tensiones aplicadas a la articulación de la cadera durante la carrera. [46]
Para los dispositivos médicos que se implantan o se fijan a la piel, otra propiedad importante que requiere consideración es la rigidez a la flexión, D. La rigidez a la flexión determinará qué tan bien la superficie del dispositivo puede mantener un contacto conformado con la superficie del tejido , lo cual es especialmente importante para los dispositivos que miden el movimiento del tejido ( tensión ), señales eléctricas ( impedancia ) o que están diseñados para adherirse a la piel sin deslaminarse . como en la electrónica epidérmica. Dado que la rigidez a la flexión depende del espesor del material, h , a la tercera potencia ( h 3 ), es muy importante que un biomaterial pueda formarse en capas delgadas en las aplicaciones mencionadas anteriormente donde la conformidad es primordial. [48]
La composición molecular de un biomaterial determina las propiedades físicas y químicas de un biomaterial. Estas composiciones crean estructuras complejas que permiten que el biomaterial funcione y, por lo tanto, es necesario definirlas y comprenderlas para desarrollar un biomaterial. Los biomateriales se pueden diseñar para replicar organismos naturales, un proceso conocido como biomimética . [49] La estructura de un biomaterial se puede observar en diferentes niveles para comprender mejor las propiedades y funciones de un material.

La disposición de los átomos e iones dentro de un material es una de las propiedades estructurales más importantes de un biomaterial. La estructura atómica de un material se puede ver en diferentes niveles, el nivel subatómico , el nivel atómico o molecular , así como la ultraestructura creada por los átomos y moléculas. Las fuerzas intermoleculares entre los átomos y moléculas que componen el material determinarán sus propiedades materiales y químicas. [50]
El nivel subatómico observa la estructura eléctrica de un átomo individual para definir sus interacciones con otros átomos y moléculas. La estructura molecular observa la disposición de los átomos dentro del material. Finalmente, la ultraestructura observa la estructura tridimensional creada a partir de las estructuras atómicas y moleculares del material. El estado sólido de un material se caracteriza por los enlaces intramoleculares entre los átomos y moléculas que componen el material. Los tipos de enlaces intramoleculares incluyen: enlaces iónicos , enlaces covalentes y enlaces metálicos . Estos enlaces dictarán las propiedades físicas y químicas del material, así como también determinarán el tipo de material ( cerámico , metal o polímero ).
La microestructura de un material se refiere a la estructura de un objeto, organismo o material visto con aumentos superiores a 25 veces. [51] Se compone de diferentes fases de forma, tamaño y distribución de granos, poros, precipitados, etc. La mayoría de las microestructuras sólidas son cristalinas , sin embargo, algunos materiales, como ciertos polímeros, no cristalizarán cuando estén en estado sólido. [52]
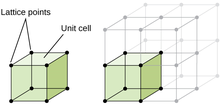
La estructura cristalina es la composición de iones, átomos y moléculas que se mantienen unidos y ordenados en una forma tridimensional. La principal diferencia entre una estructura cristalina y una estructura amorfa es el orden de los componentes. Cristalino tiene el nivel más alto de orden posible en el material donde la estructura amorfa consiste en irregularidades en el patrón de ordenamiento. [53] Una forma de describir estructuras cristalinas es a través de la red cristalina , que es una representación tridimensional de la ubicación de un factor repetitivo ( celda unitaria ) en la estructura denotada con redes . [54] Hay 14 configuraciones diferentes de disposición de átomos en una estructura cristalina, y todas están representadas bajo redes de Bravais . [ cita necesaria ]
Durante la formación de una estructura cristalina se pueden formar diferentes impurezas, irregularidades y otros defectos. Estas imperfecciones pueden formarse por deformación del sólido, enfriamiento rápido o radiación de alta energía. [55] Los tipos de defectos incluyen defectos puntuales, defectos lineales y dislocaciones de bordes.
La macroestructura se refiere a las propiedades geométricas generales que influirán en la fuerza de falla, la rigidez, la flexión, la distribución de tensiones y el peso del material. Se requiere poco o ningún aumento para revelar la macroestructura de un material. La observación de la macroestructura revela propiedades como cavidades, porosidad , burbujas de gas, estratificación y fisuras . [56] La resistencia y el módulo elástico del material son independientes de la macroestructura.
Los biomateriales se pueden construir utilizando únicamente materiales procedentes de plantas y animales para alterar, reemplazar o reparar tejidos/órganos humanos. El uso de biomateriales naturales se utilizó ya en el antiguo Egipto, donde los indígenas utilizaban piel de animal como sutura. Un ejemplo más moderno es un reemplazo de cadera con material de marfil que se registró por primera vez en Alemania en 1891. [57]
Criterios valiosos para biomateriales naturales viables:
Ejemplos de biomateriales naturales:
Los biopolímeros son polímeros producidos por organismos vivos. La celulosa y el almidón , las proteínas y los péptidos , el ADN y el ARN son todos ejemplos de biopolímeros, en los que las unidades monoméricas , respectivamente, son azúcares , aminoácidos y nucleótidos . [60] La celulosa es a la vez el biopolímero más común y el compuesto orgánico más común en la Tierra. Aproximadamente el 33% de toda la materia vegetal es celulosa. [61] [62] De manera similar, la seda (biopolímero proteico) ha despertado un tremendo interés de investigación en una multitud de dominios que incluyen ingeniería de tejidos y medicina regenerativa, microfluidos y administración de fármacos. [63] [64]
{{cite book}}: Mantenimiento CS1: falta el editor de la ubicación ( enlace )