El niobio es un elemento químico ; tiene símbolo Nb (antes columbio , Cb ) y número atómico 41. Es un metal de transición de color gris claro, cristalino y dúctil . El niobio puro tiene una dureza de Mohs similar al titanio puro , [4] y tiene una ductilidad similar a la del hierro . El niobio se oxida en la atmósfera terrestre muy lentamente, de ahí su aplicación en joyería como alternativa hipoalergénica al níquel . El niobio se encuentra a menudo en los minerales pirocloro y columbita , de ahí el nombre anterior "columbio". Su nombre proviene de la mitología griega : Niobe , hija de Tántalo , homónimo del tantalio . El nombre refleja la gran similitud entre ambos elementos en sus propiedades físicas y químicas, lo que dificulta su distinción. [5]
El químico inglés Charles Hatchett informó sobre un nuevo elemento similar al tantalio en 1801 y lo llamó columbio. En 1809, el químico inglés William Hyde Wollaston concluyó erróneamente que el tantalio y el columbium eran idénticos. El químico alemán Heinrich Rose determinó en 1846 que los minerales de tantalio contienen un segundo elemento, al que llamó niobio. En 1864 y 1865, una serie de hallazgos científicos aclararon que el niobio y el columbio eran el mismo elemento (a diferencia del tantalio), y durante un siglo ambos nombres se usaron indistintamente. El niobio se adoptó oficialmente como nombre del elemento en 1949, pero el nombre columbio sigue utilizándose actualmente en la metalurgia de los Estados Unidos.
No fue hasta principios del siglo XX que el niobio se utilizó comercialmente por primera vez. El niobio es una adición importante a los aceros de baja aleación de alta resistencia. Brasil es el principal productor de niobio y ferroniobio , una aleación de 60 a 70% de niobio con hierro. El niobio se utiliza principalmente en aleaciones, la mayor parte en aceros especiales como el utilizado en gasoductos . Aunque estas aleaciones contienen un máximo de 0,1%, el pequeño porcentaje de niobio mejora la resistencia del acero al eliminar el carburo y el nitruro . La estabilidad de la temperatura de las superaleaciones que contienen niobio es importante para su uso en motores a reacción y cohetes .
El niobio se utiliza en varios materiales superconductores . Estas aleaciones , que también contienen titanio y estaño , se utilizan ampliamente en los imanes superconductores de los escáneres de resonancia magnética . Otras aplicaciones del niobio incluyen soldadura, industrias nucleares, electrónica, óptica, numismática y joyería. En las dos últimas aplicaciones, la baja toxicidad y la iridiscencia producida por la anodización son propiedades muy deseadas. El niobio se considera un elemento tecnológico crítico .
.jpg/440px-Charles_Hatchett._Soft-ground_etching_by_F._C._Lewis_after_T_Wellcome_V0002614_(cropped).jpg)
_-_n._2990_-_Niobe_madre_-_Firenze.jpg/440px-Sommer,_Giorgio_(1834-1914)_-_n._2990_-_Niobe_madre_-_Firenze.jpg)
El niobio fue identificado por el químico inglés Charles Hatchett en 1801. [6] [7] [8] Encontró un nuevo elemento en una muestra de mineral que había sido enviada a Inglaterra desde Connecticut , Estados Unidos, en 1734 por John Winthrop FRS (nieto de John Winthrop el Joven ) y nombró al mineral columbita y al nuevo elemento columbium en honor a Columbia , el nombre poético de los Estados Unidos. [9] [10] [11] El columbio descubierto por Hatchett era probablemente una mezcla del nuevo elemento con tantalio. [9]
Posteriormente, hubo una considerable confusión [12] sobre la diferencia entre el columbio (niobio) y el tantalio, estrechamente relacionado. En 1809, el químico inglés William Hyde Wollaston comparó los óxidos derivados del columbio (columbita, con una densidad de 5,918 g/cm 3 ) , y del tantalio ( tantalita) , con una densidad superior a 8 g/cm 3 , y concluyó que los dos óxidos, a pesar de la diferencia significativa en densidad, fueron idénticas; por eso mantuvo el nombre de tantalio. [12] Esta conclusión fue cuestionada en 1846 por el químico alemán Heinrich Rose , quien argumentó que había dos elementos diferentes en la muestra de tantalita, y los nombró en honor a los hijos de Tantalus : niobio (de Niobe ) y pelopio (de Pélope ). [13] [14] Esta confusión surgió de las diferencias mínimas observadas entre tantalio y niobio. Los nuevos elementos reivindicados pelopio , ilmenio y dianio [15] eran en realidad idénticos al niobio o a mezclas de niobio y tantalio. [dieciséis]
Las diferencias entre tantalio y niobio fueron demostradas inequívocamente en 1864 por Christian Wilhelm Blomstrand [16] y Henri Étienne Sainte-Claire Deville , así como por Louis J. Troost , quien determinó las fórmulas de algunos de los compuestos en 1865 [16] [17 ] y finalmente por el químico suizo Jean Charles Galissard de Marignac [18] en 1866, quienes demostraron que sólo existían dos elementos. Los artículos sobre el ilmenio siguieron apareciendo hasta 1871. [19]
De Marignac fue el primero en preparar el metal en 1864, cuando redujo el cloruro de niobio calentándolo en una atmósfera de hidrógeno . [20] Aunque de Marignac pudo producir niobio sin tantalio a mayor escala en 1866, no fue hasta principios del siglo XX que el niobio se utilizó en filamentos de lámparas incandescentes , la primera aplicación comercial. [17] Este uso rápidamente quedó obsoleto debido a la sustitución del niobio por tungsteno , que tiene un punto de fusión más alto. El hecho de que el niobio mejora la resistencia del acero se descubrió por primera vez en la década de 1920, y esta aplicación sigue siendo su uso predominante. [17] En 1961, el físico estadounidense Eugene Kunzler y sus compañeros de trabajo en Bell Labs descubrieron que el niobio-estaño continúa exhibiendo superconductividad en presencia de fuertes corrientes eléctricas y campos magnéticos, [21] convirtiéndolo en el primer material que soporta altas corrientes y campos necesarios para imanes útiles de alta potencia y maquinaria de energía eléctrica . Este descubrimiento permitió, dos décadas después, la producción de cables largos de varios hilos enrollados en bobinas para crear electroimanes grandes y potentes para maquinaria giratoria, aceleradores de partículas y detectores de partículas. [22] [23]
Columbium (símbolo Cb) [24] fue el nombre dado originalmente por Hatchett tras su descubrimiento del metal en 1801. [7] El nombre reflejaba que el espécimen tipo del mineral procedía de los Estados Unidos de América ( Columbia ). [25] Este nombre siguió utilizándose en las revistas estadounidenses (el último artículo publicado por la American Chemical Society con columbium en su título data de 1953 [26] ), mientras que el niobio se utilizó en Europa. Para poner fin a esta confusión, se eligió el nombre niobio para el elemento 41 en la 15ª Conferencia de la Unión de Química en Ámsterdam en 1949. [27] Un año más tarde, este nombre fue adoptado oficialmente por la Unión Internacional de Química Pura y Aplicada (IUPAC). después de 100 años de controversia, a pesar de la precedencia cronológica del nombre columbium . [27] Esto fue una especie de compromiso; [27] la IUPAC aceptó tungsteno en lugar de wolframio en deferencia al uso norteamericano; y niobio en lugar de columbium en deferencia al uso europeo. Si bien muchas sociedades químicas y organizaciones gubernamentales de EE. UU. suelen utilizar el nombre oficial IUPAC, algunos metalúrgicos y sociedades del metal todavía utilizan el nombre estadounidense original, " columbio " . [28] [29] [30] [31]
El niobio es un metal paramagnético , dúctil, gris, brillante , del grupo 5 de la tabla periódica (ver tabla), con una configuración electrónica en las capas más externas atípica del grupo 5. Configuraciones atípicas similares ocurren en las proximidades del rutenio (44), el rodio (45) y paladio (46).
Aunque se cree que tiene una estructura cristalina cúbica centrada en el cuerpo desde el cero absoluto hasta su punto de fusión, las mediciones de alta resolución de la expansión térmica a lo largo de los tres ejes cristalográficos revelan anisotropías que son inconsistentes con una estructura cúbica. [32] Por lo tanto, se esperan más investigaciones y descubrimientos en esta área.
El niobio se convierte en un superconductor a temperaturas criogénicas . A presión atmosférica, tiene la temperatura crítica más alta de los superconductores elementales con 9,2 K. [33] El niobio tiene la mayor profundidad de penetración magnética de cualquier elemento. [33] Además, es uno de los tres superconductores elementales de Tipo II , junto con el vanadio y el tecnecio . Las propiedades superconductoras dependen en gran medida de la pureza del niobio metálico. [34]
Cuando es muy puro, es comparativamente blando y dúctil, pero las impurezas lo hacen más duro. [35]
El metal tiene una sección transversal de captura baja para neutrones térmicos ; [36] por lo tanto, se utiliza en las industrias nucleares donde se desean estructuras transparentes a los neutrones. [37]
El metal adquiere un tinte azulado cuando se expone al aire a temperatura ambiente durante períodos prolongados. [38] A pesar de un alto punto de fusión en forma elemental (2468 °C), es menos denso que otros metales refractarios . Además, es resistente a la corrosión, presenta propiedades de superconductividad y forma capas de óxido dieléctrico .
El niobio es ligeramente menos electropositivo y más compacto que su predecesor en la tabla periódica, el circonio , mientras que es prácticamente idéntico en tamaño a los átomos de tantalio más pesados, como resultado de la contracción de los lantánidos . [35] Como resultado, las propiedades químicas del niobio son muy similares a las del tantalio, que aparece directamente debajo del niobio en la tabla periódica . [17] Aunque su resistencia a la corrosión no es tan sobresaliente como la del tantalio, el precio más bajo y la mayor disponibilidad hacen que el niobio sea atractivo para aplicaciones menos exigentes, como revestimientos de cubas en plantas químicas. [35]
El niobio en la corteza terrestre comprende un isótopo estable , 93 Nb. [39] En 2003, se habían sintetizado al menos 32 radioisótopos , con masas atómicas comprendidas entre 81 y 113. El más estable es el 92 Nb con una vida media de 34,7 millones de años. Uno de los menos estables es el 113 Nb; Vida media estimada de 30 milisegundos. Los isótopos más ligeros que el 93 Nb estable tienden a desintegrarse β + , y los que son más pesados tienden a desintegrarse β − , con algunas excepciones. 81 Nb, 82 Nb y 84 Nb tienen rutas de desintegración de emisión de protones retardadas β + menores , 91 Nb desintegra por captura de electrones y emisión de positrones , y 92 Nb desintegra por desintegración β + y β − . [39]
Se han descrito al menos 25 isómeros nucleares , con masas atómicas comprendidas entre 84 y 104. Dentro de este rango, sólo 96 Nb, 101 Nb y 103 Nb no tienen isómeros. El más estable de los isómeros del niobio es el 93m Nb con una vida media de 16,13 años. El isómero menos estable es el 84m Nb con una vida media de 103 ns. Todos los isómeros del niobio se desintegran por transición isomérica o desintegración beta, excepto 92m1 Nb, que tiene una rama de captura de electrones menor. [39]
Se estima que el niobio es el elemento número 34 más común en la corteza terrestre , con 20 ppm . [40] Algunos creen que la abundancia en la Tierra es mucho mayor y que la alta densidad del elemento lo ha concentrado en el núcleo de la Tierra. [29] El elemento libre no se encuentra en la naturaleza, pero el niobio se encuentra en combinación con otros elementos en los minerales. [35] Los minerales que contienen niobio a menudo también contienen tantalio. Los ejemplos incluyen columbita ( (Fe,Mn)Nb 2 O 6 ) y columbita-tantalita (o coltán , (Fe,Mn)(Ta,Nb) 2 O 6 ). [41] Minerales de columbita-tantalita (las especies más comunes son columbita-(Fe) y tantalita-(Fe), donde "-(Fe)" es el sufijo de Levinson que indica la prevalencia del hierro sobre otros elementos como el manganeso [42] [43] [44] [45] ) que generalmente se encuentran como minerales accesorios en intrusiones de pegmatita y en rocas intrusivas alcalinas . Menos comunes son los niobatos de calcio , uranio , torio y las tierras raras . Ejemplos de tales niobatos son pirocloro ( (Na,Ca) 2 Nb 2 O 6 (OH,F) ) (ahora un nombre de grupo, siendo un ejemplo relativamente común, por ejemplo, fluorcalciopirocloro [44] [45] [46] [47 ] [48] ) y euxenita (correctamente denominada euxenita-(Y) [44] [45] [49] ) ( (Y,Ca,Ce,U,Th)(Nb,Ta,Ti) 2 O 6 ). Estos grandes depósitos de niobio se han encontrado asociados a carbonatitas ( rocas ígneas carbonato - silicato ) y como constituyente del pirocloro. [50]
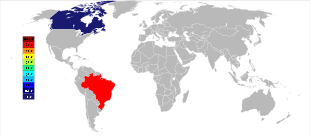
Los tres mayores depósitos de pirocloro actualmente explotados, dos en Brasil y uno en Canadá, se descubrieron en la década de 1950 y siguen siendo los principales productores de concentrados minerales de niobio. [17] El depósito más grande se encuentra dentro de una intrusión de carbonatita en Araxá , estado de Minas Gerais , Brasil, propiedad de CBMM ( Companhia Brasileira de Metalurgia e Mineração ); El otro depósito brasileño activo está ubicado cerca de Catalão , estado de Goiás , y es propiedad de China Molybdenum , también alojado dentro de una intrusión de carbonatita. [51] Juntas, esas dos minas producen alrededor del 88% del suministro mundial. [52] Brasil también tiene un depósito grande pero aún sin explotar cerca de São Gabriel da Cachoeira , estado de Amazonas , así como algunos depósitos más pequeños, notablemente en el estado de Roraima . [52] [53]
El tercer mayor productor de niobio es la mina Niobec , albergada en carbonatita , en Saint-Honoré , cerca de Chicoutimi , Quebec , Canadá, propiedad de Magris Resources. [54] Produce entre el 7% y el 10% del suministro mundial. [51] [52]
Después de la separación de los demás minerales, se obtienen los óxidos mixtos de tantalio Ta 2 O 5 y niobio Nb 2 O 5 . El primer paso en el procesamiento es la reacción de los óxidos con ácido fluorhídrico : [41]
La primera separación a escala industrial, desarrollada por el químico suizo de Marignac , aprovecha las diferentes solubilidades de los complejos fluoruros de niobio y tantalio , oxipentafluoroniobato monohidrato ( K 2 [NbOF 5 ]·H 2 O ) y heptafluorotantalato dipotásico ( K 2 [TaF 7 ] ) en agua. Los procesos más nuevos utilizan la extracción líquida de los fluoruros de una solución acuosa mediante disolventes orgánicos como la ciclohexanona . [41] Los fluoruros complejos de niobio y tantalio se extraen por separado del disolvente orgánico con agua y se precipitan mediante la adición de fluoruro de potasio para producir un complejo de fluoruro de potasio, o se precipitan con amoníaco como pentóxido: [55]
Seguido por:
Se utilizan varios métodos para la reducción a niobio metálico. La electrólisis de una mezcla fundida de K 2 [ NbOF 5 ] y cloruro de sodio es una; la otra es la reducción del fluoruro con sodio . Con este método se puede obtener niobio de pureza relativamente alta. En la producción a gran escala, el Nb 2 O 5 se reduce con hidrógeno o carbono. [55] En la reacción aluminotérmica , se hace reaccionar una mezcla de óxido de hierro y óxido de niobio con aluminio :
Se añaden pequeñas cantidades de oxidantes como nitrato de sodio para mejorar la reacción. El resultado es óxido de aluminio y ferroniobio , una aleación de hierro y niobio utilizada en la producción de acero. [56] [57] El ferroniobio contiene entre 60 y 70% de niobio. [51] Sin óxido de hierro, el proceso aluminotérmico se utiliza para producir niobio. Es necesaria una mayor purificación para alcanzar el grado de aleaciones superconductoras . La fusión por haz de electrones al vacío es el método utilizado por los dos principales distribuidores de niobio. [58] [59]
En 2013 [actualizar], CBMM de Brasil controlaba el 85 por ciento de la producción mundial de niobio. [60] El Servicio Geológico de Estados Unidos estima que la producción aumentó de 38.700 toneladas en 2005 a 44.500 toneladas en 2006. [61] [62] Los recursos mundiales se estiman en 4,4 millones de toneladas. [62] Durante el período de diez años comprendido entre 1995 y 2005, la producción se duplicó con creces, a partir de 17.800 toneladas en 1995. [63] Entre 2009 y 2011, la producción se mantuvo estable en 63.000 toneladas por año, [64] con una ligera disminuirá en 2012 a sólo 50.000 toneladas por año. [sesenta y cinco]
Se encuentran cantidades menores en el depósito Kanyika de Malawi ( mina Kanyika ).
En muchos aspectos, el niobio es similar al tantalio y al circonio . Reacciona con la mayoría de los no metales a altas temperaturas; con flúor a temperatura ambiente; con cloro a 150°C e hidrógeno a 200° C ; y con nitrógeno a 400 °C, con productos frecuentemente intersticiales y no estequiométricos. [35] El metal comienza a oxidarse en el aire a 200° C . [55] Resiste la corrosión por ácidos, incluidos el agua regia , el ácido clorhídrico , el sulfúrico , el nítrico y el fosfórico . [35] El niobio es atacado por ácido sulfúrico concentrado caliente, ácido fluorhídrico y mezclas de ácido fluorhídrico y nítrico. También es atacado por soluciones saturadas y calientes de hidróxido de metal alcalino.
Aunque el niobio exhibe todos los estados de oxidación formales de +5 a -1, los compuestos más comunes tienen niobio en el estado +5. [35] Característicamente, los compuestos en estados de oxidación inferiores a 5+ muestran enlaces Nb-Nb. En soluciones acuosas, el niobio sólo presenta el estado de oxidación +5. También es fácilmente propenso a la hidrólisis y es apenas soluble en soluciones diluidas de ácidos clorhídrico , sulfúrico , nítrico y fosfórico debido a la precipitación de óxido de Nb hidratado. [58] El Nb(V) también es ligeramente soluble en medios alcalinos debido a la formación de especies de polioxoniobato solubles. [69] [70]
El niobio forma óxidos en los estados de oxidación +5 ( Nb 2 O 5 ), [71] +4 ( NbO 2 ) y el estado de oxidación más raro, +2 ( NbO ). [72] El más común es el pentóxido, precursor de casi todos los compuestos y aleaciones de niobio. [55] [73] Los niobatos se generan disolviendo el pentóxido en soluciones de hidróxido básico o fundiéndolo en óxidos de metales alcalinos. Algunos ejemplos son el niobato de litio ( LiNbO 3 ) y el niobato de lantano ( LaNbO 4 ). En el niobato de litio hay una estructura similar a una perovskita distorsionada trigonalmente , mientras que el niobato de lantano contiene NbO solitario. 3-4
_iones. [55] También se conoce el sulfuro de niobio en capas ( NbS 2 ). [35]
Los materiales pueden recubrirse con una fina película de óxido de niobio (V) por deposición química de vapor o mediante procesos de deposición de capas atómicas , producidos por la descomposición térmica del etóxido de niobio (V) por encima de 350 °C. [74] [75]


El niobio forma haluros en los estados de oxidación +5 y +4 así como diversos compuestos subestequiométricos . [55] [58] Los pentahaluros ( NbX
5) presentan centros Nb octaédricos. El pentafluoruro de niobio ( NbF 5 ) es un sólido blanco con un punto de fusión de 79,0 °C y el pentacloruro de niobio ( NbCl 5 ) es amarillo (ver imagen a la derecha) con un punto de fusión de 203,4 °C. Ambos se hidrolizan para dar óxidos y oxihaluros, como NbOCl 3 . El pentacloruro es un reactivo versátil que se utiliza para generar compuestos organometálicos , como el dicloruro de nioboceno ( (C
5h
5)
2NbCl
2). [76] Los tetrahaluros ( NbX
4) son polímeros de color oscuro con enlaces Nb-Nb; por ejemplo, el tetrafluoruro de niobio higroscópico negro ( NbF 4 ) y el tetracloruro de niobio marrón ( NbCl 4 ).
Los compuestos de haluros aniónicos de niobio son bien conocidos, debido en parte a la acidez de Lewis de los pentahaluros. El más importante es [NbF 7 ] 2− , un intermedio en la separación de Nb y Ta de los minerales. [41] Este heptafluoruro tiende a formar oxopentafluoruro más fácilmente que el compuesto de tantalio. Otros complejos de haluro incluyen octaédrico [ NbCl 6 ] − :
Al igual que con otros metales con números atómicos bajos, se conoce una variedad de iones de grupo de haluros reducidos, siendo el mejor ejemplo [ Nb 6 Cl 18 ] 4- . [77]
Otros compuestos binarios de niobio incluyen el nitruro de niobio (NbN), que se convierte en superconductor a bajas temperaturas y se utiliza en detectores de luz infrarroja. [78] El principal carburo de niobio es el NbC, un material cerámico refractario extremadamente duro , utilizado comercialmente en brocas para herramientas de corte .

De las 44.500 toneladas de niobio extraídas en 2006, se estima que el 90% se utilizó en acero estructural de alta calidad. La segunda aplicación más importante son las superaleaciones . [79] Los superconductores y componentes electrónicos de aleación de niobio representan una proporción muy pequeña de la producción mundial. [79]
El niobio es un elemento de microaleación eficaz para el acero, dentro del cual se forma carburo de niobio y nitruro de niobio . [29] Estos compuestos mejoran el refinado del grano y retardan la recristalización y el endurecimiento por precipitación . Estos efectos a su vez aumentan la tenacidad , resistencia , conformabilidad y soldabilidad . [29] Dentro de los aceros inoxidables microaleados , el contenido de niobio es una pequeña (menos del 0,1%) [80] pero importante adición a los aceros de alta resistencia y baja aleación que se utilizan ampliamente estructuralmente en los automóviles modernos. [29] El niobio a veces se utiliza en cantidades considerablemente mayores para componentes de máquinas y cuchillas altamente resistentes al desgaste , hasta un 3% en el acero inoxidable Crucible CPM S110V. [81]
Estas mismas aleaciones de niobio se utilizan a menudo en la construcción de tuberías. [82] [83]

Se utilizan cantidades de niobio en superaleaciones a base de níquel, cobalto y hierro en proporciones de hasta el 6,5% [80] para aplicaciones tales como componentes de motores a reacción , turbinas de gas , subconjuntos de cohetes, sistemas de turbocompresores, resistencia al calor y combustión. equipo. El niobio precipita una fase γ'' de endurecimiento dentro de la estructura de grano de la superaleación. [84]
Un ejemplo de superaleación es Inconel 718 , que consta de aproximadamente 50 % de níquel , 18,6 % de cromo , 18,5 % de hierro , 5 % de niobio, 3,1 % de molibdeno , 0,9 % de titanio y 0,4 % de aluminio . [85] [86]
Estas superaleaciones se utilizaron, por ejemplo, en sistemas avanzados de estructuras aéreas para el programa Gemini . Se utilizó otra aleación de niobio [ se necesita aclaración ] para la boquilla del módulo de servicio Apollo . Debido a que el niobio se oxida a temperaturas superiores a 400 °C, es necesaria una capa protectora para estas aplicaciones para evitar que la aleación se vuelva quebradiza . [87]
La aleación C-103 fue desarrollada a principios de la década de 1960 conjuntamente por Wah Chang Corporation y Boeing Co. DuPont , Union Carbide Corp., General Electric Co. y varias otras empresas estaban desarrollando aleaciones a base de Nb simultáneamente, en gran medida impulsadas por la Guerra Fría y Carrera en el espacio . Está compuesto por 89% de niobio, 10% de hafnio y 1% de titanio y se utiliza para las boquillas de los propulsores de cohetes líquidos , como el motor principal de los módulos lunares Apollo . [87]
La reactividad del niobio con el oxígeno obliga a trabajarlo al vacío o en atmósfera inerte , lo que aumenta notablemente el coste y la dificultad de producción. La refundición por arco al vacío (VAR) y la fusión por haz de electrones (EBM), procesos novedosos en ese momento, permitieron el desarrollo del niobio y otros metales reactivos. El proyecto que dio como resultado el C-103 comenzó en 1959 con hasta 256 aleaciones experimentales de niobio de la "serie C" ( C que surge posiblemente del columbio ) que podían fundirse como botones y enrollarse en láminas . Wah Chang Corporation tenía un inventario de hafnio , refinado a partir de aleaciones de circonio de grado nuclear , que quería darle uso comercial. La composición experimental número 103 de las aleaciones de la serie C, Nb-10Hf-1Ti, tuvo la mejor combinación de conformabilidad y propiedades de alta temperatura. Wah Chang fabricó el primer calor de 500 libras de C-103 en 1961, de lingote a hoja, utilizando EBM y VAR. Las aplicaciones previstas incluían motores de turbina e intercambiadores de calor de metales líquidos . Las aleaciones de niobio competidoras de esa época incluían FS85 (Nb-10W-28Ta-1Zr) de Fansteel Metallurgical Corp. , Cb129Y (Nb-10W-10Hf-0.2Y) de Wah Chang y Boeing, Cb752 (Nb-10W-2.5Zr) de Union Carbide y Nb1Zr de Superior Tube Co. [87]

La boquilla de la serie de motores Merlin Vacuum desarrollada por SpaceX para la etapa superior de su cohete Falcon 9 está hecha de una aleación de niobio [ se necesita aclaración ] . [88]

Niobio-germanio ( Nb
3Ge ), niobio-estaño ( Nb
3Sn ), así como las aleaciones de niobio y titanio , se utilizan como alambre superconductor de tipo II para imanes superconductores . [89] [90] Estos imanes superconductores se utilizan en instrumentos de resonancia magnética nuclear y de imágenes por resonancia magnética , así como en aceleradores de partículas . [91] Por ejemplo, el Gran Colisionador de Hadrones utiliza 600 toneladas de hebras superconductoras, mientras que el Reactor Experimental Termonuclear Internacional utiliza unas 600 toneladas de hebras de Nb 3 Sn y 250 toneladas de hebras de NbTi. [92] Sólo en 1992, se construyeron sistemas clínicos de imágenes por resonancia magnética por valor de más de mil millones de dólares con alambre de niobio-titanio. [22]

Las cavidades de radiofrecuencia superconductora (SRF) utilizadas en los láseres de electrones libres FLASH (resultado del proyecto cancelado del acelerador lineal TESLA) y XFEL están hechas de niobio puro. [93] Un equipo de criomódulos en Fermilab utilizó la misma tecnología SRF del proyecto FLASH para desarrollar cavidades SRF de nueve celdas de 1,3 GHz hechas de niobio puro. Las cavidades se utilizarán en el acelerador lineal de partículas de 30 kilómetros (19 millas) del Colisionador Lineal Internacional . [94] La misma tecnología se utilizará en LCLS-II en el Laboratorio Nacional del Acelerador SLAC y en PIP-II en Fermilab. [95]
La alta sensibilidad de los bolómetros superconductores de nitruro de niobio los convierte en un detector ideal de radiación electromagnética en la banda de frecuencia THz. Estos detectores fueron probados en el Telescopio Submilimétrico , el Telescopio del Polo Sur , el Telescopio del Laboratorio Receptor y en APEX , y ahora se utilizan en el instrumento HIFI a bordo del Observatorio Espacial Herschel . [96]
El niobato de litio , que es un ferroeléctrico , se utiliza ampliamente en teléfonos móviles y moduladores ópticos , y para la fabricación de dispositivos de ondas acústicas de superficie . Pertenece a los ferroeléctricos de estructura ABO 3 como el tantalato de litio y el titanato de bario . [97] Los condensadores de niobio están disponibles como alternativa a los condensadores de tantalio , [98] pero los condensadores de tantalio aún predominan. El niobio se añade al vidrio para obtener un índice de refracción más alto, lo que hace posible vidrios correctores más delgados y livianos .
El niobio y algunas aleaciones de niobio son fisiológicamente inertes e hipoalergénicos . Por este motivo, el niobio se utiliza en prótesis y dispositivos de implante, como los marcapasos. [99] El niobio tratado con hidróxido de sodio forma una capa porosa que ayuda a la osteointegración . [100]
Al igual que el titanio, el tantalio y el aluminio, el niobio se puede calentar y anodizar (" anodización reactiva de metales ") para producir una amplia gama de colores iridiscentes para joyería, [101] [102] donde su propiedad hipoalergénica es muy deseable. [103]
El niobio se utiliza como metal precioso en monedas conmemorativas, a menudo con plata u oro. Por ejemplo, Austria produjo una serie de monedas de euro de niobio y plata a partir de 2003; El color de estas monedas se crea por la difracción de la luz mediante una fina capa de óxido anodizado. [104] En 2012, hay diez monedas disponibles que muestran una amplia variedad de colores en el centro de la moneda: azul, verde, marrón, morado, violeta o amarillo. Dos ejemplos más son la moneda conmemorativa del ferrocarril alpino de Semmering de 150 años de 25 € de Austria de 2004 , [105] y la moneda conmemorativa de la navegación por satélite europea de 25 € de Austria de 2006 . [106] La Casa de la Moneda de Austria produjo para Letonia una serie similar de monedas a partir de 2004, [107] seguida de una en 2007. [108] En 2011, la Real Casa de la Moneda de Canadá comenzó la producción de una moneda de plata esterlina y niobio de 5 dólares llamada Hunter's Moon. [109] en el que el niobio se oxidó selectivamente, creando así acabados únicos en los que no hay dos monedas exactamente iguales.
Las juntas del tubo de arco de las lámparas de vapor de sodio de alta presión están hechas de niobio, a veces aleado con un 1% de circonio ; El niobio tiene un coeficiente de expansión térmica muy similar, que coincide con la cerámica del tubo de arco de alúmina sinterizada , un material translúcido que resiste el ataque químico o la reducción del sodio líquido caliente y el vapor de sodio contenidos dentro de la lámpara de operación. [110] [111] [112]
El niobio se utiliza en varillas de soldadura por arco para algunos grados estabilizados de acero inoxidable [113] y en ánodos para sistemas de protección catódica en algunos tanques de agua, que luego generalmente se recubren con platino. [114] [115]
El niobio se utiliza para fabricar el cable de alto voltaje del módulo receptor de partículas de la corona solar de la sonda solar Parker . [116]
Se han realizado investigaciones para permitir el uso de catalizadores a base de niobio para reciclar tereftalato de polietileno (PET). [117] [118]
El niobio no tiene ningún papel biológico conocido. Si bien el polvo de niobio irrita los ojos y la piel y representa un riesgo potencial de incendio, el niobio elemental a mayor escala es fisiológicamente inerte (y por lo tanto hipoalergénico) e inofensivo. Se utiliza a menudo en joyería y se ha probado su uso en algunos implantes médicos. [119] [120]
Se ha probado en ratas la exposición a corto y largo plazo a niobatos y cloruro de niobio, dos sustancias químicas solubles en agua. Las ratas tratadas con una única inyección de pentacloruro de niobio o niobatos muestran una dosis letal media (LD50 ) de entre 10 y 100 mg/kg. [121] [122] [123] Para la administración oral, la toxicidad es menor; un estudio con ratas arrojó una DL50 después de siete días de 940 mg/kg. [121]
{{cite book}}: |journal=ignorado ( ayuda ){{cite book}}: |journal=ignorado ( ayuda ){{cite book}}: Mantenimiento CS1: falta el editor de la ubicación ( enlace ){{cite book}}: |journal=ignorado ( ayuda ){{cite book}}: |journal=ignorado ( ayuda )