En bioquímica , medicina y ciencias relacionadas, el término inositol se refiere generalmente al mioinositol ( anteriormente mesoinositol ), el estereoisómero más importante del compuesto químico ciclohexano-1,2,3,4,5,6-hexol . Su fórmula es C6H12O6 ; la molécula tiene un anillo de seis átomos de carbono , cada uno con un átomo de hidrógeno y un grupo hidroxilo (–OH). En el mioinositol , dos de los hidroxilos, ni adyacentes ni opuestos, se encuentran por encima de los respectivos hidrógenos en relación con el plano medio del anillo.
El compuesto es un carbohidrato , específicamente un alcohol de azúcar (a diferencia de las aldosas como la glucosa ) con la mitad de dulzura que la sacarosa (azúcar de mesa). Es uno de los componentes más antiguos de los seres vivos con múltiples funciones en eucariotas, incluidos lípidos estructurales y mensajeros secundarios . [3] Un riñón humano produce alrededor de dos gramos por día de glucosa , pero otros tejidos también la sintetizan. La concentración más alta está en el cerebro, donde juega un papel importante en la unión de otros neurotransmisores y algunas hormonas esteroides a sus receptores. [4] En otros tejidos, media la transducción de señales celulares en respuesta a una variedad de hormonas , neurotransmisores y factores de crecimiento y participa en la osmorregulación . [5] En la mayoría de las células de mamíferos, las concentraciones de mioinositol son de 5 a 500 veces mayores dentro de las células que fuera de ellas. [6]
Un metanálisis de 2023 concluyó que el inositol es un tratamiento seguro y eficaz para el tratamiento del síndrome de ovario poliquístico (SOP). [7] Sin embargo, solo hay evidencia de muy baja calidad sobre su eficacia para aumentar la fertilidad en mujeres con SOP mediante FIV. [8]
Los otros estereoisómeros naturales del ciclohexano-1,2,3,4,5,6-hexol son escilo , muco , D - quiro , L - quiro y neo -inositol , aunque se encuentran en cantidades mínimas en comparación con el mio -inositol. Los otros isómeros posibles son alo , epi y cis -inositol .
El mio -inositol fue aislado por primera vez de extractos musculares por Johanes Joseph Scherer (1814-1869) en 1850. [3] Anteriormente se lo llamaba meso -inositol para distinguirlo de los isómeros quiro- . Sin embargo, dado que todos los demás isómeros son compuestos meso (no quirales ), ahora se prefiere el nombre mio -inositol ( myo- es un prefijo médico para "músculo").
El inositol alguna vez fue considerado un miembro del complejo de vitamina B , es decir, la vitamina B8 antes de que se descubriera que se produce naturalmente en el cuerpo humano y, por lo tanto, no puede ser una vitamina o un nutriente esencial . [9]
El mio -inositol es un compuesto meso , lo que significa que es ópticamente inactivo porque tiene un plano de simetría . [10] Es un polvo cristalino blanco, relativamente estable en el aire. Es muy soluble en agua, ligeramente soluble en ácido acético glacial , etanol , glicol y glicerina , pero insoluble en cloroformo y éter . [3]
En su conformación más estable , el isómero myo -inositol asume la conformación de silla , que mueve el número máximo de hidroxilos a la posición ecuatorial, donde están más separados entre sí. En esta conformación, el isómero myo natural tiene una estructura en la que cinco de los seis hidroxilos (el primero, tercero, cuarto, quinto y sexto) son ecuatoriales , mientras que el segundo grupo hidroxilo es axial . [11]
El mio -inositol desempeña un papel importante como base estructural de varios mensajeros secundarios en las células eucariotas , los diversos fosfatos de inositol . Además, el inositol sirve como un componente importante de los lípidos estructurales fosfatidilinositol (PI) y sus diversos fosfatos, los lípidos fosfatidilinositol fosfato (PIP).
En los seres humanos, el mioinositol se sintetiza de novo, pero el D - quiroinositol no. [6] El mioinositol se sintetiza a partir de glucosa 6-fosfato (G6P) en dos pasos. Primero, la G6P es isomerizada por una enzima inositol-3-fosfato sintasa (por ejemplo, ISYNA1) a mioinositol 1-fosfato, que luego es desfosforilado por una enzima inositol monofosfatasa (por ejemplo, IMPA1 ) para dar mioinositol libre . En los seres humanos, la mayor parte del inositol se sintetiza en los riñones, seguido de los testículos, típicamente en cantidades de unos pocos gramos por día. [5]
A nivel periférico, el mio -inositol se convierte en D - quiro -inositol por una epimerasa específica. Sólo una fracción menor del mio -inositol se convierte en D - quiro- inositol . [6] La actividad de esta epimerasa es dependiente de la insulina, causando una reducción del D - quiro -inositol en músculo, grasa e hígado cuando hay resistencia a la insulina . [12] [6] El D - quiro -inositol reduce la conversión de testosterona a estrógeno, por lo que aumenta los niveles de testosterona y empeora el SOP. [6]
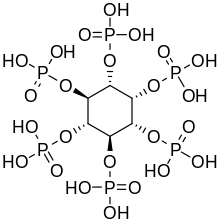
El hexafosfato de inositol, también llamado ácido fítico o IP6, es un fitoquímico y la principal forma de almacenamiento de fósforo en muchos tejidos vegetales , especialmente el salvado y las semillas . [13] El fósforo y el inositol en forma de fitato generalmente no son biodisponibles para los animales no rumiantes porque estos animales carecen de la enzima digestiva fitasa requerida para eliminar los grupos fosfato. Los rumiantes digieren fácilmente el fitato debido a la fitasa producida por microorganismos en el rumen . [14] Además, el ácido fítico también quela minerales importantes como calcio , magnesio , hierro y zinc , haciéndolos inabsorbibles y contribuyendo a las deficiencias minerales en personas cuyas dietas dependen en gran medida del salvado y las semillas para su ingesta mineral, como ocurre en los países en desarrollo . [15] [16]
El penta- (IP5), tetra- (IP4) y trifosfato (IP3) de inositol también se denominan "fitatos".
El inositol o sus fosfatos y lípidos asociados se encuentran en muchos alimentos, en particular frutas, especialmente melón y naranjas . [17] En las plantas, el hexafosfato de inositol, ácido fítico o sus sales, los fitatos, sirven como reservas de fosfato en las semillas, por ejemplo en nueces y frijoles. [18] El ácido fítico también se encuentra en cereales con alto contenido de salvado . Sin embargo, el fitato no está directamente biodisponible para los humanos en la dieta, ya que no es digerible. Algunas técnicas de preparación de alimentos descomponen parcialmente los fitatos para cambiar esto. Sin embargo, el inositol en forma de fosfolípidos , como se encuentra en ciertas sustancias derivadas de plantas como las lecitinas , se absorbe bien y es relativamente biodisponible.
El inositol, el fosfatidilinositol y algunos de sus monofosfatos y polifosfatos funcionan como mensajeros secundarios en diversas vías de transducción de señales intracelulares . Intervienen en diversos procesos biológicos, entre ellos:
En una importante familia de vías, el fosfatidilinositol 4,5-bisfosfato (PIP 2 ) se almacena en las membranas celulares hasta que es liberado por alguna de varias proteínas de señalización y se transforma en varios mensajeros secundarios, por ejemplo, diacilglicerol y trifosfato de inositol . [25]
' El mio -inositol tiene una toxicidad muy baja, con una DL50 informada de 10 000 mg/kg de peso corporal (oral) en ratas. [3]
En la reunión de la Sociedad Química Americana de 1936 , el profesor Edward Bartow de la Universidad de Iowa presentó un método comercialmente viable para extraer grandes cantidades de inositol del ácido fítico presente de forma natural en los desechos de maíz. Como posible uso para el producto químico, sugirió el "nitrato de inositol" como una alternativa más estable a la nitroglicerina . [26] Hoy en día, el nitrato de inositol se utiliza para gelatinizar la nitrocelulosa en muchos explosivos modernos y propulsores sólidos para cohetes. [27]
Cuando las plantas se exponen a concentraciones cada vez mayores de sal para carreteras , las células vegetales se vuelven disfuncionales y sufren apoptosis , lo que conduce a una inhibición del crecimiento. El pretratamiento con inositol podría reducir estos efectos. [28]
Se pueden utilizar dosis altas de inositol para tratar la tricotilomanía (arrancarse compulsivamente el cabello) y trastornos relacionados. [29]
El D- quiro -inositol es una molécula mensajera importante en la señalización de la insulina. [30] Se ha demostrado que la suplementación con inositol reduce significativamente los triglicéridos y el colesterol LDL en pacientes con enfermedades metabólicas . [30]
El mioinositol es importante para la síntesis de la hormona tiroidea . [31] La depleción de mioinositol puede predisponer al desarrollo de hipotiroidismo . [31] Los pacientes con hipotiroidismo tienen una mayor demanda de mioinositol que los sujetos sanos. [31]
El inositol no debe administrarse de forma rutinaria en el tratamiento de bebés prematuros que padecen o corren riesgo de padecer síndrome de dificultad respiratoria infantil (SDR). [32] El mioinositol ayuda a prevenir defectos del tubo neural con particular eficacia en combinación con ácido fólico . [33]
El inositol se considera un tratamiento seguro y eficaz para el síndrome de ovario poliquístico (SOP). [7] Funciona aumentando la sensibilidad a la insulina, lo que ayuda a mejorar la función ovárica y reducir el hiperandrogenismo . [34] También se ha demostrado que reduce el riesgo de enfermedad metabólica en mujeres con SOP. [35] Además, gracias a su papel como segundo mensajero de la FSH, el mioinositol es eficaz para restablecer la relación FSH/LH y la regularización del ciclo menstrual. [36] El papel del mioinositol como segundo mensajero de la FSH conduce a una correcta maduración del folículo ovárico y, en consecuencia, a una mayor calidad de los ovocitos. Al mejorar la calidad de los ovocitos tanto en mujeres con SOP como sin él, el mioinositol puede considerarse un posible enfoque para aumentar las posibilidades de éxito en las tecnologías de reproducción asistida. [37] [38] Por el contrario, el D - quiro -inositol puede perjudicar la calidad de los ovocitos de forma dependiente de la dosis. [39] El alto nivel de DCI parece estar relacionado con los niveles elevados de insulina recuperados en aproximadamente el 70% de las mujeres con SOP. [40] En este sentido, la insulina estimula la conversión irreversible de mioinositol a D - quiroinositol causando una reducción drástica de mioinositol . El agotamiento de mioinositol es particularmente dañino para los folículos ováricos porque está involucrado en la señalización de FSH, que se ve afectada debido al agotamiento de mioinositol . [12] La evidencia reciente informa una mejora más rápida de los parámetros metabólicos y hormonales cuando estos dos isómeros se administran en su proporción fisiológica. La proporción plasmática de mioinositol y D - quiroinositol en sujetos sanos es 40:1 de mioinositol y D - quiroinositol respectivamente. [41] El uso de la proporción 40:1 muestra la misma eficacia del mioinositol solo pero en un tiempo más corto. Además, la proporción fisiológica no afecta la calidad de los ovocitos. [42]
El uso de inositoles en el SOP está ganando cada vez más importancia, y se ha informado de una eficacia superior al 70% con un fuerte perfil de seguridad. Por otro lado, alrededor del 30% de los pacientes podrían mostrarse resistentes al inositol. [43] Nuevas evidencias sobre la etiopatogenia del SOP describen una alteración en las especies y la cantidad de cada cepa que caracteriza la flora gastrointestinal normal. Esta alteración podría conducir a una inflamación crónica de bajo nivel y malabsorción. [44] Una posible solución podría estar representada por la combinación de mioinositol y α-lactoalbúmina . Esta combinación muestra un efecto sinérgico en el aumento de la absorción de mioinositol. [45] Un estudio reciente informó que la combinación de mioinositol y α-lactoalbúmina aumenta el contenido plasmático de mioinositol en pacientes resistentes al inositol con una mejora relativa de los parámetros hormonales y metabólicos. [46]
El inositol se ha utilizado como adulterante o agente de corte para muchas drogas ilegales, como la cocaína , la metanfetamina y, a veces, la heroína , [47] probablemente debido a su solubilidad, textura en polvo o dulzura reducida (50%) en comparación con los azúcares más comunes.
El inositol también se utiliza como sustituto de la cocaína en el cine . [48] [49]
El mio -inositol está presente de forma natural en una variedad de alimentos, aunque las tablas de composición de alimentos no siempre distinguen entre lecitina , la forma lipídica relativamente biodisponible y la forma de fitato/fosfato bioindisponible. [17] Los alimentos que contienen las concentraciones más altas de mio -inositol y sus compuestos incluyen frutas, frijoles, granos y nueces. [17] Las frutas en particular, especialmente las naranjas y el melón, contienen las mayores cantidades de mio -inositol. [50] También está presente en frijoles, nueces y granos, sin embargo, estos contienen grandes cantidades de mio -inositol en forma de fitato, que no es biodisponible sin la transformación por las enzimas fitasas . Bacillus subtilis , el microorganismo que produce el alimento fermentado natto , produce enzimas fitasas que pueden convertir el ácido fítico en una forma más biodisponible de polifosfato de inositol en el intestino. [51] Además, las especies de Bacteroides en el intestino secretan vesículas que contienen una enzima activa que convierte la molécula de fitato en fósforo biodisponible y polifosfato de inositol, que es una molécula de señalización importante en el cuerpo humano. [52]
El mio -inositol también se puede encontrar como ingrediente en bebidas energéticas , [53] ya sea en combinación con la glucosa o como sustituto de esta. [54]
En los seres humanos, el mioinositol se produce naturalmente a partir de glucosa-6-fosfato mediante desfosforilación enzimática. [50]
A partir de 2021, el principal proceso industrial para la producción de mioinositol (principalmente en China y Japón) comenzó con el fitato (IP6) extraído del agua de remojo resultante del procesamiento del salvado de maíz y arroz. Después de la purificación, el fitato se hidroliza y el mioinositol se separa por cristalización. [3]
Otra ruta es la fermentación microbiana de carbohidratos por varios organismos, como el hongo Neurospora crassa (Beadle y Tatum, 1945), Candida boidini (Shirai et al., 1997), Saccharomyces cerevisiae (Culbertson et al., 1976), Escherichia coli (Hansen, 1999). [3] Alternativamente, los extractos enzimáticos de cultivos microbianos se pueden utilizar in vitro para obtener mioinositol a partir de varios sustratos, incluyendo glucosa, sacarosa , almidón , xilosa y amilosa . [3]
{{cite web}}: CS1 maint: URL no apta ( enlace ){{cite web}}: CS1 maint: URL no apta ( enlace )