Las pruebas prenatales son una herramienta que se puede utilizar para detectar algunos defectos de nacimiento en varias etapas antes del nacimiento. Las pruebas prenatales consisten en la detección prenatal y el diagnóstico prenatal , que son aspectos de la atención prenatal que se centran en detectar problemas con el embarazo lo antes posible. [1] Estos pueden ser problemas anatómicos y fisiológicos con la salud del cigoto , embrión o feto , ya sea antes de que comience la gestación (como en el diagnóstico genético preimplantacional ) o lo más temprano posible en la gestación. La detección puede detectar problemas como defectos del tubo neural , anomalías cromosómicas y mutaciones genéticas que darían lugar a trastornos genéticos y defectos de nacimiento , como espina bífida , paladar hendido , síndrome de Down , trisomía 18 , enfermedad de Tay-Sachs , anemia de células falciformes , talasemia , fibrosis quística , distrofia muscular y síndrome del cromosoma X frágil . Algunas pruebas están diseñadas para descubrir problemas que afectan principalmente a la salud de la madre, como la PAPP-A para detectar la preeclampsia o las pruebas de tolerancia a la glucosa para diagnosticar la diabetes gestacional . Las pruebas de detección también pueden detectar defectos anatómicos como la hidrocefalia , la anencefalia , los defectos cardíacos y el síndrome de banda amniótica .
El cribado prenatal se centra en la detección de problemas en una gran población con métodos asequibles y no invasivos. El diagnóstico prenatal se centra en la búsqueda de información detallada adicional una vez que se ha encontrado un problema particular, y a veces puede ser más invasivo. Los procedimientos de cribado más comunes son las ecografías de rutina , los análisis de sangre y la medición de la presión arterial. Los procedimientos de diagnóstico comunes incluyen la amniocentesis y la toma de muestras de vellosidades coriónicas . En algunos casos, las pruebas se realizan para determinar si el feto será abortado , aunque los médicos y los pacientes también encuentran útil diagnosticar los embarazos de alto riesgo de forma temprana para que el parto pueda programarse en un hospital de atención terciaria donde el bebé pueda recibir la atención adecuada.
En los últimos años, las pruebas prenatales se han orientado hacia métodos no invasivos para determinar el riesgo fetal de trastornos genéticos. El rápido avance de las modernas tecnologías moleculares de alto rendimiento junto con el descubrimiento del ADN fetal libre de células (cffDNA) en el plasma materno ha dado lugar a nuevos métodos para la determinación de aneuploidías cromosómicas fetales . Este tipo de pruebas se denominan pruebas prenatales no invasivas (NIPT) o detección prenatal no invasiva. Sin embargo, los procedimientos invasivos siguen siendo importantes, especialmente por su valor diagnóstico para confirmar hallazgos no invasivos positivos y detectar trastornos genéticos. [3] Los defectos congénitos tienen una incidencia de entre el 1 y el 6 %. [4]
El diagnóstico prenatal tiene tres objetivos: (1) permitir el tratamiento médico o quirúrgico oportuno de una afección antes o después del nacimiento, (2) dar a los padres la oportunidad de abortar un feto con la afección diagnosticada y (3) dar a los padres la oportunidad de prepararse psicológica, social, financiera y médicamente para un bebé con un problema de salud o discapacidad, o para la probabilidad de un nacimiento sin vida. La información previa sobre los problemas en el embarazo significa que el personal de atención médica, así como los padres, pueden prepararse mejor para el nacimiento de un niño con un problema de salud. Por ejemplo, el síndrome de Down se asocia con defectos cardíacos que pueden requerir una intervención inmediatamente después del nacimiento. [5]
La detección del suero materno en el primer trimestre permite verificar los niveles de β- hCG libre , PAPP-A , hCG intacta o beta o h-hCG en el suero de la mujer y combinarlos con la medición de la translucencia nucal (TN). Algunas instituciones también buscan la presencia de un hueso nasal fetal en la ecografía.
El cribado de suero maternal del segundo trimestre ( detección de AFP , pantalla triple, pantalla cuádruple o pantalla Penta) puede verificar los niveles de fetoproteína alfa , β- HCG , inhibina -a, estriol y H-HCG (HCG hiperglicosolado) en el suero de la mujer .
La prueba triple mide los niveles séricos de AFP , estriol y beta-hCG , con una sensibilidad del 70% y una tasa de falsos positivos del 5% . Se complementa en algunas regiones de los Estados Unidos con la prueba cuádruple (añadiendo inhibina A al panel, lo que da como resultado una sensibilidad del 81% y una tasa de falsos positivos del 5% para detectar el síndrome de Down cuando se realiza entre las 15 y 18 semanas de edad gestacional ). [25]
Los biomarcadores PAPP-A y β- hCG parecen estar alterados en los embarazos resultantes de ICSI, lo que provoca una mayor tasa de falsos positivos. Se han desarrollado factores de corrección que deberían utilizarse en el cribado del síndrome de Down en embarazos de feto único después de ICSI, [26] pero en los embarazos gemelares dichos factores de corrección no han sido completamente dilucidados. [26] En los embarazos gemelares que desaparecen con un segundo saco gestacional con un feto muerto, el cribado del primer trimestre debería basarse únicamente en la edad materna y la ecografía de translucencia nucal, ya que en estos casos los biomarcadores están alterados. [26]
La medición de las proteínas fetales en el suero materno es parte de la detección prenatal estándar de aneuploidía fetal y defectos del tubo neural . [27] [28] El modelo predictivo computacional muestra que durante el embarazo se produce un tráfico extenso y diverso de proteínas fetomaternas y se puede detectar fácilmente de forma no invasiva en la sangre completa materna . [29] Este enfoque computacional eludió una limitación importante, la abundancia de proteínas maternas que interfieren con la detección de proteínas fetales, para el análisis proteómico fetal de la sangre materna. La introducción de transcripciones de genes fetales previamente identificadas en la sangre completa materna en un modelo predictivo computacional ayudó a desarrollar una red proteómica integral del neonato a término. También muestra que las proteínas fetales detectadas en la sangre de la mujer embarazada se originan a partir de un grupo diverso de tejidos y órganos del feto en desarrollo. Las redes proteómicas del desarrollo dominan la caracterización funcional de las proteínas predichas, lo que ilustra la posible aplicación clínica de esta tecnología como una forma de monitorear el desarrollo fetal normal y anormal.
La diferencia en la metilación de secuencias específicas de ADN entre la madre y el feto se puede utilizar para identificar ADN específico del feto en la circulación sanguínea de la madre. En un estudio publicado en la edición en línea del 6 de marzo de 2011 de Nature , utilizando esta técnica no invasiva, un grupo de investigadores de Grecia y el Reino Unido logró el diagnóstico correcto de 14 casos de trisomía 21 ( síndrome de Down ) y 26 casos normales. [30] [31] Utilizando secuenciación paralela masiva , un estudio que probó solo la trisomía 21, detectó con éxito 209 de 212 casos (98,6%) con 3 falsos positivos en 1471 embarazos (0,2%). [32] Con las pruebas (de sangre) no invasivas disponibles comercialmente para el síndrome de Down que se han vuelto disponibles para los pacientes en los Estados Unidos y ya están disponibles en China, en octubre de 2011, la Sociedad Internacional para el Diagnóstico Prenatal creó algunas pautas. Por su sensibilidad y especificidad , constituye una prueba de cribado avanzada y sus resultados positivos requieren confirmación mediante una prueba invasiva, y si bien es eficaz en el diagnóstico del síndrome de Down, no puede evaluar la mitad de las anomalías detectadas mediante pruebas invasivas. La prueba no se recomienda para uso general hasta que se hayan publicado los resultados de estudios más amplios, pero puede ser útil en pacientes de alto riesgo junto con el asesoramiento genético. [33]
Un estudio de 2012 descubrió que la prueba de ADN libre de células plasmáticas maternas también pudo detectar la trisomía 18 (síndrome de Edwards) en el 100% de los casos (59/59) con una tasa de falsos positivos del 0,28%, y la trisomía 13 (síndrome de Patau) en el 91,7% de los casos (11/12) con una tasa de falsos positivos del 0,97%. La prueba interpretó el 99,1% de las muestras (1.971/1.988); Entre las 17 muestras sin interpretación, tres eran trisomía 18. El estudio afirmó que si los puntos de corte de la puntuación z para la trisomía 18 y 13 se aumentaran ligeramente, las tasas generales de falsos positivos para las tres aneuploidías podrían ser tan bajas como 0,1% (2/1.688) con una tasa de detección general de 98,9% (280/283) para aneuploidías comunes (esto incluye las tres trisomías: Down, Edwards y Patau). [34]
El objetivo de las pruebas genéticas prenatales es identificar embarazos con alto riesgo de anomalías, lo que permite una intervención temprana, la interrupción o las medidas de manejo y preparación adecuadas. [35] Las pruebas genéticas prenatales se realizan mediante diferentes pruebas de detección y pruebas de diagnóstico. Una prueba de detección informa a una persona sobre la posibilidad de que se produzcan ciertas anomalías, mientras que la prueba de diagnóstico se utiliza para confirmar/diagnosticar anomalías específicas existentes dentro del feto. Las pruebas de detección prenatales suelen ser menos invasivas que las pruebas de diagnóstico prenatales. Tienen un riesgo mucho menor, sin embargo, los resultados no son tan definitivos como las pruebas de diagnóstico. Los proveedores a menudo recomiendan realizar un seguimiento con una prueba de diagnóstico después de recibir un resultado positivo de una prueba de detección específica.
Las técnicas médicamente invasivas son aquellas en las que se utiliza una herramienta para acceder a algo dentro del cuerpo. Hay distintos grados de invasividad, dependiendo de qué muestra se requiera para completar la prueba. La extracción de sangre típica administrada por un profesional de la salud es una de las prácticas médicas invasivas más comunes. [36] Dado que causa una incomodidad mínima y existe un riesgo muy bajo asociado con la recolección de la muestra, una extracción de sangre se considera menos invasiva. La toma de muestras de vellosidades coriónicas (CVS) y la amniocentesis son las pruebas prenatales más invasivas porque existe un mayor riesgo asociado y la muestra es más difícil de acceder. Estos procedimientos se realizan mediante la inserción de una aguja en el abdomen para recolectar una muestra dentro del útero, lo que significa que se requiere un cuidado y una precisión excepcionales. [37] Las pruebas genéticas prenatales pueden identificar varias anomalías cromosómicas, afecciones autosómicas, varios defectos de nacimiento y algunos trastornos sanguíneos fetales.
Las anormalidades cromosómicas son el resultado de un número anormal o estructuración de cromosomas.
- Síndrome de Prader-Willi/Angelman
Las enfermedades autosómicas recesivas ocurren cuando ambos padres transmiten una mutación dentro de un cromosoma autosómico (no sexual). [39] Algunos ejemplos de enfermedades autosómicas recesivas son:
Los defectos del tubo neural son un tipo de defecto congénito que ocurre cuando el tubo neural de un feto no se forma o cierra correctamente, lo que puede afectar otros sistemas en todo el cuerpo. [40] Algunos ejemplos de defectos del tubo neural son:
Los defectos de la pared abdominal son un tipo de defecto de nacimiento que ocurre cuando la pared abdominal de un feto no se forma correctamente, lo que puede afectar a otros órganos en todo el cuerpo.
Los trastornos sanguíneos pueden ocurrir por una interacción negativa entre la sangre materna y la sangre fetal. [42] Un ejemplo de un trastorno sanguíneo fetal es la enfermedad hemolítica del feto .
La ecografía permite realizar una ecografía de translucencia nucal (TN) para detectar anomalías cromosómicas, como el síndrome de Down (trisomía 21), el síndrome de Edwards (trisomía 18) y el síndrome de Patau (trisomía 13). Con la información obtenida en la ecografía de translucencia nucal, se puede ofrecer a la madre una prueba diagnóstica invasiva para detectar anomalías cromosómicas fetales. Los marcadores séricos se utilizan de forma similar para identificar gestaciones que deberían recomendarse para realizar más pruebas. Cuando la ecografía de translucencia nucal o los marcadores séricos despiertan sospechas de anomalías cromosómicas, se pueden realizar las siguientes pruebas genéticas en muestras de tejido fetal o placentario: hibridación in situ con fluorescencia interfásica (FISH), PCR cuantitativa y preparación directa de cromosomas a partir de vellosidades coriónicas . [43]
La prueba de detección de portadores es una prueba general de ADN que utiliza una muestra de sangre o un hisopo bucal para determinar si los padres son portadores de ciertas afecciones genéticas. Esta prueba se puede realizar en cualquier momento, ya sea que la persona esté considerando formar una familia o ya haya quedado embarazada. Existen varios tipos de pruebas de detección de portadores que detectan progresivamente más anomalías genéticas. La prueba de detección de un solo gen o afección detecta una afección específica, mientras que la prueba de detección de portadores ampliada detecta cientos de anomalías diferentes que pueden ser heredadas por un feto. También hay tres pruebas de detección de portadores específicas de genes o afecciones y de grupos étnicos. En el caso de un resultado positivo, a menudo se recomiendan más pruebas, ya que la prueba de detección de portadores solo determina si el padre o los padres son portadores, no si el gen se ha transmitido definitivamente al feto. [10]
La prueba de ADN acelular placentario (libre de células fetales) (pa-ADN) permite la detección de células placentarias apoptóticas y ADN placentario circulante en la sangre materna para el diagnóstico no invasivo de aneuploidía fetal. [43] [44] Un metanálisis que investigó la tasa de éxito del uso de ADN acelular placentario de la sangre materna para detectar aneuploidías encontró que esta técnica detectó trisomía 13 en el 99% de los casos, trisomía 18 en el 98% de los casos y trisomía 21 en el 99% de los casos. [44] [45] Es más probable que las pruebas fallidas que utilizan ADN acelular placentario ocurran en fetos con trisomía 13 y trisomía 18, pero no con trisomía 21. [46] Estudios previos encontraron niveles elevados de ADN placentario acelular para trisomía 13 y 21 del suero materno en comparación con mujeres con embarazos euploides. [47] [48] [49] [50] Sin embargo, no se observó una elevación del ADN acelular para la trisomía 18. [47] Las células nucleadas placentarias circulantes comprenden solo del tres al seis por ciento del ADN del plasma sanguíneo materno, lo que reduce la tasa de detección de anomalías del desarrollo fetal. [50] Se han desarrollado dos enfoques alternativos para la detección de aneuploidía fetal. El primero implica la medición de la proporción alélica de polimorfismos de un solo nucleótido (SNP) en la región codificante del ARNm en la placenta . El siguiente enfoque es analizar el ADN materno y placentario y buscar diferencias en los patrones de metilación del ADN . [12] [50]
Las pruebas de detección del primer, segundo, combinado y tercer trimestre consisten típicamente en una ecografía (abdominal y/o transvaginal) y análisis de sangre/suero materno. La ecografía se utiliza para evaluar visualmente el crecimiento, desarrollo y actividad del feto a través de observaciones y mediciones de imágenes. La parte de la ecografía de la prueba de detección del primer trimestre puede incluir una prueba de translucencia nucal y una prueba de determinación del hueso nasal fetal. Los análisis de sangre disponibles de la prueba de detección del primer trimestre pueden evaluar la proteína plasmática A y la gonadotropina coriónica humana. La prueba de detección del segundo trimestre analiza marcadores sanguíneos específicos, que incluyen las hormonas estriol, inhibina y gonadotropina coriónica humana y, a menudo, consiste en la prueba de alfafetoproteína (AFP). Cualquier resultado anormal de estas pruebas de detección puede indicar la posibilidad de afecciones anormales como trisomía 18, trisomía 21 (síndrome de Down) y espina bífida. [13]
La prueba de AFP se realiza a menudo en el segundo trimestre utilizando el suero de la extracción de sangre materna. Esta prueba analiza una proteína específica que se forma en el hígado del feto y se libera en el contenido líquido del útero, que luego se absorbe en el torrente sanguíneo de la madre. Múltiples determinaciones se derivan de los resultados de la prueba de AFP. Genéticamente, puede revelar defectos cromosómicos y neuronales. [51]
La muestra de vellosidades coriónicas (CVS) es una prueba diagnóstica invasiva que se puede realizar durante el primer trimestre del embarazo en mujeres que buscan identificar anomalías cromosómicas o que tienen un mayor riesgo de transmitirlas. Se obtiene una muestra de tejido de la placenta por vía abdominal mediante una aguja o mediante la inserción vaginal de un catéter o jeringa en el cuello uterino en combinación con una ecografía para guiar el procedimiento. Los resultados positivos de la muestra de vellosidades coriónicas requieren un análisis de sangre para su confirmación. [51]
La amniocentesis es una prueba de diagnóstico invasiva que se puede hacer durante el segundo trimestre de embarazo para las personas que buscan identificar o tienen un mayor riesgo de pasar las anormalidades cromosómicas y/o del tubo neural que se realiza típicamente a través de la aguja, en combinación con ultrasonido, para obtener una muestra del fluido amniótico que rodea el fetus .
La cordocentesis es una prueba diagnóstica invasiva que se puede realizar durante el segundo trimestre del embarazo en personas que buscan identificar anomalías cromosómicas o sanguíneas o que tienen un mayor riesgo de transmitirlas. La demanda de pruebas de cordocentesis está disminuyendo porque ha sido reemplazada por la toma de vellosidades coriónicas y la amniocentesis, que conllevan menos riesgo. El procedimiento se realiza típicamente a través de una aguja en el abdomen de la madre, en combinación con una ecografía como guía, para obtener una muestra de sangre del cordón umbilical del feto. [18]
Recientemente [ cuando ?
Una variación de la técnica de PCR llamada amplificación de sonda dependiente de ligación múltiple (MLPA), dirigida al ADN, se ha aplicado sucesivamente para diagnosticar la aneuploidía fetal como un ensayo específico de cromosomas o genes. [53]
El ADN fetal libre se ha secuenciado directamente mediante la tecnología de secuenciación shotgun . En un estudio, se obtuvo ADN del plasma sanguíneo de dieciocho mujeres embarazadas. A continuación, se realizó un mapeo del cromosoma mediante la cuantificación de fragmentos. Esto se hizo utilizando métodos avanzados de secuenciación de ADN, lo que dio como resultado la secuenciación paralela del ADN fetal. Se contó la cantidad de etiquetas de secuencia asignadas a cada cromosoma. Si había un excedente o deficiencia en cualquiera de los cromosomas, esto significaba que había un aneuploide fetal. Usando este método de secuenciación shotgun, fue posible la identificación exitosa de la trisomía 21 (síndrome de Down), la trisomía 18 (síndrome de Edward) y la trisomía 13 (síndrome de Patau). Este método de diagnóstico no invasivo ahora está comenzando a usarse ampliamente y a investigarse más. [54]
El análisis de microarrays, el cariotipo y las diferentes técnicas de secuenciación del genoma también se utilizan para detectar anormalidades .

Las pruebas de diagnóstico prenatal se pueden realizar mediante métodos invasivos o no invasivos . Un método invasivo implica la inserción de sondas o agujas en el útero , por ejemplo, la amniocentesis , que se puede realizar a partir de las 14 semanas de gestación, y generalmente hasta aproximadamente las 20 semanas, y la muestra de vellosidades coriónicas , que se puede realizar antes (entre las 9,5 y las 12,5 semanas de gestación), pero que puede ser ligeramente más riesgosa para el feto. Un estudio que comparó la muestra de vellosidades coriónicas transabdominal con la amniocentesis del segundo trimestre no encontró diferencias significativas en la pérdida total del embarazo entre los dos procedimientos. [55] Sin embargo, la toma de muestras de vellosidades coriónicas transcervicales conlleva un riesgo significativamente mayor, en comparación con una amniocentesis en el segundo trimestre, de pérdida total del embarazo ( riesgo relativo 1,40; intervalo de confianza del 95% : 1,09 a 1,81) y aborto espontáneo (riesgo del 9,4%; riesgo relativo 1,50; intervalo de confianza del 95%: 1,07 a 2,11). [55]

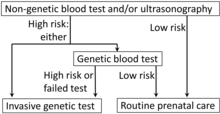
Las técnicas no invasivas incluyen exámenes del útero de la mujer mediante ecografía y pruebas de detección del suero materno (es decir, alfafetoproteína ). Se han puesto a disposición análisis de sangre para trisomías seleccionadas (síndrome de Down en los Estados Unidos, síndromes de Down y Edwards en China) basados en la detección de ADN placentario libre de células presente en la sangre materna, también conocido como prueba prenatal no invasiva (NIPT). [32] Si una prueba de detección no invasiva indica un riesgo elevado de anomalía cromosómica o genética, se puede emplear una técnica más invasiva para recopilar más información. [33] En el caso de defectos del tubo neural, una ecografía detallada puede proporcionar un diagnóstico definitivo de forma no invasiva. [ cita requerida ]
Una de las principales ventajas de las pruebas prenatales no invasivas es que la posibilidad de un resultado falso positivo es muy baja .
Las pautas del Colegio Estadounidense de Obstetras y Ginecólogos ( ACOG ) actualmente recomiendan que cualquier persona que esté embarazada, independientemente de su edad, debe discutir y se le deben ofrecer opciones de pruebas de diagnóstico y detección genética prenatal no invasiva. [58] La detección genética prenatal no invasiva se realiza típicamente al final del primer trimestre (11 a 14 semanas) o durante el comienzo del segundo trimestre (15 a 20 semanas). Esto implica que la mujer embarazada recibe una extracción de sangre con una aguja y una jeringa y una ecografía del feto. Las pruebas de detección pueden incluir la detección de analitos séricos o ADN fetal libre de células y la ecografía de translucencia nucal [NT], respectivamente. [59] Es importante señalar que las pruebas de detección no son diagnósticas y los resultados de detección preocupantes deben ser seguidos con pruebas de diagnóstico invasivas para un diagnóstico confirmado. Las pruebas genéticas prenatales de diagnóstico invasivas pueden implicar una muestra de vellosidades crónicas (CVS) o una amniocentesis . [60] El ACOG recomienda la detección genética antes del embarazo a todas las mujeres embarazadas que planean tener una familia. [61] Después de un asesoramiento y una discusión exhaustivos que reconozcan los riesgos residuales, es importante respetar el derecho de los pacientes a elegir si desean o no someterse a algún componente de las pruebas genéticas. [ cita requerida ]
Las siguientes son algunas razones por las que una mujer podría considerar que su riesgo de defectos congénitos ya es lo suficientemente alto como para justificar omitir la detección y pasar directamente a una prueba invasiva: [60]
Se llevó a cabo una investigación para determinar qué pensaban las mujeres sobre el diagnóstico no invasivo de aneuploidía fetal utilizando sangre materna. Este estudio se realizó mediante encuestas. Se informó que el ochenta y dos por ciento de las mujeres embarazadas y el setenta y nueve por ciento de las estudiantes de medicina ven este tipo de diagnóstico de manera positiva y coinciden en que es importante para la atención prenatal. En general, las mujeres respondieron con optimismo que esta forma de diagnóstico estará disponible en el futuro. [62]
Antes de la concepción, las parejas pueden optar por hacerse pruebas genéticas para determinar las probabilidades de concebir un hijo con una anomalía genética conocida. Las más comunes en la población caucásica son: [ cita requerida ]
Se conocen cientos de enfermedades adicionales y se descubren más con regularidad. Sin embargo, la justificación económica para realizar pruebas a nivel de población de todas las enfermedades conocidas no está bien sustentada, en particular una vez que se tienen en cuenta el costo de los posibles resultados falsos positivos y las pruebas de seguimiento concomitantes. [72] También existen preocupaciones éticas relacionadas con este o cualquier tipo de prueba genética . [ cita requerida ]
Uno o ambos miembros de la pareja pueden saber que otros miembros de la familia padecen estas enfermedades. La realización de pruebas antes de la concepción puede aliviar la preocupación, preparar a la pareja para las posibles consecuencias a corto o largo plazo de tener un hijo con la enfermedad, orientar a la pareja hacia la adopción o la crianza temporal, o impulsar la realización de pruebas genéticas preimplantacionales durante la fertilización in vitro . Si se detecta un trastorno genético, generalmente se recomienda asesoramiento genético profesional debido a la gran cantidad de consideraciones éticas relacionadas con las decisiones posteriores de los miembros de la pareja y el posible impacto en sus familias extendidas. La mayoría de estas enfermedades, pero no todas, siguen patrones de herencia mendeliana . El síndrome del cromosoma X frágil está relacionado con la expansión de ciertos segmentos repetidos de ADN y puede cambiar de generación en generación. [ cita requerida ]
En las primeras etapas del embarazo, alrededor de las 6 semanas, se puede ofrecer una ecografía de datación temprana para ayudar a confirmar la edad gestacional del embrión y verificar si se trata de un embarazo único o gemelar, pero dicha ecografía no puede detectar anomalías comunes. Se pueden proporcionar detalles sobre las opciones de detección y análisis prenatales. [ cita requerida ]
Alrededor de las semanas 11 a 13, se puede ofrecer una ecografía de translucencia nucal (TN), que se puede combinar con análisis de sangre para PAPP-A y beta-hCG, dos marcadores séricos que se correlacionan con anomalías cromosómicas, en lo que se denomina la prueba combinada del primer trimestre. Los resultados del análisis de sangre se combinan luego con las mediciones de la ecografía de translucencia nucal, la edad materna y la edad gestacional del feto para obtener una puntuación de riesgo de síndrome de Down, trisomía 18 y trisomía 13. La prueba combinada del primer trimestre tiene una sensibilidad (es decir, tasa de detección de anomalías) del 82 al 87 % y una tasa de falsos positivos de alrededor del 5 %. [73] [74]
El ADN fetal libre de células también está disponible durante el primer trimestre del embarazo.
La ecografía de anomalías se realiza entre las 18 y 22 semanas de edad gestacional . La Sociedad Internacional de Ultrasonido en Obstetricia y Ginecología (ISUOG) recomienda que esta ecografía se realice como una cuestión de atención prenatal de rutina , para medir al feto de modo que las anomalías del crecimiento se puedan reconocer rápidamente más adelante en el embarazo y para evaluar malformaciones congénitas y embarazos múltiples (es decir, gemelos). [75] La exploración puede detectar anencefalia , espina bífida abierta , labio leporino , hernia diafragmática , gastrosquisis , onfalocele , defecto cardíaco congénito , agenesia renal bilateral , osteocondrodisplasia , síndrome de Edwards y síndrome de Patau . [76]
Se puede realizar un análisis de sangre cuádruple en el segundo trimestre (la prueba triple se considera ampliamente obsoleta, pero en algunos estados, como Missouri, donde Medicaid solo cubre la prueba triple, eso es lo que generalmente se realiza la paciente). Con el cribado integrado , se realiza una prueba combinada del primer trimestre y una prueba triple/cuádruple, y solo se produce un informe después de que se hayan analizado ambas pruebas. Sin embargo, es posible que las pacientes no deseen esperar entre estos dos conjuntos de pruebas. Con el cribado secuencial , se produce un primer informe después de que se haya enviado la muestra del primer trimestre y un informe final después de la segunda muestra. Con el cribado contingente , las pacientes con riesgos muy altos o muy bajos recibirán informes después de que se haya enviado la muestra del primer trimestre. Solo a las pacientes con riesgo moderado (puntuación de riesgo entre 1:50 y 1:2000) se les pedirá que envíen una muestra del segundo trimestre, después de lo cual recibirán un informe que combina la información de ambas muestras de suero y la medición de NT . La prueba combinada del primer trimestre y la prueba triple/cuádruple juntas tienen una sensibilidad del 88-95% con una tasa de falsos positivos del 5% para el síndrome de Down, aunque también se pueden analizar de manera tal que ofrezcan una sensibilidad del 90% con una tasa de falsos positivos del 2%. Finalmente, las pacientes que no reciben una ecografía NT en el primer trimestre aún pueden recibir una prueba integrada en suero que implica medir los niveles séricos de PAPP-A en el primer trimestre y luego hacer una prueba cuádruple en el segundo trimestre. Esto ofrece una sensibilidad del 85-88% y una tasa de falsos positivos del 5% para el síndrome de Down. Además, una paciente puede omitir por completo la detección del primer trimestre y recibir solo una prueba cuádruple del segundo trimestre, con una sensibilidad del 81% para el síndrome de Down y una tasa de falsos positivos del 5%. [77]
Las pruebas prenatales del tercer trimestre generalmente se centran en el bienestar materno y en la reducción de la morbilidad y la mortalidad fetales. Se puede ofrecer la prueba de la infección por estreptococo del grupo B (también llamada estreptococo del grupo B), que es una de las principales causas de morbilidad y mortalidad neonatal. El estreptococo del grupo B es una infección que puede transmitirse al bebé durante el parto. La detección vaginal del síndrome de Guillain-Barré se realiza entre las 34 y las 37 semanas de edad gestacional, de modo que las madres que dan positivo a la bacteria puedan recibir tratamiento antes del parto. Durante el tercer trimestre, algunas instituciones pueden exigir evaluaciones de hemoglobina/hematocrito, serología de sífilis y detección del VIH. Además, antes del parto, se documenta una evaluación de la posición fetal y el peso fetal estimado. [78]
El diagnóstico prenatal (DPN) está permitido en toda Europa , con excepción de Irlanda . Ocho (8) países no tienen legislación al respecto. Sin embargo, existen diferencias entre estados. Por ejemplo, en Polonia , el plazo límite para el DPN es de 22 semanas. En Malta , el Comité Parlamentario de Asuntos Sociales especificó en su informe de 2005 que el DPN sólo debería permitirse en condiciones para las que existan opciones terapéuticas. Sin embargo, todos los países prohíben el DPN para fines no médicos (como la selección del sexo), por ejemplo. [79]
El artículo L2131-1 del Código de Salud Pública, derivado de la ley de bioética de julio de 2011, establece que «el diagnóstico prenatal se refiere a las prácticas médicas, incluida la ecografía obstétrica y fetal, destinadas a detectar, en el útero, una afección particularmente grave en el embrión o el feto». La ley exige que las mujeres embarazadas reciban una información clara sobre estas técnicas con el fin de «evaluar el riesgo de que el embrión o el feto presenten una afección que pueda alterar el curso o la gestión del embarazo». [80]
Los padres deben tomar decisiones informadas sobre las pruebas de detección, el diagnóstico y las medidas que se deben tomar como resultado. Muchas pruebas de detección son inexactas, por lo que un resultado preocupante suele dar lugar a pruebas adicionales más invasivas. Si las pruebas prenatales confirman una discapacidad grave, muchos padres se ven obligados a decidir si continúan con el embarazo o buscan un aborto. La "opción" de la detección se convierte en un requisito inesperado para tomar una decisión. Véase aborto injustificado .
En algunas enfermedades genéticas, como la fibrosis quística , solo se puede detectar una anomalía si se obtiene ADN del feto. Por lo general, se necesita un método invasivo para hacerlo. [ cita requerida ]
La ecografía del feto, que se considera una prueba de detección, a veces puede pasar por alto anomalías sutiles. Por ejemplo, los estudios muestran que una ecografía detallada del segundo trimestre, también llamada ecografía de nivel 2, puede detectar alrededor del 97 % de los defectos del tubo neural, como la espina bífida [ cita requerida ] . Los resultados de la ecografía también pueden mostrar "signos leves", como un foco intracardíaco ecogénico o un quiste del plexo coroideo , que suelen ser normales, pero pueden estar asociados con un mayor riesgo de anomalías cromosómicas .
Otras pruebas de detección, como la prueba Quad, también pueden tener falsos positivos y falsos negativos. Incluso cuando los resultados de la prueba Quad son positivos (o, para ser más precisos, cuando la prueba Quad arroja una puntuación que muestra al menos un riesgo de anomalía de 1 en 270), por lo general el embarazo es normal, pero se ofrecen pruebas diagnósticas adicionales. De hecho, considere que el síndrome de Down afecta a aproximadamente 1:400 embarazos; si examinara 4000 embarazos con una prueba Quad, probablemente habría 10 embarazos con síndrome de Down de los cuales la prueba Quad, con su sensibilidad del 80%, calificaría a 8 de ellos de alto riesgo. La prueba Quad también le diría al 5% (~200) de las 3990 mujeres normales que son de alto riesgo. Por lo tanto, a unas 208 mujeres se les diría que son de alto riesgo, pero cuando se sometan a una prueba invasiva, solo 8 (o el 4% del grupo de alto riesgo) serán confirmadas como positivas y a 200 (96%) se les dirá que sus embarazos son normales. Dado que la amniocentesis tiene aproximadamente un 0,5% de posibilidades de aborto espontáneo, uno de esos 200 embarazos normales podría resultar en un aborto espontáneo debido al procedimiento invasivo, por lo tanto. La prueba de Ening en realidad tiene un feto afectado .
En comparación, en las mismas 4000 mujeres, una prueba de detección con una sensibilidad del 99% y una tasa de falsos positivos del 0,5% detectaría los 10 positivos y les diría a 20 mujeres normales que son positivas. Por lo tanto, 30 mujeres se someterían a un procedimiento invasivo de confirmación y 10 de ellas (33%) serían confirmadas como positivas y a 20 se les diría que tienen un embarazo normal. De las 3970 mujeres a las que la prueba les dice que son negativas, ninguna de ellas tendría un embarazo afectado. Por lo tanto, una prueba de detección de este tipo tendría un valor predictivo positivo del 33%.
La tasa de falsos positivos en el mundo real para la prueba cuádruple (así como para la prueba combinada del primer trimestre, la prueba integrada, etc.) es superior al 5 %. El 5 % fue la tasa citada en los grandes estudios clínicos que fueron realizados por los mejores investigadores y médicos, donde todas las ecografías fueron realizadas por ecografistas bien capacitados y la edad gestacional del feto se calculó con la mayor precisión posible. En el mundo real, donde calcular la edad gestacional puede ser un arte menos preciso, las fórmulas que generan la puntuación de riesgo de un paciente no son tan precisas y la tasa de falsos positivos puede ser mayor, incluso del 10 %.
Debido a la baja precisión de las pruebas de detección convencionales, entre el 5 y el 10 % de las mujeres, a menudo las mayores, optarán por una prueba invasiva incluso si recibieron una puntuación de riesgo bajo en la prueba de detección. Una paciente que recibió una puntuación de riesgo de 1:330, aunque técnicamente sea de bajo riesgo (ya que el límite para el riesgo alto se cita comúnmente como 1:270), podría tener más probabilidades de optar por una prueba invasiva de confirmación. Por otro lado, una paciente que recibe una puntuación de riesgo de 1:1000 tiene más probabilidades de sentirse tranquila de que su embarazo es normal.
Tanto los falsos positivos como los falsos negativos tendrán un gran impacto en la pareja cuando se les comunique el resultado o cuando nazca el niño. Se considera que las pruebas diagnósticas , como la amniocentesis, son muy precisas para los defectos que detectan, aunque incluso estas pruebas no son perfectas, con una tasa de error informada del 0,2 % (a menudo debido a anomalías raras como el síndrome de Down en mosaico, en el que solo algunas de las células fetales o placentarias son portadoras de la anomalía genética).
Un nivel elevado de AFP en el suero materno indica un mayor riesgo de anencefalia y espina bífida abierta. Esta prueba tiene una sensibilidad del 80 % y del 90 % para la espina bífida y la anencefalia, respectivamente. [ cita requerida ]
La acetilcolinesterasa en el líquido amniótico y el nivel de AFP son más sensibles y específicos que la AFP para predecir defectos del tubo neural.
Muchos especialistas materno-fetales ni siquiera se molestan en hacer una prueba de AFP a sus pacientes porque les hacen una ecografía detallada a todas ellas en el segundo trimestre, que tiene una tasa de detección del 97% para defectos del tubo neural como la anencefalia y la espina bífida abierta. Realizar pruebas para determinar posibles defectos de nacimiento es obligatorio en todos los estados de EE . UU . [ cita requerida ] No detectar problemas de forma temprana puede tener consecuencias peligrosas tanto para la madre como para el bebé. Los obstetras y ginecólogos pueden ser considerados culpables. En un caso, un hombre que nació con espina bífida recibió una indemnización de 2 millones de dólares, aparte de los gastos médicos, debido a la negligencia del obstetra y ginecólogo al realizar pruebas de AFP. [81]
Ninguna prueba prenatal puede detectar todas las formas de defectos y anomalías congénitas.
Otro tema importante es la incertidumbre de las pruebas genéticas prenatales. La incertidumbre en las pruebas genéticas se debe a varias razones: la prueba genética está asociada con una enfermedad pero el pronóstico y/o la probabilidad son desconocidos, la prueba genética proporciona información diferente a la enfermedad familiar para la que se realizó la prueba, las variantes genéticas encontradas tienen un significado desconocido y, finalmente, los resultados pueden no estar asociados con las anomalías fetales encontradas. [82] Richardson y Ormond abordaron en profundidad la cuestión de la incertidumbre de las pruebas genéticas y explicaron sus implicaciones para la bioética. En primer lugar, se asume el principio de beneficencia en las pruebas prenatales al disminuir el riesgo de aborto espontáneo, sin embargo, la información incierta derivada de las pruebas genéticas puede dañar a los padres al provocar ansiedad y llevar a la interrupción del embarazo de un feto que probablemente esté sano. En segundo lugar, el principio de autonomía se ve socavado debido a la falta de comprensión resultante de las nuevas tecnologías y el cambio de conocimiento en el campo de la genética. Y en tercer lugar, el principio de justicia planteó cuestiones relacionadas con la igualdad de acceso a las pruebas prenatales emergentes.
Si se detecta una enfermedad genética, a menudo no existe ningún tratamiento que pueda ayudar al feto hasta que nace. Sin embargo, en los EE. UU., existen cirugías prenatales para fetos con espina bífida . [ cita requerida ] El diagnóstico temprano les da a los padres tiempo para investigar y hablar sobre el tratamiento y la atención posnatal o, en algunos casos, el aborto. Por lo general, se recurre a los asesores genéticos para ayudar a las familias a tomar decisiones informadas sobre los resultados del diagnóstico prenatal.
Los investigadores han estudiado cómo afecta la ansiedad materna la divulgación de los resultados de la amniocentesis o de la muestra de vellosidades coriónicas (CVS) en una fecha fija en comparación con una fecha variable (es decir, "cuando estén disponibles"). La revisión sistemática de los artículos pertinentes no encontró evidencia concluyente que respalde la divulgación de los resultados de la amniocentesis tan pronto como estén disponibles (en comparación con la divulgación de los resultados en una fecha fija predefinida). Los investigadores concluyeron que se necesitan más estudios que evalúen el efecto de diferentes estrategias para divulgar los resultados de la CVS en la ansiedad materna. [83]
Los activistas y académicos en defensa de los derechos de las personas con discapacidad han sugerido una visión más crítica de las pruebas prenatales y sus implicaciones para las personas con discapacidad. Sostienen que existe presión para abortar fetos que podrían nacer con discapacidades, y que estas presiones se basan en intereses eugenésicos y estereotipos capacitistas. [84] Este aborto selectivo se basa en las ideas de que las personas con discapacidad no pueden vivir vidas deseables, que son "defectuosas" y que son una carga, mientras que los académicos en materia de discapacidad sostienen que "la opresión es lo más incapacitante de la discapacidad". Marsha Saxton sugiere que las mujeres deberían preguntarse si se basan o no en información real y factual sobre las personas con discapacidad o en estereotipos si deciden abortar un feto con una discapacidad. [85]
La amniocentesis se ha convertido en el estándar de atención para las visitas de atención prenatal para mujeres que están "en riesgo" o que superan cierta edad. El uso amplio de la amniocentesis se ha definido como consumista. [86] y algunos argumentan que esto puede estar en conflicto con el derecho a la privacidad, [87] La mayoría de los obstetras (según el país) ofrecen a las pacientes la prueba triple de AFP , la prueba de VIH y ecografías de forma rutinaria. Sin embargo, casi todas las mujeres se reúnen con un asesor genético antes de decidir si se someten a un diagnóstico prenatal. Es función del asesor genético informar con precisión a las mujeres sobre los riesgos y beneficios del diagnóstico prenatal. Los asesores genéticos están capacitados para no ser directivos y apoyar la decisión de la paciente. Algunos médicos sí recomiendan a las mujeres que se realicen ciertas pruebas prenatales y la pareja de la paciente también puede influir en la decisión de la mujer. [ cita requerida ]
En agosto de 2023, el gobierno iraní prohibió la importación y fabricación de kits de prueba necesarios para las pruebas de detección del primer trimestre, lo que afectará a la población según la Sociedad de Medicina Genética انجمن ژنتیک پزشکی ایران . [88] La organización de bienestar estatal iraní tenía un programa de condición genética desde 1997. [89]