El ácido etilendiaminotetraacético ( EDTA ), también llamado ácido EDTA por su propia abreviatura, es un ácido aminopolicarboxílico con la fórmula [CH 2 N (CH 2 CO 2 H) 2 ] 2 . Este sólido blanco insoluble en agua se usa ampliamente para unirse a iones de hierro (Fe 2+ /Fe 3+ ) y calcio (Ca 2+ ), formando complejos solubles en agua incluso a pH neutro. Por lo tanto, se utiliza para disolver incrustaciones que contienen Fe y Ca, así como para liberar iones de hierro en condiciones en las que sus óxidos son insolubles. El EDTA está disponible en forma de varias sales, en particular EDTA disódico , edetato sódico y cálcico y EDTA tetrasódico , pero todas funcionan de manera similar. [4]
En la industria, el EDTA se utiliza principalmente para secuestrar (unir o confinar) iones metálicos en solución acuosa. En la industria textil , evita que las impurezas de iones metálicos modifiquen los colores de los productos teñidos. En la industria de la pulpa y el papel , el EDTA inhibe la capacidad de los iones metálicos, especialmente Mn 2+ , de catalizar la desproporción del peróxido de hidrógeno , que se utiliza en el blanqueo sin cloro .
De manera similar, el EDTA se agrega a algunos alimentos como conservante o estabilizador para prevenir la decoloración oxidativa catalítica, que es catalizada por iones metálicos. [5]
La reducción de la dureza del agua en aplicaciones de lavandería y la disolución de incrustaciones en calderas dependen del EDTA y complejantes relacionados para unir Ca 2+ , Mg 2+ y otros iones metálicos. Una vez unidos al EDTA, es menos probable que estos complejos metálicos formen precipitados o interfieran con la acción de los jabones y detergentes . [ cita necesaria ] Por razones similares, las soluciones de limpieza a menudo contienen EDTA. De manera similar, el EDTA se utiliza en la industria del cemento para la determinación de cal libre y magnesia libre en cemento y clínker . [6] [ página necesaria ]
La solubilización de iones Fe 3+ a un pH casi neutro o inferior se puede lograr utilizando EDTA. Esta propiedad es útil en agricultura , incluida la hidroponía. Sin embargo, dada la dependencia del pH en la formación de ligandos, el EDTA no es útil para mejorar la solubilidad del hierro en suelos por encima de la neutralidad. [7] De lo contrario, a un pH casi neutro y superior, el hierro (III) forma sales insolubles, que son menos biodisponibles para las especies de plantas susceptibles.
Acuoso [Fe(EDTA)] - se utiliza para eliminar (" depurar ") el sulfuro de hidrógeno de las corrientes de gas. Esta conversión se logra oxidando el sulfuro de hidrógeno a azufre elemental, que no es volátil:
En esta aplicación, el centro de hierro (III) se reduce a su derivado de hierro (II), que luego puede reoxidarse con aire. De manera similar, los óxidos de nitrógeno se eliminan de las corrientes de gas usando [Fe(EDTA)] 2− .
Las propiedades oxidantes del [Fe(EDTA)] también se aprovechan en fotografía , donde se utiliza para solubilizar partículas de plata . [4]
Se utilizó EDTA en la separación de los metales lantánidos mediante cromatografía de intercambio iónico . Perfeccionado por F. H. Spedding et al . En 1954, el método se basa en el aumento constante de la constante de estabilidad de los complejos de lantánidos EDTA con número atómico . [8] Utilizando perlas de poliestireno sulfonado y Cu 2+ como ion de retención, el EDTA hace que los lantánidos migren hacia la columna de resina mientras se separan en bandas de lantánidos puros. Los lantánidos eluyen en orden decreciente de número atómico. Debido al coste de este método, en relación con la extracción con disolventes a contracorriente , el intercambio iónico ahora se utiliza sólo para obtener las purezas más altas de lantánidos (normalmente superiores al 99,99%). [ cita necesaria ]
El edetato de sodio y calcio , un derivado del EDTA, se utiliza para unir iones metálicos en la práctica de la terapia de quelación , como por ejemplo para el tratamiento del envenenamiento por mercurio y plomo . [9] Se utiliza de manera similar para eliminar el exceso de hierro del cuerpo. Esta terapia se utiliza para tratar la complicación de transfusiones de sangre repetidas , como se aplicaría para tratar la talasemia .
Los dentistas y endodoncistas utilizan soluciones de EDTA para eliminar residuos inorgánicos ( capa de barrillo ) y lubricar los conductos radiculares en endodoncia. Este procedimiento ayuda a preparar los conductos radiculares para la obturación . Además, las soluciones de EDTA con la adición de un surfactante aflojan las calcificaciones dentro de un conducto radicular y permiten la instrumentación (conformación del canal) y facilitan el avance apical de una lima en un conducto radicular estrecho o calcificado hacia el ápice.
Sirve como conservante (normalmente para potenciar la acción de otro conservante como el cloruro de benzalconio o el tiomersal ) en preparados oculares y colirios .
En el diagnóstico médico y en las pruebas de función de los órganos (aquí, prueba de función renal ), el complejo de cromo (III) [Cr(EDTA)] − (como cromo-51 radiactivo ( 51 Cr)) se administra por vía intravenosa y se controla su filtración en la orina. . Este método es útil para evaluar la tasa de filtración glomerular (TFG) en medicina nuclear . [10]
El EDTA se utiliza ampliamente en el análisis de sangre. Es un anticoagulante para muestras de sangre para CBC/FBC , donde el EDTA quela el calcio presente en la muestra de sangre, deteniendo el proceso de coagulación y preservando la morfología de las células sanguíneas. [11] Los tubos que contienen EDTA están marcados con tapas de color lavanda (púrpura) o rosa. [12] El EDTA también se encuentra en tubos con tapa canela para pruebas de plomo y se puede utilizar en tubos con tapa azul real para pruebas de trazas de metales. [12]
El EDTA es un dispersante de limo y se ha descubierto que es muy eficaz para reducir el crecimiento bacteriano durante la implantación de lentes intraoculares (LIO). [13]
Algunos médicos alternativos creen que el EDTA actúa como antioxidante , evitando que los radicales libres dañen las paredes de los vasos sanguíneos y, por lo tanto, reduciendo la aterosclerosis . [14] Estas ideas no están respaldadas por estudios científicos y parecen contradecir algunos principios actualmente aceptados. [15] La FDA de EE. UU. no lo ha aprobado para el tratamiento de la aterosclerosis. [dieciséis]
En champús , limpiadores y otros productos de cuidado personal, las sales de EDTA se utilizan como agente secuestrante para mejorar su estabilidad en el aire. [17]
En el laboratorio, el EDTA se usa ampliamente para eliminar iones metálicos: en bioquímica y biología molecular , el agotamiento de iones se usa comúnmente para desactivar enzimas dependientes de metales , ya sea como un ensayo para determinar su reactividad o para suprimir el daño al ADN , las proteínas y los polisacáridos . [18] El EDTA también actúa como un inhibidor selectivo contra las enzimas hidrolizantes de dNTP ( Taq polimerasa , dUTPasa , MutT), [19] arginasa hepática [20] y peroxidasa de rábano picante [21] independientemente de la quelación de iones metálicos . Estos hallazgos instan a repensar la utilización de EDTA como eliminador de iones metálicos bioquímicamente inactivos en experimentos enzimáticos. En química analítica, el EDTA se utiliza en valoraciones complexométricas y análisis de la dureza del agua o como agente enmascarante para secuestrar iones metálicos que interferirían con los análisis.
El EDTA encuentra muchos usos especializados en los laboratorios biomédicos, como en oftalmología veterinaria como anticolagenasa para prevenir el empeoramiento de las úlceras corneales en animales . En cultivo de tejidos , el EDTA se utiliza como agente quelante que se une al calcio e impide la unión de cadherinas entre las células, evitando la aglutinación de las células cultivadas en suspensión líquida o el desprendimiento de las células adherentes para su paso . En histopatología , el EDTA se puede utilizar como agente descalcificante permitiendo cortar secciones mediante un micrótomo una vez desmineralizada la muestra de tejido.
También se sabe que el EDTA inhibe una variedad de metalopeptidasas ; el método de inhibición se produce mediante la quelación del ión metálico necesario para la actividad catalítica. [22] El EDTA también se puede utilizar para probar la biodisponibilidad de metales pesados en sedimentos . Sin embargo, puede influir en la biodisponibilidad de los metales en solución, lo que puede plantear preocupaciones con respecto a sus efectos en el medio ambiente, especialmente teniendo en cuenta sus usos y aplicaciones generalizados.
El EDTA también se utiliza para eliminar la suciedad (metales corroídos) de las barras de combustible en los reactores nucleares. [23]
El EDTA presenta una toxicidad aguda baja con una LD50 (rata) de 2,0 g/kg a 2,2 g/kg. [4] Se ha descubierto que es citotóxico y débilmente genotóxico en animales de laboratorio. Se ha observado que las exposiciones orales causan efectos en la reproducción y el desarrollo. [17] El mismo estudio [17] también encontró que tanto la exposición dérmica al EDTA en la mayoría de las formulaciones cosméticas como la exposición por inhalación al EDTA en formulaciones cosméticas en aerosol producirían niveles de exposición inferiores a los que se consideran tóxicos en los estudios de dosificación oral.
El compuesto fue descrito por primera vez en 1935 por Ferdinand Münz , [24] quien preparó el compuesto a partir de etilendiamina y ácido cloroacético . [25] Hoy en día, el EDTA se sintetiza principalmente a partir de etilendiamina (1,2-diaminoetano), formaldehído y cianuro de sodio . [26] Esta ruta produce el EDTA tetrasódico, que se convierte en un paso posterior en las formas ácidas:
Este proceso se utiliza para producir alrededor de 80.000 toneladas de EDTA cada año. Las impurezas cogeneradas por esta ruta incluyen glicina y ácido nitrilotriacético ; surgen de reacciones del coproducto amoníaco . [4]
Para describir el EDTA y sus diversas formas protonadas , los químicos distinguen entre EDTA 4- , la base conjugada que es el ligando , y H 4 EDTA, el precursor de ese ligando. A pH muy bajo (condiciones muy ácidas) predomina la forma H 6 EDTA 2+ completamente protonada , mientras que a pH muy alto o condiciones muy básicas, prevalece la forma EDTA 4- completamente desprotonada. En este artículo, el término EDTA se utiliza para significar H 4− x EDTA x − , mientras que en sus complejos EDTA 4− representa el ligando tetraanión.
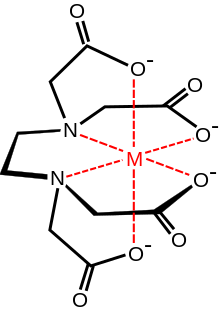

En química de coordinación , EDTA 4− es un miembro de la familia de ligandos de los ácidos aminopolicarboxílicos . EDTA 4- normalmente se une a un catión metálico a través de sus dos aminas y cuatro carboxilatos, es decir, es un agente quelante hexadentado ("seis dientes") . Muchos de los compuestos de coordinación resultantes adoptan geometría octaédrica . Aunque tienen pocas consecuencias para sus aplicaciones, estos complejos octaédricos son quirales . El anión cobalto (III) [Co(EDTA)] - se ha resuelto en enantiómeros . [28] Muchos complejos de EDTA 4- adoptan estructuras más complejas debido a la formación de un enlace adicional con el agua, es decir, complejos de siete coordenadas, o al desplazamiento de un brazo de carboxilato por el agua. El complejo de hierro (III) del EDTA tiene siete coordenadas. [29] Los primeros trabajos sobre el desarrollo de EDTA fueron realizados por Gerold Schwarzenbach en la década de 1940. [30] El EDTA forma complejos especialmente fuertes con Mn(II) , Cu(II) , Fe(III), Pb(II) y Co(III). [31] [ página necesaria ]
Varias características de los complejos de EDTA son relevantes para sus aplicaciones. Primero, debido a su alta denticidad , este ligando tiene una alta afinidad por los cationes metálicos:
Escrito de esta manera, el cociente de equilibrio muestra que los iones metálicos compiten con los protones para unirse al EDTA. Debido a que los iones metálicos están ampliamente envueltos por EDTA, sus propiedades catalíticas a menudo se suprimen. Finalmente, dado que los complejos de EDTA 4− son aniónicos , tienden a ser muy solubles en agua. Por este motivo, el EDTA es capaz de disolver depósitos de óxidos y carbonatos metálicos .
Los valores de p K a del EDTA libre son 0, 1,5, 2, 2,66 ( desprotonación de los cuatro grupos carboxilo ) y 6,16, 10,24 (desprotonación de los dos grupos amino ). [32]
El uso del EDTA es tan generalizado que se han planteado dudas sobre si se trata de un contaminante orgánico persistente . Si bien el EDTA cumple muchas funciones positivas en diferentes ámbitos industriales, farmacéuticos y de otro tipo, la longevidad del EDTA puede plantear problemas graves en el medio ambiente. La degradación del EDTA es lenta. Ocurre principalmente de forma abiótica en presencia de luz solar. [33]
El proceso más importante para la eliminación del EDTA de las aguas superficiales es la fotólisis directa en longitudes de onda inferiores a 400 nm. [34] Dependiendo de las condiciones de luz, la vida media de la fotólisis del hierro (III) EDTA en aguas superficiales puede variar desde 11,3 minutos hasta más de 100 horas. [35] La degradación del FeEDTA, pero no del EDTA en sí, produce complejos de hierro de triacetato (ED3A), diacetato (EDDA) y monoacetato (EDMA): el 92% de EDDA y EDMA se biodegrada en 20 horas, mientras que ED3A muestra una resistencia significativamente mayor. Muchas especies de EDTA ambientalmente abundantes (como Mg 2+ y Ca 2+ ) son más persistentes.
En muchas plantas de tratamiento de aguas residuales industriales , la eliminación del EDTA se puede lograr en aproximadamente un 80% utilizando microorganismos . [36] Los subproductos resultantes son ED3A y ácido iminodiacético (IDA), lo que sugiere que tanto el grupo principal como el acetilo fueron atacados. Incluso se ha descubierto que algunos microorganismos forman nitratos a partir de EDTA, pero funcionan de manera óptima en condiciones moderadamente alcalinas de pH 9,0 a 9,5. [37]
Varias cepas bacterianas aisladas de plantas de tratamiento de aguas residuales degradan eficazmente el EDTA. Las cepas específicas incluyen Agrobacterium radiobacter ATCC 55002 [38] y las subramas de Pseudomonadota como BNC1, BNC2, [39] y la cepa DSM 9103. [40] Las tres cepas comparten propiedades similares de respiración aeróbica y se clasifican como bacterias gramnegativas. . A diferencia de la fotólisis, la especie quelada no es exclusiva del hierro (III) para poder ser degradada. Más bien, cada cepa consume de forma única distintos complejos de metal-EDTA a través de varias vías enzimáticas. Agrobacterium radiobacter solo degrada Fe (III) EDTA [39], mientras que BNC1 y DSM 9103 no son capaces de degradar hierro (III) EDTA y son más adecuados para complejos de calcio , bario , magnesio y manganeso (II) . [41] Los complejos de EDTA requieren disociación antes de la degradación.
El interés en la seguridad ambiental ha generado preocupaciones sobre la biodegradabilidad de los aminopolicarboxilatos como el EDTA. Estas preocupaciones incentivan la investigación de aminopolicarboxilatos alternativos. [33] Los agentes quelantes candidatos incluyen ácido nitrilotriacético (NTA), ácido iminodisuccínico (IDS), ácido poliaspártico , ácido S,S -etilendiamina - N , N ′-disuccínico (EDDS) , ácido metilglicinadiacético (MGDA) y ácido L -glutámico. Sal tetrasódica del ácido N , N -diacético (GLDA). [42]
Utilizado comercialmente desde 1998, el ácido iminodisuccínico (IDS) se biodegrada aproximadamente en un 80% después de sólo 7 días. IDS se une excepcionalmente bien al calcio y forma compuestos estables con otros iones de metales pesados. Además de tener una menor toxicidad después de la quelación, el IDS es degradado por Agrobacterium tumefaciens (BY6), que puede recolectarse a gran escala. Las enzimas implicadas, IDS epimerasa y C-N liasa , no requieren ningún cofactor . [43]
El ácido poliaspártico , como el IDS, se une al calcio y otros iones de metales pesados. Tiene muchas aplicaciones prácticas, incluidos inhibidores de corrosión, aditivos para aguas residuales y polímeros agrícolas. Un detergente para ropa a base de ácido poliaspártico fue el primer detergente para ropa del mundo en recibir la etiqueta ecológica floral de la UE . [44] La capacidad de unión al calcio del ácido poliaspártico se ha aprovechado para dirigir los nanoportadores cargados de fármacos al hueso. [45] La preparación de hidrogeles a base de ácido poliaspártico, en una variedad de formas físicas que van desde fibra hasta partículas , puede permitir potencialmente una fácil separación de los iones quelados de una solución. [46] Por lo tanto, a pesar de ser más débil que el EDTA, el ácido poliaspártico aún puede considerarse una alternativa viable debido a estas características, así como a su biocompatibilidad y biodegradabilidad . [47]
Un isómero estructural del EDTA, el ácido etilendiamino -N , N' -disuccínico (EDDS), es fácilmente biodegradable a un ritmo elevado en su forma S , S. [48]
Alaninato de dicarboximetilo trisódico , también conocido como ácido metilglicinadiacético (MGDA), tiene una alta tasa de biodegradación, superior al 68%, pero a diferencia de muchos otros agentes quelantes, puede degradarse sin la ayuda de bacterias adaptadas. Además, a diferencia de EDDS o IDS, MGDA puede soportar temperaturas más altas manteniendo una alta estabilidad y todo el rango de pH. [ cita necesaria ] MGDA ha demostrado ser un agente quelante eficaz, con una capacidad de movilización comparable a la del ácido nitrilotriacético (NTA), con aplicación al agua para uso industrial y para la eliminación del oxalato cálcico de la orina de pacientes con problemas renales. piedras . [49]
El método más sensible para detectar y medir EDTA en muestras biológicas es la espectrometría de masas por electroforesis capilar de control de reacción seleccionada (SRM-CE/MS), que tiene un límite de detección de 7,3 ng/ml en plasma humano y un límite de cuantificación de 15 ng/ml. . [50] Este método funciona con volúmenes de muestra tan pequeños como 7 a 8 nL. [50]
El EDTA también se ha medido en bebidas no alcohólicas mediante cromatografía líquida de alta resolución (HPLC) a un nivel de 2,0 μg/ml. [51] [52]
En la película Blade (1998), el EDTA se utiliza como arma para matar vampiros y explota cuando entra en contacto con la sangre del vampiro. [53]