La fiebre aftosa ( FA ) o fiebre aftosa ( EHM ) es una enfermedad viral infecciosa y en ocasiones mortal que afecta a los animales ungulados , incluidos los bóvidos domésticos y salvajes . [1] [2] El virus causa fiebre alta que dura de dos a seis días, seguida de ampollas dentro de la boca y cerca de la pezuña que pueden romperse y causar cojera .
La fiebre aftosa tiene implicaciones muy graves para la ganadería , ya que es altamente infecciosa y puede ser transmitida por animales infectados con relativa facilidad a través del contacto con equipos, vehículos, ropa y piensos agrícolas contaminados, y por depredadores domésticos y salvajes . [3] Su contención exige esfuerzos considerables en materia de vacunación , vigilancia estricta, restricciones comerciales , cuarentenas y sacrificio de animales tanto infectados como sanos (no infectados).

Los animales susceptibles incluyen ganado vacuno , búfalos de agua , ovejas , cabras , cerdos , [4] [5] antílopes , ciervos y bisontes . También se sabe que infecta a erizos y elefantes ; [3] [6] las llamas y alpacas pueden desarrollar síntomas leves, pero son resistentes a la enfermedad y no la transmiten a otras personas de la misma especie. [3] En experimentos de laboratorio, ratones , ratas y pollos han sido infectados artificialmente, pero no se cree que contraigan la enfermedad en condiciones naturales. [3] El ganado vacuno, los búfalos asiáticos y africanos, las ovejas y las cabras pueden convertirse en portadores después de una infección aguda, lo que significa que todavía están infectados con una pequeña cantidad de virus pero parecen sanos. Los animales pueden ser portadores hasta por 1 o 2 años y se considera muy poco probable que infecten a otros animales, aunque la evidencia de laboratorio sugiere que la transmisión a través de portadores es posible. [7] [8]
Los seres humanos son muy raramente infectados por el virus de la fiebre aftosa (FMDV) . (Los seres humanos, especialmente los niños pequeños, pueden verse afectados por la enfermedad de manos, pies y boca (HFMDV), que a menudo se confunde con el virus de la fiebre aftosa. De manera similar, el HFMDV es una infección viral que pertenece a la familia Picornaviridae, pero es distinta del virus de la fiebre aftosa. también afecta al ganado vacuno, ovino y porcino [9] )
El virus responsable de la fiebre aftosa es un aftovirus , el virus de la fiebre aftosa . La infección ocurre cuando la partícula del virus ingresa a una célula del huésped. Luego, la célula se ve obligada a fabricar miles de copias del virus y, finalmente, estalla, liberando las nuevas partículas en la sangre. El virus es genéticamente muy variable, [10] lo que limita la eficacia de la vacunación. La enfermedad se documentó por primera vez en 1870.
El período de incubación del virus de la fiebre aftosa oscila entre uno y 12 días. [11] [12] La enfermedad se caracteriza por fiebre alta que disminuye rápidamente después de dos o tres días, ampollas dentro de la boca que provocan una secreción excesiva de saliva fibrosa o espumosa y babeo, y ampollas en los pies que pueden romperse y causar cojera. [4] [13] Los animales adultos pueden sufrir una pérdida de peso de la que no se recuperan durante varios meses, así como hinchazón en los testículos de los machos maduros, y la producción de leche de las vacas puede disminuir significativamente. Aunque la mayoría de los animales finalmente se recuperan de la fiebre aftosa, la enfermedad puede provocar miocarditis (inflamación del músculo cardíaco) [14] y la muerte, especialmente en animales recién nacidos. Algunos rumiantes infectados siguen siendo portadores asintomáticos , pero aun así son portadores del virus y pueden transmitirlo a otros. Los cerdos no pueden actuar como portadores asintomáticos. [15]
Las infecciones subclínicas (asintomáticas) se pueden clasificar como neotéricas o persistentes según cuándo ocurren y si el animal es infeccioso. Las infecciones subclínicas neotéricas son infecciones agudas, lo que significa que ocurren poco después de que un animal está expuesto al virus de la fiebre aftosa (aproximadamente 1 a 2 días) y duran aproximadamente de 8 a 14 días. [16] Las infecciones agudas se caracterizan por un alto grado de replicación del virus en la faringe . En una infección subclínica neotérica, el virus permanece en la faringe y no se propaga a la sangre como lo haría en una infección clínica. Aunque los animales con infecciones subclínicas neotéricas no parecen tener la enfermedad, eliminan cantidades sustanciales de virus en las secreciones nasales y la saliva, por lo que pueden transmitir el virus de la fiebre aftosa a otros animales. Las infecciones subclínicas neotéricas ocurren a menudo en animales vacunados, pero también pueden ocurrir en animales no vacunados. [7]
La infección subclínica persistente (también conocida como estado de portador) ocurre cuando un animal se recupera de una infección aguda pero continúa teniendo una pequeña cantidad de virus en replicación presente en la faringe. El ganado vacuno, los búfalos, las ovejas y las cabras pueden convertirse en portadores, pero los cerdos no. [7] [17] [18] [19] Los animales pueden convertirse en portadores después de infecciones agudas con o sin síntomas. Tanto los animales vacunados como los no vacunados pueden convertirse en portadores. [19] La transmisión del virus de la fiebre aftosa de portadores a animales susceptibles se considera muy improbable en condiciones naturales y no se ha demostrado de manera concluyente en estudios de campo.
Sin embargo, en un experimento en el que se recogió virus de la faringe de ganado portador y se insertó en la faringe de ganado susceptible, el ganado susceptible se infectó y desarrolló ampollas características en la boca y las patas. [8] Esto respalda la teoría de que, si bien la probabilidad de que un portador propague la fiebre aftosa es bastante baja, no es imposible. No se comprende del todo por qué los rumiantes, pero no los cerdos, pueden convertirse en portadores o por qué algunos animales desarrollan una infección persistente mientras que otros no. Ambas son áreas de estudio continuo.
Dado que los animales vacunados pueden convertirse en portadores, el período de espera para demostrar que están libres de fiebre aftosa es más largo cuando se utiliza la vacunación en lugar del sacrificio como estrategia de control de brotes. Como resultado, muchos países libres de fiebre aftosa se resisten a la vacunación de emergencia en caso de un brote, debido a la preocupación por las graves implicaciones comerciales y económicas de un período prolongado sin el estatus de libres de fiebre aftosa. [7]
Aunque se considera que el riesgo de transmisión de un portador individual de fiebre aftosa es muy bajo, hay muchos portadores en regiones endémicas de fiebre aftosa, lo que posiblemente aumenta el número de posibilidades de que se produzca la transmisión por portador. Además, puede ser difícil determinar si una infección asintomática es neotérica o persistente en el campo, ya que ambos serían animales aparentemente sanos que dan positivo al virus de la fiebre aftosa. Este hecho complica el control de la enfermedad, ya que los dos tipos de infecciones subclínicas tienen riesgos significativamente diferentes de propagar la enfermedad. [7]
De los siete serotipos [20] de este virus, A, C, O, Asia 1 y SAT3 parecen ser linajes distintos; SAT 1 y SAT 2 son clados no resueltos. [21] Se ha estimado que la tasa de mutación de las secuencias codificantes de proteínas de las cepas aisladas entre 1932 y 2007 es de 1,46 × 10 −3 sustituciones/sitio/año, una tasa similar a la de otros virus de ARN. El ancestro común más reciente parece haber evolucionado hace unos 481 años (principios del siglo XVI). Este ancestro luego se dividió en dos clados que han dado lugar a los clados euroasiático y sudafricano circulantes existentes. SAT 1 divergió primero hace 397 años, seguido de la divergencia secuencial del serotipo SAT 2 (hace 396 años), A (hace 147 años), O (hace 121 años), Asia 1 (hace 89 años), C (hace 86 años). y SAT 3 (hace 83 años). El gráfico bayesiano del horizonte revela una expansión de la población a principios del siglo XX seguida de una rápida disminución del tamaño de la población desde finales del siglo XX hasta la actualidad. Dentro de cada serotipo, no hubo influencia aparente periódica, geográfica o de la especie huésped en la evolución de los virus globales de la fiebre aftosa. Se conocen al menos siete genotipos del serotipo Asia 1. [22]
El virus de la fiebre aftosa se puede transmitir de varias maneras, incluido el contacto cercano, la propagación de animal a animal, la propagación por aerosoles a larga distancia y fómites u objetos inanimados, generalmente forrajes y vehículos de motor. La ropa y la piel de los cuidadores de animales, como los granjeros, el agua estancada y los restos de comida cruda y los complementos alimenticios que contienen productos animales infectados también pueden albergar el virus. Las vacas también pueden contraer la fiebre aftosa a través del semen de toros infectados. Las medidas de control incluyen la cuarentena y destrucción del ganado infectado y sano (no infectado), y la prohibición de exportar carne y otros productos animales a países no infectados con la enfermedad. [ cita necesaria ]
Existe una variación significativa tanto en la susceptibilidad a la infección como en la capacidad de propagar enfermedades entre diferentes especies, cepas de virus y rutas de transmisión. Por ejemplo, el ganado vacuno es mucho más vulnerable que los cerdos a la infección con virus en aerosol, y los cerdos infectados producen 30 veces más cantidad de virus en aerosol en comparación con el ganado vacuno y ovino infectado. [23] [24] Además, los cerdos son particularmente vulnerables a la infección por vía oral. [25] Se ha demostrado experimentalmente que la fiebre aftosa se puede transmitir a los cerdos cuando comen productos alimenticios comerciales contaminados por el virus de la fiebre aftosa. Además, el virus puede permanecer activo durante períodos prolongados en ciertos ingredientes de los piensos, especialmente en la harina de soja. Las prácticas de bioseguridad de los piensos se han convertido en un importante área de estudio desde un brote de virus de la diarrea epidémica porcina (PEDV) en 2013 en los EE. UU., que se cree que se introdujo a través de piensos contaminados. [26]
Así como los humanos pueden transmitir la enfermedad al portar el virus en su ropa y cuerpo, los animales que no son susceptibles a la enfermedad aún pueden ayudar a propagarla. Este fue el caso de Canadá en 1952, cuando un brote volvió a estallar después de que los perros se llevaran huesos de animales muertos. [3] Se cree que los lobos desempeñan un papel similar en la antigua Unión Soviética . [27]
Daniel Rossouw Kannemeyer (1843-1925) publicó una nota en Transactions of the South African Philosophical Society, volumen 8, parte 1, en la que vincula las langostas cubiertas de saliva con la propagación de la enfermedad. [28]
La transmisión del virus de la fiebre aftosa es posible antes de que un animal presente signos aparentes de enfermedad, un factor que aumenta el riesgo de que se haya producido una propagación significativa del virus antes de que se detecte un brote. Un experimento realizado en 2011 midió el tiempo de transmisión en ganado infectado con el virus del serotipo O exponiendo al ganado susceptible en incrementos de 24 horas. Se estimó que el período infeccioso del ganado infectado era de 1,7 días, pero demostró que el ganado sólo era infeccioso durante unas pocas horas antes de desarrollar fiebre o lesiones clásicas de fiebre aftosa. Los autores también demostraron que se habría estimado que el período infeccioso sería mucho mayor (4,2 a 8,2 días) si la detección del virus se hubiera utilizado como sustituto de la infecciosidad. [29] Un experimento similar realizado en 2016 utilizando el virus del serotipo A expuso a cerdos susceptibles a cerdos infectados durante períodos de 8 horas y descubrió que los cerdos podían transmitir la enfermedad durante un día completo antes de desarrollar signos de enfermedad. [30] El análisis de estos datos experimentales estimó que el período infeccioso fue de aproximadamente 7 días. [31] Una vez más, el estudio demostró que la detección del virus no era una sustitución precisa de la infecciosidad. Una comprensión precisa de los parámetros de infecciosidad es un componente importante en la construcción de modelos epidemiológicos que sirvan de base para las estrategias y políticas de control de enfermedades.
Los humanos pueden infectarse con fiebre aftosa a través del contacto con animales infectados, pero esto es extremadamente raro. [32] Algunos casos fueron causados por accidentes de laboratorio. Debido a que el virus que causa la fiebre aftosa es sensible al ácido del estómago, no puede transmitirse a los humanos mediante el consumo de carne infectada, excepto en la boca antes de tragarla. En el Reino Unido, el último caso humano confirmado ocurrió en 1966, [33] [34] y sólo se han registrado unos pocos casos más en países de Europa continental , África y América del Sur. Los síntomas de la fiebre aftosa en humanos incluyen malestar, fiebre, vómitos, lesiones ulcerosas rojas (puntos dañados que erosionan la superficie) de los tejidos bucales y, a veces, lesiones vesiculares (pequeñas ampollas) de la piel. Según un informe periodístico, la fiebre aftosa mató a dos niños en Inglaterra en 1884, supuestamente debido a la leche infectada. [35]
Otra enfermedad viral con síntomas similares, la enfermedad de manos, pies y boca , se presenta con mayor frecuencia en humanos, especialmente en niños pequeños; la causa, el virus Coxsackie A , es diferente del virus de la fiebre aftosa. Los virus Coxsackie pertenecen a los enterovirus dentro de Picornaviridae . [ cita necesaria ]
Debido a que la fiebre aftosa rara vez infecta a los humanos, pero se propaga rápidamente entre los animales, es una amenaza mucho mayor para la industria agrícola que para la salud humana. [ cita necesaria ]
Al igual que otros virus de ARN, el virus de la fiebre aftosa evoluciona y muta continuamente, por lo que una de las dificultades para vacunar contra él es la enorme variación entre los serotipos, e incluso dentro de ellos . No se ha observado protección cruzada entre serotipos (una vacuna para un serotipo no protegerá contra ningún otro) y, además, dos cepas dentro de un serotipo determinado pueden tener secuencias de nucleótidos que difieren hasta en un 30% para un gen determinado. Esto significa que las vacunas contra la fiebre aftosa deben ser muy específicas para la cepa involucrada. La vacunación sólo proporciona inmunidad temporal que dura de meses a años.
Actualmente, la Organización Mundial de Sanidad Animal reconoce que los países se encuentran en uno de tres estados patológicos con respecto a la fiebre aftosa: fiebre aftosa presente con o sin vacunación, libre de fiebre aftosa con vacunación y libre de fiebre aftosa sin vacunación. [36] Los países designados libres de fiebre aftosa sin vacunación tienen el mayor acceso a los mercados de exportación, por lo que muchas naciones desarrolladas, incluidos Canadá, Estados Unidos y el Reino Unido, trabajan arduamente para mantener su estatus actual. Algunos países como Brasil y Argentina , que tienen grandes industrias exportadoras de carne vacuna, practican la vacunación en algunas zonas, pero tienen otras zonas libres de vacunación.
Las razones citadas para restringir las exportaciones de los países que utilizan vacunas contra la fiebre aftosa incluyen, probablemente la más importante, que los análisis de sangre de rutina que se basan en anticuerpos no pueden distinguir entre un animal infectado y uno vacunado, [37] lo que dificulta gravemente la detección de los animales utilizados en los productos de exportación, con el riesgo de una propagación de la enfermedad. fiebre aftosa a los países importadores. Una vacunación preventiva generalizada también ocultaría la existencia del virus en un país. A partir de ahí, podría extenderse a países sin programas de vacunas. Por último, un animal infectado poco después de haber sido vacunado puede albergar y propagar la fiebre aftosa sin mostrar síntomas, lo que dificulta la contención y el sacrificio de los animales enfermos como remedio.
Muchas de las primeras vacunas utilizaron muestras muertas del virus de la fiebre aftosa para inocular animales, pero esas primeras vacunas a veces causaron brotes reales. En la década de 1970, los científicos descubrieron que se podía fabricar una vacuna utilizando sólo una proteína clave del virus. La tarea consistía en producir cantidades suficientes de proteína para utilizarla en la vacunación. El 18 de junio de 1981, el gobierno de Estados Unidos anunció la creación de una vacuna dirigida contra la fiebre aftosa, la primera vacuna genéticamente modificada del mundo .
El Banco Norteamericano de Vacunas contra la Fiebre Aftosa está ubicado en el Laboratorio de Diagnóstico de Enfermedades Animales Exóticas del Departamento de Agricultura de los Estados Unidos en el Centro de Enfermedades Animales de Plum Island . El centro, ubicado a 2,4 km de la costa de Long Island, Nueva York, es el único lugar en los Estados Unidos donde los científicos pueden realizar investigaciones y trabajos de diagnóstico sobre enfermedades animales altamente contagiosas como la fiebre aftosa. Debido a esta limitación, las empresas estadounidenses que trabajan con la fiebre aftosa suelen utilizar instalaciones en otros países donde dichas enfermedades son endémicas.

Estados Unidos ha tenido nueve brotes de fiebre aftosa desde que se reconoció por primera vez en la costa noreste en 1870; [38] la más devastadora ocurrió en 1914. Originaria de Michigan , pero su entrada en los corrales de Chicago la convirtió en una epizootia . Alrededor de 3.500 rebaños de ganado resultaron infectados en todo Estados Unidos, con un total de más de 170.000 cabezas de ganado vacuno, ovino y porcino. La erradicación tuvo un costo de 4,5 millones de dólares (equivalente a 131 millones de dólares en 2022).
Un brote en California en 1924 resultó no sólo en la matanza de 109.000 animales de granja, sino también de 22.000 ciervos .
Estados Unidos tuvo su último brote de fiebre aftosa en Montebello, California , en 1929. Este brote se originó en cerdos que habían comido restos de carne infectada de un barco de vapor turístico que había almacenado carne en Argentina. Se sacrificaron más de 3.600 animales y la enfermedad quedó contenida en menos de un mes. [39] [40]
El 26 de diciembre de 1946, Estados Unidos y México declararon conjuntamente que se había encontrado fiebre aftosa en México. Inicialmente, las propuestas de los texanos eran para un muro a prueba de animales, para evitar que los animales cruzaran la frontera y propagaran la enfermedad, pero los dos países finalmente lograron cooperar en un esfuerzo bilateral y erradicaron la enfermedad sin construir un muro. Para evitar tensiones entre los ganaderos y los veterinarios, se utilizaron transmisiones públicas por radio y con parlantes en los camiones para informar a los ganaderos mexicanos por qué los veterinarios estadounidenses estaban trabajando en su ganado. Los ganaderos que perdieran ganado debido al sacrificio de los veterinarios recibirían una compensación económica. Sin embargo, la tensión persistió y provocó enfrentamientos entre los ciudadanos locales y los veterinarios estadounidenses protegidos por el ejército. Estos equipos de veterinarios trabajaron desde fuera de la zona de infección de la enfermedad y se abrieron camino hasta el corazón de la epidemia. A finales de 1950 se administraron más de 60.000.000 de inyecciones al ganado. [41] [42]
En octubre de 1967, un granjero de Shropshire informó sobre una cerda coja, a la que más tarde se le diagnosticó fiebre aftosa. Se creía que la fuente eran restos de cordero infectado importado legalmente de Argentina y Chile. El virus se propagó y, en total, se sacrificaron 442.000 animales y el brote tuvo un coste estimado de 370 millones de libras esterlinas (equivalente a 7.000 millones de libras esterlinas en 2021). [ cita necesaria ]

Taiwán tuvo epidemias anteriores de fiebre aftosa en 1913–14 y 1924–29, pero desde entonces se había salvado [44] y se consideraba libre de fiebre aftosa hasta la década de 1990. El 19 de marzo de 1997, a una cerda de una granja de Hsinchu , Taiwán , se le diagnosticó una cepa de fiebre aftosa que sólo infecta a los cerdos. La mortalidad fue alta, cercana al 100% en el rebaño infectado. No se determinó la causa de la epidemia, pero la granja estaba cerca de una ciudad portuaria conocida por su industria de contrabando de cerdos y mataderos ilegales. Por lo tanto, los cerdos de contrabando o la carne contaminada son fuentes probables de la enfermedad.
La enfermedad se propagó rápidamente entre las piaras de cerdos de Taiwán, infectándose diariamente entre 200 y 300 nuevas granjas. Las causas de esto incluyen la alta densidad porcina en la zona, con hasta 6.500 cerdos por milla cuadrada, la alimentación de los cerdos con basura no tratada y la proximidad de las granjas a los mataderos. Contribuyeron a ello otros problemas sistémicos, como la falta de instalaciones de laboratorio, la lentitud de la respuesta y la falta inicial de un programa de vacunación.
Un factor que complica la situación es la propagación endémica de la enfermedad vesicular porcina (EVP) en Taiwán. Los síntomas son indistinguibles de los de la fiebre aftosa, lo que puede haber llevado a un diagnóstico erróneo previo de la fiebre aftosa como enfermedad vesicular porcina. Rara vez se utilizaban análisis de laboratorio para el diagnóstico, por lo que es posible que la fiebre aftosa haya pasado desapercibida durante algún tiempo.
La despoblación porcina fue una tarea enorme, y los militares contribuyeron con una mano de obra sustancial. En su máxima capacidad, se eliminaban 200.000 cerdos por día, principalmente mediante electrocución . Los cadáveres se eliminaban mediante quema y entierro, pero se evitaba la quema en las zonas de protección de los recursos hídricos. En abril, las incineradoras industriales funcionaban las 24 horas del día para eliminar los cadáveres.
Inicialmente estaban disponibles 40.000 dosis de vacunas combinadas para las cepas O-1, A-24 y Asia-1, que se administraron a animales del zoológico y a valiosos cerdos reproductores. A finales de marzo se pusieron a disposición medio millón de nuevas dosis para O-1 y Asia-1. El 3 de mayo llegaron 13 millones de dosis de la vacuna O-1 y los envíos de marzo y mayo se distribuyeron gratuitamente. Ante el peligro de que los equipos de vacunación propagaran la enfermedad, sólo los agricultores capacitados podían administrar la vacuna bajo supervisión veterinaria.
Taiwán había sido anteriormente el principal exportador de carne de cerdo a Japón, [45] y entre los 15 principales productores de carne de cerdo del mundo en 1996. [46] Durante el brote, más de 3,8 millones de cerdos fueron destruidos a un costo de 6.900 millones de dólares (equivalente a a 12.600 millones de dólares en 2022). Como resultado, la industria porcina taiwanesa quedó devastada y el mercado de exportación quedó en ruinas. [39] [47] En 2007, Taiwán se consideraba libre de fiebre aftosa, pero todavía estaba llevando a cabo un programa de vacunación que restringe la exportación de carne de Taiwán.
La epidemia de fiebre aftosa en el Reino Unido en la primavera y el verano de 2001 fue causada por la cepa de la enfermedad "Tipo O panasiático". [48] Este episodio provocó más de 2.000 casos de la enfermedad en granjas de toda la campiña británica. Más de seis millones de ovejas y vacas fueron sacrificadas en un intento finalmente exitoso de detener la enfermedad. [49] El condado de Cumbria fue la zona más gravemente afectada del país, con 843 casos. Cuando se detuvo la enfermedad en octubre de 2001, se estimaba que la crisis le había costado a Gran Bretaña £8 mil millones (equivalente a £14 mil millones en 2021) [49] a las industrias agrícolas y de apoyo, y a la industria al aire libre. Lo que hizo que este brote fuera tan grave fue el tiempo transcurrido entre la aparición de la infección en el primer lugar del brote y el momento en que se pusieron en marcha contramedidas contra la enfermedad, como prohibiciones de transporte y lavado con detergente tanto de los vehículos como del personal que ingresaba a las zonas ganaderas. La epidemia probablemente fue causada por cerdos que habían sido alimentados con basura infectada que no había sido esterilizada térmicamente adecuadamente. Además, se cree que la basura contenía restos de carne infectada que había sido importada ilegalmente a Gran Bretaña. [50]
En abril de 2005, apareció una cepa Asia-1 de fiebre aftosa en las provincias orientales de Shandong y Jiangsu . Durante abril y mayo, se extendió a los suburbios de Beijing, la provincia norteña de Hebei y la región autónoma de Xinjiang en el noroeste de China . El 13 de mayo, China informó del brote de fiebre aftosa a la Organización Mundial de la Salud y a la OIE. Esta fue la primera vez que China admitió públicamente tener fiebre aftosa. [51] [52] China todavía informa brotes de fiebre aftosa. En 2007, informes presentados ante la OIE documentaron brotes nuevos o en curso en las provincias de Gansu , Qinghai y Xinjiang . Esto incluyó informes de yaks domésticos que mostraban signos de infección. [53] La fiebre aftosa es endémica en las regiones pastorales de China, desde la provincia de Heilongjiang en el noreste hasta la provincia de Sichuan y la región autónoma tibetana en el suroeste. Los informes de los medios nacionales chinos a menudo utilizan el eufemismo "Enfermedad número cinco" (五号病wǔhàobìng ) en lugar de fiebre aftosa en los informes debido a la sensibilidad del tema de la fiebre aftosa. En marzo de 2010, Southern Rural News ( Nanfang Nongcunbao ), en un artículo "Rompiendo el tabú de la fiebre aftosa", señaló que la fiebre aftosa ha sido encubierta durante mucho tiempo en China al referirse a ella de esa manera. [54] La fiebre aftosa también se llama cancro (口疮, literalmente "úlceras bucales" kǒuchuāng ) o ictericia de las pezuñas (蹄癀tíhuáng ) en China, por lo que se puede encontrar información sobre la fiebre aftosa en China utilizando esas palabras como términos de búsqueda. [55] Se pueden encontrar en línea muchas órdenes y regulaciones provinciales sobre el control de la fiebre aftosa anteriores al reconocimiento de China de que la enfermedad existía en China, por ejemplo, la regulación de 1991 de la Región Autónoma Zhuang de Guangxi sobre la prevención de la propagación de la Enfermedad No.5. [56]
El Departamento de Medio Ambiente, Alimentación y Asuntos Rurales confirmó una infección de fiebre aftosa en el Reino Unido , el 3 de agosto de 2007, en unas tierras agrícolas situadas en Normandía , Surrey. [57] [58] Todo el ganado de los alrededores fue sacrificado el 4 de agosto. Se impuso una prohibición a nivel nacional sobre el movimiento de ganado vacuno y porcino, con una zona de protección de 3 km (1,9 millas) alrededor de los sitios del brote y los establecimientos cercanos de investigación de virus y producción de vacunas, junto con una zona de protección de 10 km (6,2 millas). ) zona de mayor vigilancia. [59]
El 4 de agosto, la cepa del virus fue identificada como un virus "similar a 01 BFS67", vinculado a vacunas y que normalmente no se encuentra en animales, y se aisló en el brote de 1967. [60] La misma cepa se utilizó en el cercano Instituto de Salud Animal y Merial Animal Health Ltd en Pirbright , a 2,5 millas (4,0 km) de distancia, que es una instalación de fabricación de vacunas BSL-4 de propiedad estadounidense y francesa, y fue identificada como la fuente probable de infección. [61]
El 12 de septiembre, se confirmó un nuevo brote de la enfermedad en Egham , Surrey , a 19 km (12 millas) del brote original, [62] y se confirmó un segundo caso en una granja cercana el 14 de septiembre. [63]
Estos brotes provocaron el sacrificio de todos los animales en riesgo en el área que rodea a Egham, incluidas dos granjas cercanas al famoso hotel de cuatro estrellas Great Fosters . Estos brotes también provocaron el cierre de Windsor Great Park debido a que el parque contenía ciervos; el parque permaneció cerrado durante tres meses. El 19 de septiembre de 2007, se descubrió un caso sospechoso de fiebre aftosa en Solihull , donde Defra creó una zona de control temporal .
En abril de 2010, un informe sobre tres incursiones de fiebre aftosa en Japón y Corea del Sur llevó a la Organización de las Naciones Unidas para la Alimentación y la Agricultura (FAO) a hacer un llamamiento para una mayor vigilancia mundial. Las autoridades veterinarias de Japón confirmaron un brote del virus de la fiebre aftosa tipo O, actualmente más común en los países asiáticos donde la fiebre aftosa es endémica.
Corea del Sur se vio afectada por la fiebre aftosa tipo A, más rara, en enero, y luego por la infección tipo O, en abril. [64] El caso más grave de brote de fiebre aftosa en la historia de Corea del Sur comenzó en noviembre de 2010 en granjas de cerdos en la ciudad de Gyeongsangbuk-do , en Andong , y desde entonces se ha extendido rápidamente por el país. [65] [66] Hasta ahora se han confirmado más de 100 casos de la enfermedad en el país, [65] y en enero de 2011, los funcionarios surcoreanos iniciaron un sacrificio masivo de aproximadamente el 12%, o alrededor de tres millones en total, de toda la población porcina doméstica, y 107.000 de los tres millones de cabezas de ganado del país para frenar el brote. [65] Según el informe basado en secuencias completas del gen 1D, el virus del serotipo A coreano estaba relacionado con los de Laos. Los virus coreanos del serotipo O se dividieron en tres clados y estaban estrechamente relacionados con aislados de Japón, Tailandia, el Reino Unido, Francia, Irlanda, Sudáfrica y Singapur, así como con Laos. [67]
El 10 de febrero de 2011, Corea del Norte informó de un brote que afectaba a los cerdos en la región alrededor de Pyongyang , que para entonces estaba en curso desde al menos diciembre de 2010. Los esfuerzos para controlar el brote se vieron obstaculizados por las ventas ilícitas de carne infectada. [68]
La fiebre aftosa, erradicada en 1986, se volvió a detectar en Indonesia en mayo de 2022. El gobierno australiano ha ofrecido su ayuda, pero sigue indiferente, considerando que el riesgo para la bioseguridad del país es bajo. El Departamento de Agricultura (DAWE) es el organismo responsable y ha estado siguiendo la situación. DAWE ha determinado que el riesgo es bajo y, de todos modos, ha almacenado vacunas desde 2004. [69] [70]
En respuesta al brote en Indonesia, las autoridades australianas comenzaron a controlar paquetes y equipajes procedentes de Indonesia y China. También se instalaron tapetes desinfectantes en los aeropuertos australianos para limpiar el calzado. El Gobierno albanés rechazó los llamamientos de los partidos de la oposición para cerrar la frontera a los viajes desde Indonesia. Además, las autoridades de Nueva Zelanda prohibieron a los viajeros de Indonesia traer productos cárnicos, equipaje revisado desde Indonesia e instalar tapetes en el piso. La Primera Ministra de Nueva Zelanda, Jacinda Ardern, y el Ministro de Bioseguridad, Damien O'Connor, han expresado su preocupación por el impacto de la fiebre aftosa en las importantes poblaciones de ganado vacuno, ovino y porcino de Nueva Zelanda, así como en la vida silvestre. [71]
Friedrich Loeffler demostró por primera vez que la causa de la fiebre aftosa era viral en 1897 . Pasó la sangre de un animal infectado a través de un filtro Chamberland y descubrió que el líquido recolectado aún podría causar la enfermedad en animales sanos.
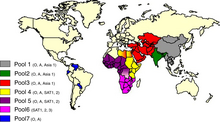
La fiebre aftosa ocurre en gran parte del mundo y, si bien algunos países han estado libres de la fiebre aftosa durante algún tiempo, su amplia gama de huéspedes y su rápida propagación representan motivo de preocupación internacional. Después de la Segunda Guerra Mundial , la enfermedad se distribuyó ampliamente por todo el mundo. En 1996, las áreas endémicas incluían Asia , África y partes de América del Sur ; A agosto de 2007, Chile se encuentra libre de la enfermedad, [72] y Uruguay y Argentina no han tenido un brote desde 2001. En mayo de 2014, la FAO informó que Bolivia , Colombia , Ecuador y Perú estaban "a sólo un paso" de la erradicación. ; [73] América del Norte y Australia han estado libres de fiebre aftosa durante muchos años. Nueva Zelanda nunca ha tenido un caso de fiebre aftosa. [74] La mayoría de los países europeos han sido reconocidos como libres de la enfermedad y los países pertenecientes a la Unión Europea han suspendido la vacunación contra la fiebre aftosa .
Sin embargo, en 2001, un grave brote de fiebre aftosa en Gran Bretaña provocó el sacrificio de numerosos animales, el aplazamiento de las elecciones generales durante un mes y la cancelación de numerosos acontecimientos deportivos y actividades de ocio, como el TT de la Isla de Man . Debido a las estrictas políticas gubernamentales sobre la venta de ganado, la desinfección de todas las personas que entran y salen de las granjas y la cancelación de grandes eventos a los que probablemente asistan los agricultores, se evitó en Irlanda una epizootia potencialmente desastrosa desde el punto de vista económico , [ cita necesaria ] con solo un caso grabado en Proleek, condado de Louth . Como resultado de ello, el Parlamento diseñó la Ley de Sanidad Animal de 2002 para otorgar a los reguladores más poderes para abordar la fiebre aftosa. [75] [76]
En agosto de 2007, se detectó fiebre aftosa en dos granjas de Surrey , Inglaterra. Todo el ganado fue sacrificado y se estableció una cuarentena en la zona. Desde entonces se han producido otros dos brotes sospechosos, aunque ahora no parecen estar relacionados con la fiebre aftosa. El único caso reportado en 2010 fue una falsa alarma de GIS Alex Baker, como lo demostró el Departamento Agrícola de Florida, y en junio se confirmó la cuarentena/sacrificio de ganado vacuno y porcino en la Prefectura de Miyazaki en Japón después de que tres vacas dieron positivo. Se ha ordenado el sacrificio de unas 270.000 cabezas de ganado tras el brote de la enfermedad.
En 2022, la enfermedad se volvió a observar en el ganado bovino de Indonesia. A otros países les preocupa que pronto se extienda a sus países. [77]
Las epidemias de fiebre aftosa han provocado el sacrificio de millones de animales infectados y sanos, a pesar de ser una enfermedad frecuentemente no mortal para los animales adultos (2-5% de mortalidad), aunque los animales jóvenes pueden tener una alta mortalidad. [78] El brote de Taiwán de 1997 que afectó sólo a los cerdos también mostró una alta mortalidad en los adultos. La destrucción de los animales tiene como objetivo principal detener una mayor propagación, ya que el crecimiento y la producción de leche pueden verse afectados permanentemente, incluso en animales que se han recuperado. Debido a los esfuerzos internacionales para erradicar la enfermedad, la infección también daría lugar a la imposición de prohibiciones comerciales a los países afectados. Los críticos de las políticas actuales de sacrificio de rebaños argumentan que el imperativo financiero debe equilibrarse con la matanza de muchos animales, en su mayoría sanos, [79] especialmente cuando una proporción significativa de los animales infectados, sobre todo los que producen leche, se recuperarían de la infección y vivirían. llevan una vida normal, aunque con una producción de leche reducida. Desde el punto de vista ético, también hay que considerar que la fiebre aftosa es una enfermedad dolorosa para los animales afectados. [80] Las vesículas y ampollas son dolorosas en sí mismas y restringen tanto la alimentación como el movimiento. A través de ampollas rotas, el animal corre el riesgo de sufrir infecciones bacterianas secundarias [80] y, en algunos casos, discapacidad permanente.
La relación entre los animales, los humanos y las enfermedades es parte de nuestra condición económica y social globalizada. Probabilidades estadísticamente mayores de zoonosis (enfermedad infecciosa que se transmite de animales no humanos a humanos) ocurren en áreas modificadas por humanos; particularmente tierras agrícolas. [81] [82] Las relaciones humanas y animales son mutuamente importantes para la salud y el bienestar y deben tenerse en cuenta en cualquier enfoque de control de la fiebre aftosa. En la producción animal occidental moderna, donde las epidemias resultan en el sacrificio masivo de ganado, el impacto psicológico para aquellos cuyos animales contraen la fiebre aftosa es inmenso y a menudo resulta en una devastación financiera para el granjero que no puede cumplir con los acuerdos contractuales existentes, enfrentándose así a las posibles consecuencias. pérdida de granja, equipo y potencial de ingresos futuros. Esto no se limita a granjas individuales, sino que se extiende a comunidades agrícolas más amplias, causando preocupaciones emocionales, psicológicas y ambientales a escala macro y puede amenazar la seguridad alimentaria a nivel internacional. [83] Debido a la devastación generalizada para quienes trabajan y viven en el sector agrícola, el costo humano, social y psicológico siempre debe considerarse dentro del marco biopolítico utilizado para gestionar la fiebre aftosa y otras enfermedades zoonóticas.
La mayor "carnificación" (aumento del consumo de carne en los patrones de consumo humano de alimentos) de los mercados globales, a través de prácticas capitalistas, postindustriales y agrícolas, deja de lado puntos de vista alternativos a la "narrativa de domesticación" dominante, que busca delimitar lo humano de lo no humano. . [84] Esto ha provocado justificaciones consecuencialistas para un mayor énfasis en los protocolos de bioseguridad impuestos por el estado para la doble regulación de los comportamientos humanos y animales. [84] Sin embargo, el impacto de las enfermedades (por ejemplo, la fiebre aftosa) en las estructuras sociales humanas, así como las consideraciones éticas relacionadas con el sacrificio masivo, continúa alineándose con el crecimiento del mercado, lo que aumenta la necesidad percibida de mayores protocolos regulatorios. [85]
Para reflejar los diversos puntos de vista y enfoques sobre la gestión de riesgos de enfermedades zoonóticas, un enfoque inclusivo y diverso producirá resultados más considerados y matizados. Al tratar de reducir la aparición de fiebre aftosa, los enfoques capitalistas implican calcular las probabilidades de riesgo de manera anticipada y esto rara vez se adapta a varios puntos de vista y a la conexión social que compartimos con los animales. [86] En lugar de una intervención reflexiva del Estado para sacrificar animales infectados o posiblemente infectados, la historia y los conceptos emergentes nos brindan formas nuevas y alternativas de enmarcar nuestras relaciones con los animales, lo que lleva a una mayor comprensión de los agricultores que psicológica y económicamente son los más afectados por el sacrificio. de manera diferente al consumidor final de la línea.
{{cite journal}}: Mantenimiento CS1: nombres numéricos: lista de autores ( enlace )