La vía de señalización Hedgehog es una vía de señalización que transmite información a las células embrionarias necesaria para la diferenciación celular adecuada . Diferentes partes del embrión tienen diferentes concentraciones de proteínas de señalización Hedgehog. La vía también tiene funciones en el adulto. Las enfermedades asociadas con el mal funcionamiento de esta vía incluyen el cáncer . [1] [2]
La vía de señalización Hedgehog es uno de los reguladores clave del desarrollo animal y está presente en todos los bilaterales . [3] La vía toma su nombre de su ligando polipeptídico , una molécula de señalización intracelular llamada Hedgehog ( Hh ) que se encuentra en las moscas de la fruta del género Drosophila ; se dice que las larvas de la mosca de la fruta que carecen del gen Hh se parecen a los erizos . Hh es uno de los productos del gen de polaridad de segmento de Drosophila , involucrado en el establecimiento de la base del plan corporal de la mosca . La molécula sigue siendo importante durante las etapas posteriores de la embriogénesis y la metamorfosis .
Los mamíferos tienen tres homólogos de Hedgehog, Desert (DHH) , Indian (IHH) y Sonic (SHH) , de los cuales Sonic es el mejor estudiado. La vía es igualmente importante durante el desarrollo embrionario de los vertebrados y, por lo tanto, es de interés en la biología del desarrollo evolutivo . En ratones knockout que carecen de componentes de la vía, el cerebro , el esqueleto , la musculatura , el tracto gastrointestinal y los pulmones no se desarrollan correctamente. Estudios recientes apuntan al papel de la señalización de Hedgehog en la regulación de las células madre adultas involucradas en el mantenimiento y la regeneración de los tejidos adultos . La vía también se ha implicado en el desarrollo de algunos cánceres . [1] Varias compañías farmacéuticas están desarrollando activamente medicamentos que se dirigen específicamente a la señalización de Hedgehog para combatir esta enfermedad .

En la década de 1970, un problema fundamental en la biología del desarrollo era entender cómo un huevo relativamente simple puede dar lugar a un plan corporal segmentado complejo . A finales de la década de 1970, Christiane Nüsslein-Volhard y Eric Wieschaus aislaron mutaciones en genes que controlan el desarrollo del eje corporal anterior-posterior segmentado de la mosca; [4] su técnica de "mutagénesis de saturación" resultó en el descubrimiento de un grupo de genes involucrados en el desarrollo de la segmentación corporal , ayudando a fundar el campo de la biología evolutiva del desarrollo . [5] En 1995, compartieron el Premio Nobel con Edward B. Lewis por su trabajo estudiando las mutaciones genéticas en la embriogénesis de Drosophila . [6]
El gen hedgehog ( hh ) de Drosophila fue identificado como uno de varios genes importantes para crear las diferencias entre las partes anterior y posterior de los segmentos corporales individuales. El gen hh de la mosca fue clonado independientemente en 1992 por los laboratorios de Jym Mohler, Philip Beachy , Thomas B. Kornberg y Saigo Kaoru. Algunos mutantes hedgehog dan como resultado embriones con forma anormal que son inusualmente cortos y rechonchos en comparación con los embriones de tipo salvaje . La función del gen de polaridad del segmento hedgehog se ha estudiado para determinar su influencia en la distribución normalmente polarizada de los dentículos cuticulares larvarios, así como en las características de los apéndices adultos, como las patas y las antenas. [7] En lugar del patrón normal de dentículos, las larvas mutantes hedgehog tienden a tener "céspedes sólidos" de dentículos (Figura 1). La apariencia de las larvas rechonchas y "peludas" inspiró el nombre ' hedgehog '.


Las células de insectos expresan un factor de transcripción de dedo de zinc de tamaño completo Cubitus interruptus (Ci), que forma un complejo con la proteína similar a la kinesina Costal-2 (Cos2) y se localiza en el citoplasma unido a los microtúbulos celulares (Figura 2). El complejo SCF se dirige a la proteína Ci de longitud completa de 155 kDa para la escisión dependiente del proteosoma , que genera un fragmento de 75 kDa (CiR). CiR se acumula en la célula y se difunde al núcleo , donde actúa como correpresor de los genes diana Hedgehog ( Hh ). [8] Los pasos que conducen a la proteólisis de la proteína Ci incluyen la fosforilación de la proteína Ci por varias proteínas quinasas ; PKA , GSK3β y CK1 (Figura 2). [9] La proteína Slimb de Drosophila es parte de un complejo SCF que se dirige a las proteínas para la ubiquitinación . Slimb se une a la proteína Ci fosforilada .
En ausencia de Hh (Figura 3), una proteína transmembrana de la superficie celular llamada Patched (PTCH) actúa para prevenir la alta expresión y actividad de un receptor que atraviesa la membrana 7 [10] llamado Smoothened (SMO). Patched tiene una similitud de secuencia con las proteínas de transporte de membrana conocidas. Cuando Hh extracelular está presente (Figura 3), se une a Patched e inhibe a Patched, lo que permite que Smoothened se acumule e inhiba la escisión proteolítica de la proteína Ci. Este proceso probablemente involucra la interacción directa de Smoothened y Costal-2 y puede involucrar el secuestro del complejo que contiene la proteína Ci a un microdominio donde se interrumpen los pasos que conducen a la proteólisis de la proteína Ci. [8] El mecanismo por el cual la unión de Hh a Patched conduce a mayores niveles de Smoothened no está claro (Paso 1 en la Figura 3). Después de la unión de Hh a Patched, los niveles de Smoothened aumentan en gran medida sobre el nivel mantenido en las células cuando Patched no está unido a Hh. [11] Se ha sugerido que la fosforilación de Smoothened juega un papel en la regulación dependiente de Hh de los niveles de Smoothened. [12]
En las células con Patched activado por Hh (Figura 3), la proteína Ci intacta se acumula en el citoplasma celular y los niveles de CiR disminuyen, lo que permite la transcripción de algunos genes como el decapentapléjico (dpp, un miembro de la familia de factores de crecimiento BMP ). Para otros genes regulados por Hh, la expresión requiere no solo la pérdida de CiR sino también la acción positiva de Ci no escindido para actuar como un activador transcripcional . [9] Costal-2 normalmente es importante para mantener la proteína Ci en el citoplasma, pero la interacción de Smoothened con Costal-2 permite que algo de proteína Ci intacta vaya al núcleo. La proteína Fused de Drosophila (Fu en la Figura 3) es una proteína quinasa que se une a Costal-2. Fused puede inhibir Suppressor of Fused (SUFU), que a su vez interactúa con Ci para regular la transcripción génica en algunos tipos de células. [13]
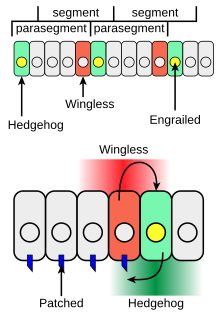
Hedgehog tiene funciones en el desarrollo de los segmentos corporales de las larvas y en la formación de los apéndices adultos. Durante la formación de los segmentos corporales en el embrión en desarrollo de Drosophila , las franjas de células que sintetizan el factor de transcripción engrailed también pueden expresar la proteína de señalización de célula a célula Hedgehog (verde en la Figura 4). Hedgehog no es libre de moverse muy lejos de las células que lo producen y, por lo tanto, solo activa una franja delgada de células adyacentes a las células que expresan engrailed. Cuando actúa de esta manera local, hedgehog funciona como un factor paracrino . Solo las células a un lado de las células que expresan engrailed son competentes para responder a Hedgehog después de la interacción de Hh con la proteína receptora Patched (azul en la Figura 4).
Las células con el receptor Patched activado por Hh sintetizan la proteína Wingless (en rojo en la Figura 4). Si se altera un embrión de Drosophila para que produzca Hh en todas sus células, todas las células competentes responden y forman una banda más amplia de células que expresan Wingless en cada segmento. El gen wingless tiene una región reguladora de la transcripción aguas arriba que se une al factor de transcripción Ci de una manera dependiente de Hh, lo que da como resultado un aumento de la transcripción wingless (interacción 2 en la Figura 3) en una franja de células adyacente a la franja de células productoras de Hh. [14]
La proteína Wingless actúa como una señal extracelular y modela las filas adyacentes de células activando su receptor de superficie celular Frizzled . Wingless actúa sobre las células que expresan engrailed para estabilizar las franjas de expresión de engrailed. Wingless es un miembro de la familia Wnt de proteínas de señalización de célula a célula. La señalización recíproca de Hedgehog y Wingless estabiliza el límite entre los parasegmentos (Figura 4, arriba). Los efectos de Wingless y Hedgehog sobre otras franjas de células en cada segmento establecen un código posicional que explica las características anatómicas distintivas a lo largo del eje anteroposterior de los segmentos. [15]
La proteína Wingless se denomina "wingless" debido al fenotipo de algunos mutantes de moscas sin alas . Wingless y Hedgehog funcionan juntas durante la metamorfosis para coordinar la formación de las alas. Hedgehog se expresa en la parte posterior de las extremidades en desarrollo de Drosophila . Hedgehog también participa en la coordinación del desarrollo de los ojos, el cerebro, las gónadas, el intestino y la tráquea. La regulación negativa de hedgehog se ha relacionado con la reducción del desarrollo de los ojos en el anfípodo Gammarus minus . [16]
El erizo también está involucrado en la segmentación en los gusanos anélidos; debido a que la evolución paralela parece poco probable, esto sugiere un origen común de segmentación entre los dos filos. [17] Si bien Hh no induce la formación de segmentos, parece actuar para estabilizar los campos segmentados una vez que han aparecido. [17]

Sonic hedgehog (SHH) es el ligando mejor estudiado de la vía de los vertebrados. La mayor parte de lo que se sabe sobre la señalización de hedgehog se ha establecido mediante el estudio de SHH. Se traduce como un precursor de ~45 kDa y sufre un procesamiento autocatalítico (Proceso "1" en la Figura 5) para producir un dominio de señalización N-terminal de ~20 kDa (denominado SHH-N) y un dominio C-terminal de ~25 kDa sin función de señalización conocida. Durante la escisión, se añade una molécula de colesterol al extremo carboxilo del dominio N-terminal, [18] que participa en el tráfico, la secreción y la interacción del ligando con el receptor. SHH puede señalizar de forma autocrina , afectando a las células en las que se produce. La secreción y la consiguiente señalización paracrina de hedgehog requieren la participación de la proteína Dispatched (DISP) (Proceso "2" en la Figura 5).
Cuando SHH llega a su célula objetivo, se une al receptor Patched-1 (PTCH1) (Proceso "3" en la Figura 5, la molécula azul). En ausencia de ligando, PTCH1 inhibe Smoothened (SMO), una proteína corriente abajo en la vía (Proceso "4"). Se ha sugerido que SMO está regulada por una pequeña molécula, cuya localización celular está controlada por PTCH. [19] PTCH1 tiene homología con la enfermedad de Niemann-Pick , tipo C1 ( NPC1 ) que se sabe que transporta moléculas lipofílicas a través de una membrana. [20] PTCH1 tiene un dominio de detección de esteroles (SSD), que se ha demostrado que es esencial para la supresión de la actividad de SMO. [21] Una teoría actual sugiere que PTCH regula SMO eliminando oxiesteroles de SMO. PTCH actúa como una bomba de esteroles y elimina oxiesteroles que han sido creados por la 7-dehidrocolesterol reductasa . [22] Tras la unión de una proteína Hh o una mutación en el SSD de PTCH, la bomba se apaga, lo que permite que los oxisteroles se acumulen alrededor de SMO.

Esta acumulación de esteroles permite que el SMO se active o permanezca en la membrana durante un período de tiempo más largo. Esta hipótesis está respaldada por la existencia de una serie de agonistas y antagonistas de moléculas pequeñas de la vía que actúan sobre el SMO. La unión de SHH alivia la inhibición del SMO, lo que lleva a la activación de los factores de transcripción GLI (Proceso "5"): los activadores Gli1 y Gli2 y el represor Gli3 . La secuencia de eventos moleculares que conectan al SMO con los GLI es poco conocida. El GLI activado se acumula en el núcleo (Proceso "6") y controla la transcripción de los genes diana de hedgehog (Proceso "7"). Recientemente se ha informado que el PTCH1 reprime la transcripción de los genes diana de hedgehog a través de un mecanismo independiente de Smoothened . [23]
Además de PTCH1, los mamíferos tienen otro receptor hedgehog, PTCH2, cuya identidad de secuencia con PTCH1 es del 54%. [24] Los tres hedgehog mamíferos se unen a ambos receptores con una afinidad similar , por lo que PTCH1 y PTCH2 no pueden discriminar entre los ligandos. Sin embargo, difieren en sus patrones de expresión. PTCH2 se expresa en niveles mucho más altos en el testículo y media la señalización del hedgehog del desierto allí. [24] Parece tener un papel de señalización descendente distinto de PTCH1. En ausencia de unión al ligando, PTCH2 tiene una capacidad reducida para inhibir la actividad de SMO. [25] Además, la sobreexpresión de PTCH2 no reemplaza a PTCH1 mutado en el carcinoma de células basales . [26]
En los invertebrados, al igual que en Drosophila , la unión de Hedgehog a PTCH conduce a la internalización y secuestro del ligando. [27] En consecuencia, in vivo , el paso de hedgehog sobre un campo receptivo que expresa el receptor conduce a la atenuación de la señal, un efecto llamado antagonismo dependiente de ligando (LDA). A diferencia de Drosophila , los vertebrados poseen otro nivel de regulación de hedgehog a través de LDA mediada por la proteína 1 que interactúa con Hh (HHIP1). HHIP1 también secuestra ligandos de hedgehog, pero a diferencia de PTCH, no tiene efecto sobre la actividad de SMO. [28]

Los miembros de la familia hedgehog desempeñan papeles clave en una amplia variedad de procesos de desarrollo. [15] Uno de los ejemplos mejor estudiados es la acción de Sonic hedgehog durante el desarrollo de la extremidad de los vertebrados. Los experimentos clásicos [29] de Saunders y Gasseling en 1968 [30] sobre el desarrollo de la yema de la extremidad del polluelo formaron la base del concepto de morfógeno . Demostraron que la identidad de los dígitos en la extremidad del polluelo estaba determinada por un factor difusible producido por la zona de actividad polarizante (ZPA), una pequeña región de tejido en el margen posterior de la extremidad. El desarrollo de los mamíferos parecía seguir el mismo patrón. Más tarde se demostró que este factor difusible era Sonic hedgehog . Sin embargo, hasta hace poco se desconocía exactamente cómo SHH determina la identidad de los dígitos. El modelo actual, propuesto por Harfe et al. , [31] afirma que tanto la concentración como el tiempo de exposición a SHH determinan en qué dígito se desarrollará el tejido en el embrión del ratón (figura 6).
Los dígitos V, IV y parte del III surgen directamente de células que expresan SHH durante la embriogénesis . En estas células, la SHH envía señales de forma autocrina y estos dígitos se desarrollan correctamente en ausencia de DISP, que es necesaria para la difusión extracelular del ligando. Estos dígitos difieren en el tiempo que la SHH continúa expresándose. El dígito V más posterior se desarrolla a partir de células que expresan el ligando durante el período de tiempo más largo. Las células del dígito IV expresan SHH durante un tiempo más corto, y las células del dígito III durante un tiempo aún más corto. El dígito II se desarrolla a partir de células que están expuestas a concentraciones moderadas de SHH extracelular. Finalmente, el desarrollo del dígito I no requiere SHH. Es, en cierto sentido, el programa predeterminado de las células de la yema de las extremidades.
La señalización Hedgehog sigue siendo importante en el adulto. Se ha demostrado que Sonic Hedgehog promueve la proliferación de células madre adultas de varios tejidos, incluidas las células hematopoyéticas primitivas , [32] mamarias [33] y neurales [34] . La activación de la vía Hedgehog es necesaria para la transición del folículo piloso de la fase de reposo a la fase de crecimiento. [35] Esto fracasó debido a las toxicidades encontradas en modelos animales. [36]
La alteración de la señalización hedgehog durante el desarrollo embrionario, ya sea a través de una mutación perjudicial o el consumo de teratógenos por parte de la madre gestante, puede conducir a graves anomalías del desarrollo. La holoprosencefalia , la incapacidad del prosencéfalo embrionario para dividirse para formar hemisferios cerebrales, ocurre con una frecuencia de aproximadamente 1 en 8.000 nacidos vivos y aproximadamente 1 en 200 abortos espontáneos en humanos y está comúnmente relacionada con mutaciones en genes involucrados en la vía hedgehog, incluyendo SHH y PTCH . [37] La ciclopía , uno de los defectos más graves de la holoprosencefalia , resulta si el inhibidor de la vía ciclopamina es consumido por mamíferos gestantes. [38]
La activación de la vía hedgehog se ha relacionado con el desarrollo de cánceres en varios órganos, incluidos el cerebro , los pulmones , la glándula mamaria , la próstata y la piel . El carcinoma basocelular , la forma más común de neoplasia maligna cancerosa, tiene la asociación más estrecha con la señalización hedgehog. Se han identificado mutaciones de pérdida de función en Patched y mutaciones activadoras en Smoothened en pacientes con esta enfermedad. [39] La activación anormal de la vía probablemente conduce al desarrollo de la enfermedad a través de la transformación de células madre adultas en células madre cancerosas que dan lugar al tumor. Los investigadores del cáncer esperan que los inhibidores específicos de la señalización hedgehog proporcionen una terapia eficiente para una amplia gama de neoplasias malignas. [40] La conexión entre la vía de señalización hedgehog y el desarrollo del cáncer es muy compleja. Sin embargo, está claro que la activación aberrante de la señalización hedgehog conduce al crecimiento, la proliferación y la invasión de células tumorales. [41] Además de su participación en el desarrollo de cánceres , la vía hedgehog también puede contribuir a enfermedades respiratorias importantes como la fibrosis pulmonar . [42] y enfermedad pulmonar obstructiva crónica . [43] [44] [45]
La forma más común de actuar sobre esta vía es modular la SMO. Ya se ha demostrado que los antagonistas y agonistas de la SMO afectan a la regulación de la vía aguas abajo. Hay varios inhibidores de la vía de señalización hedgehog disponibles para el tratamiento del cáncer, como vismodegib y sonidegib. Estos medicamentos se consideran terapias prometedoras contra el cáncer, especialmente para pacientes con cánceres refractarios/avanzados. Los inhibidores de la SMO representan un tratamiento potencial para algunos tipos de cáncer. Sin embargo, debido a los efectos secundarios dañinos y potencialmente tóxicos de los inhibidores de la SMO, la seguridad indeterminada en niños y la evidencia de que algunos pacientes desarrollan resistencia a los inhibidores de la SMO, se necesitan nuevas clases de medicamentos. [41] Los agentes dirigidos a la SMO clínicamente más avanzados son los competitivos con la ciclopamina . También se ha demostrado que el itraconazol ( Sporanox ) actúa sobre la SMO a través de un mecanismo distinto al de la ciclopamina y el vismodegib . [46] El itraconazol (ITZ) inhibe la SMO en presencia de mutaciones que confieren resistencia al vismodegib y otros antagonistas competitivos de la ciclopamina , como el IPI-926 y el LDE-225 de Novartis. [47] Los anticuerpos PTCH [48] y Gli3 (5E1) [49] también son una forma de regular la vía. Se ha utilizado un efector descendente y un fuerte activador transcripcional siRNA Gli1 para inhibir el crecimiento celular y promover la apoptosis. [50] También se ha demostrado que el trióxido de arsénico ( Trisenox ) inhibe la señalización de hedgehog al interferir con la función y la transcripción de Gli. [51] [52]
Se han identificado varios modificadores ambientales de la señalización Hedgehog, que son peligros potenciales para la salud o el desarrollo. Se ha demostrado que los alcaloides dietéticos que se encuentran en los tomates (tomatodina), [53] las patatas (solanidina), [53] las solanáceas como los pimientos y las berenjenas (solasodina) [53] y la cúrcuma (curcumina) [54] antagonizan el SMO y perturban la señalización Hedgehog. Además, ciertos tóxicos ambientales pueden bloquear la señalización Hedgehog. El butóxido de piperonilo (PBO) es un aditivo pesticida semisintético desarrollado en la década de 1940, que se puede encontrar en miles de productos domésticos y agrícolas. [55] A pesar de su uso generalizado, la capacidad del PBO para inhibir la señalización Hedgehog y actuar como un potente teratógeno del desarrollo no se reconoció hasta hace poco. [56] [57]
La activación de la vía Hedgehog conduce a un aumento en la expresión de la proteína Snail y una disminución de la E-cadherina y las uniones estrechas . [58]
La activación de la vía Hedgehog conduce a un aumento de los factores angiogénicos (angiopoyetina-1 y angiopoyetina-2), [59] ciclinas (ciclina D1 y B1), [60] genes antiapoptóticos y una disminución de los genes apoptóticos (Fas). [61] La disfunción o activación aberrante de la vía de señalización Hh se asocia con deformidades del desarrollo y cánceres, incluido el síndrome del nevo de células basales (BCNS), el carcinoma de células basales (BCC), los meduloblastomas (MB), los rabdomiosarcomas y los meningiomas. Aproximadamente un tercio de los tumores malignos están relacionados con la activación aberrante de la vía Hh. Existen tres mecanismos propuestos de activación aberrante de la señalización de Hh en diferentes tipos de cáncer: el tipo I implica una señalización independiente del ligando debido a mutaciones en Smo o reguladores negativos, el tipo II implica una señalización autocrina/yuxtacrina dependiente del ligando con sobreexpresión del ligando Hh, y el tipo III implica una señalización paracrina dependiente del ligando entre células tumorales y células del estroma. Estas desregulaciones en la vía de Hh pueden conducir a la proliferación de células tumorales, la supervivencia y la presencia de células madre cancerosas, que contribuyen a la iniciación y progresión del tumor. [62]

Los lancelets , que son cordados primitivos , poseen solo un homólogo de Drosophila Hh (figura 7). Los vertebrados, por otro lado, tienen varios ligandos Hedgehog que caen dentro de tres subgrupos: Desert , Indian y Sonic , cada uno representado por un solo gen de mamífero. Esto es una consecuencia de las dos rondas de duplicación del genoma completo que ocurrieron temprano en la historia evolutiva de los vertebrados. [65] Dos de estos eventos habrían producido cuatro genes homólogos, uno de los cuales debe haberse perdido. Los erizos del desierto son los más estrechamente relacionados con Drosophila Hh . Se produjeron duplicaciones de genes adicionales dentro de algunas especies [15] como el pez cebra Danio rerio , que tiene un gen de erizo tiggywinkle adicional en el grupo sonic . Varios linajes de vertebrados han adaptado a los erizos a procesos de desarrollo únicos. Por ejemplo, un homólogo del erizo bandeado de X. laevis está involucrado en la regeneración de la extremidad de la salamandra . [66]
La shh ha experimentado una evolución acelerada en el linaje de los primates que condujo a los humanos. [67] Dorus et al. plantean la hipótesis de que esto permitió una regulación más compleja de la proteína y puede haber jugado un papel en el aumento del volumen y la complejidad del cerebro humano.
La familia frizzled de receptores WNT tiene cierta similitud de secuencia con Smoothened . [68] Smoothened parece ser un miembro funcionalmente divergente de la superfamilia de receptores acoplados a proteína G (GPCR). Se han revisado otras similitudes entre las vías de señalización WNT y Hh. [69] Nusse observó que "un sistema de señalización basado en proteínas modificadas con lípidos y translocadores de membrana específicos es antiguo y puede haber sido el fundador de los sistemas de señalización Wnt y Hh".
Se ha sugerido que la señalización de invertebrados y vertebrados aguas abajo de Smoothened ha divergido significativamente. [70] El papel del supresor de Fused (SUFU) se ha mejorado en vertebrados en comparación con Drosophila , donde su papel es relativamente menor. Costal-2 es particularmente importante en Drosophila . La proteína quinasa Fused es un regulador de SUFU en Drosophila , pero puede no desempeñar un papel en la vía Hh de los vertebrados. [71] En vertebrados, la señalización de Hh ha estado fuertemente implicada en el desarrollo de los cilios . [72]
Hay una sorprendente evolución a nivel de dominio presente en la familia de proteínas Hedgehog, el dominio N-terminal (Hedge) y el dominio C-terminal (Hog), que luego se empalmaron juntos en una sola unidad transcripcional. [73] [74] El dominio Hog contiene una secuencia llamada Hint (INTeína Hedgehog), que es similar en secuencia y función a las inteínas bacterianas y fúngicas . [75] El dominio Hog está presente en muchas ramas eucariotas, es decir, algas rojas, musgos, dinoflagelados, jakobids y otros eucariotas unicelulares. [76] Los coanoflagelados contienen un gen llamado hoglet que también codifica el dominio Hog del dominio C-terminal del hedgehog. Sin embargo, los coanoflagelados y los eucariotas inferiores no contienen ninguna región similar al dominio hedge, lo que sugiere que hog evolucionó primero. [75] [76] Los poríferos tienen proteínas similares a hedge (denominadas hedgling) y proteínas similares a hog, pero existen como dos unidades transcripcionales completamente separadas. [73] [74] Los cnidarios contienen los genes hedgling y hog, pero también tienen un gen hedgehog completo, lo que indica que hedge y hog se empalmaron en hedgehog después del último ancestro común de poríferos y cnidarios. [74]
Los bilaterales no contienen genes hedgling, lo que sugiere que estos se perdieron por deleción antes de que esta rama se separara de los otros metazoos. [3] Sin embargo, los genes que contienen el dominio Hog sin un dominio Hedge están presentes en varios linajes bilaterales. Se encuentran en Lophotrochozoa y Nematoda . [77] Existen genes similares a Hedgehog, 2 homólogos de Patched y genes relacionados con Patched en el gusano C. elegans . [78] [79] Se ha demostrado que estos genes codifican proteínas que tienen funciones en el desarrollo de C. elegans . [78] [79] Mientras que los nematodos Enoplea han conservado un Hedgehog genuino, los Chromadoreans han perdido el Hedgehog arquetípico y en su lugar han desarrollado un repertorio expandido de 61 genes semiortólogos divergentes con nuevos dominios N-terminales asociados con Hog. [76] [77] Estos dominios N-terminales asociados con Hog en C. elegans fueron posteriormente clasificados, inicialmente Warthog (WRT) y Groundhog (GRD), seguidos por Ground-like (GRL) y Quahog (QUA). [78] [79] C. elegans , junto con otras especies de nematodos, han perdido el GPCR Smoothened. [78] [79]
Se plantea la hipótesis de que el origen último de la vía de señalización de Hedgehog es una vía reguladora bacteriana de los hopanoides , que son componentes lipídicos comunes en las bacterias y son análogos estructurales de los esteroides . [80]