Un mastocito (también conocido como mastocito o labrocito [1] ) es una célula residente del tejido conectivo que contiene muchos gránulos ricos en histamina y heparina . En concreto, es un tipo de granulocito derivado de la célula madre mieloide que forma parte de los sistemas inmunológico y neuroinmune . Los mastocitos fueron descubiertos por Paul Ehrlich en 1877. [2] Aunque son más conocidos por su papel en la alergia y la anafilaxia , los mastocitos también desempeñan un papel protector importante, ya que están íntimamente involucrados en la cicatrización de heridas, la angiogénesis , la tolerancia inmune y la defensa contra patógenos . y permeabilidad vascular en tumores cerebrales. [3] [4]
El mastocito es muy similar tanto en apariencia como en función al basófilo , otro tipo de glóbulo blanco . Aunque alguna vez se pensó que los mastocitos eran basófilos residentes en los tejidos, se ha demostrado que las dos células se desarrollan a partir de diferentes linajes hematopoyéticos y, por lo tanto, no pueden ser las mismas células. [5]
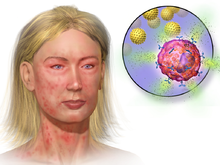
Los mastocitos son muy similares a los granulocitos basófilos (una clase de glóbulos blancos ) en la sangre , en el sentido de que ambos son células granuladas que contienen histamina y heparina , un anticoagulante . Sus núcleos se diferencian en que el núcleo de los basófilos es lobulado mientras que el núcleo de los mastocitos es redondo. La región Fc de la inmunoglobulina E (IgE) se une a los mastocitos y basófilos, y cuando los paratopos de la IgE se unen a un antígeno, hace que las células liberen histamina y otros mediadores inflamatorios. [6] Estas similitudes han llevado a muchos a especular que los mastocitos son basófilos que se han "localizado" en los tejidos. Además, comparten un precursor común en la médula ósea que expresa la molécula CD34 . Los basófilos salen de la médula ósea ya maduros, mientras que los mastocitos circulan en una forma inmadura y solo maduran una vez en un sitio de tejido. El sitio en el que se asienta un mastocito inmaduro probablemente determina sus características precisas. [7] La primera diferenciación y crecimiento in vitro de una población pura de mastocitos de ratón se ha llevado a cabo utilizando un medio condicionado derivado de esplenocitos estimulados con concanavalina A. [8] Más tarde, se descubrió que la interleucina 3 derivada de células T era el componente presente en el medio condicionado que se requería para la diferenciación y el crecimiento de los mastocitos. [9]
Los mastocitos en roedores se dividen clásicamente en dos subtipos: mastocitos de tipo tejido conectivo y mastocitos de la mucosa . La actividad de estos últimos depende de las células T. [10]
Los mastocitos están presentes en la mayoría de los tejidos que característicamente rodean los vasos sanguíneos, los nervios y los vasos linfáticos, [11] y son especialmente prominentes cerca de los límites entre el mundo exterior y el medio interno, como la piel , la mucosa de los pulmones y el tracto digestivo . así como la boca , la conjuntiva y la nariz . [7]

Los mastocitos juegan un papel clave en el proceso inflamatorio. Cuando se activa, un mastocito puede liberar selectivamente ( desgranulación gradual ) o liberar rápidamente ( desgranulación anafiláctica ) "mediadores", o compuestos que inducen inflamación, desde los gránulos de almacenamiento al microambiente local. [3] [12] Los alérgenos pueden estimular la desgranulación de los mastocitos mediante el entrecruzamiento con receptores de inmunoglobulina E (p. ej., FcεRI ), lesiones físicas mediante receptores de reconocimiento de patrones para patrones moleculares asociados a daños (DAMP), patógenos microbianos mediante el reconocimiento de patrones. receptores para patrones moleculares asociados a patógenos (PAMP) y diversos compuestos a través de sus receptores acoplados a proteína G asociados (p. ej., morfina a través de receptores opioides ) o canales iónicos activados por ligando . [3] [12] Las proteínas del complemento pueden activar receptores de membrana en los mastocitos para ejercer también diversas funciones. [7]
Los mastocitos expresan un receptor de alta afinidad ( FcεRI ) para la región Fc de IgE, el miembro menos abundante de los anticuerpos. Este receptor tiene una afinidad tan alta que la unión de moléculas de IgE es, en esencia, irreversible. Como resultado, los mastocitos están recubiertos con IgE, que es producida por las células plasmáticas (las células productoras de anticuerpos del sistema inmunológico). Los anticuerpos IgE suelen ser específicos de un antígeno en particular .
En las reacciones alérgicas, los mastocitos permanecen inactivos hasta que un alérgeno se une a la IgE que ya recubre la célula. Otros eventos de activación de la membrana pueden preparar los mastocitos para una desgranulación posterior o actuar en sinergia con la transducción de señales de FcεRI. [13] En general, los alérgenos son proteínas o polisacáridos . El alérgeno se une a los sitios de unión al antígeno, que se encuentran en las regiones variables de las moléculas de IgE unidas a la superficie de los mastocitos. Parece que se requiere la unión de dos o más moléculas de IgE (entrecruzamiento) para activar los mastocitos. La agrupación de los dominios intracelulares de los receptores Fc unidos a las células, que están asociados con las moléculas de IgE entrecruzadas, provoca una secuencia compleja de reacciones dentro del mastocito que conducen a su activación. Aunque esta reacción se comprende mejor en términos de alergia, parece haber evolucionado como un sistema de defensa contra parásitos y bacterias. [14]
Un conjunto único y específico de estímulo de mediadores de mastocitos se libera mediante la degranulación después de la activación de los receptores de la superficie celular en los mastocitos. [12] Ejemplos de mediadores que se liberan en el ambiente extracelular durante la desgranulación de los mastocitos incluyen: [7] [12] [15]
La histamina dilata las vénulas poscapilares, activa el endotelio y aumenta la permeabilidad de los vasos sanguíneos. Esto provoca edema local (hinchazón), calor, enrojecimiento y la atracción de otras células inflamatorias hacia el lugar de liberación. También despolariza las terminaciones nerviosas (lo que provoca picazón o dolor ). Los signos cutáneos de liberación de histamina son la reacción de "brote y roncha ". El bulto y el enrojecimiento inmediatamente después de la picadura de un mosquito son un buen ejemplo de esta reacción, que ocurre segundos después de la exposición de los mastocitos a un alérgeno. [7]
Las otras actividades fisiológicas de los mastocitos se conocen mucho menos. Varias líneas de evidencia sugieren que los mastocitos pueden tener un papel bastante fundamental en la inmunidad innata : son capaces de elaborar una amplia gama de citoquinas importantes y otros mediadores inflamatorios como el TNF-α; expresan múltiples "receptores de reconocimiento de patrones" que se cree que participan en el reconocimiento de amplias clases de patógenos; y los ratones sin mastocitos parecen ser mucho más susceptibles a una variedad de infecciones. [ cita necesaria ]
Los gránulos de mastocitos contienen una variedad de sustancias químicas bioactivas. Se ha descubierto que estos gránulos se transfieren a células adyacentes del sistema inmunológico y a neuronas en un proceso de transgranulación a través de pseudópodos de mastocitos . [dieciséis]
A diferencia de otras células hematopoyéticas del sistema inmunológico , los mastocitos se encuentran naturalmente en el cerebro humano , donde interactúan con el sistema neuroinmune . [4] En el cerebro, los mastocitos se encuentran en una serie de estructuras que median las funciones sensoriales viscerales (por ejemplo, el dolor) o neuroendocrinas o que se encuentran a lo largo de la barrera hematoencefálica , incluido el tallo pituitario , la glándula pineal , el tálamo y hipotálamo , área postrema , plexo coroideo y en la capa dural de las meninges cerca de los nociceptores meníngeos . [4] Los mastocitos cumplen las mismas funciones generales en el cuerpo y el sistema nervioso central, como efectuar o regular las respuestas alérgicas, la inmunidad innata y adaptativa, la autoinmunidad y la inflamación. [4] [17] En todos los sistemas, los mastocitos sirven como la principal célula efectora a través de la cual los patógenos pueden afectar el eje intestino-cerebro . [18] [19]
En el tracto gastrointestinal, los mastocitos de la mucosa se encuentran muy cerca de las fibras nerviosas sensoriales, que se comunican bidireccionalmente. [20] [18] [19] Cuando estos mastocitos inicialmente se desgranulan, liberan mediadores (p. ej., histamina, triptasa y serotonina) que activan, sensibilizan y regulan positivamente la expresión de membrana de los nociceptores (es decir, TRPV1 ) en las neuronas aferentes viscerales a través de sus receptores (respectivamente, HRH1 , HRH2 , HRH3 , PAR2 , 5-HT3 ); [20] a su vez, se produce inflamación neurogénica, hipersensibilidad visceral y dismotilidad intestinal (es decir, alteración de la peristalsis ). [20] La activación neuronal induce la señalización del neuropéptido ( sustancia P y péptido relacionado con el gen de la calcitonina ) a los mastocitos donde se unen a sus receptores asociados y desencadenan la degranulación de un conjunto distinto de mediadores ( β-hexosaminidasa , citocinas , quimiocinas , PGD2 , leucotrienos , y eoxinas ). [20] [12]

FcεR1 es un receptor de IgE de alta afinidad que se expresa en la superficie de los mastocitos. FcεR1 es un tetrámero formado por una cadena alfa (α), una cadena beta (β) y dos cadenas gamma (γ) idénticas unidas por disulfuro. El sitio de unión de la IgE está formado por la porción extracelular de la cadena α que contiene dos dominios similares a la Ig. Un dominio transmembrana contiene un residuo de ácido aspártico y el otro contiene una cola citoplasmática corta. [21] La cadena β contiene un único motivo de activación ITAM basado en tirosina de inmunorreceptor , en la región citoplasmática. Cada cadena γ tiene un ITAM en la región citoplasmática. La cascada de señalización del receptor se inicia cuando la tirosina fosforila los ITAM de las cadenas β y γ. Esta señal es necesaria para la activación de los mastocitos. [22] Las células T auxiliares tipo 2 ( Th2 ) y muchos otros tipos de células carecen de la cadena β, por lo que la señalización está mediada únicamente por la cadena γ. Esto se debe a que la cadena α contiene señales de retención del retículo endoplásmico que hacen que las cadenas α permanezcan degradadas en el RE. El ensamblaje de la cadena α con las cadenas β y γ cotransfectadas enmascara la retención del ER y permite que el complejo α β γ se exporte al aparato de Golgi hacia la membrana plasmática en ratas. En los seres humanos, sólo se necesita el complejo γ para contrarrestar la retención del RE de la cadena α. [21]
Las señales de entrecruzamiento de FcεR1 mediadas por alérgenos son muy similares al evento de señalización que resulta en la unión del antígeno a los linfocitos . La tirosina quinasa Lyn está asociada con el extremo citoplasmático de la cadena β de FcεR1. El antígeno entrecruza las moléculas de FcεR1 y la tirosina quinasa Lyn fosforila los ITAM en las cadenas β y γ de FcεR1 en el citoplasma. Tras la fosforilación , la tirosina quinasa Syk se recluta en los ITAM ubicados en las cadenas γ. Esto provoca la activación de la tirosina quinasa Syk, provocando su fosforilación. [22] Syk funciona como una señal que amplifica la actividad de la quinasa debido al hecho de que se dirige a múltiples proteínas y provoca su activación. [23] Esta fosforilación estimulada por antígeno provoca la activación de otras proteínas en la cascada de señalización mediada por FcεR1. [24]
Una proteína adaptadora importante activada por el paso de fosforilación de Syk es el conector para la activación de las células T (LAT). LAT puede modificarse mediante fosforilación para crear nuevos sitios de unión. [23] La fosfolipasa C gamma (PLCγ) se fosforila una vez unida a LAT y luego se usa para catalizar la descomposición del bisfosfato de fosfatidilinositol para producir trifosfato de inositol (IP3) y diaciglicerol (DAG). IP3 eleva los niveles de calcio y DAG activa la proteína quinasa C (PKC). Esta no es la única forma en que se elabora la PKC. La tirosina quinasa FYN fosforila la proteína 2 de unión asociada a Grb2 (Gab2), que se une a la fosfoinositida 3-quinasa , que activa la PKC. La PKC conduce a la activación de los movimientos de los gránulos de fosforilación de la cadena ligera de miosina, que desmontan los complejos de actina-miosina para permitir que los gránulos entren en contacto con la membrana plasmática. [22] El gránulo de mastocitos ahora puede fusionarse con la membrana plasmática. El complejo SNARE del receptor de proteína de unión de fusión sensible a N-etilmaleimida soluble media en este proceso. Diferentes proteínas SNARE interactúan para formar diferentes complejos que catalizan la fusión. Las guanosina trifosfatasas Rab3 y las quinasas y fosfatasas asociadas a Rab regulan la fusión de la membrana granular en los mastocitos en reposo.
El receptor MRGPRX2 acoplado a proteína G específico de mastocitos humanos desempeña un papel clave en el reconocimiento de patrones moleculares asociados a patógenos (PAMP) y en el inicio de una respuesta antibacteriana. MRGPRX2 es capaz de unirse al péptido estimulante de la competencia (CSP) 1, una molécula sensora de quórum (QSM) producida por bacterias grampositivas. [25] Esto conduce a la transducción de señales a una proteína G y a la activación de los mastocitos. La activación de los mastocitos induce la liberación de mediadores antibacterianos, incluidos ROS, TNF-α y PRGD2, que instituyen el reclutamiento de otras células inmunes para inhibir el crecimiento bacteriano y la formación de biopelículas.
El receptor MRGPRX2 es un posible objetivo terapéutico y puede activarse farmacológicamente utilizando el compuesto agonista 48/80 para controlar la infección bacteriana. [26] También se plantea la hipótesis de que otros QSM e incluso señales de bacterias Gram negativas pueden activar este receptor. Este podría ser particularmente el caso durante las infecciones crónicas por Bartonella , donde aparece claramente en la sintomatología humana que todos estos pacientes tienen un síndrome de activación de mastocitos debido a la presencia de una molécula sensora de quórum aún no definida (¿histamina basal en sí?). Esos pacientes son propensos a sufrir intolerancia alimentaria impulsada por otra vía menos específica que la vía del receptor de IgE: ciertamente la ruta MRGPRX2. Estos pacientes también muestran patergia cutánea y dermografismo cíclicos, cada vez que la bacteria sale de su ubicación intracelular oculta.
Los mastocitos se activan en respuesta a la infección por parásitos patógenos, como ciertos helmintos y protozoos , a través de la señalización de IgE .
Los trastornos de activación de los mastocitos ( MCAD ) son un espectro de trastornos inmunitarios que no están relacionados con la infección patógena e involucran síntomas similares que surgen de los intermediarios de los mastocitos secretados, pero difieren ligeramente en su fisiopatología , enfoque de tratamiento y síntomas distintivos. [27] [28] La clasificación de los trastornos de activación de los mastocitos se estableció en 2010. [27] [28]
Las alergias están mediadas por la señalización de IgE que desencadena la desgranulación de los mastocitos. [27] Recientemente, se cree que las reacciones " pseudoalérgicas " independientes de IgE también están mediadas por la activación del receptor MRGPRX2 de los mastocitos (por ejemplo, fármacos como relajantes musculares , opioides , icatibant y fluoroquinolonas ). [29]
Muchas formas de alergia cutánea y mucosa están mediadas en gran parte por mastocitos; Desempeñan un papel central en el asma , el eczema , el picor (por diversas causas), la rinitis alérgica y la conjuntivitis alérgica . Los antihistamínicos actúan bloqueando la acción de la histamina en las terminaciones nerviosas. Los fármacos a base de cromoglicato (cromoglicato de sodio, nedocromil) bloquean un canal de calcio esencial para la degranulación de los mastocitos, estabilizando la célula y previniendo la liberación de histamina y mediadores relacionados. Los antagonistas de los leucotrienos (como montelukast y zafirlukast ) bloquean la acción de los mediadores de leucotrienos y se utilizan cada vez más en enfermedades alérgicas. [7]
El calcio desencadena la secreción de histamina de los mastocitos después de una exposición previa al fluoruro de sodio. El proceso secretor se puede dividir en un paso de activación con fluoruro y un paso secretor inducido por calcio. Se observó que el paso de activación del fluoruro va acompañado de una elevación de los niveles de monofosfato de adenosina cíclico (AMPc) dentro de las células. Los altos niveles alcanzados de AMPc persisten durante la liberación de histamina. Se descubrió además que las catecolaminas no alteran notablemente la liberación de histamina inducida por fluoruro. También se confirmó que la teofilina inhibe el segundo paso, pero no el primero, en la secreción de histamina inducida por fluoruro de sodio. [30] La vasodilatación y el aumento de la permeabilidad de los capilares son el resultado de los tipos de receptores H1 y H2. [31]
La estimulación de la histamina activa una adenilato ciclasa sensible a la histamina (H2) de las células oxínticas, y hay un rápido aumento del [cAMP] celular que participa en la activación del transporte de H+ y otros cambios asociados de las células oxínticas. [32]
En la anafilaxia (una reacción sistémica grave a alérgenos , como nueces, picaduras de abeja o medicamentos), la desgranulación de los mastocitos en todo el cuerpo provoca vasodilatación y, si es grave, síntomas de shock potencialmente mortal . [ cita necesaria ]
La histamina es una sustancia vasodilatadora liberada durante la anafilaxia. [31]
Los mastocitos pueden estar implicados en la patología asociada con trastornos inflamatorios autoinmunes de las articulaciones. Se ha demostrado que participan en el reclutamiento de células inflamatorias en las articulaciones (p. ej., artritis reumatoide ) y la piel (p. ej., penfigoide ampolloso ), y esta actividad depende de los anticuerpos y los componentes del complemento. [33]
La mastocitosis es un trastorno clonal poco frecuente de mastocitos que implica la presencia de demasiados mastocitos ( mastocitos ) y precursores de mastocitos CD34 +. [34] Las mutaciones en c-Kit están asociadas con la mastocitosis. [27]
Los mastocitomas , o tumores de mastocitos, pueden secretar cantidades excesivas de productos de degranulación. [27] [28] A menudo se ven en perros y gatos. [35] Otros trastornos neoplásicos asociados con los mastocitos incluyen el sarcoma de mastocitos y la leucemia de mastocitos .
El síndrome de activación de mastocitos (MCAS) es un trastorno inmunológico idiopático que implica una desgranulación excesiva y recurrente de los mastocitos y que produce síntomas similares a otros trastornos de activación de los mastocitos. [27] [28] El síndrome se diagnostica según cuatro conjuntos de criterios que incluyen la respuesta al tratamiento, los síntomas, el diagnóstico diferencial y los biomarcadores de la desgranulación de los mastocitos. [27] [28]
Los mastocitos fueron descritos por primera vez por Paul Ehrlich en su tesis doctoral de 1878 basándose en sus características de tinción únicas y sus grandes gránulos. Estos gránulos también le llevaron a la creencia errónea de que existían para nutrir el tejido circundante, por lo que los llamó Mastzellen (del alemán Mast 'engorde', como de animales). [36] [37] Ahora se consideran parte del sistema inmunológico .
La investigación sobre una contribución inmunológica al autismo sugiere que los niños con trastorno del espectro autista (TEA) pueden presentar problemas "similares a los alérgicos" en ausencia de IgE sérica elevada y urticaria crónica , lo que sugiere una activación de mastocitos no alérgicos en respuesta a desencadenantes ambientales y de estrés. . Esta activación de los mastocitos podría contribuir a la inflamación cerebral y a problemas de desarrollo neurológico. [38]
Azul de toluidina : uno de los colorantes más comunes para los mucopolisacáridos ácidos y los glicoaminoglicanos , componentes de los gránulos de los mastocitos. [39]
Marrón Bismarck: tiñe los gránulos de mastocitos de color marrón. [40]
Marcadores de superficie: Heneberg analizó en detalle los marcadores de superficie celular de los mastocitos, [41] afirmando que los mastocitos pueden incluirse inadvertidamente en los aislados de células madre o progenitoras, ya que parte de ellos es positivo para el antígeno CD34. Los marcadores de mastocitos clásicos incluyen el receptor de IgE de alta afinidad, CD117 (c-Kit) y CD203c (para la mayoría de las poblaciones de mastocitos). La expresión de algunas moléculas puede cambiar en el curso de la activación de los mastocitos. [42]
Los mastocitos y las células enterocromafines son la fuente de la mayor parte de la serotonina en el estómago de los roedores . [43]
Los mastocitos pueden reconocer patógenos a través de diferentes mecanismos, incluida la unión directa de patógenos o sus componentes a los receptores PAMP en la superficie de los mastocitos, la unión de anticuerpos o bacterias recubiertas de complemento a receptores de inmunoglobulina o complemento, o el reconocimiento de péptidos endógenos producidos por infectados. o células lesionadas (Hofmann y Abraham 2009).
El patrón de expresión de estos receptores varía considerablemente entre los diferentes subtipos de mastocitos.
Los TLR (1–7 y 9), los NLR, los RLR y los receptores del complemento son responsables de la mayoría de las respuestas innatas de los mastocitos.
Los MC se originan a partir de un progenitor de la médula ósea y posteriormente desarrollan diferentes características fenotípicas localmente en los tejidos.
Su gama de funciones es amplia e incluye participación en reacciones alérgicas, inmunidad innata y adaptativa, inflamación y autoinmunidad [34].
En el cerebro humano, los CM pueden ubicarse en diversas áreas, como el tallo pituitario, la glándula pineal, el área postrema, el plexo coroideo, el tálamo, el hipotálamo y la eminencia media [35].
En las meninges, se encuentran dentro de la capa dural en asociación con vasos y terminales de los nociceptores meníngeos [36].
Las MC tienen una característica distintiva en comparación con otras células hematopoyéticas porque residen en el cerebro [37].
Los MC contienen numerosos gránulos y secretan una gran cantidad de mediadores prealmacenados, como la hormona liberadora de corticotropina (CRH), la neurotensina (NT), la sustancia P (SP), la triptasa, la quimasa, el péptido intestinal vasoactivo (VIP) y el factor de crecimiento endotelial vascular (VEGF). , TNF, prostaglandinas, leucotrienos y variedades de quimiocinas y citocinas, algunas de las cuales se sabe que alteran la integridad de la barrera hematoencefálica (BHE) [38-40].
[El] papel clave de los CM en la inflamación [34] y en la alteración de la BHE [41-43] sugiere áreas de importancia para la investigación de nuevas terapias.
Cada vez hay más evidencia que indica que los CM participan en la neuroinflamación directamente [44-46] y a través de la estimulación de la microglía [47], contribuyendo a la patogénesis de afecciones como dolores de cabeza, [48] autismo [49] y síndrome de fatiga crónica [50].
De hecho, una revisión reciente indicó que los estímulos inflamatorios periféricos pueden causar la activación de la microglía [51], lo que posiblemente involucre a los CM fuera del cerebro.
{{cite journal}}: Mantenimiento CS1: varios nombres: lista de autores ( enlace )Se han descrito dos tipos de degranulación para MC: degranulación gradual (PMD) y degranulación anafiláctica (AND) (Figuras 1 y 2).
Tanto la PMD como la AND ocurren in vivo, ex vivo e in vitro en MC en humanos (78–82), ratones (83) y ratas (84).
PMD es la liberación selectiva de porciones del contenido de los gránulos, sin fusiones de gránulo a gránulo y/o de gránulo a membrana plasmática.
... A diferencia de la PMD, la AND es la liberación explosiva del contenido de los gránulos o de gránulos completos al exterior de las células después de fusiones de gránulo a gránulo y/o de gránulo a membrana plasmática (Figuras 1 y 2).
Los estudios ultraestructurales muestran que la Y comienza con la hinchazón de los gránulos y la alteración de la matriz después de una estimulación adecuada (p. ej., reticulación de FcεRI).
Los receptores P2X son canales catiónicos no selectivos activados por ligando que se activan mediante ATP extracelular.
... Es probable que haya mayores concentraciones locales de ATP alrededor de los mastocitos en tejidos inflamados debido a su liberación a través de lesión o muerte celular y activación plaquetaria [40].
Además, los propios mastocitos almacenan ATP dentro de los gránulos secretores, que se libera tras la activación [41].
Por lo tanto, existe la posibilidad de que se produzca una entrada significativa de Ca2+ en los mastocitos a través de los receptores P2X.
Los miembros de la familia P2X difieren tanto en la concentración de ATP que requieren para la activación como en el grado en que se desensibilizan después de la activación del agonista [37, 38].
Esto abre la posibilidad de que, al expresar varios receptores P2X diferentes, los mastocitos puedan adaptar su respuesta al ATP de una manera dependiente de la concentración [37].
En el tejido digestivo, H. pylori puede alterar la señalización en el eje cerebro-intestino mediante mastocitos, el principal efector del eje cerebro-intestino.
Los trastornos gastrointestinales funcionales (TFGID) se caracterizan por molestias crónicas que surgen de interacciones desorganizadas entre el cerebro y el intestino que provocan dismotilidad e hipersensibilidad.
Los dos FGID más prevalentes, que afectan hasta entre el 16% y el 26% de la población mundial, son la dispepsia funcional y el síndrome del intestino irritable.
... Está bien establecido que la activación de los mastocitos puede generar disfunción epitelial y neuromuscular y promover hipersensibilidad visceral y patrones de motilidad alterados en TFG, íleo posoperatorio, alergia alimentaria y enfermedad inflamatoria intestinal.
▸ Los mastocitos desempeñan un papel fisiopatológico central en el SII y posiblemente en la dispepsia funcional, aunque no está bien definido.
▸ El aumento de la activación de los mastocitos es un hallazgo común en la mucosa de pacientes con trastornos gastrointestinales funcionales.
...
▸ El tratamiento con estabilizadores de mastocitos ofrece una opción razonablemente segura y prometedora para el tratamiento de aquellos pacientes con SII que no responden a los enfoques convencionales, aunque se justifican estudios futuros para evaluar la eficacia y las indicaciones.
Tabla 1
Clasificación de enfermedades asociadas con la activación de mastocitos de Akin et al.
[14]
1. Primaria
a.
Anafilaxia con un trastorno clonal asociado de mastocitos
b.
Síndrome de activación monoclonal de mastocitos (MMAS), consulte el texto para obtener una explicación
2. Secundaria
a.
Trastornos alérgicos
b.
Activación de mastocitos asociada con trastornos inflamatorios crónicos o neoplásicos
c.
Urticarias físicas (requiere estimulación primaria)
d.
Urticaria autoinmune crónica
3. Idiopática (cuando se ha documentado la desgranulación de los mastocitos; puede ser primaria o secundaria. El angioedema puede estar asociado con angioedema hereditario o adquirido, donde puede ser independiente de los mastocitos y resultar de la generación de quininas)
a.
Anafilaxia
b.
Angioedema
c.
Urticaria
d.
Síndrome de activación de mastocitos (MCAS)... La
anafilaxia idiopática recurrente se presenta con signos y síntomas alérgicos (urticaria y angioedema, que es una característica distintiva), elimina etiologías alérgicas identificables, considera mastocitosis y síndrome carcinoide, y se trata con antihistamínicos H1 y H2, epinefrina. y esteroides [21, 22].