
La desintegración radiactiva (también conocida como desintegración nuclear , radiactividad , desintegración radiactiva o desintegración nuclear ) es el proceso por el cual un núcleo atómico inestable pierde energía por radiación . Un material que contiene núcleos inestables se considera radiactivo . Tres de los tipos más comunes de desintegración son la desintegración alfa , beta y gamma . La fuerza débil es el mecanismo responsable de la desintegración beta, mientras que las otras dos se rigen por el electromagnetismo y la fuerza nuclear . [1]
La desintegración radiactiva es un proceso aleatorio a nivel de átomos individuales. Según la teoría cuántica , es imposible predecir cuándo se desintegrará un átomo en particular, independientemente de cuánto tiempo haya existido. [2] [3] [4] Sin embargo, para un número significativo de átomos idénticos, la tasa de desintegración general se puede expresar como una constante de desintegración o como vida media . Las vidas medias de los átomos radiactivos tienen un rango enorme; desde casi instantáneo hasta mucho más largo que la edad del universo .
El núcleo en descomposición se llama radionucleido padre (o radioisótopo padre [nota 1] ), y el proceso produce al menos un nucleido hijo . Excepto por la desintegración gamma o la conversión interna de un estado nuclear excitado , la desintegración es una transmutación nuclear que da como resultado una hija que contiene un número diferente de protones o neutrones (o ambos). Cuando cambia el número de protones, se crea un átomo de un elemento químico diferente.
Hay 28 elementos químicos naturales en la Tierra que son radiactivos, compuestos por 35 radionúclidos (siete elementos tienen dos radionúclidos diferentes) que datan de antes del momento de formación del Sistema Solar . Estos 35 se conocen como radionucleidos primordiales . Ejemplos bien conocidos son el uranio y el torio , pero también se incluyen radioisótopos naturales de larga vida, como el potasio-40 .

La radiactividad fue descubierta en 1896 por los científicos Henri Becquerel y Marie Curie , mientras trabajaban con materiales fosforescentes . [5] [6] [7] [8] [9] Estos materiales brillan en la oscuridad después de la exposición a la luz, y Becquerel sospechaba que el brillo producido en los tubos de rayos catódicos por los rayos X podría estar asociado con la fosforescencia. Envolvió una placa fotográfica en papel negro y le colocó varias sales fosforescentes. Todos los resultados fueron negativos hasta que utilizó sales de uranio . Las sales de uranio provocaron un ennegrecimiento de la placa a pesar de que estaba envuelta en papel negro. Estas radiaciones recibieron el nombre de "rayos Becquerel".
Pronto quedó claro que el ennegrecimiento de la placa no tenía nada que ver con la fosforescencia, ya que el ennegrecimiento también era producido por sales de uranio no fosforescentes y por uranio metálico. A partir de estos experimentos quedó claro que había una forma de radiación invisible que podía atravesar el papel y hacía que la placa reaccionara como si estuviera expuesta a la luz.
Al principio parecía que la nueva radiación era similar a los rayos X recientemente descubiertos. Investigaciones posteriores realizadas por Becquerel, Ernest Rutherford , Paul Villard , Pierre Curie , Marie Curie y otros demostraron que esta forma de radiactividad era significativamente más complicada. Rutherford fue el primero en darse cuenta de que todos esos elementos se desintegran de acuerdo con la misma fórmula matemática exponencial. Rutherford y su alumno Frederick Soddy fueron los primeros en darse cuenta de que muchos procesos de descomposición daban como resultado la transmutación de un elemento en otro. Posteriormente se formuló la ley de desplazamiento radiactivo de Fajans y Soddy para describir los productos de la desintegración alfa y beta . [10] [11]
Los primeros investigadores también descubrieron que muchos otros elementos químicos , además del uranio, tienen isótopos radiactivos. Una búsqueda sistemática de la radiactividad total en los minerales de uranio también llevó a Pierre y Marie Curie a aislar dos nuevos elementos: polonio y radio . Excepto por la radiactividad del radio, la similitud química del radio con el bario hacía que estos dos elementos fueran difíciles de distinguir.
El estudio de la radiactividad de Marie y Pierre Curie es un factor importante en la ciencia y la medicina. Después de que sus investigaciones sobre los rayos de Becquerel les llevaran al descubrimiento tanto del radio como del polonio, acuñaron el término "radiactividad" [12] para definir la emisión de radiaciones ionizantes por parte de algunos elementos pesados. [13] (Más tarde el término se generalizó a todos los elementos). Su investigación sobre los rayos penetrantes en el uranio y el descubrimiento del radio iniciaron una era en el uso del radio para el tratamiento del cáncer. Su exploración del radio podría verse como el primer uso pacífico de la energía nuclear y el inicio de la medicina nuclear moderna . [12]

Los peligros de las radiaciones ionizantes debidas a la radiactividad y los rayos X no fueron reconocidos de inmediato.
El descubrimiento de los rayos X por Wilhelm Röntgen en 1895 dio lugar a una experimentación generalizada por parte de científicos, médicos e inventores. Muchas personas comenzaron a contar historias de quemaduras, pérdida de cabello y cosas peores en revistas técnicas ya en 1896. En febrero de ese año, el profesor Daniel y el Dr. Dudley de la Universidad de Vanderbilt realizaron un experimento que incluía radiografías de la cabeza de Dudley que resultaron en su pérdida de cabello. . Un informe del Dr. HD Hawks, sobre cómo sufrió graves quemaduras en las manos y el pecho en una demostración de rayos X, fue el primero de muchos otros informes en Electrical Review . [14]
Otros experimentadores, incluidos Elihu Thomson y Nikola Tesla , también informaron de quemaduras. Thomson expuso deliberadamente un dedo a un tubo de rayos X durante un período de tiempo y sufrió dolor, hinchazón y ampollas. [15] A veces se culpaba a otros efectos, incluidos los rayos ultravioleta y el ozono, por el daño, [16] y muchos médicos aún afirmaban que la exposición a los rayos X no producía ningún efecto. [15]
A pesar de esto, hubo algunas investigaciones tempranas sistemáticas sobre los peligros, y ya en 1902 William Herbert Rollins escribió casi desesperado que sus advertencias sobre los peligros implicados en el uso descuidado de los rayos X no estaban siendo atendidas, ni por la industria ni por sus colegas. Para entonces, Rollins había demostrado que los rayos X podían matar animales de experimentación, provocar el aborto de una cobaya preñada y matar a un feto. También destacó que "los animales varían en susceptibilidad a la acción externa de la luz X" y advirtió que estas diferencias deben tenerse en cuenta cuando los pacientes sean tratados mediante rayos X. [ cita necesaria ]

Sin embargo, los efectos biológicos de la radiación debida a sustancias radiactivas fueron menos fáciles de medir. Esto dio a muchos médicos y corporaciones la oportunidad de comercializar sustancias radiactivas como medicamentos patentados . Algunos ejemplos eran los tratamientos con enemas de radio y las aguas que contenían radio para beber como tónico. Marie Curie protestó contra este tipo de tratamiento, advirtiendo que "el radio es peligroso en manos no capacitadas". [17] Curie murió más tarde de anemia aplásica , probablemente causada por la exposición a radiación ionizante. En la década de 1930, después de varios casos de necrosis ósea y muerte de entusiastas del tratamiento con radio, los medicamentos que contenían radio habían sido retirados en gran medida del mercado ( charlatanería radioactiva ).
Sólo un año después del descubrimiento de los rayos X por parte de Röntgen , el ingeniero estadounidense Wolfram Fuchs (1896) dio lo que probablemente sea el primer consejo de protección, pero no fue hasta 1925 que se celebró y consideró el primer Congreso Internacional de Radiología (ICR). establecer estándares internacionales de protección. Los efectos de la radiación sobre los genes, incluido el efecto del riesgo de cáncer, se reconocieron mucho más tarde. En 1927, Hermann Joseph Muller publicó una investigación que demostraba los efectos genéticos y, en 1946, recibió el Premio Nobel de Fisiología o Medicina por sus hallazgos.
La segunda ICR se celebró en Estocolmo en 1928 y propuso la adopción de la unidad röntgen , y se formó el Comité Internacional de Protección contra Radio y Rayos X (IXRPC). Rolf Sievert fue nombrado presidente, pero una fuerza impulsora fue George Kaye del Laboratorio Nacional de Física Británico . El comité se reunió en 1931, 1934 y 1937.
Después de la Segunda Guerra Mundial , la mayor variedad y cantidad de sustancias radiactivas que se manipulaban como resultado de los programas nucleares militares y civiles llevó a que grandes grupos de trabajadores y el público quedaran potencialmente expuestos a niveles nocivos de radiación ionizante. Esto se consideró en la primera ICR de posguerra convocada en Londres en 1950, cuando nació la actual Comisión Internacional de Protección Radiológica (CIPR). [18] Desde entonces, la CIPR ha desarrollado el actual sistema internacional de protección radiológica, que abarca todos los aspectos de los riesgos radiológicos.
En 2020, Hauptmann y otros 15 investigadores internacionales de ocho países, entre ellos: Institutos de Bioestadística, Investigación de Registros, Centros de Epidemiología del Cáncer, Epidemiología de la Radiación, y también el Instituto Nacional del Cáncer de EE.UU. (NCI), la Agencia Internacional para la Investigación del Cáncer (IARC ) y la Radiation Effects Research Foundation de Hiroshima estudiaron de forma definitiva mediante un metaanálisis los daños resultantes de las "bajas dosis" que han afectado a los supervivientes de los bombardeos atómicos de Hiroshima y Nagasaki y también de los numerosos accidentes ocurridos en las centrales nucleares. Estos científicos informaron, en JNCI Monographs: Epidemiological Studies of Low Dose Ionizing Radiation and Cancer Risk , que los nuevos estudios epidemiológicos respaldan directamente el exceso de riesgos de cáncer debido a las bajas dosis de radiación ionizante. [19] En 2021, el investigador italiano Sebastiano Venturi informó de las primeras correlaciones entre el radiocesio y el cáncer de páncreas con el papel del cesio en la biología, en la pancreatitis y en la diabetes de origen pancreático. [20]

La unidad de actividad radiactiva del Sistema Internacional de Unidades (SI) es el becquerel (Bq), llamado así en honor al científico Henri Becquerel . Un Bq se define como una transformación (o decadencia o desintegración) por segundo.
Una unidad de radiactividad más antigua es el curie , Ci, que originalmente se definió como "la cantidad o masa de emanación de radio en equilibrio con un gramo de radio (elemento)". [21] Hoy en día, la curie se define como3,7 × 10 10 desintegraciones por segundo, de modo que 1 curie (Ci) =3,7 × 10 10 Bq . Para fines de protección radiológica, aunque la Comisión Reguladora Nuclear de los Estados Unidos permite el uso de la unidad curie junto con las unidades SI, [22] las directivas europeas de unidades de medida de la Unión Europea exigieron que su uso para "fines de salud pública..." se elimine gradualmente. antes del 31 de diciembre de 1985. [23]
Los efectos de la radiación ionizante a menudo se miden en unidades de gris para mecánicas o sievert para daños a los tejidos.
La desintegración radiactiva produce una reducción de la masa en reposo sumada , una vez que la energía liberada (la energía de desintegración ) ha escapado de alguna manera. Aunque la energía de desintegración a veces se define como asociada con la diferencia entre la masa de los productos del nucleido original y la masa de los productos de desintegración, esto es cierto sólo para las mediciones de masa en reposo, donde se ha eliminado algo de energía del sistema producto. Esto es cierto porque la energía de desintegración siempre debe llevar masa consigo, dondequiera que aparezca (ver masa en relatividad especial ) según la fórmula E = mc 2 . La energía de desintegración se libera inicialmente como la energía de los fotones emitidos más la energía cinética de las partículas masivas emitidas (es decir, partículas que tienen masa en reposo). Si estas partículas alcanzan el equilibrio térmico con su entorno y se absorben fotones, entonces la energía de desintegración se transforma en energía térmica, que conserva su masa.
La energía de desintegración, por lo tanto, permanece asociada con una cierta medida de la masa del sistema de desintegración, llamada masa invariante , que no cambia durante la desintegración, aunque la energía de desintegración se distribuya entre las partículas de desintegración. La energía de los fotones, la energía cinética de las partículas emitidas y, más tarde, la energía térmica de la materia circundante contribuyen a la masa invariante del sistema. Así, si bien la suma de las masas en reposo de las partículas no se conserva en la desintegración radiactiva, la masa del sistema y la masa invariante del sistema (y también la energía total del sistema) se conservan durante cualquier proceso de desintegración. Esta es una reformulación de las leyes equivalentes de conservación de energía y conservación de masa .

Los primeros investigadores descubrieron que un campo eléctrico o magnético podría dividir las emisiones radiactivas en tres tipos de haces. Los rayos recibieron los nombres de alfa , beta y gamma, en orden creciente de su capacidad para penetrar la materia. La desintegración alfa se observa sólo en elementos más pesados de número atómico 52 ( telurio ) y mayores, con la excepción del berilio-8 (que se desintegra en dos partículas alfa). Los otros dos tipos de descomposición se observan en todos los elementos. El plomo, número atómico 82, es el elemento más pesado que tiene isótopos estables (hasta el límite de medición) ante la desintegración radiactiva. La desintegración radiactiva se observa en todos los isótopos de todos los elementos de número atómico 83 ( bismuto ) o mayor. El bismuto-209 , sin embargo, es sólo ligeramente radiactivo y tiene una vida media mayor que la edad del universo; Los radioisótopos con vidas medias extremadamente largas se consideran efectivamente estables a efectos prácticos.

Al analizar la naturaleza de los productos de desintegración, resultó obvio, a partir de la dirección de las fuerzas electromagnéticas aplicadas a las radiaciones por los campos magnéticos y eléctricos externos, que las partículas alfa tenían una carga positiva, las partículas beta tenían una carga negativa y los rayos gamma eran neutros. Por la magnitud de la desviación, estaba claro que las partículas alfa eran mucho más masivas que las partículas beta . Pasar partículas alfa a través de una ventana de vidrio muy delgada y atraparlas en un tubo de descarga permitió a los investigadores estudiar el espectro de emisión de las partículas capturadas y, finalmente, demostró que las partículas alfa son núcleos de helio . Otros experimentos demostraron que la radiación beta, resultante de la desintegración y los rayos catódicos , eran electrones de alta velocidad . Asimismo, se descubrió que la radiación gamma y los rayos X son radiaciones electromagnéticas de alta energía .
También se empezó a examinar la relación entre los tipos de desintegración: por ejemplo, la desintegración gamma casi siempre estaba asociada con otros tipos de desintegración y ocurría aproximadamente al mismo tiempo o después. Se descubrió que la desintegración gamma como un fenómeno separado, con su propia vida media (ahora denominada transición isomérica ), en la radiactividad natural era el resultado de la desintegración gamma de isómeros nucleares metaestables excitados , que a su vez se crearon a partir de otros tipos de desintegración. Aunque las radiaciones alfa, beta y gamma fueron las más comunes, con el tiempo se descubrieron otros tipos de emisiones. Poco después del descubrimiento del positrón en los productos de los rayos cósmicos, se descubrió que el mismo proceso que opera en la desintegración beta clásica también puede producir positrones ( emisión de positrones ), junto con neutrinos (la desintegración beta clásica produce antineutrinos).
En la captura de electrones, se descubrió que algunos nucleidos ricos en protones capturan sus propios electrones atómicos en lugar de emitir positrones y, posteriormente, estos nucleidos emiten sólo un neutrino y un rayo gamma del núcleo excitado (y a menudo también electrones Auger y rayos X característicos). , como resultado del reordenamiento de los electrones para llenar el lugar del electrón capturado faltante). Estos tipos de desintegración implican la captura nuclear de electrones o la emisión de electrones o positrones y, por lo tanto, actúan para mover un núcleo hacia la proporción de neutrones a protones que tiene la menor energía para un número total determinado de nucleones . En consecuencia, esto produce un núcleo más estable (de menor energía).
Un proceso hipotético de captura de positrones, análogo a la captura de electrones, es teóricamente posible en los átomos de antimateria, pero no se ha observado, ya que los átomos de antimateria complejos más allá del antihelio no están disponibles experimentalmente. [24] Tal desintegración requeriría átomos de antimateria al menos tan complejos como el berilio-7 , que es el isótopo más ligero conocido de la materia normal que sufre desintegración por captura de electrones. [25]
Poco después del descubrimiento del neutrón en 1932, Enrico Fermi se dio cuenta de que determinadas raras reacciones de desintegración beta producían inmediatamente neutrones como partícula de desintegración adicional, la llamada emisión de neutrones beta retardada . La emisión de neutrones generalmente ocurre a partir de núcleos que están en un estado excitado, como el 17 O* excitado producido por la desintegración beta del 17 N. El proceso de emisión de neutrones en sí está controlado por la fuerza nuclear y, por lo tanto, es extremadamente rápido, a veces denominado como "casi instantáneo". Finalmente se observó emisión aislada de protones en algunos elementos. También se descubrió que algunos elementos pesados pueden sufrir fisión espontánea en productos que varían en composición. En un fenómeno llamado desintegración de cúmulos , se descubrió que los átomos emitían espontáneamente combinaciones específicas de neutrones y protones distintas de las partículas alfa (núcleos de helio).
Se descubrió que otros tipos de desintegración radiactiva emiten partículas vistas anteriormente, pero a través de mecanismos diferentes. Un ejemplo es la conversión interna , que da como resultado una emisión inicial de electrones y luego, a menudo, más emisiones características de rayos X y electrones Auger , aunque el proceso de conversión interna no implica desintegración beta ni gamma. Un neutrino no se emite y ninguno de los electrones y fotones emitidos se origina en el núcleo, aunque la energía para emitirlos todos sí se origina allí. La desintegración por conversión interna, como la desintegración gamma de transición isomérica y la emisión de neutrones, implica la liberación de energía por un nucleido excitado, sin la transmutación de un elemento en otro.
Se conocen eventos raros que involucran una combinación de dos eventos de tipo desintegración beta que ocurren simultáneamente (ver más abajo). Se permite que ocurra cualquier proceso de desintegración que no viole las leyes de conservación de la energía o del momento (y quizás otras leyes de conservación de partículas), aunque no todos han sido detectados. Un ejemplo interesante que se analiza en una sección final es la desintegración beta del renio-187 en estado ligado . En este proceso, la desintegración de los electrones beta del nucleido original no va acompañada de la emisión de electrones beta, porque la partícula beta ha sido capturada en la capa K del átomo emisor. Se emite un antineutrino, como en todas las desintegraciones beta negativas.
Si las circunstancias energéticas son favorables, un radionucleido determinado puede sufrir muchos tipos competitivos de desintegración, desintegrándose algunos átomos por una ruta y otros por otra. Un ejemplo es el cobre-64 , que tiene 29 protones y 35 neutrones, que se desintegra con una vida media de12.7004(13) horas. [26] Este isótopo tiene un protón desapareado y un neutrón desapareado, por lo que el protón o el neutrón pueden desintegrarse en la otra partícula, que tiene isospin opuesto . Es más probable que este nucleido en particular (aunque no todos los nucleidos en esta situación) se desintegre mediante desintegración beta plus (61,52(26) % [26] ) que mediante captura de electrones (38,48(26) % [26] ). Los estados de energía excitados resultantes de estas desintegraciones que no terminan en un estado de energía fundamental, también producen una conversión interna posterior y una desintegración gamma en casi el 0,5% del tiempo.
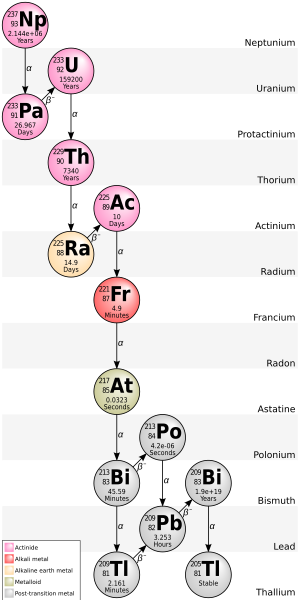
El nucleido hijo de un evento de desintegración también puede ser inestable (radiactivo). En este caso, también se descompondrá y producirá radiación. El segundo nucleido hijo resultante también puede ser radiactivo. Esto puede conducir a una secuencia de varios eventos de desintegración llamado cadena de desintegración (consulte este artículo para obtener detalles específicos de importantes cadenas de desintegración natural). Finalmente, se produce un nucleido estable. Cualquier hija de desintegración que sea el resultado de una desintegración alfa también dará como resultado la creación de átomos de helio.
Algunos radionucleidos pueden tener varias vías de desintegración diferentes. Por ejemplo,El 35,94(6) % [26] del bismuto-212 se desintegra, mediante emisión alfa, en talio-208, mientras queEl 64,06(6) % [26] del bismuto-212 se desintegra, mediante emisión beta, en polonio-212 . Tanto el talio-208 como el polonio-212 son productos hijos radiactivos del bismuto-212, y ambos se desintegran directamente formando plomo-208 estable .
Según la teoría del Big Bang , los isótopos estables de los tres elementos más ligeros ( H , He y trazas de Li ) se produjeron muy poco después del surgimiento del universo, en un proceso llamado nucleosíntesis del Big Bang . Estos nucleidos estables más ligeros (incluido el deuterio ) sobreviven hasta hoy, pero los isótopos radiactivos de los elementos ligeros producidos en el Big Bang (como el tritio ) hace tiempo que se desintegraron. Los isótopos de elementos más pesados que el boro no se produjeron en absoluto en el Big Bang, y estos primeros cinco elementos no tienen radioisótopos de vida larga. Por lo tanto, todos los núcleos radiactivos son relativamente jóvenes con respecto al nacimiento del universo, y se formaron más tarde en varios otros tipos de nucleosíntesis en estrellas (en particular, supernovas ), y también durante las interacciones en curso entre isótopos estables y partículas energéticas. Por ejemplo, el carbono-14 , un nucleido radiactivo con una vida media de sólo5700(30) años, [26] se produce constantemente en la atmósfera superior de la Tierra debido a las interacciones entre los rayos cósmicos y el nitrógeno.
Los nucleidos que se producen por desintegración radiactiva se denominan nucleidos radiogénicos , sean ellos mismos estables o no. Existen nucleidos radiogénicos estables que se formaron a partir de radionucleidos extintos de vida corta en el Sistema Solar temprano. [28] [29] La presencia adicional de estos nucleidos radiogénicos estables (como el xenón-129 del yodo-129 extinto ) en comparación con los nucleidos estables primordiales se puede inferir por varios medios.
La desintegración radiactiva se ha utilizado en la técnica del marcaje radioisotópico , que se utiliza para rastrear el paso de una sustancia química a través de un sistema complejo (como un organismo vivo ). Se sintetiza una muestra de la sustancia con una alta concentración de átomos inestables. La presencia de una sustancia en una u otra parte del sistema se determina detectando la ubicación de los eventos de desintegración.
Partiendo de la premisa de que la desintegración radiactiva es verdaderamente aleatoria (en lugar de simplemente caótica ), se ha utilizado en generadores de números aleatorios de hardware . Debido a que no se cree que el proceso varíe significativamente en su mecanismo a lo largo del tiempo, también es una herramienta valiosa para estimar las edades absolutas de ciertos materiales. En el caso de los materiales geológicos, los radioisótopos y algunos de sus productos de desintegración quedan atrapados cuando una roca se solidifica y luego pueden usarse (sujeto a muchas calificaciones bien conocidas) para estimar la fecha de la solidificación. Estos incluyen comparar los resultados de varios procesos simultáneos y sus productos entre sí, dentro de la misma muestra. De manera similar, y también sujeto a matizaciones, se puede estimar la tasa de formación del carbono-14 en varias épocas, la fecha de formación de la materia orgánica dentro de un período determinado relacionado con la vida media del isótopo, porque el carbono-14 queda atrapado cuando la materia orgánica crece e incorpora el nuevo carbono-14 del aire. A partir de entonces, la cantidad de carbono-14 en la materia orgánica disminuye según procesos de descomposición que también pueden verificarse independientemente por otros medios (como, por ejemplo, verificar el carbono-14 en los anillos individuales de los árboles).
El efecto Szilard-Chalmers es la ruptura de un enlace químico como resultado de una energía cinética impartida por la desintegración radiactiva. Funciona mediante la absorción de neutrones por un átomo y la posterior emisión de rayos gamma, a menudo con cantidades significativas de energía cinética. Esta energía cinética, por la tercera ley de Newton , empuja hacia atrás al átomo en descomposición, lo que hace que se mueva con suficiente velocidad como para romper un enlace químico. [30] Este efecto se puede utilizar para separar isótopos por medios químicos.
El efecto Szilard-Chalmers fue descubierto en 1934 por Leó Szilárd y Thomas A. Chalmers. [31] Observaron que después del bombardeo con neutrones, la rotura de un enlace en el yoduro de etilo líquido permitía eliminar el yodo radiactivo. [32]
Los nucleidos primordiales radiactivos encontrados en la Tierra son residuos de antiguas explosiones de supernovas que ocurrieron antes de la formación del Sistema Solar . Son la fracción de radionucleidos que sobrevivieron desde aquella época, mediante la formación de la nebulosa solar primordial , mediante la acreción de planetas , y hasta la actualidad. Los radionucleidos radiogénicos de vida corta que se encuentran naturalmente en las rocas actuales son hijos de aquellos nucleidos radiactivos primordiales. Otra fuente menor de nucleidos radiactivos naturales son los nucleidos cosmogénicos , que se forman mediante el bombardeo de material de la atmósfera o la corteza terrestre con rayos cósmicos . La desintegración de los radionucleidos en las rocas del manto y la corteza terrestre contribuye significativamente al balance de calor interno de la Tierra .
La tasa de desintegración , o actividad , de una sustancia radiactiva se caracteriza por los siguientes parámetros independientes del tiempo:
Aunque son constantes, están asociadas con el comportamiento estadístico de poblaciones de átomos. En consecuencia, las predicciones que utilizan estas constantes son menos precisas para muestras minúsculas de átomos.
En principio, una vida media, una tercera vida o incluso una vida media (1/√2) se pueden utilizar exactamente de la misma manera que la vida media; pero la vida media y la vida media t 1/2 se han adoptado como tiempos estándar asociados con el decaimiento exponencial.
Esos parámetros pueden estar relacionados con los siguientes parámetros dependientes del tiempo:
Estos están relacionados de la siguiente manera:
donde N 0 es la cantidad inicial de sustancia activa, sustancia que tiene el mismo porcentaje de partículas inestables que cuando se formó la sustancia.
Las matemáticas de la desintegración radiactiva dependen de una suposición clave de que el núcleo de un radionúclido no tiene "memoria" ni forma de traducir su historia a su comportamiento actual. Un núcleo no "envejece" con el paso del tiempo. Por tanto, la probabilidad de que se descomponga no aumenta con el tiempo sino que permanece constante, sin importar cuánto tiempo haya existido el núcleo. Esta probabilidad constante puede diferir mucho entre un tipo de núcleo y otro, lo que lleva a las diferentes tasas de desintegración observadas. Sin embargo, cualquiera que sea la probabilidad, no cambia con el tiempo. Esto contrasta marcadamente con los objetos complejos que sí muestran envejecimiento, como los automóviles y los humanos. Estos sistemas envejecidos tienen una probabilidad de fallar por unidad de tiempo que aumenta desde el momento en que comienzan su existencia.
Los procesos agregados, como la desintegración radiactiva de un conjunto de átomos, para los cuales la probabilidad de realización de un solo evento es muy pequeña pero en el que el número de intervalos de tiempo es tan grande que, no obstante, existe una tasa razonable de eventos, se modelan mediante la distribución de Poisson , que es discreta. La desintegración radiactiva y las reacciones de partículas nucleares son dos ejemplos de tales procesos agregados. [33] Las matemáticas de los procesos de Poisson se reducen a la ley de desintegración exponencial , que describe el comportamiento estadístico de un gran número de núcleos, en lugar de un núcleo individual. En el siguiente formalismo, el número de núcleos o la población de núcleos N es, por supuesto, una variable discreta (un número natural ), pero para cualquier muestra física N es tan grande que puede tratarse como una variable continua. El cálculo diferencial se utiliza para modelar el comportamiento de la desintegración nuclear.
Considere el caso de un nucleido A que se desintegra en otro B mediante algún proceso A → B (emisión de otras partículas, como neutrinos electrónicos
v
miy los electrones e − como en la desintegración beta , son irrelevantes en lo que sigue). La desintegración de un núcleo inestable es completamente aleatoria en el tiempo, por lo que es imposible predecir cuándo se desintegrará un átomo en particular. Sin embargo, es igualmente probable que se descomponga en cualquier instante. Por lo tanto, dada una muestra de un radioisótopo particular, el número de eventos de desintegración −d N que se espera que ocurran en un pequeño intervalo de tiempo d t es proporcional al número de átomos presentes N , es decir [34]
Ciertos radionucleidos se desintegran a diferentes velocidades, por lo que cada uno tiene su propia constante de desintegración λ . La caída esperada −d N / N es proporcional a un incremento de tiempo, d t :
El signo negativo indica que N disminuye a medida que aumenta el tiempo, ya que los eventos de desintegración se suceden uno tras otro. La solución de esta ecuación diferencial de primer orden es la función :
donde N 0 es el valor de N en el momento t = 0, con la constante de caída expresada como λ [34]
Tenemos para todos los tiempos t :
donde N total es el número constante de partículas a lo largo del proceso de desintegración, que es igual al número inicial de nucleidos A ya que esta es la sustancia inicial.
Si el número de núcleos A no desintegrados es:
entonces el número de núcleos de B (es decir, el número de núcleos A desintegrados ) es
El número de desintegraciones observadas en un intervalo determinado obedece a la estadística de Poisson . Si el número promedio de desintegraciones es ⟨ N ⟩ , la probabilidad de un número dado de desintegraciones N es [34]
Consideremos ahora el caso de una cadena de dos desintegraciones: un nucleido A desintegrándose en otro B mediante un proceso, luego B desintegrándose en otro C mediante un segundo proceso, es decir, A → B → C. La ecuación anterior no se puede aplicar a la cadena de desintegración, pero se puede generalizar de la siguiente manera. Dado que A se desintegra en B , luego B se desintegra en C , la actividad de A se suma al número total de nucleidos B en la presente muestra, antes de que esos nucleidos B se descompongan y reduzcan el número de nucleidos que conducen a la muestra posterior. En otras palabras, el número de núcleos B de segunda generación aumenta como resultado de la desintegración de los núcleos de primera generación de A , y disminuye como resultado de su propia desintegración en los núcleos C de tercera generación . [35] La suma de estos dos términos da la ley de una cadena de desintegración para dos nucleidos:
La tasa de cambio de NB , es decir, d N B / d t , está relacionada con los cambios en las cantidades de A y B , NB puede aumentar a medida que B se produce a partir de A y disminuir a medida que B produce C.
Reescribiendo usando los resultados anteriores:
Los subíndices simplemente se refieren a los respectivos nucleidos, es decir, N A es el número de nucleidos de tipo A ; N A 0 es el número inicial de nucleidos de tipo A ; λ A es la constante de desintegración de A – y de manera similar para el nucleido B. Resolver esta ecuación para NB da :
En el caso de que B sea un nucleido estable ( λ B = 0), esta ecuación se reduce a la solución anterior:
como se muestra arriba para una decadencia. La solución se puede encontrar mediante el método del factor de integración , donde el factor integrante es e λ B t . Este caso es quizás el más útil ya que puede derivar más directamente tanto la ecuación de una desintegración (arriba) como la ecuación para cadenas de múltiples desintegraciones (abajo).
Para el caso general de cualquier número de desintegraciones consecutivas en una cadena de desintegración, es decir, A 1 → A 2 ··· → A i ··· → A D , donde D es el número de desintegraciones e i es un índice ficticio ( i = 1, 2, 3, ..., D ), cada población de nucleidos se puede encontrar en términos de la población anterior. En este caso N 2 = 0 , N 3 = 0 , ..., N D = 0 . Usando el resultado anterior en forma recursiva:
La solución general al problema recursivo viene dada por las ecuaciones de Bateman : [36]
En todos los ejemplos anteriores, el nucleido inicial se desintegra en un solo producto. [37] Considere el caso de un nucleido inicial que puede desintegrarse en cualquiera de dos productos, es decir, A → B y A → C en paralelo. Por ejemplo, en una muestra de potasio-40 , el 89,3% de los núcleos se desintegran en calcio-40 y el 10,7% en argón-40 . Tenemos para todos los tiempos t :
que es constante, ya que el número total de nucleidos permanece constante. Diferenciando con respecto al tiempo:
definiendo la constante de desintegración total λ en términos de la suma de las constantes de desintegración parcial λ B y λ C :
Resolviendo esta ecuación para N A :
donde N A 0 es el número inicial de nucleido A. Al medir la producción de un nucleido, solo se puede observar la constante de desintegración total λ . Las constantes de desintegración λ B y λ C determinan la probabilidad de que la desintegración dé como resultado los productos B o C de la siguiente manera:
porque la fracción λ B / λ de núcleos se desintegra en B mientras que la fracción λ C / λ de núcleos se desintegra en C.
Las ecuaciones anteriores también se pueden escribir usando cantidades relacionadas con el número de partículas de nucleidos N en una muestra;
donde N A =6.022 140 76 × 10 23 mol −1 38] es la constante de Avogadro , M es la masa molar de la sustancia en kg/mol y la cantidad de la sustancia n está en moles .
Para la solución de una desintegración A → B :
la ecuación indica que la constante de desintegración λ tiene unidades de t −1 y, por lo tanto, también se puede representar como 1/ τ , donde τ es un tiempo característico del proceso llamado constante de tiempo .
En un proceso de desintegración radiactiva, esta constante de tiempo es también la vida media de los átomos en descomposición. Cada átomo "vive" durante un período de tiempo finito antes de desintegrarse, y se puede demostrar que esta vida media es la media aritmética de la vida útil de todos los átomos, y que es τ , que nuevamente está relacionada con la constante de desintegración como sigue:
Esta forma también es válida para procesos de dos desintegraciones simultáneamente A → B + C , insertando los valores equivalentes de las constantes de desintegración (como se indica arriba)
en la solución de descomposición conduce a:
Un parámetro más comúnmente utilizado es la vida media T 1/2 . Dada una muestra de un radionucleido en particular, la vida media es el tiempo que tardan en desintegrarse la mitad de los átomos del radionucleido. Para el caso de reacciones nucleares de una desintegración:
la vida media está relacionada con la constante de desintegración de la siguiente manera: establezca N = N 0 /2 y t = T 1/2 para obtener
Esta relación entre la vida media y la constante de desintegración muestra que las sustancias altamente radiactivas se agotan rápidamente, mientras que las que irradian débilmente duran más. Las vidas medias de los radionucleidos conocidos varían en casi 54 órdenes de magnitud, desde más de2,25(9) × 10 24 años (6,9 × 10 31 seg) para el nucleido casi estable 128 Te , para8,6 (6) × 10 −23 segundos para el nucleido altamente inestable 5 H . [26]
El factor de ln(2) en las relaciones anteriores resulta del hecho de que el concepto de "vida media" es simplemente una forma de seleccionar una base diferente a la base natural e para la expresión del tiempo de vida. La constante de tiempo τ es la vida e −1 , el tiempo hasta que sólo queda 1/ e , alrededor del 36,8%, en lugar del 50% en la vida media de un radionucleido. Por tanto, τ es más largo que t 1/2 . Se puede demostrar que la siguiente ecuación es válida:
Dado que la desintegración radiactiva es exponencial con una probabilidad constante, cada proceso podría describirse fácilmente con un período de tiempo constante diferente que (por ejemplo) dio su "(1/3) de vida" (cuánto tiempo hasta que solo quede 1/3) o "(1/10)-vida" (un período de tiempo hasta que sólo queda el 10%), y así sucesivamente. Por lo tanto, la elección de τ y t 1/2 para los tiempos de marcador es solo por conveniencia y por convención. Reflejan un principio fundamental sólo en la medida en que muestran que la misma proporción de una sustancia radiactiva determinada se desintegrará durante cualquier período de tiempo que uno elija.
Matemáticamente, la enésima vida para la situación anterior se encontraría de la misma manera que antes: estableciendo N = N 0 /n , t = T 1/ n y sustituyendo en la solución de desintegración para obtener
El carbono 14 tiene una vida media de5700(30) años [26] y una tasa de desintegración de 14 desintegraciones por minuto (dpm) por gramo de carbono natural.
Si se descubre que un artefacto tiene una radiactividad de 4 dpm por gramo de su C actual, podemos encontrar la edad aproximada del objeto usando la ecuación anterior:
dónde:
Se sabe que los modos de desintegración radiactiva de captura de electrones y conversión interna son ligeramente sensibles a los efectos químicos y ambientales que cambian la estructura electrónica del átomo, lo que a su vez afecta la presencia de electrones 1s y 2s que participan en el proceso de desintegración. Un pequeño número de nucleidos se ven afectados. [39] Por ejemplo, los enlaces químicos pueden afectar la tasa de captura de electrones en un pequeño grado (en general, menos del 1%) dependiendo de la proximidad de los electrones al núcleo. En 7 Be se ha observado una diferencia del 0,9% entre las vidas medias en ambiente metálico y aislante. [40] Este efecto relativamente grande se debe a que el berilio es un átomo pequeño cuyos electrones de valencia están en orbitales atómicos 2s , que están sujetos a captura de electrones en 7 Be porque (como todos los orbitales atómicos s en todos los átomos) penetran naturalmente en el núcleo.
En 1992, Jung et al. del grupo de investigación de iones pesados de Darmstadt observaron una desintegración β acelerada de 163 Dy 66+ . Aunque el 163 Dy neutro es un isótopo estable, el 163 Dy 66+ completamente ionizado sufre una desintegración β en las capas K y L hasta 163 Ho 66+ con una vida media de 47 días. [41]
El renio-187 es otro ejemplo espectacular. 187 Re normalmente sufre desintegración beta a 187 Os con una vida media de 41,6 × 10 9 años, [42] pero estudios que utilizan átomos de 187 Re completamente ionizados (núcleos desnudos) han encontrado que esto puede disminuir a solo 32,9 años. [43] Esto se atribuye a la " desintegración β en estado ligado " del átomo completamente ionizado: el electrón se emite a la "capa K" ( orbital atómico 1s ), lo que no puede ocurrir en átomos neutros en los que todos los átomos bajos Los estados vinculados están ocupados. [44]
Varios experimentos han descubierto que las tasas de desintegración de otros modos de radioisótopos artificiales y naturales no se ven afectados, con un alto grado de precisión, por condiciones externas como la temperatura, la presión, el entorno químico y los campos eléctricos, magnéticos o gravitacionales. [45] Comparación de experimentos de laboratorio durante el último siglo, estudios del reactor nuclear natural de Oklo (que ejemplificó los efectos de los neutrones térmicos en la desintegración nuclear) y observaciones astrofísicas de las desintegraciones de luminosidad de supernovas distantes (que ocurrieron muy lejos, por lo que la luz ha tardado mucho tiempo en llegar hasta nosotros), por ejemplo, indican claramente que las tasas de desintegración no perturbadas han sido constantes (al menos dentro de las limitaciones de pequeños errores experimentales) también en función del tiempo. [ cita necesaria ]
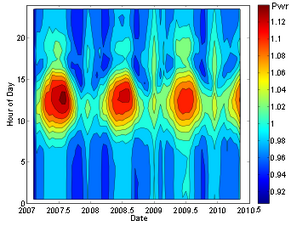
Resultados recientes sugieren la posibilidad de que las tasas de descomposición tengan una débil dependencia de factores ambientales. Se ha sugerido que las mediciones de las tasas de desintegración del silicio-32 , el manganeso-54 y el radio-226 presentan pequeñas variaciones estacionales (del orden del 0,1%). [46] [47] [48] Sin embargo, tales mediciones son muy susceptibles a errores sistemáticos, y un artículo posterior [49] no ha encontrado evidencia de tales correlaciones en otros siete isótopos ( 22 Na, 44 Ti, 108 Ag, 121 Sn , 133 Ba, 241 Am, 238 Pu), y establece límites superiores a la magnitud de dichos efectos. Alguna vez se informó que la desintegración del radón-222 exhibía grandes variaciones estacionales de pico a pico del 4% (ver gráfico), [50] que se propuso que estuvieran relacionadas con la actividad de las llamaradas solares o con la distancia al Sol, pero un análisis detallado Los defectos de diseño del experimento, junto con las comparaciones con otros experimentos mucho más estrictos y sistemáticamente controlados, refutan esta afirmación. [51]
Una serie inesperada de resultados experimentales sobre la velocidad de desintegración de iones radiactivos pesados y altamente cargados que circulan en un anillo de almacenamiento ha provocado actividad teórica en un esfuerzo por encontrar una explicación convincente. Se ha descubierto que las velocidades de desintegración débil de dos especies radiactivas con vidas medias de aproximadamente 40 s y 200 s tienen una modulación oscilatoria significativa , con un período de aproximadamente 7 s. [52] El fenómeno observado se conoce como anomalía GSI , ya que el anillo de almacenamiento es una instalación en el Centro GSI Helmholtz para la Investigación de Iones Pesados en Darmstadt , Alemania . Como el proceso de desintegración produce un neutrino electrónico , algunas de las explicaciones propuestas para la oscilación de velocidad observada invocan propiedades del neutrino. Las ideas iniciales relacionadas con la oscilación del sabor fueron recibidas con escepticismo. [53] Una propuesta más reciente implica diferencias de masa entre estados propios de masa de neutrinos . [54]
Los neutrones y protones que constituyen los núcleos, así como otras partículas que se acercan lo suficiente a ellos, se rigen por varias interacciones. La fuerza nuclear (también conocida como fuerza fuerte residual ), que no se observa en la escala macroscópica familiar , es la fuerza más poderosa en distancias subatómicas. La fuerza electrostática es casi siempre significativa y, en el caso de la desintegración beta , también interviene la fuerza nuclear débil .
Los efectos combinados de estas fuerzas producen una serie de fenómenos diferentes en los que la energía puede liberarse mediante la reordenación de partículas en el núcleo, o bien el cambio de un tipo de partícula en otro. Estos reordenamientos y transformaciones pueden verse obstaculizados energéticamente para que no ocurran inmediatamente. La vida media de desintegración radiactiva de los nucleidos se ha medido en escalas de tiempo de 54 órdenes de magnitud, desde8,6(6) × 10 −23 segundos (para hidrógeno-5 ) a7,10(28) × 10 31 segundos (para telurio-128 ). [26] Los límites de estas escalas de tiempo están establecidos únicamente por la sensibilidad de la instrumentación, y no se conocen límites naturales sobre cuán breve [ cita necesaria ] o larga puede ser la vida media de desintegración radiactiva de un radionúclido. Un núcleo radiactivo (o cualquier sistema excitado en mecánica cuántica) es inestable y, por lo tanto, puede estabilizarse espontáneamente en un sistema menos excitado. La transformación resultante altera la estructura del núcleo y da como resultado la emisión de un fotón o de una partícula de alta velocidad que tiene masa (como un electrón, una partícula alfa u otro tipo). [55]
![]() Portal de tecnología nuclear
Portal de tecnología nuclear![]() Portal de física
Portal de física
[1] [2]