
La quiralidad ( / k aɪ ˈ r æ l ɪ t i / ) es una propiedad de asimetría importante en varias ramas de la ciencia. La palabra quiralidad se deriva del griego χείρ ( kheir ), "mano", un objeto quiral familiar.
Un objeto o un sistema es quiral si es distinguible de su imagen especular ; es decir, no puede superponerse (no confundirse con superponerse) a él. Por el contrario, una imagen especular de un objeto aquiral , como una esfera, no puede distinguirse del objeto. Un objeto quiral y su imagen especular se denominan enantiomorfos (del griego, "formas opuestas") o, cuando se hace referencia a moléculas, enantiómeros . Un objeto no quiral se denomina aquiral (a veces también anfiquiral ) y puede superponerse a su imagen especular.
El término fue utilizado por primera vez por Lord Kelvin en 1893 en la segunda conferencia Robert Boyle en el Club Científico Juvenil de la Universidad de Oxford , que se publicó en 1894:
Llamo a cualquier figura geométrica o grupo de puntos "quiral", y digo que tiene quiralidad si su imagen en un espejo plano, idealmente realizado, no puede hacerse coincidir consigo misma. [1]
Las manos humanas son quizás el ejemplo más reconocido de quiralidad. La mano izquierda es una imagen especular no superponible de la mano derecha; sin importar cómo estén orientadas las dos manos, es imposible que todas las características principales de ambas manos coincidan en todos los ejes. [2] Esta diferencia de simetría se hace evidente si alguien intenta estrechar la mano derecha de una persona usando su mano izquierda, o si se coloca un guante de mano izquierda en una mano derecha. En matemáticas, la quiralidad es la propiedad de una figura que no es idéntica a su imagen especular.


En matemáticas , una figura es quiral (y se dice que tiene quiralidad) si no se puede representar en su imagen especular solo mediante rotaciones y traslaciones . Por ejemplo, un zapato derecho es diferente de un zapato izquierdo, y el sentido de las agujas del reloj es diferente del sentido contrario a las agujas del reloj. Véase [3] para una definición matemática completa.
Se dice que un objeto quiral y su imagen especular son enantiomorfos. La palabra enantiomorfo proviene del griego ἐναντίος ( enantios ) 'opuesto' + μορφή ( morphe ) 'forma'. Una figura no quiral se llama aquiral o anfiquiral.
La hélice (y por extensión una cuerda hilada, un tornillo, una hélice, etc.) y la banda de Möbius son objetos quirales bidimensionales en un espacio ambiental tridimensional. Los tetrominós en forma de J, L, S y Z del popular videojuego Tetris también presentan quiralidad, pero solo en un espacio bidimensional.
Muchos otros objetos familiares presentan la misma simetría quiral del cuerpo humano, como los guantes, las gafas (a veces) y los zapatos. Una noción similar de quiralidad se considera en la teoría de nudos , como se explica a continuación.
A algunos objetos tridimensionales quirales, como la hélice, se les puede asignar lateralidad derecha o izquierda, según la regla de la mano derecha .
En geometría , una figura es aquiral si y solo si su grupo de simetría contiene al menos una isometría de inversión de orientación . En dos dimensiones, toda figura que posee un eje de simetría es aquiral, y se puede demostrar que toda figura aquiral acotada debe tener un eje de simetría. En tres dimensiones, toda figura que posee un plano de simetría o un centro de simetría es aquiral. Sin embargo, existen figuras aquirales que carecen tanto de plano como de centro de simetría. En términos de grupos puntuales , todas las figuras quirales carecen de un eje de rotación impropio (S n ). Esto significa que no pueden contener un centro de inversión (i) o un plano de simetría (σ). Solo las figuras con una designación de grupo puntual de C 1 , C n , D n , T, O o I pueden ser quirales.
Un nudo se denomina aquiral si puede deformarse continuamente hasta convertirse en su imagen especular; de lo contrario, se denomina quiral. Por ejemplo, el nudo desuniforme y el nudo en forma de ocho son aquirales, mientras que el nudo de trébol es quiral.
En física, la quiralidad se puede encontrar en el espín de una partícula, donde la lateralidad del objeto está determinada por la dirección en la que gira la partícula. [4] No debe confundirse con la helicidad , que es la proyección del espín a lo largo del momento lineal de una partícula subatómica, la quiralidad es una propiedad mecánica cuántica intrínseca, como el espín. Aunque tanto la quiralidad como la helicidad pueden tener propiedades levógiras o dextrógiras, solo en el caso sin masa son idénticas. [5] En particular, para una partícula sin masa, la helicidad es la misma que la quiralidad, mientras que para una antipartícula tienen signo opuesto.
La lateralidad tanto en la quiralidad como en la helicidad se relaciona con la rotación de una partícula mientras se mueve linealmente con referencia a las manos humanas. El pulgar de la mano apunta hacia la dirección del movimiento lineal mientras que los dedos se curvan hacia la palma, lo que representa la dirección de rotación de la partícula (es decir, en el sentido de las agujas del reloj y en el sentido contrario). Dependiendo del movimiento lineal y rotacional, la partícula puede definirse por lateralidad zurda o derecha. [5] Una transformación de simetría entre las dos se llama paridad . La invariancia bajo paridad por un fermión de Dirac se llama simetría quiral .
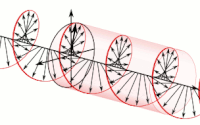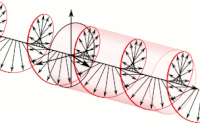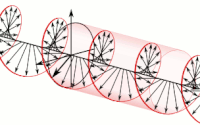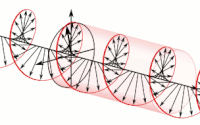
Las ondas electromagnéticas pueden tener una lateralidad asociada a su polarización . La polarización de una onda electromagnética es la propiedad que describe la orientación , es decir, la dirección y amplitud variables en el tiempo , del vector de campo eléctrico . Por ejemplo, los vectores de campo eléctrico de ondas polarizadas circularmente, tanto dextrógiras como levógiras, forman hélices de lateralidad opuesta en el espacio.
Las ondas polarizadas circularmente de quiralidad opuesta se propagan a través de medios quirales a diferentes velocidades ( birrefringencia circular ) y con diferentes pérdidas ( dicroísmo circular ). Ambos fenómenos se conocen conjuntamente como actividad óptica. La birrefringencia circular provoca la rotación del estado de polarización de las ondas electromagnéticas en medios quirales y puede causar un índice de refracción negativo para las ondas de quiralidad única cuando el efecto es suficientemente grande. [6] [7]
Si bien la actividad óptica ocurre en estructuras que son quirales en tres dimensiones (como las hélices), el concepto de quiralidad también se puede aplicar en dos dimensiones. Los patrones quirales 2D , como las espirales planas, no se pueden superponer con su imagen especular por traslación o rotación en un espacio bidimensional (un plano). La quiralidad 2D está asociada con la transmisión asimétrica direccional (reflexión y absorción) de ondas polarizadas circularmente. Los materiales quirales 2D, que también son anisotrópicos y con pérdidas, exhiben diferentes niveles de transmisión total (reflexión y absorción) para la misma onda polarizada circularmente incidente en su parte frontal y posterior. El fenómeno de transmisión asimétrica surge de diferentes eficiencias de conversión de polarización circular, por ejemplo, de izquierda a derecha, para direcciones de propagación opuestas de la onda incidente y, por lo tanto, el efecto se conoce como dicroísmo de conversión circular. De la misma manera que la torsión de un patrón quiral bidimensional parece invertirse para direcciones de observación opuestas, los materiales quirales bidimensionales tienen propiedades intercambiadas para ondas polarizadas circularmente dextrógiras y levógiras que inciden en su parte frontal y posterior. En particular, las ondas polarizadas circularmente dextrógiras y levógiras experimentan asimetrías de transmisión direccionales opuestas (reflexión y absorción). [8] [9]
Si bien la actividad óptica está asociada con la quiralidad 3D y la conversión circular está asociada con la quiralidad 2D, ambos efectos también se han observado en estructuras que no son quirales por sí mismas. Para la observación de estos efectos electromagnéticos quirales, la quiralidad no tiene que ser una propiedad intrínseca del material que interactúa con la onda electromagnética. En cambio, ambos efectos también pueden ocurrir cuando la dirección de propagación de la onda electromagnética junto con la estructura de un material (aquiral) forman una disposición experimental quiral. [10] [11] Este caso, donde la disposición mutua de los componentes aquirales forma una disposición quiral (experimental), se conoce como quiralidad extrínseca. [12] [13]
Los espejos quirales son una clase de metamateriales que reflejan la luz polarizada circularmente de una determinada helicidad de una manera que preserva la lateralidad, mientras que absorben la polarización circular de la lateralidad opuesta. [14] Sin embargo, la mayoría de los espejos quirales absorbentes operan solo en una banda de frecuencia estrecha, tal como lo limita el principio de causalidad. Al emplear una metodología de diseño diferente que permite que las ondas no deseadas pasen a través de ellos en lugar de absorber la forma de onda no deseada, los espejos quirales pueden mostrar un buen rendimiento de banda ancha. [15]

Una molécula quiral es un tipo de molécula que tiene una imagen especular no superponible . La característica que suele ser la causa de la quiralidad en las moléculas es la presencia de un átomo de carbono asimétrico . [16] [17]
El término "quiral" en general se utiliza para describir el objeto que no es superponible en su imagen especular. [18]
En química, la quiralidad generalmente se refiere a moléculas. Dos imágenes especulares de una molécula quiral se denominan enantiómeros o isómeros ópticos . Los pares de enantiómeros a menudo se designan como " diestros ", "levógiros" o, si no tienen sesgo, "aquirales". A medida que la luz polarizada pasa a través de una molécula quiral, el plano de polarización, cuando se observa a lo largo del eje hacia la fuente, rotará en el sentido de las agujas del reloj (hacia la derecha) o en el sentido contrario a las agujas del reloj (hacia la izquierda). Una rotación hacia la derecha es dextrógira (d); la hacia la izquierda es levógira (l). Los isómeros d y l son el mismo compuesto, pero se denominan enantiómeros . Una mezcla equimolar de los dos isómeros ópticos, que se denomina mezcla racémica , no producirá una rotación neta de la luz polarizada a medida que pasa a través de ella. [19] Las moléculas zurdas tienen l- como prefijo en sus nombres; d- se antepone a las moléculas diestras. Sin embargo, esta notación d y l para distinguir enantiómeros no dice nada sobre la disposición espacial real de los ligandos/sustituyentes alrededor del centro estereogénico , que se define como configuración. Otro sistema de nomenclatura empleado para especificar la configuración es la convención de Fischer. [20] Esto también se conoce como el sistema D y L. Aquí la configuración relativa se asigna con referencia a D-(+)-gliceraldehído y L-(−)-gliceraldehído, que se toman como estándar. La convención de Fischer se usa ampliamente en la química del azúcar y para los α-aminoácidos. Debido a los inconvenientes de la convención de Fischer, se reemplaza casi por completo por la convención de Cahn-Ingold-Prelog , también conocida como la regla de secuencia o nomenclatura R y S. [21] [22] Esto se amplió aún más para asignar la configuración absoluta a los isómeros cis-trans con la notación EZ.
La quiralidad molecular es de interés debido a su aplicación a la estereoquímica en química inorgánica , química orgánica , química física , bioquímica y química supramolecular .
Los desarrollos más recientes en la química quiral incluyen el desarrollo de nanopartículas inorgánicas quirales que pueden tener una geometría tetraédrica similar a los centros quirales asociados con los átomos de carbono sp3 tradicionalmente asociados con los compuestos quirales, pero a mayor escala. [23] [24] También se obtuvieron simetrías helicoidales y de otro tipo de nanomateriales quirales . [25]
Todas las formas de vida conocidas muestran propiedades quirales específicas en las estructuras químicas, así como en la anatomía macroscópica, el desarrollo y el comportamiento. [26] En cualquier organismo específico o conjunto de ellos relacionados evolutivamente, los compuestos, órganos o comportamientos individuales se encuentran en la misma forma enantiomórfica única. La desviación (tener la forma opuesta) podría encontrarse en un pequeño número de compuestos químicos, o en ciertos órganos o comportamientos, pero esa variación depende estrictamente de la constitución genética del organismo. Desde el nivel químico (escala molecular), los sistemas biológicos muestran una estereoespecificidad extrema en la síntesis, la absorción, la detección y el procesamiento metabólico. Un sistema vivo generalmente trata con dos enantiómeros del mismo compuesto de formas drásticamente diferentes.
En biología, la homoquiralidad es una propiedad común de los aminoácidos y los carbohidratos . Los aminoácidos quirales que forman proteínas , que se traducen a través del ribosoma a partir de la codificación genética, se presentan en la forma L. Sin embargo, los aminoácidos D también se encuentran en la naturaleza. Los monosacáridos (unidades de carbohidratos) se encuentran comúnmente en la configuración D. La doble hélice del ADN es quiral (como cualquier tipo de hélice es quiral), y la forma B del ADN muestra un giro hacia la derecha.
A veces, cuando se encuentran dos enantiómeros de un compuesto en los organismos, difieren significativamente en su sabor, olor y otras acciones biológicas. Por ejemplo, la (+)- carvona es responsable del olor del aceite de semilla de alcaravea , mientras que la (–)-carvona es responsable del olor del aceite de menta verde . [27] Sin embargo, es un error común creer que el (+)-limoneno se encuentra en las naranjas (causando su olor) y el (–)-limoneno se encuentra en los limones (causando su olor). En 2021, después de una experimentación rigurosa, se descubrió que todos los frutos cítricos contienen solo (+)-limoneno y la diferencia de olor se debe a otros factores contribuyentes. [28]
Además, en el caso de compuestos artificiales, incluidos medicamentos, en el caso de fármacos quirales , los dos enantiómeros a veces muestran una diferencia notable en el efecto de sus acciones biológicas. [29] Darvon ( dextropropoxifeno ) es un analgésico, mientras que su enantiómero, Novrad ( levopropoxifeno ), es un agente antitusivo. En el caso de la penicilamina , el ( S -isómero se utiliza en el tratamiento de la artritis crónica primaria, mientras que el ( R )-isómero no tiene efecto terapéutico, además de ser altamente tóxico. [30] En algunos casos, el enantiómero menos activo terapéuticamente puede causar efectos secundarios. Por ejemplo, ( S -naproxeno es un analgésico pero el ( R -isómero causa problemas renales. [31] En tales situaciones donde uno de los enantiómeros de un fármaco racémico es activo y el otro socio tiene un efecto indeseable o tóxico, uno puede cambiar de racemato a un fármaco de un solo enantiómero para un mejor valor terapéutico. [1] Tal cambio de un fármaco racémico a un fármaco enantiopuro se llama cambio quiral .
La forma natural de alfa-tocoferol ( vitamina E ) en la planta es RRR-α-tocoferol, mientras que la forma sintética (vitamina E totalmente racémica o dl-tocoferol) es partes iguales de los estereoisómeros RRR, RRS, RSS, SSS, RSR, SRS, SRR y SSR con equivalencia biológica progresivamente decreciente, de modo que 1,36 mg de dl-tocoferol se considera equivalente a 1,0 mg de d-tocoferol. [32]
Se encuentran ejemplos macroscópicos de quiralidad en el reino vegetal, el reino animal y todos los demás grupos de organismos. Un ejemplo sencillo es la dirección de enrollamiento de cualquier planta trepadora, que puede crecer formando una hélice levógira o dextrógira.
En anatomía, la quiralidad se encuentra en la simetría de imagen especular imperfecta de muchos tipos de cuerpos animales. Organismos como los gasterópodos exhiben quiralidad en sus conchas enrolladas, lo que resulta en una apariencia asimétrica. Más del 90% de las especies de gasterópodos [33] tienen conchas dextrales (diestras) en su enrollamiento, pero una pequeña minoría de especies y géneros son virtualmente siempre sinistrales (zurdas). Unas pocas especies (por ejemplo Amphidromus perversus [34] ) muestran una mezcla igual de individuos dextrales y sinistrales.
En los seres humanos, la quiralidad (también denominada lateralidad o lateralidad ) es un atributo de los seres humanos definido por su distribución desigual de la motricidad fina entre la mano izquierda y la derecha . Un individuo que es más diestro con la mano derecha se denomina diestro y uno que es más hábil con la izquierda se dice que es zurdo . La quiralidad también se observa en el estudio de la asimetría facial y se conoce como asimetría aurofacial. [35]

Según la teoría del giro axial , los animales vertebrados evolucionan hacia una quiralidad levógira, por lo que el cerebro gira 90 ° y el corazón y los intestinos 90°. [36]
En el caso de la condición de salud situs inversus totalis , en la que todos los órganos internos están invertidos horizontalmente (es decir, el corazón se coloca ligeramente a la derecha en lugar de a la izquierda), la quiralidad plantea algunos problemas si el paciente requiere un trasplante de hígado o corazón, ya que estos órganos son quirales, lo que significa que los vasos sanguíneos que irrigan estos órganos necesitarían reorganizarse si se requiriera un órgano normal, no situs inversus ( situs solitus ).
En la familia de las monocotiledóneas , las especies de los géneros Wachendorfia y Barberetta tienen solo individuos que tienen el estilo apuntando hacia la derecha o el estilo apuntando hacia la izquierda, y ambos morfos aparecen dentro de las mismas poblaciones. Se cree que esto aumenta el cruzamiento y, por lo tanto, impulsa la diversidad genética, lo que a su vez puede ayudar a sobrevivir en un entorno cambiante. Sorprendentemente, el género relacionado Dilatris también tiene flores quiralmente dimórficas, pero aquí ambos morfos ocurren en la misma planta. [37] En los peces planos, la platija de verano o la platija son de ojo izquierdo, mientras que el fletán es de ojo derecho.