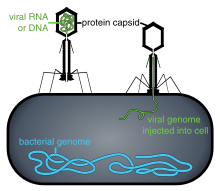

La fagoterapia , terapia con fagos virales o fagoterapia es el uso terapéutico de los bacteriófagos para el tratamiento de infecciones bacterianas patógenas . [1] [2] [3] Este enfoque terapéutico surgió a principios del siglo XX pero fue progresivamente reemplazado por el uso de antibióticos en la mayor parte del mundo después de la Segunda Guerra Mundial . Los bacteriófagos, conocidos como fagos, son una forma de virus [4] que se adhieren a las células bacterianas e inyectan su genoma en la célula. [5] La producción del genoma viral por parte de la bacteria interfiere con su capacidad de funcionar, deteniendo la infección bacteriana. [5] La célula bacteriana que causa la infección no puede reproducirse y, en cambio, produce fagos adicionales. [4] Los fagos son muy selectivos en las cepas de bacterias contra las que son eficaces. [5]
Las ventajas incluyen efectos secundarios reducidos y riesgo reducido de que la bacteria desarrolle resistencia, ya que [5] los bacteriófagos son mucho más específicos que los antibióticos. Por lo general, son inofensivos no sólo para el organismo huésped sino también para otras bacterias beneficiosas, como la microbiota intestinal , lo que reduce las posibilidades de infecciones oportunistas . [6] Tienen un alto índice terapéutico ; es decir, se esperaría que la terapia con fagos produjera pocos efectos secundarios , incluso a niveles superiores a los terapéuticos. [7] Debido a que los fagos se replican in vivo (en células de organismos vivos), se puede utilizar una dosis eficaz más pequeña. [8]
Las desventajas incluyen la dificultad de encontrar un fago eficaz para una infección particular; un fago matará una bacteria sólo si coincide con la cepa específica . [5] Sin embargo, los fagos virulentos se pueden aislar mucho más fácilmente que otros compuestos y productos naturales. [8] En consecuencia, a veces se utilizan mezclas de fagos ("cócteles") para mejorar las posibilidades de éxito. [9] Alternativamente, las muestras tomadas de pacientes en recuperación a veces contienen fagos apropiados que pueden cultivarse para curar a otros pacientes infectados con la misma cepa. [10] Los desafíos actuales incluyen la necesidad de aumentar las colecciones de fagos de los bancos de fagos de referencia, el desarrollo de métodos eficientes de detección de fagos para la identificación rápida de los fagos terapéuticos, el establecimiento de estrategias eficientes de terapia con fagos para abordar las biopelículas infecciosas, la validación de protocolos factibles de producción de fagos que aseguren la calidad y seguridad de las preparaciones de fagos, y la garantía de estabilidad de las preparaciones de fagos durante la fabricación, almacenamiento y transporte.
Los fagos tienden a tener más éxito que los antibióticos cuando hay una biopelícula cubierta por una capa de polisacárido, que los antibióticos normalmente no pueden penetrar. [11] La terapia con fagos puede dispersar la biopelícula generada por bacterias resistentes a los antibióticos. [12] Sin embargo, las interacciones entre fagos y biopelículas pueden ser complejas, y los fagos desarrollan relaciones simbióticas y depredadoras con las biopelículas. [9]
Actualmente, los fagos se utilizan terapéuticamente para tratar infecciones bacterianas que no responden a los antibióticos convencionales, [2] [1] [13] particularmente en Rusia [14] y Georgia . [15] [16] [17] También hay una unidad de terapia con fagos en Wrocław , Polonia, establecida en 2005, que continúa la investigación de varias décadas por parte del Instituto de Inmunología y Terapia Experimental de la Academia Polaca de Ciencias , la única dicho centro en un país de la Unión Europea. [18] Los fagos son objeto de renovada atención clínica en los países occidentales, como los Estados Unidos. En 2019, la Administración de Medicamentos y Alimentos de los Estados Unidos aprobó el primer ensayo clínico estadounidense para la terapia con fagos intravenosos. [19]
La terapia con fagos tiene muchas aplicaciones potenciales en la medicina humana, así como en odontología, veterinaria y agricultura. [20] Si el huésped objetivo de un tratamiento de terapia con fagos no es un animal, generalmente se emplea el término " biocontrol " (como en el biocontrol de bacterias mediado por fagos), en lugar de "terapia con fagos". [9]



El descubrimiento de los bacteriófagos fue informado por el bacteriólogo británico Frederick Twort en 1915 [21] y por el microbiólogo francés Felix d'Hérelle en 1917. [22] [23] D'Hérelle dijo que los fagos siempre aparecían en las heces de los pacientes con disentería por Shigella poco después. antes de que comenzaran a recuperarse. [24] "Aprendió rápidamente que los bacteriófagos se encuentran dondequiera que prosperen las bacterias: en las alcantarillas, en los ríos que recogen los desechos de las tuberías y en las heces de los pacientes convalecientes". [25] Muchos reconocieron inmediatamente que la terapia con fagos era un camino clave para la erradicación de infecciones bacterianas patógenas. Un georgiano, George Eliava , estaba haciendo descubrimientos similares. Viajó al Instituto Pasteur de París, donde conoció a d'Hérelle, y en 1923 fundó el Instituto de Bacteriología, que más tarde pasó a ser conocido como Instituto George Eliava , en Tbilisi , Georgia, dedicado al desarrollo de la terapia con fagos. [26] La terapia con fagos se utiliza en Rusia, [27] Georgia y Polonia, y se utilizó de forma profiláctica durante un tiempo en el ejército soviético, sobre todo durante la Segunda Guerra Mundial . [26]
En Rusia pronto se inició una extensa investigación y desarrollo en este campo. En los Estados Unidos, durante la década de 1940, la comercialización de la terapia con fagos estuvo a cargo de Eli Lilly and Company . [28]
Si bien se acumulaban conocimientos sobre la biología de los fagos y cómo utilizar correctamente los cócteles de fagos, los primeros usos de la terapia con fagos a menudo no eran fiables. [29] Desde principios del siglo XX, también se habían llevado a cabo investigaciones sobre el desarrollo de antibióticos terapéuticos viables, y en 1942, el antibiótico penicilina G se había purificado con éxito y se utilizó durante la Segunda Guerra Mundial. El fármaco demostró ser extraordinariamente eficaz en el tratamiento de soldados aliados heridos cuyas heridas se habían infectado. En 1944, se hizo posible la producción a gran escala de penicilina y, en 1945, estuvo disponible públicamente en las farmacias. Debido al éxito del fármaco, se comercializó ampliamente en EE. UU. y Europa, lo que llevó a los científicos occidentales a perder en su mayor parte el interés en un mayor uso y estudio de la terapia con fagos durante algún tiempo. [30]
Aislados de los avances occidentales en la producción de antibióticos en la década de 1940, los científicos rusos continuaron desarrollando una terapia con fagos que ya era exitosa para tratar las heridas de los soldados en los hospitales de campaña . Durante la Segunda Guerra Mundial, la Unión Soviética utilizó bacteriófagos para tratar a los soldados infectados con diversas enfermedades bacterianas, como la disentería y la gangrena. [31] Los investigadores rusos continuaron desarrollando y perfeccionando sus tratamientos y publicando sus investigaciones y resultados. Sin embargo, debido a las barreras científicas de la Guerra Fría , este conocimiento no fue traducido y no proliferó por todo el mundo. [32] [33] Un resumen de estas publicaciones se publicó en inglés en 2009 en "A Literature Review of the Practical Application of Bacteriophage Research". [34]
Hay una extensa biblioteca y un centro de investigación en el Instituto George Eliava en Tbilisi, Georgia. La terapia con fagos es hoy una forma de tratamiento muy extendida en esa región. [25] [24]
Como resultado del desarrollo de resistencia a los antibióticos desde la década de 1950 y el avance del conocimiento científico, ha habido un interés renovado en todo el mundo en la capacidad de la terapia con fagos para erradicar infecciones bacterianas y biopelículas polimicrobianas crónicas (incluso en situaciones industriales). [35]
Los fagos se han investigado como un medio potencial para eliminar patógenos como Campylobacter en alimentos crudos [36] y Listeria en alimentos frescos o para reducir las bacterias que deterioran los alimentos. [37] En la práctica agrícola, los fagos se han utilizado para combatir patógenos como Campylobacter , Escherichia y Salmonella en animales de granja, patógenos Lactococcus y Vibrio en la acuicultura de peces, y Erwinia , Xanthomonas y otros en plantas de importancia agrícola. [38] [39] [40] Sin embargo, el uso más antiguo se encuentra en la medicina humana. Los fagos se han utilizado contra enfermedades diarreicas causadas por E. coli , Shigella o Vibrio y contra infecciones de heridas causadas por patógenos facultativos de la piel como estafilococos y estreptococos . Recientemente, el enfoque de la terapia con fagos se ha aplicado a infecciones sistémicas e incluso intracelulares, y se han agregado al arsenal antimicrobiano fagos no replicantes y enzimas fago aisladas como las lisinas . Sin embargo, no se dispone de pruebas reales de la eficacia de estos métodos de fagos en el campo o en el hospital. [37]
Parte del interés en Occidente se remonta a 1994, cuando James Soothill demostró (en un modelo animal) que el uso de fagos podría mejorar el éxito de los injertos de piel al reducir la infección subyacente por Pseudomonas aeruginosa . [41] Estudios recientes han proporcionado apoyo adicional para estos hallazgos en el sistema modelo. [42]
Aunque no es una "terapia con fagos" en el sentido original, el uso de fagos como mecanismos de administración de antibióticos tradicionales constituye otro posible uso terapéutico. [43] [44] El uso de fagos para administrar agentes antitumorales también se ha descrito en experimentos preliminares in vitro para células en cultivo de tejidos. [45]
En junio de 2015, la Agencia Europea de Medicamentos organizó un taller de un día sobre el uso terapéutico de bacteriófagos, [46] y en julio de 2015, los Institutos Nacionales de Salud de EE. UU . organizaron un taller de dos días titulado "Terapia con bacteriófagos: una estrategia alternativa para Combatir la resistencia a los medicamentos". [47]
En enero de 2016, Benjamin Chan utilizó con éxito fagos en la Universidad de Yale para tratar una infección crónica por Pseudomonas aeruginosa en el oftalmólogo Ali Asghar Khodadoust . [48] Este tratamiento exitoso de una infección potencialmente mortal provocó un resurgimiento del interés en la terapia con fagos en los Estados Unidos. [ cita necesaria ]
En 2017, un par de fagos modificados genéticamente junto con uno natural (llamado "fago Muddy"), cada uno de los catalogados por SEA-PHAGES (Science Education Alliance-Phage Hunters Advancing Genomics and Evolutionary Science) en el Howard Hughes Medical Instituto de Graham Hatfull y colegas, fue utilizado por el microbiólogo James Soothill en el Hospital Infantil Great Ormond Street de Londres para tratar una infección bacteriana resistente a los antibióticos ( Mycobacterium abscessus ) en una mujer joven con fibrosis quística . [49] [50] [51] [52]
En 2022, se administraron dos micobacteriófagos por vía intravenosa dos veces al día a un hombre joven con infección pulmonar por Mycobacterium abscessus refractaria al tratamiento y enfermedad pulmonar por fibrosis quística grave. [53] Los cultivos de las vías respiratorias para M. abscessus se volvieron negativos después de aproximadamente 100 días de tratamiento combinado con fagos y antibióticos, y una variedad de biomarcadores confirmaron la respuesta terapéutica. El individuo recibió un trasplante de pulmón bilateral después de 379 días de tratamiento y los cultivos del tejido pulmonar explantado confirmaron la erradicación de la bacteria. [53] En un segundo caso, se informó un tratamiento exitoso de Mycobacterium chelonae cutáneo diseminado con un solo fago administrado por vía intravenosa dos veces al día junto con tratamiento antibiótico y quirúrgico. [54]

El tratamiento con bacteriófagos ofrece una posible alternativa a los tratamientos con antibióticos convencionales para la infección bacteriana. [55] Es concebible que, aunque las bacterias pueden desarrollar resistencia a los fagos, la resistencia podría ser más fácil de superar que la resistencia a los antibióticos. [56] [57] Los virus, al igual que las bacterias, pueden desarrollar resistencia a diferentes tratamientos. [58]
Los bacteriófagos son muy específicos y se dirigen sólo a una o unas pocas cepas de bacterias. [59] Los antibióticos tradicionales tienen un efecto más amplio, matando bacterias tanto dañinas como útiles, como las que facilitan la digestión de los alimentos . [60] La especificidad de especies y cepas de los bacteriófagos hace que sea poco probable que se eliminen bacterias inofensivas o útiles al combatir una infección. [61]
Unos pocos grupos de investigación en Occidente están diseñando un fago de espectro más amplio y también una variedad de formas de tratamientos para MRSA , incluidos apósitos impregnados para heridas, tratamientos preventivos para víctimas de quemaduras y suturas impregnadas de fagos. [62] [57] Los enzibióticos son un nuevo desarrollo en la Universidad Rockefeller que crean enzimas a partir de fagos. Las enzimas de fagos recombinantes purificadas se pueden utilizar como agentes antibacterianos separados por derecho propio. [63]
La terapia con fagos también tiene el potencial de prevenir o tratar enfermedades infecciosas de los corales . Esto podría mitigar la disminución global de los corales. [64]
Los fagos para uso terapéutico se pueden recolectar de fuentes ambientales que probablemente contengan grandes cantidades de bacterias y bacteriófagos, como salidas de efluentes , aguas residuales o incluso suelo. [15] Las muestras se toman y se aplican a los cultivos bacterianos que se van a seleccionar. Si las bacterias mueren, los fagos se pueden cultivar en cultivos líquidos. [10]
Los fagos son "específicos de la bacteria" y, por lo tanto, en muchos casos es necesario tomar un hisopo del paciente y cultivarlo antes del tratamiento. En ocasiones, el aislamiento de fagos terapéuticos puede tardar algunos meses en completarse, pero las clínicas generalmente mantienen suministros de cócteles de fagos para las cepas bacterianas más comunes en un área geográfica. [ cita necesaria ]
Los cócteles de fagos se venden habitualmente en farmacias de países de Europa del Este, como Rusia y Georgia . [65] [66] [67] La composición de los cócteles bacteriófagos se ha modificado periódicamente para agregar fagos eficaces contra cepas patógenas emergentes. [67]
En la práctica, los fagos se aplican por vía oral, tópica sobre heridas infectadas o se extienden sobre superficies o durante procedimientos quirúrgicos. Rara vez se utiliza la inyección, lo que evita cualquier riesgo de trazas de contaminantes químicos que puedan estar presentes en la etapa de amplificación de las bacterias y reconoce que el sistema inmunológico lucha naturalmente contra los virus introducidos en el torrente sanguíneo o el sistema linfático. [ cita necesaria ]
Las revisiones de la terapia con fagos indican que se necesita más investigación clínica y microbiológica para cumplir con los estándares actuales. [68]
La financiación para la investigación de la terapia con fagos y los ensayos clínicos es generalmente insuficiente y difícil de obtener, ya que patentar productos de bacteriófagos es un proceso largo y complejo. Debido a la especificidad de los fagos, la terapia con fagos sería más efectiva como una inyección de cóctel, una modalidad generalmente rechazada por la Administración de Alimentos y Medicamentos de EE. UU. (FDA). Por lo tanto, investigadores y observadores han predicho que para que la terapia con fagos gane terreno, la FDA debe cambiar su postura regulatoria sobre los cócteles de medicamentos combinados. [6] La concientización pública y la educación sobre la terapia con fagos generalmente se limitan a investigaciones científicas o independientes en lugar de a los medios de comunicación convencionales. [69]
En 2007, se completaron los ensayos clínicos de fase 1 y 2 en el Royal National Throat, Nose and Ear Hospital de Londres para infecciones por Pseudomonas aeruginosa ( otitis ). [70] [71] [72] [73] Se llevaron a cabo ensayos clínicos de fase 1 en el Centro Regional de Atención de Heridas del Suroeste de Lubbock , Texas, para un cóctel de fagos contra P. aeruginosa , Staphylococcus aureus y Escherichia coli , desarrollado por Intralytix . [74] PhagoBurn , un ensayo de fase 1 y 2 de terapia con fagos contra la infección de heridas por P. aeruginosa en Francia y Bélgica entre 2015 y 2017, finalizó anticipadamente debido a su falta de eficacia. [75]
Locus Biosciences ha creado un cóctel de tres fagos modificados con CRISPR . Un estudio de 2019 examinó su eficacia contra E. coli en el tracto urinario , [76] y poco antes de marzo de 2021 se completó un ensayo de fase 1. [77] En febrero de 2019, la FDA aprobó el primer ensayo clínico de terapia con fagos administrados por vía intravenosa. en los Estados Unidos. [78]
En julio de 2020, la FDA aprobó el primer ensayo clínico de terapia con fagos nebulizados en los Estados Unidos. [79] Este estudio doble ciego controlado con placebo en la Universidad de Yale se centrará en el tratamiento de infecciones por P. aeruginosa en pacientes con fibrosis quística.
En febrero de 2020, la FDA aprobó un ensayo clínico para evaluar la terapia con bacteriófagos en pacientes con infecciones del tracto urinario. [80] El estudio comenzó en diciembre de 2020 y tiene como objetivo identificar regímenes ideales de tratamiento con bacteriófagos basados en mejoras en las tasas de control de enfermedades.
En febrero de 2021, la FDA aprobó un ensayo clínico para evaluar la terapia con bacteriófagos en pacientes con infecciones crónicas de prótesis articulares (PJI). [81] El estudio debía comenzar en octubre de 2022 y ser realizado por Adaptive Phage Therapeutics, en colaboración con la Clínica Mayo .
Por lo general, los fagos se pueden liofilizar y convertir en píldoras sin reducir materialmente su eficiencia. [15] Se ha demostrado una estabilidad de temperatura de hasta 55 °C y una vida útil de 14 meses para algunos tipos de fagos en forma de píldora. [15] Es posible la aplicación en forma líquida, conservada preferentemente en viales refrigerados. [15] La administración oral funciona mejor cuando se incluye un antiácido , ya que esto aumenta la cantidad de fagos que sobreviven al paso a través del estómago. [15] La administración tópica a menudo implica la aplicación de gasas que se colocan sobre el área a tratar. [15]
Benjamin Chan utilizó con éxito fagos en la Universidad de Yale para tratar una infección por Pseudomonas en 2016. [48] La terapia por goteo de fagos intravenosos se utilizó con éxito para tratar a un paciente con Acinetobacter baumannii multirresistente en el Hospital Thornton de UC San Diego en 2017. [82 ] La terapia con fagos nebulizados se ha utilizado con éxito para tratar a numerosos pacientes con fibrosis quística y bacterias multirresistentes en la Universidad de Yale como parte de su programa de uso compasivo . [83] [84] En 2019, un residente de Brownsville , Minnesota, con una infección bacteriana de larga data en la rodilla, recibió un tratamiento con fagos en la Clínica Mayo que eliminó la necesidad de amputarle la parte inferior de la pierna. [85] Robert T. Schooley y otros también utilizaron con éxito la terapia individualizada con fagos para tratar un caso de Acinetobacter baumannii multirresistente en 2015. [86] [87] En 2022, se utilizó una combinación de fagos y antibióticos ajustada individualmente como El tratamiento de la resistencia a los antimicrobianos se demostró y describió en detalle. [88] [89] Los científicos pidieron ampliar la investigación [90] y seguir desarrollando este enfoque. [91]

La terapia con fagos se está utilizando con gran efecto en el tratamiento de infecciones por biopelículas , especialmente Pseudomonas aeruginosa y Staphylococcus aureus . [92] [93] De 78 casos recientes de tratamiento de infecciones por biopelículas, el 96% de los pacientes experimentaron una mejoría clínica utilizando la terapia con fagos, y el 52% de los pacientes vieron un alivio completo de los síntomas o una eliminación completa de las bacterias afectadas. [92] Las infecciones por biopelículas son muy difíciles de tratar con antibióticos. La matriz de la biopelícula y las membranas bacterianas circundantes pueden unirse a los antibióticos, impidiendo que penetren en la biopelícula. La matriz puede contener enzimas que desactivan los antibióticos. Las biopelículas también tienen una baja actividad metabólica, lo que significa que los antibióticos que se dirigen a los procesos de crecimiento tienen una eficacia mucho menor. Estos factores hacen que la terapia con fagos sea una opción atractiva para el tratamiento de este tipo de infecciones, y actualmente existen dos formas de realizar dicho tratamiento. La primera es aislar la bacteria inicial y crear un fago de tratamiento específico para atacarla, mientras que la segunda forma es utilizar una combinación de fagos más generales. [93] La ventaja del segundo método es que puede comercializarse fácilmente para el tratamiento, aunque existen algunas preocupaciones de que pueda ser sustancialmente menos eficaz. [92]

La alta especificidad de cepa bacteriana de la terapia con fagos puede hacer necesario que las clínicas preparen diferentes cócteles para el tratamiento de la misma infección o enfermedad, porque los componentes bacterianos de dichas enfermedades pueden diferir de una región a otra o incluso de una persona a otra. Además, esto significa que se deben mantener y actualizar periódicamente "bancos" que contengan muchos fagos diferentes con nuevos fagos. [6]
Además, las bacterias pueden desarrollar diferentes receptores antes o durante el tratamiento. Esto puede evitar que los fagos los erradiquen por completo. [15]
La necesidad de bancos de fagos hace que las pruebas regulatorias de seguridad sean más difíciles y costosas según las normas actuales en la mayoría de los países. Un proceso así dificultaría el uso a gran escala de la terapia con fagos. Además, las cuestiones de patentes (específicamente sobre organismos vivos) pueden complicar la distribución para las empresas farmacéuticas que deseen tener derechos exclusivos sobre su "invención", lo que disuadiría a una corporación comercial de invertir capital en esto.
Como se sabe desde hace al menos treinta años, las micobacterias como Mycobacterium tuberculosis tienen bacteriófagos específicos. [94] Aún no se ha descubierto ningún fago lítico para Clostridium difficile , que es responsable de muchas enfermedades nosocomiales , pero se conocen algunos fagos templados (integrados en el genoma, también llamados lisogénicos ) para esta especie; Esto abre vías alentadoras pero con riesgos adicionales, como se analiza más adelante.
La percepción pública negativa de los virus también puede influir en la renuencia a adoptar la terapia con fagos. [95]
Una de las principales preocupaciones generalmente asociadas con la terapia con fagos es la aparición de mutantes insensibles a los fagos (BIM) que podrían obstaculizar el éxito de esta terapia. De hecho, varios estudios in vitro han informado de una rápida aparición de BIM en un corto período de tiempo después del tratamiento con fagos. [96] [97] [98] La aparición de BIM también se ha observado in vivo utilizando diferentes modelos animales, aunque esto suele ocurrir más tarde que in vitro (revisado en [99] ). Esta rápida adaptación de las bacterias al ataque de los fagos suele ser causada por mutaciones en genes que codifican los receptores de los fagos, [97] [100] que incluyen lipopolisacáridos (LPS), proteínas de la membrana externa , cápsulas , flagelos y pili , entre otros. [101] Sin embargo, algunos estudios sugieren que cuando la resistencia a los fagos es causada por mutaciones en los receptores de los fagos, esto podría generar costos de aptitud para la bacteria resistente, que en última instancia se volverá menos virulenta. [99] [102] Además, se ha demostrado que la evolución de la resistencia bacteriana al ataque de fagos cambia el mecanismo de la bomba de eflujo, lo que provoca una mayor sensibilidad a los fármacos de varias clases de antibióticos. [103] Por lo tanto, es concebible pensar que la terapia con fagos que utiliza fagos que ejercen una selección para que las bacterias resistentes a múltiples medicamentos se vuelvan sensibles a los antibióticos podría reducir potencialmente la incidencia de infecciones resistentes a los antibióticos.
Además de la prevención de la adsorción de fagos por pérdida o modificación de receptores bacterianos, la insensibilidad a los fagos puede ser causada por: (i) prevención de la entrada del ADN de los fagos mediante sistemas de exclusión de superinfección; (ii) degradación del ADN del fago mediante sistemas de modificación de restricción o mediante sistemas CRISPR-Cas ; y (iii) uso de sistemas de infección abortivos que bloquean la replicación, transcripción o traducción de fagos, generalmente junto con el suicidio de la célula huésped. [104] En conjunto, estos mecanismos promueven una rápida adaptación de las bacterias al ataque de los fagos y, por lo tanto, la aparición de mutantes resistentes a los fagos es frecuente e inevitable.
Aún no está claro si el uso generalizado de fagos causaría una resistencia similar a la que se ha observado con los antibióticos. En teoría, esto no es muy probable que ocurra, ya que los fagos son muy específicos y, por tanto, su presión selectiva afectaría a un grupo muy reducido de bacterias. Sin embargo, también debemos considerar el hecho de que muchos sistemas de resistencia de fagos están montados en elementos genéticos móviles, incluidos profagos y plásmidos, y por lo tanto pueden propagarse con bastante rapidez incluso sin selección directa. Sin embargo, a diferencia de los antibióticos, se espera que las preparaciones de fagos para aplicaciones terapéuticas se desarrollen de forma personalizada debido a la alta especificidad de los fagos. Además, se han propuesto estrategias para contrarrestar el problema de la resistencia de los fagos. Una de las estrategias es el uso de cócteles de fagos con rangos de huéspedes complementarios (diferentes rangos de huéspedes que, cuando se combinan, dan como resultado un rango de huéspedes más amplio) y dirigidos a diferentes receptores bacterianos. Otra estrategia es la combinación de fagos con otros antimicrobianos como antibióticos, desinfectantes o enzimas que podrían potenciar su actividad antibacteriana. La manipulación genética de los genomas de los fagos también puede ser una estrategia para evitar la resistencia de los fagos.
Los bacteriófagos son virus bacterianos que evolucionaron para infectar células bacterianas. Para ello, los fagos deben utilizar estructuras características en la superficie celular (receptores) y, para propagarse, necesitan herramientas moleculares apropiadas dentro de las células. Las bacterias son procariotas y sus células difieren sustancialmente de las de los eucariotas , incluidos los humanos o los animales. [105] Por esta razón, los fagos cumplen con el principal requisito de seguridad: no infectan a las personas tratadas. Incluso los fagos modificados genéticamente y la internalización artificial inducida de fagos en células de mamíferos no dan como resultado la propagación de fagos. [106] La transcitosis natural de fagos no modificados, es decir, la captación y el transporte interno al otro lado de una célula, que se observó en las células epiteliales humanas, no resultó en propagación de fagos ni daño celular. [107] Sin embargo, recientemente se informó que los fagos filamentosos templados de P. aeruginosa pueden endocitarse en leucocitos humanos y murinos, lo que da como resultado la transcripción del ADN del fago. A su vez, el ARN producto desencadena respuestas de reconocimiento de patrones virales innatos desadaptativas y, por lo tanto, inhibe la eliminación inmune de las bacterias. [108] Aún no se ha establecido si esto también se aplica a los fagos de ADNds como Caudovirales ; Esta es una cuestión importante que debe abordarse, ya que puede afectar la seguridad general de la terapia con fagos.
Debido a muchos tratamientos experimentales en pacientes humanos realizados en las últimas décadas y a los ECA ya existentes (ver sección: Experiencia clínica y ensayos controlados aleatorios), la seguridad de los fagos se puede evaluar directamente. El primer ensayo de seguridad de un fago en voluntarios humanos sanos fue realizado por Bruttin y Brüssow en 2005. [109] Investigaron la administración oral del fago T4 de Escherichia coli y no encontraron efectos adversos del tratamiento. Los registros históricos muestran que los fagos son seguros y tienen efectos secundarios leves, si los hay. Las reacciones adversas más frecuentes (aunque aún raras) a las preparaciones de fagos encontradas en pacientes fueron síntomas del tracto digestivo, reacciones locales en el lugar de administración de la preparación de fagos, sobreinfecciones y aumento de la temperatura corporal. [110] [29] [111] En particular, estas reacciones pueden haber sido (i) debidas a la liberación de endotoxinas de bacterias lisadas in vivo por los fagos, ya que tales efectos también se pueden observar cuando se usan antibióticos, [112] o (ii) causado por restos bacterianos que acompañaban al fago en los casos en que se utilizaron lisados no purificados.
Los bacteriófagos deben producirse en bacterias que se lisan (es decir, se fragmentan) durante la propagación de los fagos. Como tal, los lisados de fagos contienen restos bacterianos que pueden afectar al organismo humano incluso cuando el fago en sí es inofensivo. Por estas y otras razones, la purificación de los bacteriófagos se considera importante y es necesario evaluar la seguridad de las preparaciones de fagos en su conjunto, particularmente cuando los fagos se van a administrar por vía intravenosa. Esto es consistente con los procedimientos generales para otros candidatos a fármacos. En 2015, un grupo de expertos en terapia con fagos resumió los requisitos de calidad y seguridad para una terapia con fagos sostenible. [113]
Los efectos de los fagos en el microbioma humano también contribuyen a problemas de seguridad en la terapia con fagos. Es importante señalar que muchos fagos, especialmente los de zonas templadas, portan genes que pueden afectar la patogenicidad del huésped. Incluso lambda, un fago templado de la cepa de laboratorio E. coli K-12, porta dos genes que proporcionan posibles beneficios de virulencia al huésped lisogénico, uno que aumenta la adherencia intestinal y el otro que confiere resistencia a la destrucción del complemento en la sangre. Por esta razón, generalmente se deben evitar los fagos templados como candidatos para la terapia con fagos, aunque en algunos casos, la falta de candidatos a fagos líticos y las condiciones de emergencia pueden hacer que tales consideraciones sean discutibles. [51] Otro problema potencial es la transducción generalizada, un término para la capacidad de algunos fagos de transferir ADN bacteriano de un huésped a otro. Esto ocurre porque los sistemas para empaquetar el ADN del fago en las cápsides pueden empaquetar por error el ADN del huésped. De hecho, en algunos fagos bien caracterizados, hasta el 5% de las partículas del virus contienen únicamente ADN bacteriano. Así, en un lisado típico, el genoma completo del huésped en propagación está presente en más de un millón de copias por mililitro. Por estas razones, es imperativo que cualquier fago que se considere para uso terapéutico se someta a un análisis genómico exhaustivo y se pruebe su capacidad de transducción generalizada. [ cita necesaria ]
Como antibacterianos, los fagos también pueden afectar la composición de los microbiomas, al infectar y matar cepas de bacterias sensibles a los fagos. Sin embargo, una ventaja importante de los bacteriófagos sobre los antibióticos es la alta especificidad de los bacteriófagos. Esta especificidad limita la actividad antibacteriana a un nivel de subespecie; normalmente, un fago mata sólo cepas bacterianas seleccionadas. Por esta razón, es mucho menos probable que los fagos (que los antibióticos) alteren la composición de un microbioma natural o induzcan disbiosis . Esto se demostró en estudios experimentales en los que se evaluó la composición del microbioma mediante secuenciación de próxima generación que no reveló cambios importantes relacionados con el tratamiento con fagos en tratamientos humanos. [114] [115] [116] [ 117] [118] [119]
Gran parte de la dificultad para obtener la aprobación regulatoria está resultando ser los riesgos de utilizar una entidad autorreplicante que tiene la capacidad de evolucionar. [35]
Al igual que ocurre con la terapia con antibióticos y otros métodos para contrarrestar las infecciones bacterianas, las bacterias liberan endotoxinas a medida que se destruyen dentro del paciente ( reacción de Jarisch-Herxheimer ). Esto puede provocar síntomas de fiebre; en casos extremos, es posible que se produzca un shock tóxico (un problema que también se observa con los antibióticos). [120] Janakiraman Ramachandran [32] sostiene que esta complicación se puede evitar en aquellos tipos de infección en los que es probable que se produzca esta reacción mediante el uso de bacteriófagos genéticamente modificados a los que se les ha eliminado el gen responsable de producir endolisina. Sin este gen, la bacteria huésped aún muere pero permanece intacta porque la lisis está desactivada. Por otro lado, esta modificación detiene el crecimiento exponencial de los fagos, por lo que un fago administrado supone como máximo una célula bacteriana muerta. [17] Con el tiempo, estas células muertas son consumidas por las tareas normales de limpieza de la casa de los fagocitos , que utilizan enzimas para descomponer toda la bacteria y su contenido en proteínas, polisacáridos y lípidos inofensivos. [121]
Los bacteriófagos templados (o lisogénicos ) generalmente no se usan terapéuticamente, ya que este grupo puede actuar como una forma para que las bacterias intercambien ADN. Esto puede ayudar a propagar la resistencia a los antibióticos o incluso, en teoría, hacer que las bacterias sean patógenas, como en los casos de cólera . Carl Merril ha afirmado que cepas inofensivas de corynebacterium pueden haberse convertido en C. diphtheriae que "probablemente mató a un tercio de todos los europeos que llegaron a América del Norte en el siglo XVII". [25] : 94 Afortunadamente, muchos fagos parecen ser líticos sólo con una probabilidad insignificante de volverse lisogénicos. [122]
En los países occidentales no se ha aprobado la terapia con fagos para su uso en humanos, con algunas excepciones. En los Estados Unidos, las leyes de Washington y Oregón permiten a los médicos naturópatas utilizar cualquier terapia que sea legal en cualquier parte del mundo con carácter experimental, [123] y en Texas, los fagos se consideran sustancias naturales y pueden usarse además (pero no como reemplazo de) la terapia tradicional (se han utilizado de forma rutinaria en una clínica de cuidado de heridas en Lubbock desde 2006). [124]
En 2013, "la vigésima conferencia bienal Evergreen International Phage Meeting... atrajo a 170 participantes de 35 países, incluidos líderes de empresas e institutos involucrados en terapias con fagos humanos de Francia, Australia, Georgia, Polonia y Estados Unidos". [125]
En Francia, la terapia con fagos desapareció oficialmente con la retirada del diccionario Vidal (directorio oficial de medicamentos de Francia), en 1978. La última preparación con fagos, producida por el Institut du Bactériophage, fue una pomada contra las infecciones cutáneas. La investigación sobre la terapia con fagos cesó aproximadamente al mismo tiempo en todo el país, con el cierre del departamento de bacteriófagos del Instituto Pasteur . Algunos médicos de hospitales continuaron ofreciendo terapia con fagos hasta la década de 1990, cuando la producción desapareció. [126]
Tras su redescubrimiento, a finales de los años 90, los preparados de fagos se clasificaron como medicamentos, es decir, "productos medicinales" en la UE o "medicamentos" en los EE.UU. [127] Sin embargo, la legislación farmacéutica que se había implementado desde su desaparición de la medicina occidental estaba diseñada principalmente para atender a los productos farmacéuticos fabricados industrialmente, desprovistos de cualquier personalización y destinados a la distribución a gran escala, [128] y no se consideró necesario para proporcionar requisitos o concesiones específicas de fagos.
Los productos de terapia con fagos actuales deben cumplir con toda la batería de requisitos de licencia de productos medicinales: fabricación según GMP , estudios preclínicos, ensayos clínicos de fase I, II y III y autorización de comercialización . Técnicamente, las preparaciones de fagos predefinidas producidas industrialmente podrían superar los procesos farmacéuticos convencionales, teniendo en cuenta algunas adaptaciones. Sin embargo, es probable que los problemas de especificidad y resistencia de los fagos hagan que estas preparaciones definidas tengan una vida útil relativamente corta. [129] La industria farmacéutica actualmente no está considerando productos de terapia con fagos. Sin embargo, un puñado de pequeñas y medianas empresas han mostrado interés, con la ayuda de capital de riesgo y/o financiación pública. Actualmente, ningún producto terapéutico definido de fagos ha llegado a los mercados de la UE o de los EE. UU.

Según algunos, [ ¿según quién? ] Los fagos terapéuticos deben prepararse individualmente y mantenerse en grandes bancos de fagos, listos para ser utilizados, tras realizar pruebas de eficacia contra los patógenos bacterianos del paciente. Podrían ser apropiados enfoques intermedios o combinados (fabricados industrialmente y preparaciones de fagos de precisión). [129] Sin embargo, resulta difícil conciliar los conceptos clásicos de terapia con fagos, que se basan en la adaptación oportuna de preparaciones de fagos, con los actuales modelos de marketing e I+D farmacéuticos occidentales. Los formuladores de políticas europeas no han atendido los repetidos llamados a favor de un marco regulatorio específico. [128] Se ha propuesto un marco de terapia con fagos basado en el concepto de archivo maestro biológico como una solución (europea) a las cuestiones regulatorias, pero las regulaciones europeas no permiten una extensión de este concepto a sustancias biológicamente activas como los fagos. [130]
Mientras tanto, representantes de las comunidades médica, académica y regulatoria han establecido algunas soluciones nacionales (temporales). Por ejemplo, las aplicaciones de fagos se han realizado en Europa bajo el amparo del Artículo 37 (Intervenciones no probadas en la práctica clínica) de la Declaración de Helsinki . Para permitir la aplicación de la terapia con fagos después de que Polonia se uniera a la UE en 2004, el Instituto de Inmunología y Terapia Experimental Ludwik Hirszfeld de Wrocław abrió su propia Unidad de Terapia con Fagos (PTU). La terapia con fagos realizada en la PTU se considera un "tratamiento experimental", cubierto por la Ley adaptada de 5 de diciembre de 1996 sobre la Profesión Médica (Boletín Jurídico Polaco, 2011, núm. 277, artículo 1634) y el artículo 37 de la Declaración de Helsinki. [131] De manera similar, en los últimos años, se han realizado una serie de intervenciones de terapia con fagos en los EE. UU. bajo el protocolo de emergencia de Nuevos Fármacos en Investigación (eIND) de la FDA. [132]
Algunos pacientes han sido tratados con fagos bajo el paraguas del "uso compasivo", que es una opción de tratamiento que permite al médico utilizar un medicamento aún no autorizado en casos desesperados. Bajo condiciones estrictas, los medicamentos en desarrollo pueden estar disponibles para su uso en pacientes para quienes no hay terapias autorizadas satisfactorias disponibles y que no pueden participar en ensayos clínicos. En principio, este enfoque sólo puede aplicarse a productos cuyos resultados de estudios anteriores hayan demostrado eficacia y seguridad, pero que aún no hayan sido aprobados. Al igual que el artículo 37 de la Declaración de Helsinki, la opción de tratamiento de uso compasivo sólo puede aplicarse cuando se espera que los fagos ayuden en enfermedades potencialmente mortales o crónicas y/o gravemente debilitantes que no se pueden tratar con productos aprobados formalmente. [ cita necesaria ]
En Francia, ANSM, la agencia francesa de medicamentos, ha organizado un comité específico, el Comité Scientifique Spécialisé Temporaire (CSST), para la terapia con fagos, que está formado por expertos en diversos campos. Su tarea es evaluar y orientar cada solicitud de terapia con fagos que llegue a la ANSM. Las solicitudes de terapia con fagos se discuten junto con los médicos tratantes y se envía un asesoramiento consensuado a la ANSM], que luego decide si concede o no el permiso. Entre 2006 y 2018, quince pacientes fueron tratados en Francia (once se recuperaron) por esta vía. [133]
En Bélgica, en 2016 y en respuesta a una serie de preguntas parlamentarias, Maggie De Block , Ministra de Asuntos Sociales y Sanidad, reconoció que efectivamente no es evidente tratar los fagos como fármacos fabricados industrialmente, por lo que propuso investigar si los La vía de preparación magistral podría ofrecer una solución. [129] Los preparados Magistral (que se venden en farmacias de los Estados Unidos) no están sujetos a determinadas limitaciones, como el cumplimiento de las BPF y la autorización de comercialización. Dado que el "marco de preparación magistral" se creó para permitir tratamientos adaptados a los pacientes y/o utilizar medicamentos sin interés comercial, parecía un marco adecuado para conceptos de terapia con fagos de precisión. Los preparados magistrales son medicamentos preparados en una farmacia según prescripción médica para un paciente individual. Son elaborados por un farmacéutico (o bajo su supervisión) a partir de los ingredientes que los constituyen, según los estándares técnicos y científicos de la tecnología farmacéutica. Los ingredientes farmacéuticos activos de fagos que se incluirán en las preparaciones magistrales deben cumplir con los requisitos de una monografía, que describe su producción y las pruebas de control de calidad. Deberán ir acompañados de un certificado de análisis, expedido por un "laboratorio belga autorizado" que haya obtenido una acreditación para realizar pruebas de liberación de lotes de medicamentos. Desde 2019, los fagos se administran en forma de preparados magistrales a pacientes nominales en Bélgica. [134]
El primer caso de terapia con fagos en China se remonta a 1958, en la Facultad de Medicina de la Universidad Jiao Tong de Shanghai . [135] Sin embargo, muchas regulaciones aún no se habían establecido en aquel entonces, y la terapia con fagos pronto perdió el interés de la gente debido a la prevalencia de los antibióticos, lo que finalmente condujo a la crisis de resistencia a los antimicrobianos . Esto llevó a los investigadores de China, así como al gobierno chino, a volver a prestar atención a la terapia con fagos y, tras el primer ensayo iniciado por un investigador (IIT) realizado por el Instituto de Fagos de Shanghai en 2019, la terapia con fagos floreció rápidamente. [136] Actualmente, las aplicaciones comerciales de terapia con fagos deben pasar por una de dos vías. El primero es para productos de fagos de ingredientes fijos. [137] La segunda vía es para productos de fagos personalizados, que deben pasar por IIT. De esta forma, los productos se consideran tecnologías médicas restrictivas. [138]
La fagoterapia ha sido un modo de tratamiento relevante en animales durante décadas. [139] Se ha propuesto como un método para tratar infecciones bacterianas en el campo de la medicina veterinaria en respuesta al uso desenfrenado de antibióticos. Los estudios han investigado la aplicación de la terapia con fagos en especies ganaderas y en animales de compañía. [140] La Universidad Brigham Young ha estado investigando el uso de la terapia con fagos para tratar la loque americana en las abejas . [141] [142] [143] La terapia con fagos también se está investigando para posibles aplicaciones en la acuicultura . [144]
La terapia con fagos se ha estudiado para la mancha bacteriana de la fruta de hueso, causada por Xanthomonas pruni (sin. X. campestris pv. pruni , sin. X. arboricola pv. pruni ) en especies de prunus . [145] [40] Algunos tratamientos han tenido mucho éxito. [145] [40]
La novela de 1925 y ganadora del Premio Pulitzer de 1926, Arrowsmith , de Sinclair Lewis, utilizó la terapia con fagos como argumento. [146] [147] [148]
La novela Vitals de Greg Bear de 2002 presenta la terapia con fagos, basada en investigaciones soviéticas, que se utiliza para transferir material genético.
La colección de ensayos de historia militar de 2012 sobre el papel cambiante de las mujeres en la guerra, Women in War - From Home Front to Front Line incluye un capítulo que presenta la terapia con fagos: "Capítulo 17: Mujeres que descongelaron la Guerra Fría". [149]
El libro de Steffanie A. Strathdee El depredador perfecto: el viaje de un epidemiólogo para salvar a su marido de una superbacteria mortal , coescrito con su marido, Thomas Patterson, fue publicado por Hachette Book Group en 2019. Describe el intento finalmente exitoso de Strathdee de introducir la terapia con fagos como tratamiento para salvar la vida de su marido, gravemente enfermo con una infección por Acinetobacter baumannii completamente resistente a los antibióticos tras una pancreatitis grave.
![]() Este artículo fue adaptado de la siguiente fuente bajo una licencia CC BY 4.0 (2021) (informes de revisores): Joana Azeredo, Jean-Paul Pirnay, Diana Priscila Pires, Mzia Kutateladze, Krystyna Dabrowska, Rob Lavigne, Bob G Blasdel (15 de diciembre de 2021 ), "Terapia con fagos" (PDF) , WikiJournal of Medicine , WikiJournal of Medicine, 8 (1): 4, doi :10.15347/WJM/2021.004, ISSN 2002-4436, Wikidata Q100400597
Este artículo fue adaptado de la siguiente fuente bajo una licencia CC BY 4.0 (2021) (informes de revisores): Joana Azeredo, Jean-Paul Pirnay, Diana Priscila Pires, Mzia Kutateladze, Krystyna Dabrowska, Rob Lavigne, Bob G Blasdel (15 de diciembre de 2021 ), "Terapia con fagos" (PDF) , WikiJournal of Medicine , WikiJournal of Medicine, 8 (1): 4, doi :10.15347/WJM/2021.004, ISSN 2002-4436, Wikidata Q100400597
Los investigadores sugieren que la terapia con bacteriófagos es un tratamiento viable para las infecciones bacterianas, aunque señalan que antes de que pueda considerarse como una terapia alternativa para pacientes infectados, se deben encontrar mejores medios para encontrar bacteriófagos.
[E]l Instituto Hirszfeld [en Polonia] casi siempre ha realizado sus estudios de investigación en ausencia de controles de doble vínculo.... Pero la gran cantidad de casos, combinada con el hecho de que casi todos los casos involucran a pacientes que no respondieron a los antibióticos, es convincente.
Además de mencionar que la ley de Texas permite a los médicos utilizar "sustancias naturales" como fagos además de (pero no en lugar de) la práctica médica estándar, Kuichment dice: "En junio de 2009, el estudio [del Dr. Randall Wolcott] se publicó en el Journal de Cuidado de Heridas.