La investigación sobre lesiones de la médula espinal busca nuevas formas de curar o tratar la lesión de la médula espinal para disminuir los efectos debilitantes de la lesión a corto o largo plazo. No existe cura para la LME y los tratamientos actuales se centran principalmente en la rehabilitación de lesiones de la médula espinal y el manejo de los efectos secundarios de la afección. [1] Dos áreas principales de investigación incluyen la neuroprotección , formas de prevenir el daño a las células causado por procesos biológicos que tienen lugar en el cuerpo después de la lesión, y la neuroregeneración , regeneración o reemplazo de circuitos neuronales dañados.
La lesión secundaria ocurre de minutos a semanas después de la lesión inicial e incluye una serie de procesos en cascada que dañan aún más los tejidos ya dañados por la lesión primaria. [2] Resulta en la formación de una cicatriz glial, que impide el crecimiento axonal. [2] Las lesiones secundarias pueden ocurrir por diferentes formas de estrés agregado a la médula espinal en formas tales como contusiones adicionales, compresiones, torceduras o estiramientos de la médula espinal.
[3]
Las complicaciones de una LME secundaria son el resultado de un desequilibrio homeostático que potencialmente conduce a cambios metabólicos y hemostáticos debido a una respuesta inflamatoria. Los posibles efectos inmediatos de la LME secundaria incluyen lesión neuronal, neuroinflamación, ruptura de la barrera hematoencefálica (BSCB), disfunción isquémica, estrés oxidativo y complicaciones de las funciones de la vida diaria.
Los animales utilizados como organismos modelo de SCI en la investigación incluyen ratones, ratas, gatos, perros, cerdos y primates no humanos; estos últimos son similares a los humanos pero plantean preocupaciones éticas sobre la experimentación con primates . [1] Existen dispositivos especiales para aplicar golpes de fuerza específica y monitorizada a la médula espinal de un animal de experimentación. [1] Existen varias clasificaciones de impacto mecánico de estas lesiones que pueden replicarse en un modelo animal. Esto incluye contusión, compresión, colagenasa e isquemia, reperfusión, distracción, dislocación y transección.
Las limitaciones de estos experimentos modelo son comunes. Por ejemplo, la LME por isquemia-reperfusión implica la interrupción del flujo sanguíneo a la médula espinal. Se ha observado que surgen complicaciones en modelos animales por la necesidad de pinzar la aorta.
Se han utilizado sillas de enfriamiento epidurales, colocadas quirúrgicamente sobre tejido de la médula espinal con traumatismo agudo, para evaluar los efectos potencialmente beneficiosos de la hipotermia localizada, con y sin glucocorticoides concomitantes . [4] [5]
Actualmente, la cirugía se utiliza para proporcionar estabilidad a la columna vertebral lesionada o para aliviar la presión de la médula espinal. [1] [6] La rapidez con la que se debe realizar una cirugía descompresiva después de la lesión es un tema controvertido, y ha sido difícil demostrar que la cirugía más temprana proporciona mejores resultados en ensayos en humanos. [1] Algunos argumentan que la cirugía temprana podría privar aún más de oxígeno a una médula espinal ya lesionada, pero la mayoría de los estudios no muestran diferencias en los resultados entre la cirugía temprana (dentro de los tres días) y la tardía (después de cinco días), y algunos muestran un beneficio con la cirugía temprana. cirugía. [7]
En 2014, Darek Fidyka se sometió a una cirugía de columna pionera que utilizó injertos nerviosos, desde su tobillo, para "cerrar la brecha" en su médula espinal cortada y células de envoltura olfatoria (OEC) para estimular las células de la médula espinal. La cirugía se realizó en Polonia en colaboración con el Prof. Geoff Raisman, catedrático de regeneración neuronal del Instituto de Neurología del University College de Londres, y su equipo de investigación. Las OEC se tomaron de los bulbos olfatorios del cerebro del paciente y luego se cultivaron en el laboratorio; luego, estas células se inyectaron por encima y por debajo del tejido espinal dañado. [8]
La neuroprotección tiene como objetivo prevenir el daño que se produce por una lesión secundaria. [2] Un ejemplo es atacar la proteína calpaína que parece estar involucrada en la apoptosis ; la inhibición de la proteína ha producido mejores resultados en ensayos con animales. [2] El hierro de la sangre daña la médula espinal a través del estrés oxidativo , por lo que una opción es utilizar un agente quelante para unir el hierro; Los animales tratados de esta manera han mostrado mejores resultados. [2] El daño de los radicales libres causado por especies reactivas de oxígeno (ROS) es otro objetivo terapéutico que ha mostrado mejoras cuando se dirige a animales. [2] Un antibiótico, la minociclina , está bajo investigación en ensayos en humanos por su capacidad para reducir el daño de los radicales libres, la excitotoxicidad , la alteración de la función mitocondrial y la apoptosis. [2] El riluzol, un anticonvulsivo, también se está investigando en ensayos clínicos por su capacidad para bloquear los canales de sodio en las neuronas, lo que podría prevenir el daño por excitotoxicidad. [2] Otros agentes potencialmente neuroprotectores que se están investigando en ensayos clínicos incluyen cetrina, eritropoyetina y dalfampridina . [2]
Un tratamiento experimental, la hipotermia terapéutica , se utiliza en el tratamiento, pero no hay evidencia de que mejore los resultados. [9] [10] Algunos tratamientos experimentales, incluida la hipotermia sistémica, se han realizado en casos aislados para llamar la atención sobre la necesidad de realizar más estudios preclínicos y clínicos para ayudar a aclarar el papel de la hipotermia en la lesión aguda de la médula espinal. [11] A pesar de la financiación limitada, varios tratamientos experimentales, como el enfriamiento local de la columna y la estimulación del campo oscilante, han llegado a ensayos controlados en humanos. [12] [13]
La inflamación y la cicatriz glial se consideran factores inhibidores importantes para la neuroregeneración después de una lesión medular. Sin embargo, aparte de la metilprednisolona , ninguno de estos avances ha alcanzado ni siquiera un uso limitado en la atención clínica de las lesiones de la médula espinal humana en los EE. UU. [14] La metilprednisolona se puede administrar poco después de la lesión, pero la evidencia de efectos secundarios dañinos supera los beneficios. [6] Se están realizando investigaciones sobre mecanismos de administración más eficientes de metilprednisolona que reducirían sus efectos nocivos. [1]
La neuroregeneración tiene como objetivo reconectar los circuitos rotos en la médula espinal para permitir que la función regrese. [2] Una forma es volver a hacer crecer los axones, lo que ocurre espontáneamente en el sistema nervioso periférico . Sin embargo, la mielina del sistema nervioso central contiene moléculas que impiden el crecimiento axonal; por lo tanto, estos factores son el objetivo de las terapias para crear un entorno propicio para el crecimiento. [2] Una de esas moléculas es Nogo-A , una proteína asociada con la mielina. Cuando esta proteína se ataca con anticuerpos inhibidores en modelos animales, los axones crecen mejor y se mejora la recuperación funcional. [2]
Las células madre son células que pueden diferenciarse para convertirse en diferentes tipos de células. [15] La esperanza es que las células madre trasplantadas en un área lesionada de la médula espinal permitan la neuroregeneración . [6] Los tipos de células que se están investigando para su uso en LME incluyen células madre embrionarias , células madre neurales , células madre mesenquimales , células envolventes olfatorias , células de Schwann , macrófagos activados y células madre pluripotentes inducidas . [1] Cuando se inyectan células madre en el área dañada de la médula espinal, secretan factores neurotróficos , y estos factores ayudan a que las neuronas y los vasos sanguíneos crezcan, ayudando así a reparar el daño. [16] [17] [18] También es necesario recrear un entorno en el que las células madre crezcan. [19]
Un ensayo de fase 2 en curso en 2016 presentó datos [20] que muestran que después de 90 días de tratamiento con células progenitoras de oligodendrocitos derivadas de células madre embrionarias, 4 de cada 4 sujetos con lesiones cervicales completas habían mejorado sus niveles motores, y 2 de 4 mejoraron dos niveles motores. niveles (en al menos un lado, y un paciente mejoró dos niveles motores en ambos lados). El criterio de valoración original del ensayo había sido que 2/5 pacientes mejoraran dos niveles en un lado en un plazo de 6 a 12 meses. Los 8 sujetos cervicales en este ensayo de Fase 1-2 habían mostrado puntuaciones motoras de las extremidades superiores (UEMS) mejoradas en relación con el valor inicial sin efectos secundarios adversos graves, y un ensayo de Fase 1 de 2010 en 5 pacientes torácicos no encontró problemas de seguridad después de 5-6 años de seguimiento.
Se esperan datos de eficacia de seis meses para enero de 2017; Mientras tanto, se está investigando una dosis más alta y el estudio ahora también recluta pacientes con lesiones incompletas. [21]
En 2022, un equipo informó sobre las primeras [22] redes neuronales (motoras) humanas funcionales diseñadas derivadas de células madre pluripotentes inducidas (iPSC) del paciente para su implantación para regenerar la médula espinal lesionada que muestran éxito en pruebas con ratones. [23] [24]
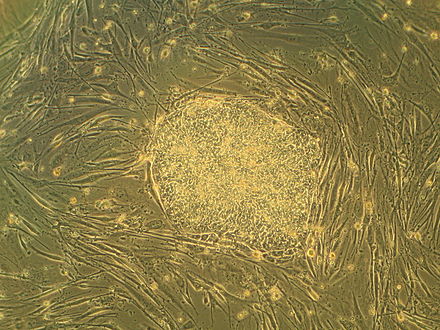
Las células madre embrionarias (ESC) son pluripotentes ; pueden convertirse en cualquier tipo de célula de un organismo, como los oligodendrocitos . . [6] Se ha predicho que los oligodendrocitos y las neuronas motoras serán un objetivo favorable para las CME en el tratamiento de trastornos neurológicos y traumas. [25] Después de que se produce una LME, hay evidencia de degradación de los oligodendrocitos, lo que eventualmente conduce a la muerte celular. Esto da como resultado una falta de mielinización , lo que mejora las señales enviadas entre las neuronas, provocando una disfunción en la señalización. Una posible solución podría ser el trasplante de oligodendrocitos derivados de hESC; sin embargo, el éxito de este proceso depende de la capacidad de la célula para diferenciarse hacia tipos de células neurales in vitro. Aquí es donde se están realizando más pruebas e investigaciones utilizando modelos animales.
Las células madre neuronales (NSC) son multipotentes ; pueden diferenciarse en diferentes tipos de células neurales, ya sean neuronas o glía , concretamente oligodendrocitos y astrocitos . [15] La esperanza es que estas células, cuando se inyectan en una médula espinal lesionada, reemplacen las neuronas y oligodendrocitos muertos y secreten factores que apoyan el crecimiento. [1] Sin embargo, es posible que no logren diferenciarse en neuronas cuando se trasplantan, ya sea que permanezcan indiferenciadas o se conviertan en glía. [15] Los ensayos clínicos de fase I/II que implantan NSC en humanos con LME comenzaron en 2011 [1] y finalizaron en junio de 2015. [26]
Las células madre mesenquimales no necesitan provenir de fetos, así que evite dificultades en torno a la ética; Provienen de tejidos que incluyen la médula ósea, el tejido adiposo y el cordón umbilical . [1] A diferencia de otros tipos de células madre, las células mesenquimales no presentan la amenaza de formación de tumores ni de desencadenar una respuesta del sistema inmunológico . [1] Los estudios en animales con inyección de células madre de la médula ósea han demostrado una mejora en la función motora; sin embargo, no fue así en un ensayo en humanos un año después de la lesión. [1] Se están realizando más ensayos. [1] Las células madre del tejido adiposo y umbilical necesitan más estudios antes de que se puedan realizar ensayos en humanos, pero se iniciaron dos estudios coreanos para investigar las células adiposas en pacientes con LME. [1]
Se ha demostrado que el trasplante de tejidos, como las células envolventes olfatorias de los bulbos olfatorios, produce efectos beneficiosos en ratas con lesión de la médula espinal. [27] Los ensayos también han comenzado a mostrar éxito cuando se trasplantan células envolventes olfativas a humanos con médula espinal cortada. [28] Las personas han recuperado la sensibilidad, el uso de los músculos anteriormente paralizados y la función de la vejiga y los intestinos después de las cirugías, [29] por ejemplo, Darek Fidyka .
Investigadores japoneses descubrieron en 2006 que agregar ciertos factores de transcripción a las células hacía que se volvieran pluripotentes y capaces de diferenciarse en múltiples tipos de células. [6] De esta manera se podrían utilizar los propios tejidos del paciente, en teoría debido a una menor posibilidad de rechazo del trasplante . [6]
Enfoques recientes han utilizado diversas técnicas de ingeniería para mejorar la reparación de lesiones de la médula espinal. El uso de biomateriales es un enfoque de ingeniería para el tratamiento de LME que se puede combinar con el trasplante de células madre. [6] Pueden ayudar a llevar células al área lesionada y crear un ambiente que fomente su crecimiento. [6] La hipótesis general detrás de los biomateriales diseñados es que unir el sitio de la lesión utilizando un andamio que permita el crecimiento puede ayudar a que los axones crezcan y, por lo tanto, mejoren su función. Los biomateriales utilizados deben ser lo suficientemente fuertes como para brindar un soporte adecuado pero lo suficientemente suaves como para no comprimir la médula espinal. [2] Deben degradarse con el tiempo para dejar paso al cuerpo para que vuelva a crecer tejido. [2] Los tratamientos diseñados no inducen una respuesta inmune como lo hacen los tratamientos biológicos, y son fácilmente sintonizables y reproducibles. Se ha demostrado que la administración in vivo de hidrogeles o nanofibras autoensamblables promueve el brote axonal y la recuperación funcional parcial. [30] [31] Además, se ha demostrado que la administración de nanotubos de carbono aumenta la extensión del axón motor y disminuye el volumen de la lesión, sin inducir dolor neuropático . [32] Además, la administración de microfibras de ácido poliláctico ha demostrado que las señales de guía topográfica por sí solas pueden promover la regeneración axonal en el sitio de la lesión. [33] Sin embargo, todos estos enfoques indujeron una modesta recuperación funcional o conductual, lo que sugiere que es necesaria más investigación.
Los hidrogeles son estructuras hechas de polímeros que están diseñados para ser similares a la matriz extracelular natural que rodea las células. [2] Pueden usarse para ayudar a administrar medicamentos de manera más eficiente a la médula espinal y para sostener las células, y pueden inyectarse en un área lesionada para rellenar una lesión. [2] Se pueden implantar en el sitio de la lesión con medicamentos o factores de crecimiento para darle a los químicos el mejor acceso al área dañada y permitir una liberación sostenida. [2]
En noviembre de 2021, se informó sobre una nueva terapia para las lesiones de la médula espinal: un gel inyectable de nanofibras que imita la matriz alrededor de las células y contiene moléculas diseñadas para moverse. Estas moléculas en movimiento se conectan con los receptores de las células, provocando señales de reparación en el interior (en particular, lo que conduce a un crecimiento vascular relativamente mayor, regeneración axonal, mielinización, supervivencia de las neuronas motoras, reducción de la gliosis y recuperación funcional), lo que permite a los ratones paralizados volver a caminar. [34] [35] [36]
Actualmente, la tecnología para crear exoesqueletos eléctricos , maquinaria portátil para ayudar con los movimientos de caminar, está logrando avances significativos. Hay productos disponibles, como el Ekso, que permite a las personas con una lesión espinal completa hasta C7 (o cualquier nivel de lesión incompleta) mantenerse erguidos y dar pasos asistidos tecnológicamente. [37] El propósito inicial de esta tecnología es la rehabilitación funcional, pero a medida que la tecnología se desarrolle, también lo harán sus usos. [37]
La estimulación eléctrica funcional (FES) utiliza descargas eléctricas coordinadas en los músculos para hacer que se contraigan siguiendo un patrón de marcha. [38] Si bien puede fortalecer los músculos, una desventaja importante para los usuarios de FES es que sus músculos se cansan después de un corto tiempo y distancia. [38] Una dirección de investigación combina FES con exoesqueletos para minimizar las desventajas de ambas tecnologías, apoyando las articulaciones de la persona y usando los músculos para reducir la potencia necesaria de la máquina y, por lo tanto, su peso. [38] Un equipo de investigación de la Escuela de Ingeniería McKelvey de la Universidad de Washington en St. Louis , dirigido por el profesor asistente de ingeniería biomédica Ismael Seáñez, está lanzando un ensayo clínico de estimulación eléctrica de la médula espinal para ayudar a restaurar el movimiento en personas paralizadas o con problemas de movimiento. pacientes. [39]
Investigaciones recientes muestran que la combinación de la interfaz cerebro-computadora y la estimulación eléctrica funcional puede restaurar el control voluntario de los músculos paralizados. Un estudio con monos demostró que es posible utilizar directamente órdenes del cerebro, sin pasar por la médula espinal y permitir un control y una función limitados de las manos. [40]
Los implantes de médula espinal, como los implantes e-dura, diseñados para implantarse en la superficie de la médula espinal, se están estudiando para la parálisis después de una lesión de la médula espinal. [41]
Los implantes E-dura están diseñados utilizando métodos de neurotecnología blanda , en los que electrodos y un sistema de administración de microfluidos se distribuyen a lo largo del implante espinal. [42] La estimulación química de la médula espinal se administra a través del canal de microfluidos de la e-dura. Los implantes e-dura, a diferencia de los implantes de superficie anteriores, imitan fielmente las propiedades físicas del tejido vivo y pueden administrar impulsos eléctricos y sustancias farmacológicas simultáneamente. La duramadre artificial se construyó mediante la utilización de PDMS e hidrogel de gelatina. [42] El hidrogel simula el tejido espinal y una membrana de silicona simula la duramadre. Estas propiedades permiten que los implantes e-dura mantengan su aplicación a largo plazo en la médula espinal y el cerebro sin provocar inflamación, acumulación de tejido cicatricial y rechazo normalmente causado por el roce de los implantes superficiales contra el tejido nervioso.
En 2018, dos equipos de investigación distintos de la Clínica Mayo de Minnesota y la Universidad de Louisville de Kentucky lograron restaurar algo de movilidad a pacientes que padecían paraplejía con un estimulador electrónico de la médula espinal. La teoría detrás del nuevo estimulador de la médula espinal es que en ciertos casos de lesión de la médula espinal, los nervios espinales entre el cerebro y las piernas todavía están vivos, pero simplemente inactivos. [43] El 1 de noviembre de 2018, un tercer equipo de investigación distinto de la Universidad de Lausana publicó resultados similares con una técnica de estimulación similar en la revista Nature . [44] [45] En 2022, los investigadores demostraron un estimulador de la médula espinal que permitía a los pacientes con lesión de la médula espinal volver a caminar mediante estimulación eléctrica epidural (EES) con un progreso sustancial de la neurorrehabilitación durante el primer día. [46] [47] En un estudio publicado en mayo de 2023 en la revista Nature , investigadores en Suiza describieron implantes que permitieron a un hombre de 40 años, paralizado desde las caderas hacia abajo durante 12 años, ponerse de pie, caminar y ascender una rampa empinada. con sólo la ayuda de un andador. Más de un año después de que le colocaron el implante, conservaba estas capacidades y caminaba con muletas incluso cuando el implante estaba desconectado. [48]
Los estimuladores de la médula espinal y la fisioterapia intensa están ayudando a los pacientes parapléjicos a volver a aprender a caminar. Los estimuladores de la médula espinal pueden ayudar potencialmente a "despertar" los nervios latentes.
Una nueva terapia que amplifica los impulsos nerviosos también puede ayudar al cuerpo a sanar