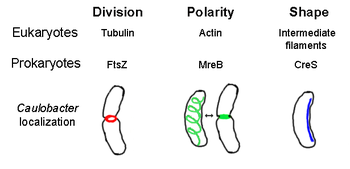
El citoesqueleto procariótico es el nombre colectivo de todos los filamentos estructurales de los procariotas . Alguna vez se pensó que las células procarióticas no poseían citoesqueletos , pero los avances en la tecnología de visualización y la determinación de la estructura llevaron al descubrimiento de filamentos en estas células a principios de los años 1990. [2] No sólo se han encontrado en procariotas análogos de todas las principales proteínas citoesqueléticas de los eucariotas , sino que también se han descubierto proteínas citoesqueléticas sin homólogos eucariotas conocidos. [3] [4] [5] [6] Los elementos citoesqueléticos desempeñan funciones esenciales en la división celular , la protección, la determinación de la forma y la determinación de la polaridad en varios procariotas. [7] [8]
FtsZ, el primer elemento citoesquelético procariótico identificado, forma una estructura de anillo filamentoso ubicada en el medio de la célula llamada anillo Z que se contrae durante la división celular , similar al anillo contráctil de actina-miosina en eucariotas. [2] El anillo Z es una estructura altamente dinámica que consta de numerosos haces de protofilamentos que se extienden y encogen, aunque el mecanismo detrás de la contracción del anillo Z y el número de protofilamentos involucrados no están claros. [1] FtsZ actúa como una proteína organizadora y es necesaria para la división celular. Es el primer componente del tabique durante la citocinesis y recluta todas las demás proteínas de división celular conocidas en el sitio de división. [9]
A pesar de esta similitud funcional con la actina , FtsZ es homóloga a la tubulina eucariota . Aunque la comparación de las estructuras primarias de FtsZ y tubulina revela una relación débil, sus estructuras tridimensionales son notablemente similares. Además, al igual que la tubulina, el FtsZ monomérico se une al GTP y se polimeriza con otros monómeros de FtsZ con la hidrólisis del GTP en un mecanismo similar a la dimerización de la tubulina . [10] Dado que FtsZ es esencial para la división celular en bacterias, esta proteína es un objetivo para el diseño de nuevos antibióticos . [11] Actualmente existen varios modelos y mecanismos que regulan la formación de anillos Z, pero estos mecanismos dependen de la especie. Varias especies con forma de bastón, incluidas Escherichia coli y Caulobacter crescentus , utilizan uno o más inhibidores del ensamblaje de FtsZ que forman un gradiente bipolar en la célula, lo que mejora la polimerización de FtsZ en el centro celular. [12] Uno de estos sistemas de formación de gradientes consta de proteínas MinCDE (ver más abajo).
MreB es una proteína bacteriana que se cree que es homóloga a la actina eucariota . MreB y actina tienen una débil coincidencia estructural primaria , pero son muy similares en términos de estructura tridimensional y polimerización de filamentos.
Casi todas las bacterias no esféricas dependen de MreB para determinar su forma. MreB se ensambla en una red helicoidal de estructuras filamentosas justo debajo de la membrana citoplasmática , cubriendo toda la longitud de la célula. [13] MreB determina la forma celular mediando la posición y actividad de las enzimas que sintetizan peptidoglicano y actuando como un filamento rígido debajo de la membrana celular que ejerce presión hacia afuera para esculpir y reforzar la célula. [1] MreB se condensa a partir de su red helicoidal normal y forma un anillo apretado en el tabique de Caulobacter crescentus justo antes de la división celular, un mecanismo que se cree que ayuda a localizar su tabique descentrado. [14] MreB también es importante para la determinación de la polaridad en bacterias polares, ya que es responsable del posicionamiento correcto de al menos cuatro proteínas polares diferentes en C. crescentus . [14]
ParM es un elemento citoesquelético que posee una estructura similar a la actina , aunque se comporta funcionalmente como tubulina . Además, polimeriza bidireccionalmente y exhibe inestabilidad dinámica , ambos comportamientos característicos de la polimerización de tubulina. [4] [15] Forma un sistema con ParR y parC que es responsable de la separación del plásmido R1 . ParM se fija a ParR, una proteína de unión al ADN que se une específicamente a 10 repeticiones directas en la región parC del plásmido R1. Esta unión se produce en ambos extremos del filamento ParM. Luego este filamento se extiende, separando los plásmidos. [16] El sistema es análogo a la segregación de cromosomas eucariotas, ya que ParM actúa como tubulina eucariota en el huso mitótico , ParR actúa como el complejo cinetocoro y parC actúa como el centrómero del cromosoma . [17]
La segregación del plásmido F ocurre en un sistema similar donde SopA actúa como filamento citoesquelético y SopB se une a la secuencia sopC en el plásmido F, como el cinetocoro y el centrómero respectivamente. [17] Últimamente se ha encontrado un homólogo de ParM similar a la actina en una bacteria grampositiva Bacillus thuringiensis , que se ensambla en una estructura similar a microtúbulos y participa en la segregación de plásmidos . [18]
La crenactina es un homólogo de actina exclusivo del reino arqueal Thermoproteota (anteriormente Crenarchaeota) que se ha encontrado en los órdenes Thermoproteales y Candidatus Korarchaeum . [19] En el momento de su descubrimiento en 2009, tiene la mayor similitud de secuencia con las actinas eucariotas de cualquier homólogo de actina conocido. [20] La crenactina se ha caracterizado bien en Pyryobaculum calidifontis ( A3MWN5 ) y ha demostrado tener una alta especificidad por ATP y GTP. [19] Las especies que contienen crenactina tienen forma de varilla o aguja. En P. calidifontis , se ha demostrado que la crenactina forma estructuras helicoidales que se extienden a lo largo de la célula, lo que sugiere un papel de la crenactina en la determinación de la forma similar al de MreB en otros procariotas. [19] [21]
Aún más cercano al sistema de actina eucariota se encuentra en el superfilo propuesto de Asgardarchaeota . Utilizan versiones primitivas de profilina , gelsolina y cofilina para regular el citoesqueleto. [22]
Crescentin (codificada por el gen creS ) es un análogo de los filamentos intermedios (IF) eucarióticos. A diferencia de otras relaciones análogas discutidas aquí, la crescentina tiene una homología primaria bastante grande con las proteínas IF además de una similitud tridimensional: la secuencia de creS tiene una coincidencia de identidad del 25 % y una similitud del 40 % con la citoqueratina 19 y una coincidencia de identidad del 24 % y 40% de similitud con la lámina nuclear A. Además, los filamentos de media luna tienen aproximadamente 10 nm de diámetro y, por lo tanto, se encuentran dentro del rango de diámetro de los IF eucariotas (8-15 nm). [23] Crescentin forma un filamento continuo de polo a polo a lo largo del lado interno cóncavo de la bacteria Caulobacter crescentus en forma de media luna . Tanto MreB como crescentin son necesarios para que C. crescentus exista en su forma característica; se cree que MreB moldea la célula en forma de varilla y la crescentina dobla esta forma en forma de media luna. [1]
El sistema MinCDE es un sistema de filamentos que posiciona adecuadamente el tabique en el medio de la célula en Escherichia coli . Según Shih et al., MinC inhibe la formación del tabique al prohibir la polimerización del anillo Z. MinC, MinD y MinE forman una estructura de hélice que enrolla alrededor de la célula y está unida a la membrana por MinD. La hélice MinCDE ocupa un polo y termina en una estructura filamentosa llamada anillo E hecha de MinE en el borde medio de la zona polar. A partir de esta configuración, el anillo E se contraerá y se moverá hacia ese polo, desmontando la hélice MinCDE a medida que avanza. Al mismo tiempo, los fragmentos desmontados se volverán a ensamblar en el extremo polar opuesto, reformando la bobina MinCDE en el polo opuesto mientras la hélice MinCDE actual se descompone. Luego, este proceso se repite, con la hélice MinCDE oscilando de polo a polo. Esta oscilación ocurre repetidamente durante el ciclo celular, manteniendo así MinC (y su efecto inhibidor del tabique) en una concentración promedio de tiempo más baja en el centro de la célula que en los extremos de la célula. [24]
El comportamiento dinámico de las proteínas Min se ha reconstituido in vitro utilizando una bicapa lipídica artificial como imitador de la membrana celular. MinE y MinD se autoorganizaron en ondas proteicas paralelas y en espiral mediante un mecanismo similar a la reacción-difusión. [25]
La bactofilina ( InterPro : IPR007607 ) es un elemento citoesquelético de hélice β que forma filamentos en todas las células de la proteobacteria en forma de bastón Myxococcus xanthus . [26] La proteína bactofilina, BacM, es necesaria para el mantenimiento adecuado de la forma celular y la integridad de la pared celular. Las células de M. xanthus que carecen de BacM tienen una morfología deformada caracterizada por un cuerpo celular doblado, y los mutantes bacM tienen una menor resistencia a los antibióticos dirigidos a la pared celular bacteriana. La proteína BacM de M. xanthus se escinde de su forma completa para permitir la polimerización. Las bactofilinas han sido implicadas en la regulación de la forma celular en otras bacterias, incluida la curvatura de las células de Proteus mirabilis , [27] la formación de tallos por Caulobacter crescentus , [28] y la forma helicoidal de Helicobacter pylori . [29]