
El péptido 1 similar al glucagón ( GLP-1 ) es una hormona peptídica de 30 o 31 aminoácidos de longitud que se deriva del procesamiento postraduccional específico de tejido del péptido proglucagón . Es producido y secretado por las células L enteroendocrinas intestinales y ciertas neuronas dentro del núcleo del tracto solitario en el tronco del encéfalo tras el consumo de alimentos. El producto inicial GLP-1 (1-37) es susceptible a la amidación y a la escisión proteolítica , lo que da lugar a dos formas biológicamente activas truncadas y equipotentes, GLP-1 (7-36) amida y GLP-1 (7-37). . La estructura secundaria de la proteína GLP-1 activa incluye dos hélices α de las posiciones de aminoácidos 13 a 20 y 24 a 35 separadas por una región conectora.
Junto con el péptido insulinotrópico dependiente de glucosa (GIP), el GLP-1 es una incretina ; por tanto, tiene la capacidad de disminuir los niveles de azúcar en sangre de forma dependiente de la glucosa al mejorar la secreción de insulina . Además de los efectos insulinotrópicos, el GLP-1 se ha asociado con numerosos efectos reguladores y protectores. A diferencia del GIP, la acción del GLP-1 se conserva en pacientes con diabetes tipo 2 . Los agonistas del receptor del péptido 1 similar al glucagón obtuvieron aprobación como fármacos para tratar la diabetes y la obesidad a partir de la década de 2000. [ cita necesaria ]
El GLP-1 endógeno se degrada rápidamente principalmente por la dipeptidil peptidasa-4 (DPP-4), así como por la endopeptidasa neutra 24.11 (NEP 24.11) y el aclaramiento renal , lo que da como resultado una vida media de aproximadamente 2 minutos. En consecuencia, sólo entre el 10 y el 15 % del GLP-1 llega intacto a la circulación, lo que lleva a niveles plasmáticos en ayunas de sólo 0 a 15 pmol/l. Para superar esto, se han desarrollado agonistas del receptor de GLP-1 e inhibidores de DPP-4 para aumentar la actividad del GLP-1. A diferencia de los agentes de tratamiento comunes como la insulina y la sulfonilurea , el tratamiento basado en GLP-1 se ha asociado con una pérdida de peso y un menor riesgo de hipoglucemia , dos consideraciones importantes para los pacientes con diabetes tipo 2.
El gen del proglucagón se expresa en varios órganos, incluido el páncreas ( células α de los islotes de Langerhans ), el intestino (células L enteroendocrinas intestinales) y el cerebro ( tronco cerebral caudal e hipotálamo ). La expresión del gen del proglucagón pancreático se promueve con el ayuno y la inducción de hipoglucemia y se inhibe con la insulina. Por el contrario, la expresión del gen intestinal del proglucagón se reduce durante el ayuno y se estimula con el consumo de alimentos. En los mamíferos, la transcripción da lugar a un ARNm idéntico en los tres tipos de células, que luego se traduce al precursor de 180 aminoácidos llamado proglucagón . Sin embargo, como resultado de mecanismos de procesamiento postraduccional específicos de cada tejido, se producen diferentes péptidos en las diferentes células. [1] [2]
En el páncreas ( células α de los islotes de Langerhans ), el proglucagón es escindido por la prohormona convertasa (PC) 2, produciendo el péptido pancreático relacionado con la glicentina (GRPP), el glucagón , el péptido 1 interviniente (IP-1) y el fragmento principal de proglucagón ( MPGF). [3]
En el intestino y el cerebro, el proglucagón es catalizado por PC 1/3 dando lugar a glicentina, que puede procesarse posteriormente en GRPP y oxintomodulina , GLP-1, el péptido 2 interviniente (IP-2) y el péptido 2 similar al glucagón ( GLP-2 ). Inicialmente, se pensó que el GLP-1 correspondía al proglucagón (72-108) adecuado al N-terminal del MGPF, pero los experimentos de secuenciación del GLP-1 endógeno revelaron una estructura correspondiente al proglucagón (78-107), de la cual se hicieron dos descubrimientos. encontró. En primer lugar, se descubrió que la endopeptidasa cataliza el GLP-1 de longitud completa (1-37) al GLP-1 biológicamente activo (7-37). En segundo lugar, se descubrió que la glicina correspondiente al proglucagón (108) sirve como sustrato para la amidación de la arginina C-terminal, lo que da como resultado la igualmente potente amida GLP-1 (7-36). En los seres humanos, casi todo (>80%) el GLP-1 secretado está amidado, mientras que una parte considerable permanece GLP-1 (7-37) en otras especies. [3] [4]
El GLP-1 se empaqueta en gránulos secretores y se secreta en el sistema portal hepático por las células L intestinales ubicadas principalmente en el íleon distal y el colon, pero también se encuentra en el yeyuno y el duodeno . Las células L son células epiteliales triangulares de tipo abierto que están en contacto directo con la luz y el tejido neurovascular y, en consecuencia, son estimuladas por diversos factores nutricionales , neurales y endocrinos . [2]
El GLP-1 se libera en un patrón bifásico con una fase temprana después de 10 a 15 minutos seguida de una segunda fase más larga después de 30 a 60 minutos después de la ingestión de la comida. Como la mayoría de las células L se encuentran en el íleon distal y el colon, la fase temprana probablemente se explica por la señalización neuronal, los péptidos intestinales o los neurotransmisores . Otra evidencia sugiere que la cantidad de células L ubicadas en el yeyuno proximal es suficiente para explicar la secreción de la fase temprana a través del contacto directo con los nutrientes luminales. De manera menos controvertida, la segunda fase probablemente sea causada por la estimulación directa de las células L por los nutrientes digeridos . Por tanto , la tasa de vaciado gástrico es un aspecto importante a considerar, ya que regula la entrada de nutrientes al intestino delgado donde se produce la estimulación directa. Una de las acciones del GLP-1 es inhibir el vaciamiento gástrico , frenando así su propia secreción tras la activación posprandial . [1] [2]
La concentración plasmática en ayunas de GLP-1 biológicamente activo oscila entre 0 y 15 pmol/L en humanos y aumenta de 2 a 3 veces con el consumo de alimentos, dependiendo del tamaño de la comida y la composición de nutrientes. También se ha demostrado que los nutrientes individuales, como los ácidos grasos , los aminoácidos esenciales y la fibra dietética, estimulan la secreción de GLP-1.
Los azúcares se han asociado con varias vías de señalización , que inician la despolarización de la membrana de las células L provocando una concentración elevada de Ca 2+ citosólico que a su vez induce la secreción de GLP-1. Los ácidos grasos se han asociado con la movilización de las reservas intracelulares de Ca 2+ y la posterior liberación de Ca 2+ en el citosol . Los mecanismos de secreción de GLP-1 desencadenada por proteínas son menos claros, pero la proporción y composición de aminoácidos parecen importantes para el efecto estimulante. [5]
Una vez secretado, el GLP-1 es extremadamente susceptible a la actividad catalítica de la enzima proteolítica dipeptidil peptidasa-4 ( DPP-4 ). Específicamente, DPP-4 escinde el enlace peptídico entre Ala 8 - Glu 9, lo que da como resultado la abundante amida GLP-1 (9–36) que constituye del 60 al 80 % del GLP-1 total en circulación. La DPP-4 se expresa ampliamente en múltiples tejidos y tipos de células y existe tanto en forma circulante soluble como anclada a la membrana. En particular, la DPP-4 se expresa en la superficie de las células endoteliales , incluidas las ubicadas directamente adyacentes a los sitios de secreción de GLP-1. [2] En consecuencia, se estima que menos del 25% del GLP-1 secretado sale del intestino intacto. Además, presumiblemente debido a la alta concentración de DPP-4 encontrada en los hepatocitos , entre el 40 y el 50% del GLP-1 activo restante se degrada en el hígado . Por tanto, debido a la actividad de la DPP-4, sólo entre el 10 y el 15 % del GLP-1 secretado llega intacto a la circulación. [3]
La endopeptidasa neutra 24.11 (NEP 24.11) es una metalopeptidasa de zinc unida a una membrana que se expresa ampliamente en varios tejidos, pero que se encuentra en concentraciones particularmente altas en los riñones , y que también se considera responsable de la rápida degradación de GLP-1. Principalmente escinde péptidos en el lado N-terminal de aminoácidos aromáticos o aminoácidos hidrofóbicos y se estima que contribuye hasta en un 50% a la degradación del GLP-1. Sin embargo, la actividad sólo se hace evidente una vez que se ha evitado la degradación de la DPP-4 , ya que la DPP-4 ya ha procesado la mayor parte del GLP-1 que llega a los riñones . De manera similar, el aclaramiento renal parece más significativo para la eliminación del GLP-1 ya inactivado. [6]
La vida media resultante del GLP-1 activo es de aproximadamente 2 minutos, pero es suficiente para activar los receptores de GLP-1 .
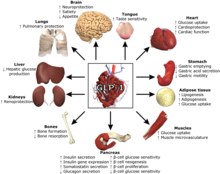
El GLP-1 posee varias propiedades fisiológicas que lo convierten (y sus análogos funcionales ) en un tema de investigación intensiva como posible tratamiento de la diabetes mellitus , ya que estas acciones inducen mejoras a largo plazo junto con los efectos inmediatos. [ necesita una cita para verificar ] [7] [8] [9] [10] Aunque la secreción reducida de GLP-1 se ha asociado anteriormente con un efecto atenuado de la incretina en pacientes con diabetes tipo 2 , ahora se acepta que la secreción de GLP-1 en pacientes con diabetes tipo 2 no difiere de los sujetos sanos. [11]
El efecto más notable del GLP-1 es su capacidad para promover la secreción de insulina de forma dependiente de la glucosa. A medida que el GLP-1 se une a los receptores de GLP-1 expresados en las células β pancreáticas , los receptores se acoplan a las subunidades de la proteína G y activan la adenilato ciclasa que aumenta la producción de AMPc a partir de ATP . [3] Posteriormente, la activación de vías secundarias, incluidas PKA y Epac2 , altera la actividad del canal iónico provocando niveles elevados de Ca 2+ citosólico que mejora la exocitosis de los gránulos que contienen insulina. Durante el proceso, la entrada de glucosa asegura suficiente ATP para mantener el efecto estimulante. [3]
Además, el GLP-1 garantiza que las reservas de insulina de las células β se repongan para evitar el agotamiento durante la secreción al promover la transcripción del gen de la insulina, la estabilidad del ARNm y la biosíntesis. [2] [12] Evidentemente, el GLP-1 también aumenta [13] la masa de células β al promover la proliferación y la neogénesis al tiempo que inhibe la apoptosis . Dado que tanto la diabetes tipo 1 como la diabetes 2 están asociadas con la reducción de las células β funcionales, este efecto es muy interesante en relación con el tratamiento de la diabetes. [12] Considerado casi tan importante como el efecto de mejorar la secreción de insulina, se ha demostrado que el GLP-1 inhibe la secreción de glucagón en niveles de glucosa superiores a los niveles en ayunas. Fundamentalmente, esto no afecta la respuesta del glucagón a la hipoglucemia, ya que este efecto también depende de la glucosa. El efecto inhibidor probablemente esté mediado indirectamente a través de la secreción de somatostatina , pero no se puede excluir por completo un efecto directo. [14] [15]
En el cerebro, la activación del receptor GLP-1 se ha relacionado con efectos neurotróficos que incluyen neurogénesis [16] [17] y efectos neuroprotectores que incluyen señalización reducida necrótica [18] y apoptótica [19] [18] , muerte celular , [20] [21 ] y disfunciones. [22] En el cerebro enfermo, el tratamiento con agonistas del receptor GLP-1 se asocia con protección contra una variedad de modelos de enfermedades experimentales como la enfermedad de Parkinson , [23] [17] la enfermedad de Alzheimer , [24] [25] accidente cerebrovascular, [23] lesión cerebral traumática , [13] [18] y esclerosis múltiple . [26] De acuerdo con la expresión del receptor de GLP-1 en el tronco del encéfalo y el hipotálamo, se ha demostrado que el GLP-1 promueve la saciedad y, por lo tanto, reduce la ingesta de alimentos y agua. En consecuencia, los sujetos diabéticos tratados con agonistas del receptor de GLP-1 a menudo experimentan pérdida de peso en contraposición al aumento de peso inducido comúnmente con otros agentes de tratamiento. [2] [15]
En el estómago, el GLP-1 inhibe el vaciado gástrico, la secreción de ácido y la motilidad, lo que en conjunto disminuye el apetito. Al desacelerar el vaciado gástrico, el GLP-1 reduce la excursión posprandial de la glucosa, que es otra propiedad atractiva para el tratamiento de la diabetes. Sin embargo, estas actividades gastrointestinales también son la razón por la cual los sujetos tratados con agentes basados en GLP-1 experimentan ocasionalmente náuseas . [14]
El GLP-1 también ha mostrado signos de ejercer efectos protectores y reguladores en muchos otros tejidos, incluidos el corazón, la lengua, el tejido adiposo, los músculos, los huesos, los riñones, el hígado y los pulmones.
En la década de 1980, Svetlana Mojsov trabajó en la identificación del GLP-1 en el Hospital General de Massachusetts , donde era jefa de una instalación de síntesis de péptidos. [27] Para tratar de identificar si un fragmento específico de GLP-q era una incretina, Mojsov creó un anticuerpo contra la incretina y desarrolló formas de rastrear su presencia. Identificó que un tramo de 31 aminoácidos en el GLP-1 era una incretina. [28] [29] Mojsov y sus colaboradores Daniel J. Drucker y Habener demostraron que pequeñas cantidades de GLP-1 sintetizado en laboratorio podrían activar la insulina. [30] [31] [32]
Mojsov luchó para que su nombre se incluyera en las patentes, y el Hospital General de Massachusetts finalmente acordó modificar cuatro patentes para incluir su nombre. Recibió su tercio de las regalías por drogas durante un año. [33]
Asociación Estadounidense de Diabetes: enlace-http://diabetes.diabetesjournals.org/content/56/1/8.full