
En química orgánica , un carbeno es una molécula que contiene un átomo de carbono neutro con una valencia de dos y dos electrones de valencia no compartidos . La fórmula general es R−:C−R' o R=C: donde R representa sustituyentes o átomos de hidrógeno.
El término "carbeno" también puede referirse al compuesto específico : CH 2 , también llamado metileno , el hidruro original del que se derivan formalmente todos los demás compuestos de carbeno. [1] [2]
Hay dos tipos de carbenos: singletes o tripletes , según su estructura electrónica. [3] Las diferentes clases sufren diferentes reacciones.
La mayoría de los carbenos son extremadamente reactivos y de vida corta. Un pequeño número (los dihalocarbenos , monóxido de carbono , [4] y monosulfuro de carbono ) se pueden aislar y estabilizar como ligandos metálicos , pero de lo contrario no se pueden almacenar a granel. Una rara excepción son los carbenos persistentes , [5] que tienen una amplia aplicación en la química organometálica moderna .
Hay dos métodos comunes para la generación de carbeno.
En la eliminación α , dos sustituyentes se eliminan del mismo átomo de carbono. Esto ocurre con reactivos sin buenos grupos salientes vecinos a un protón ácido que se exponen a una base fuerte; por ejemplo, el fenillitio extraerá HX de un haloformo (CHX 3 ). [6] Este tipo de reacciones normalmente requieren condiciones de transferencia de fase . [ cita necesaria ]
Las moléculas sin protones ácidos también pueden formar carbenos. Un dihaluro geminal expuesto a organolitios sufre un intercambio metal-halógeno y luego elimina una sal de litio para dar un carbeno, y el metal zinc extrae los halógenos de manera similar en la reacción de Simmons-Smith . [7]
Sigue siendo incierto si estas condiciones forman carbenos verdaderamente libres o un complejo metal-carbeno. Sin embargo, los metalocarbenos así formados dan los productos orgánicos esperados. [7] En un caso especializado pero instructivo, los compuestos de α-halo de mercurio se pueden aislar y termolizar por separado. El "reactivo de Seyferth" libera CCl 2 al calentarse:
Por otra parte, los carbenos se pueden producir a partir de una reacción de extrusión con un gran cambio de energía libre. Las diazirinas y los epóxidos se fotolizan con una tremenda liberación en la tensión del anillo a los carbenos. Los primeros extruyen gas nitrógeno inerte , pero los epóxidos normalmente dan desechos de carbonilo reactivos , y los epóxidos asimétricos pueden formar potencialmente dos carbenos diferentes. Normalmente, el enlace CO con un orden de enlace fraccional menor (menos estructuras de resonancia de doble enlace) se rompe. Por ejemplo, cuando un sustituyente es alquilo y otro arilo , el carbono sustituido con arilo suele liberarse como un fragmento de carbeno.
La tensión del anillo no es necesaria para una fuerza motriz termodinámica fuerte. Los catalizadores de fotólisis , calor o metales de transición (típicamente rodio y cobre ) descomponen los diazoalcanos en carbeno y nitrógeno gaseoso ; esto ocurre en la reacción de Bamford-Stevens y el reordenamiento de Wolff . Al igual que en el caso de los metalocarbenos, algunas reacciones de los diazoalcanos que formalmente proceden a través de carbenos pueden formar en cambio un cicloaducto intermedio [3+2] que extruye nitrógeno.
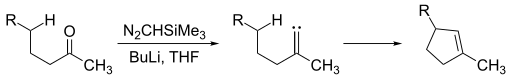
Para generar un alquiliden carbeno, se puede exponer una cetona a trimetilsilil diazometano y luego a una base fuerte.

Las dos clases de carbenos son carbenos singletes y tripletes . Los carbenos tripletes son dirradicales con dos electrones desapareados, generalmente se forman a partir de reacciones que rompen dos enlaces σ (eliminación α y algunas reacciones de extrusión) y no rehibridan el átomo de carbeno. Los carbenos singlete tienen un solo par solitario , generalmente se forman a partir de descomposiciones diazo y adoptan una estructura orbital sp 2 . [8] Los ángulos de enlace (según lo determinado por EPR ) son de 125 a 140° para el metileno triplete y de 102° para el metileno singlete.
La mayoría de los carbenos tienen un estado fundamental triplete no lineal . Para los hidrocarburos simples, los carbenos tripletes suelen ser sólo 8 kcal / mol (33 kJ /mol) más estables que los carbenos singlete, comparable a la inversión de nitrógeno . La estabilización se atribuye en parte a la regla de máxima multiplicidad de Hund . Sin embargo, las estrategias para estabilizar los carbenos tripletes a temperatura ambiente son difíciles de alcanzar. Se ha demostrado que el 9-fluorenilideno es una mezcla que se equilibra rápidamente de estados singlete y triplete con una diferencia de energía de aproximadamente 1,1 kcal/mol (4,6 kJ/mol), aunque la extensa deslocalización de electrones en los anillos complica cualquier conclusión extraída de los diarilcarbenos . [9] Las simulaciones sugieren que los heteroátomos electropositivos pueden estabilizar termodinámicamente los carbenos tripletes, como los sililo y sililoxi carbenos, especialmente los trifluorosilil carbenos. [10]
Los sustituyentes básicos de Lewis de nitrógeno, oxígeno, azufre o haluro unidos al carbono divalente pueden deslocalizar un par de electrones en un orbital p vacío para estabilizar el estado singlete. Este fenómeno subyace a la notable estabilidad de los carbenos persistentes .
Los carbenos se comportan como ácidos de Lewis muy agresivos . Pueden atacar pares solitarios , pero su principal utilidad sintética surge de los ataques a los enlaces π , que dan ciclopropanos; y en los enlaces σ , que provocan la inserción de carbeno . Otras reacciones incluyen reordenamientos y dimerizaciones. La reactividad de un carbeno particular depende de los sustituyentes , incluidos los metales presentes.

Los carbenos singlete y triplete exhiben reactividad divergente. [11] [ página necesaria ] [12]
Los carbenos tripletes son dirradicales y participan en adiciones radicales graduales . La adición de carbeno triplete implica necesariamente (al menos un) intermediario con dos electrones desapareados.
Los carbenos singletes pueden reaccionar (y lo hacen) como electrófilos , nucleófilos o ambífilos. [4] Sus reacciones suelen ser concertadas y, a menudo, queletrópicas . [ cita necesaria ] Los carbenos singlete suelen ser electrófilos, [4] a menos que tengan un orbital p lleno , en cuyo caso pueden reaccionar como bases de Lewis. La reacción de Bamford-Stevens da carbenos en disolventes apróticos e iones carbenio en disolventes próticos .
Los diferentes mecanismos implican que las adiciones de carbeno singlete son estereoespecíficas pero las adiciones de carbeno triplete son estereoselectivas . El metileno de la fotólisis del diazometano reacciona con cis o trans - 2-buteno para dar un único diastereómero de 1,2-dimetilciclopropano : cis de cis y trans de trans . Por tanto, el metileno es un carbeno singlete; si fuera triplete, el producto no dependería de la geometría del alqueno inicial. [13]
Los carbenos se añaden a dobles enlaces para formar ciclopropanos , [14] y, en presencia de un catalizador de cobre , a alquinos para dar ciclopropenos . Las reacciones de adición suelen ser muy rápidas y exotérmicas , y la generación de carbeno limita la velocidad de reacción.
En la ciclopropanación Simmons-Smith , el yoduro de yodometilzinc normalmente forma complejos con cualquier grupo hidroxi alílico de modo que la adición sea sinérgica al grupo hidroxi .

Las inserciones son otro tipo común de reacción de carbeno, [15] una forma de adición oxidativa . Las inserciones pueden ocurrir o no en un solo paso (ver arriba). El resultado final es que el carbeno se interpone en un enlace existente, preferiblemente X-H (X, no carbono), en caso contrario C-H o (en su defecto) un enlace C-C. Los alquilcarbenos se insertan mucho más selectivamente que el metileno, que no diferencia entre enlaces CH primarios, secundarios y terciarios.

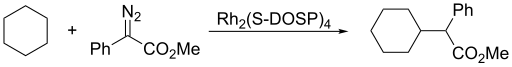
El reordenamiento 1,2 producido por la inserción intramolecular en un enlace adyacente al centro carbeno es una molestia en algunos esquemas de reacción, ya que consume el carbeno para producir el mismo efecto que una reacción de eliminación tradicional . [16] Generalmente, las estructuras rígidas favorecen las inserciones intramoleculares . En estructuras flexibles, se prefiere la formación de anillos de cinco miembros a la formación de anillos de seis miembros. Cuando tales inserciones son posibles, no se observan inserciones intermoleculares . Tanto las inserciones intermoleculares como intramoleculares admiten la inducción asimétrica de un catalizador metálico quiral.
Los carbenos pueden formar aductos con nucleófilos y son un precursor común de varios 1,3-dipolos . [dieciséis]

Los carbenos y sus precursores carbenoides pueden dimerizarse a alquenos . Esto suele ser, pero no siempre, una reacción secundaria no deseada; La dimerización del carbeno metálico se ha utilizado en la síntesis de polialquiniletenos y es la principal ruta industrial hacia el teflón (ver Carbeno § Aplicaciones industriales). Los carbenos persistentes se equilibran con sus respectivos dímeros, el equilibrio de Wanzlick .
En especies organometálicas , los complejos metálicos con fórmulas L n MCRR' se describen a menudo como complejos de carbeno. [17] Sin embargo, estas especies no reaccionan como los carbenos libres y rara vez se generan a partir de precursores de carbeno, a excepción de los carbenos persistentes. [ cita necesaria ] [18] Los complejos de carbeno de metales de transición se pueden clasificar según su reactividad, siendo las dos primeras clases las más claramente definidas:

Una aplicación a gran escala de los carbenos es la producción industrial de tetrafluoroetileno , el precursor del teflón . El tetrafluoroetileno se genera mediante la intermediación del difluorocarbeno : [22]
La inserción de carbenos en enlaces C-H se ha explotado ampliamente, por ejemplo, la funcionalización de materiales poliméricos [23] y el electrocurado de adhesivos . [24] Muchas aplicaciones se basan en 3-aril-3-trifluorometil diazirinas sintéticas [25] [26] (un precursor de carbeno que puede activarse mediante calor, [27] luz, [26] [27] o voltaje ) [28] [24] pero existe toda una familia de colorantes carbeno .
Los carbenos fueron postulados por primera vez por Eduard Buchner en 1903 en estudios de ciclopropanación de diazoacetato de etilo con tolueno. [29] En 1912 Hermann Staudinger [30] también convirtió alquenos en ciclopropanos con diazometano y CH 2 como intermediario. Doering en 1954 demostró su utilidad sintética con diclorocarbeno . [31]