El curio es un elemento químico sintético ; tiene símbolo Cm y número atómico 96. Este elemento actínido transuránico recibió su nombre de los eminentes científicos Marie y Pierre Curie , ambos conocidos por sus investigaciones sobre la radiactividad . El curio fue fabricado intencionalmente por primera vez por el equipo de Glenn T. Seaborg , Ralph A. James y Albert Ghiorso en 1944, utilizando el ciclotrón de Berkeley . Bombardearon el elemento recién descubierto plutonio (el isótopo 239 Pu ) con partículas alfa . Luego se envió al Laboratorio Metalúrgico de la Universidad de Chicago , donde finalmente se separó e identificó una pequeña muestra de curio. El descubrimiento se mantuvo en secreto hasta después del final de la Segunda Guerra Mundial . La noticia se hizo pública en noviembre de 1947. La mayor parte del curio se produce bombardeando uranio o plutonio con neutrones en reactores nucleares : una tonelada de combustible nuclear gastado contiene ~20 gramos de curio.
El curio es un metal duro, denso y plateado con un alto punto de fusión y ebullición para un actínido. Es paramagnético en condiciones ambientales , pero se vuelve antiferromagnético al enfriarse, y también se observan otras transiciones magnéticas en muchos compuestos de curio. En compuestos, el curio suele tener valencia +3 y, a veces, +4; la valencia +3 es predominante en las soluciones. El curio se oxida fácilmente y sus óxidos son una forma dominante de este elemento. Forma complejos fuertemente fluorescentes con diversos compuestos orgánicos, pero no hay evidencia de su incorporación a bacterias y arqueas . Si ingresa al cuerpo humano, el curio se acumula en los huesos, los pulmones y el hígado, donde promueve el cáncer .
Todos los isótopos conocidos del curio son radiactivos y tienen una masa crítica pequeña para una reacción nuclear en cadena . En su mayoría emiten partículas α ; Los generadores termoeléctricos de radioisótopos pueden utilizar el calor de este proceso, pero esto se ve obstaculizado por la rareza y el alto costo del curio. El curio se utiliza para fabricar actínidos más pesados y el radionúclido 238 Pu como fuente de energía en marcapasos cardíacos artificiales y RTG para naves espaciales. Sirvió como fuente α en los espectrómetros de rayos X de partículas alfa de varias sondas espaciales, incluidos los vehículos exploradores de Marte Sojourner , Spirit , Opportunity y Curiosity y el módulo de aterrizaje Philae en el cometa 67P/Churyumov-Gerasimenko , para analizar la composición y estructura. de la superficie.


Aunque el curio probablemente se había producido en experimentos nucleares anteriores, así como en el reactor de fisión nuclear natural de Oklo, Gabón, fue sintetizado , aislado e identificado intencionalmente por primera vez en 1944, en la Universidad de California, Berkeley , por Glenn T. Seaborg , Ralph A. James y Albert Ghiorso . En sus experimentos utilizaron un ciclotrón de 60 pulgadas (150 cm) . [5]
El curio fue identificado químicamente en el Laboratorio Metalúrgico (ahora Laboratorio Nacional Argonne ), de la Universidad de Chicago . Fue el tercer elemento transuránico descubierto, aunque es el cuarto de la serie; el elemento más ligero, el americio, aún era desconocido. [6] [7]
La muestra se preparó de la siguiente manera: primero se recubrió una solución de nitrato de plutonio sobre una lámina de platino de aproximadamente 0,5 cm 2 de área, la solución se evaporó y el residuo se convirtió en óxido de plutonio (IV) (PuO 2 ) mediante recocido . Después de la irradiación del óxido con ciclotrón, el recubrimiento se disolvió con ácido nítrico y luego se precipitó como hidróxido usando una solución acuosa concentrada de amoníaco . El residuo se disolvió en ácido perclórico y se realizó una separación adicional mediante intercambio iónico para producir un determinado isótopo de curio. La separación de curio y americio fue tan minuciosa que el grupo de Berkeley inicialmente llamó a esos elementos pandemonium (del griego para todos los demonios o infierno ) y delirium (del latín para locura ). [8] [9]
El curio-242 se produjo en julio-agosto de 1944 bombardeando 239 Pu con partículas α para producir curio con la liberación de un neutrón :
El curio-242 se identificó inequívocamente por la energía característica de las partículas α emitidas durante la desintegración:
La vida media de esta desintegración alfa se midió primero en 150 días y luego se corrigió a 162,8 días. [10]
En marzo de 1945 se produjo otro isótopo de 240 Cm en una reacción similar:
La vida media de desintegración α de 240 Cm se determinó correctamente en 26,7 días. [10]
El descubrimiento del curio y el americio en 1944 estuvo estrechamente relacionado con el Proyecto Manhattan , por lo que los resultados fueron confidenciales y no se desclasificaron hasta 1945. Seaborg filtró la síntesis de los elementos 95 y 96 en el programa de radio infantil estadounidense Quiz Kids , cinco días antes de la presentación oficial en una reunión de la Sociedad Química Estadounidense el 11 de noviembre de 1945, cuando un oyente preguntó si durante la guerra se había descubierto algún nuevo elemento transuránico además del plutonio y el neptunio . [8] El descubrimiento del curio ( 242 Cm y 240 Cm), su producción y sus compuestos fueron posteriormente patentados y solo se menciona a Seaborg como inventor. [11]
El elemento lleva el nombre de Marie Curie y su marido Pierre Curie , conocidos por descubrir el radio y por su trabajo en radioactividad . Siguió el ejemplo del gadolinio , un elemento lantánido situado por encima del curio en la tabla periódica, que lleva el nombre del explorador de elementos de tierras raras Johan Gadolin : [12]
Como nombre para el elemento de número atómico 96 nos gustaría proponer "curio", de símbolo Cm. La evidencia indica que el elemento 96 contiene siete electrones 5f y, por tanto, es análogo al elemento gadolinio, con sus siete electrones 4f en la serie regular de tierras raras. Sobre esta base, el elemento 96 recibe el nombre de los Curie de forma análoga a la denominación del gadolinio, con la que se honraba al químico Gadolin. [6]
Las primeras muestras de curio eran apenas visibles y fueron identificadas por su radiactividad. Louis Werner e Isadore Perlman fabricaron la primera muestra sustancial de 30 µg de hidróxido de curio-242 en la Universidad de California, Berkeley, en 1947, bombardeando americio -241 con neutrones. [13] [14] [15] Cantidades macroscópicas de fluoruro de curio (III) fueron obtenidas en 1950 por WWT Crane, JC Wallmann y BB Cunningham. Su susceptibilidad magnética era muy cercana a la del GdF 3 , proporcionando la primera evidencia experimental de la valencia +3 del curio en sus compuestos. [13] El curio metálico no se produjo hasta 1951 mediante la reducción de CmF 3 con bario . [16] [17]

3·H2O_PL_420_nm.jpg/440px-Cm(HDPA)3·H2O_PL_420_nm.jpg)
El curio, un elemento radiactivo sintético, es un metal duro y denso con una apariencia de color blanco plateado y propiedades físicas y químicas similares al gadolinio . Su punto de fusión de 1344 °C es significativamente más alto que el de los elementos anteriores neptunio (637 °C), plutonio (639 °C) y americio (1176 °C). En comparación, el gadolinio se funde a 1312 °C. El curio hierve a 3556 °C. Con una densidad de 13,52 g/cm 3 , el curio es más ligero que el neptunio (20,45 g/cm 3 ) y el plutonio (19,8 g/cm 3 ), pero más pesado que la mayoría de los demás metales. De las dos formas cristalinas de curio, el α-Cm es más estable en condiciones ambientales. Tiene simetría hexagonal, grupo espacial P6 3 /mmc, parámetros de red a = 365 pm yc = 1182 pm , y cuatro unidades fórmula por celda unitaria . [18] El cristal consta de un empaquetamiento cerrado de doble hexágono con la secuencia de capas ABAC y, por lo tanto, es isotípico con el α-lantano. A una presión >23 GPa , a temperatura ambiente, α-Cm se convierte en β-Cm, que tiene simetría cúbica centrada en las caras , grupo espacial Fm 3 m y constante de red a = 493 pm. [18] Tras una mayor compresión a 43 GPa, el curio se convierte en una estructura ortorrómbica γ-Cm similar al α-uranio, sin que se observen más transiciones hasta 52 GPa. Estas tres fases de curio también se denominan Cm I, II y III. [19] [20]
El curio tiene propiedades magnéticas peculiares. Su elemento vecino, el americio, no muestra desviación del paramagnetismo de Curie-Weiss en todo el rango de temperatura, pero α-Cm se transforma a un estado antiferromagnético al enfriarse a 65-52 K, [21] [22] y β-Cm exhibe una transición ferrimagnética en ~205 K. Las pnictidas de curio muestran transiciones ferromagnéticas al enfriarse: 244 CmN y 244 CmAs a 109 K, 248 CmP a 73 K y 248 CmSb a 162 K. El análogo de lantánido del curio, el gadolinio y sus pnictidas, también muestran transiciones magnéticas al enfriarse. enfriamiento, pero el carácter de transición es algo diferente: Gd y GdN se vuelven ferromagnéticos, y GdP, GdAs y GdSb muestran un orden antiferromagnético. [23]
Según los datos magnéticos, la resistividad eléctrica del curio aumenta con la temperatura (aproximadamente el doble entre 4 y 60 K) y luego es casi constante hasta la temperatura ambiente. Hay un aumento significativo en la resistividad con el tiempo (~10 µΩ·cm/h ) debido al autodaño de la red cristalina por desintegración alfa. Esto hace incierta la verdadera resistividad del curio (~125 µΩ·cm ). La resistividad del curio es similar a la del gadolinio y a la de los actínidos plutonio y neptunio, pero significativamente mayor que la del americio, uranio, polonio y torio . [3] [24]
Bajo iluminación ultravioleta, los iones de curio (III) muestran una fluorescencia de color amarillo anaranjado fuerte y estable con un máximo en el rango de 590 a 640 nm, dependiendo de su entorno. [25] La fluorescencia se origina en las transiciones del primer estado excitado 6 D 7/2 y el estado fundamental 8 S 7/2 . El análisis de esta fluorescencia permite monitorear las interacciones entre iones Cm (III) en complejos orgánicos e inorgánicos. [26]

El ion curio en solución casi siempre tiene un estado de oxidación +3 , el estado de oxidación más estable del curio. [27] Un estado de oxidación +4 se observa principalmente en unas pocas fases sólidas, como CmO 2 y CmF 4 . [28] [29] El curio (IV) acuoso sólo se conoce en presencia de oxidantes fuertes como el persulfato de potasio , y se reduce fácilmente a curio (III) mediante radiólisis e incluso con el agua misma. [30] El comportamiento químico del curio es diferente del de los actínidos torio y uranio, y es similar al del americio y muchos lantánidos . En solución acuosa, el ion Cm 3+ es de incoloro a verde pálido; [31] El ion Cm 4+ es de color amarillo pálido. [32] La absorción óptica del ion Cm 3+ contiene tres picos agudos a 375,4, 381,2 y 396,5 nm y su fuerza se puede convertir directamente en la concentración de los iones. [33] El estado de oxidación +6 sólo se ha informado una vez en solución en 1978, como el ion curilo ( CmO2+
2): esto se preparó a partir de la desintegración beta del americio-242 en el ion americio (V)242
AmO+
2. [2] No obtener Cm(VI) de la oxidación de Cm(III) y Cm(IV) puede deberse al alto potencial de ionización de Cm 4+ /Cm 3+ y a la inestabilidad de Cm(V). [30]
Los iones de curio son ácidos de Lewis duros y, por tanto, forman la mayoría de los complejos estables con bases duras. [34] El enlace es principalmente iónico, con un pequeño componente covalente. [35] El curio en sus complejos comúnmente exhibe un entorno de coordinación de 9 veces, con una geometría molecular prismática trigonal tricapeada . [36]
Se conocen unos 19 radioisótopos y 7 isómeros nucleares , de 233 Cm a 251 Cm; ninguno es estable . Las vidas medias más largas son 15,6 millones de años ( 247 Cm) y 348.000 años ( 248 Cm). Otros longevos son 245 Cm (8500 años), 250 Cm (8300 años) y 246 Cm (4760 años). El curio-250 es inusual: en su mayor parte (~86%) se desintegra por fisión espontánea . Los isótopos más utilizados son 242 Cm y 244 Cm con vidas medias de 162,8 días y 18,1 años, respectivamente. [10]
Todos los isótopos comprendidos entre 242 Cm y 248 Cm, así como los 250 Cm, sufren una reacción nuclear en cadena autosostenida y, por lo tanto, en principio pueden ser combustible nuclear en un reactor. Como ocurre con la mayoría de los elementos transuránicos, la sección transversal de fisión nuclear es especialmente alta para los isótopos de curio de masa impar 243 Cm, 245 Cm y 247 Cm. Estos se pueden utilizar en reactores de neutrones térmicos , mientras que una mezcla de isótopos de curio sólo es adecuada para reactores reproductores rápidos , ya que los isótopos de masa uniforme no son fisibles en un reactor térmico y se acumulan a medida que aumenta el quemado. [40] El combustible de óxido mixto (MOX), que se utilizará en los reactores de potencia, debe contener poco o nada de curio porque la activación de neutrones de 248 Cm creará californio . El californio es un potente emisor de neutrones y contaminaría la parte final del ciclo del combustible y aumentaría la dosis recibida por el personal del reactor. Por lo tanto, si se van a utilizar actínidos menores como combustible en un reactor de neutrones térmicos, el curio debe excluirse del combustible o colocarse en barras de combustible especiales donde sea el único actínido presente. [41]
La tabla adyacente enumera las masas críticas de isótopos de curio para una esfera, sin moderador ni reflector. Con un reflector metálico (30 cm de acero), las masas críticas de los isótopos impares son de unos 3 a 4 kg. Cuando se utiliza agua (espesor ~20–30 cm) como reflector, la masa crítica puede ser tan pequeña como 59 gramos para 245 cm, 155 gramos para 243 cm y 1550 gramos para 247 cm. Existe una incertidumbre significativa en estos valores de masa crítica. Si bien suele ser del orden del 20%, algunos grupos de investigación enumeraron valores de 242 cm y 246 cm de hasta 371 kg y 70,1 kg, respectivamente. [40] [43]
Actualmente el curio no se utiliza como combustible nuclear debido a su baja disponibilidad y elevado precio. [44] Los 245 Cm y 247 Cm tienen una masa crítica muy pequeña y, por lo tanto, podrían usarse en armas nucleares tácticas , pero no se sabe que se haya fabricado ninguno. El curio-243 no es adecuado para ello debido a su corta vida media y su fuerte emisión α, que provocaría un calor excesivo. [45] El curio-247 sería muy adecuado debido a su larga vida media, que es 647 veces más larga que la del plutonio-239 (utilizado en muchas armas nucleares existentes ).

El isótopo más longevo, 247 Cm, tiene una vida media de 15,6 millones de años; por lo que cualquier curio primordial , es decir, presente en la Tierra cuando se formó, ya debería haberse descompuesto. Su presencia pasada como radionúclido extinto es detectable como un exceso de su hija primordial y de larga vida, 235 U. [46] Pueden aparecer rastros de 242 Cm de forma natural en minerales de uranio debido a la captura de neutrones y la desintegración beta ( 239 Pu → 240 Pu → 241 Am → 242 Cm), aunque las cantidades serían pequeñas y esto no ha sido confirmado: incluso con estimaciones "extremadamente generosas" para las posibilidades de absorción de neutrones, la cantidad de 242 Cm presente en 1 × 10 8 kg de pechblenda con 18% de uranio sería ni siquiera ser un átomo. [47] [48] [49] Es probable que también se traigan a la Tierra rastros de 247 Cm en rayos cósmicos , pero esto tampoco ha sido confirmado. [47] También existe la posibilidad de que 244 Cm se produzca como hija de la doble desintegración beta del 244 Pu natural . [47] [50]
El curio se produce artificialmente en pequeñas cantidades con fines de investigación. También se encuentra como uno de los productos de desecho del combustible nuclear gastado . [51] [52] El curio está presente en la naturaleza en algunas áreas utilizadas para pruebas de armas nucleares . [53] El análisis de los restos en el sitio de pruebas de la primera arma termonuclear de los Estados Unidos , Ivy Mike (1 de noviembre de 1952, atolón de Enewetak ), además del einstenio , el fermio , el plutonio y el americio , también reveló isótopos de berkelio, californio y curio, en en particular 245 Cm, 246 Cm y cantidades menores de 247 Cm, 248 Cm y 249 Cm. [54]
Los compuestos de curio atmosférico son poco solubles en solventes comunes y en su mayoría se adhieren a las partículas del suelo. El análisis del suelo reveló una concentración de curio aproximadamente 4.000 veces mayor en las partículas arenosas del suelo que en el agua presente en los poros del suelo. En suelos francos se midió una proporción aún mayor, de aproximadamente 18.000 . [55]
Los elementos transuránicos , desde el americio hasta el fermio, incluido el curio, se encontraban de forma natural en el reactor de fisión nuclear natural de Oklo , pero ya no lo hacen. [56]
También se sospecha que el curio y otros actínidos no primordiales existen en el espectro de la estrella de Przybylski . [57]
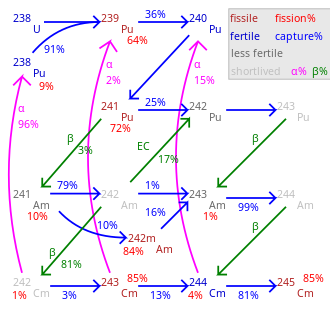
El curio se fabrica en pequeñas cantidades en los reactores nucleares , y hasta ahora sólo se han acumulado kilogramos de 242 Cm y 244 Cm, y gramos o incluso miligramos para los isótopos más pesados. De ahí el alto precio del curio, que se ha cotizado entre 160 y 185 dólares por miligramo, [13] con una estimación más reciente de 2.000 dólares por gramo para 242 Cm y 170 dólares por gramo para 244 Cm. [58] En los reactores nucleares, el curio se forma a partir de 238 U en una serie de reacciones nucleares. En la primera cadena, 238 U captura un neutrón y lo convierte en 239 U, que a través de la desintegración β se transforma en 239 Np y 239 Pu.
Una mayor captura de neutrones seguida de una desintegración β da como resultado el americio ( 241 Am), que se convierte en 242 Cm:
Para fines de investigación, el curio se obtiene irradiando no uranio sino plutonio, que se encuentra disponible en grandes cantidades a partir del combustible nuclear gastado. Se utiliza un flujo de neutrones mucho mayor para la irradiación, lo que da como resultado una cadena de reacción diferente y la formación de 244 Cm: [7]
El curio-244 alfa se desintegra a 240 Pu, pero también absorbe neutrones, de ahí una pequeña cantidad de isótopos de curio más pesados. De ellos, 247 Cm y 248 Cm son populares en la investigación científica debido a su larga vida media. Pero la tasa de producción de 247 Cm en los reactores de neutrones térmicos es baja porque es propenso a la fisión debido a los neutrones térmicos. [59] La síntesis de 250 Cm mediante captura de neutrones es poco probable debido a la corta vida media del intermedio 249 Cm (64 min), que β − se desintegra en el isótopo de berkelio 249 Bk. [59]
La cascada anterior de reacciones (n,γ) da una mezcla de diferentes isótopos de curio. Su separación post-síntesis es engorrosa, por lo que se desea una síntesis selectiva. El curio-248 es el preferido para fines de investigación debido a su larga vida media. La forma más eficaz de preparar este isótopo es mediante la desintegración α del isótopo de californio 252 Cf, que está disponible en cantidades relativamente grandes debido a su larga vida media (2,65 años). Por tanto, se producen entre 35 y 50 mg de 248 Cm al año. La reacción asociada produce 248 Cm con una pureza isotópica del 97%. [59]
Otro isótopo, el 245 Cm, puede obtenerse para investigación a partir de la desintegración α de 249 Cf; este último isótopo se produce en pequeñas cantidades a partir de la desintegración β de 249 Bk .

La mayoría de las rutinas de síntesis producen una mezcla de isótopos actínidos en forma de óxidos , de los cuales es necesario separar un determinado isótopo de curio. Un procedimiento de ejemplo podría ser disolver el combustible gastado del reactor (por ejemplo, combustible MOX ) en ácido nítrico y eliminar la mayor parte del uranio y el plutonio mediante una extracción de tipo PUREX ( Plutonio – Urano EX tracción) con fosfato de tributilo en un hidrocarburo. A continuación, los lantánidos y los actínidos restantes se separan del residuo acuoso ( refinado ) mediante una extracción basada en diamidas para dar, después de la extracción, una mezcla de actínidos y lantánidos trivalentes. Luego se extrae selectivamente un compuesto de curio mediante técnicas de cromatografía y centrifugación de varios pasos con un reactivo adecuado. [60] Recientemente se ha propuesto el complejo de bis -triazinil bipiridina como reactivo altamente selectivo para el curio. [61] La separación del curio del americio, químicamente muy similar, también se puede realizar tratando una suspensión de sus hidróxidos en bicarbonato de sodio acuoso con ozono a temperatura elevada. Tanto el americio como el curio están presentes en soluciones principalmente en el estado de valencia +3; El americio se oxida a complejos solubles de Am(IV), pero el curio permanece sin cambios y, por lo tanto, puede aislarse mediante centrifugación repetida. [62]
El curio metálico se obtiene por reducción de sus compuestos. Inicialmente se utilizó para este fin fluoruro de curio(III). La reacción se realizó en un ambiente libre de agua y oxígeno, en un aparato hecho de tantalio y tungsteno , utilizando bario elemental o litio como agentes reductores. [7] [16] [63] [64] [65]
Otra posibilidad es la reducción del óxido de curio (IV) utilizando una aleación de magnesio y zinc en una masa fundida de cloruro de magnesio y fluoruro de magnesio . [66]
El curio reacciona fácilmente con el oxígeno formando principalmente óxidos de Cm 2 O 3 y CmO 2 , [53] pero también se conoce el óxido divalente CmO. [67] El CmO 2 negro se puede obtener quemando oxalato de curio ( Cm
2(C
2oh
4)
3), nitrato ( Cm(NO
3)
3), o hidróxido en oxígeno puro. [29] [68] Al calentarse a 600–650 °C en vacío (aproximadamente 0,01 Pa ), se transforma en Cm 2 O 3 blanquecino : [29] [69]
O bien, se puede obtener Cm 2 O 3 reduciendo CmO 2 con hidrógeno molecular : [70]
También se conocen varios óxidos ternarios del tipo M(II)CmO3 , donde M representa un metal divalente, como por ejemplo el bario. [71]
Se ha informado que la oxidación térmica de trazas de hidruro de curio (CmH 2-3 ) produce una forma volátil de CmO 2 y el trióxido volátil CmO 3 , uno de los dos ejemplos conocidos del muy raro estado +6 del curio. [2] Se informó que otra especie observada se comportaba de manera similar a un supuesto tetróxido de plutonio y se caracterizó tentativamente como CmO 4 , con curio en el extremadamente raro estado +8; [72] pero nuevos experimentos parecen indicar que el CmO 4 no existe y también han puesto en duda la existencia del PuO 4 . [73]
El fluoruro de curio (III) incoloro (CmF 3 ) se puede obtener añadiendo iones fluoruro a soluciones que contienen curio (III). El fluoruro de curio (IV) tetravalente de color marrón (CmF 4 ), por otro lado, sólo se obtiene haciendo reaccionar el fluoruro de curio (III) con flúor molecular : [7]
Se conocen una serie de fluoruros ternarios de la forma A 7 Cm 6 F 31 (A = metal alcalino ). [74]
El cloruro de curio (III) incoloro (CmCl 3 ) se obtiene haciendo reaccionar hidróxido de curio (Cm(OH) 3 ) con gas cloruro de hidrógeno anhidro . Se puede convertir en otros haluros como el bromuro de curio (III) (de incoloro a verde claro) y el yoduro de curio (III) (incoloro), haciéndolo reaccionar con la sal de amoníaco del haluro correspondiente a temperaturas de ~400–450 °. C: [75]
O bien, se puede calentar el óxido de curio a ~600 °C con el ácido correspondiente (como el bromhídrico para el bromuro de curio). [76] [77] La hidrólisis en fase de vapor del cloruro de curio (III) da oxicloruro de curio: [78]
Los sulfuros, seleniuros y telururos de curio se han obtenido tratando el curio con azufre , selenio o telurio gaseosos al vacío a temperatura elevada. [79] [80] Las pnictidas de curio del tipo CmX son conocidas por su contenido en nitrógeno , fósforo , arsénico y antimonio . [7] Se pueden preparar haciendo reaccionar hidruro de curio (III) (CmH 3 ) o curio metálico con estos elementos a temperatura elevada. [81]
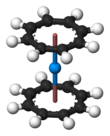
Se conocen complejos organometálicos análogos al uranoceno también para otros actínidos, como el torio, el protactinio, el neptunio, el plutonio y el americio. La teoría de los orbitales moleculares predice un complejo "curoceno" estable (η 8 -C 8 H 8 ) 2 Cm, pero aún no se ha informado experimentalmente. [82] [83]
Formación de complejos del tipo Cm(nC
3h
7-BTP)
3(BTP = 2,6-di(1,2,4-triazin-3-il)piridina), en soluciones que contienen iones nC 3 H 7 -BTP y Cm 3+ ha sido confirmado por EXAFS . Algunos de estos complejos de tipo BTP interactúan selectivamente con el curio y, por tanto, son útiles para separarlo de los lantánidos y otros actínidos. [25] [84] Los iones Cm 3+ disueltos se unen a muchos compuestos orgánicos, como el ácido hidroxámico , [85] urea , [86] fluoresceína [87] y trifosfato de adenosina . [88] Muchos de estos compuestos están relacionados con la actividad biológica de diversos microorganismos . Los complejos resultantes muestran una fuerte emisión de color amarillo anaranjado bajo excitación con luz UV, lo cual es conveniente no sólo para su detección, sino también para estudiar las interacciones entre el ion Cm 3+ y los ligandos a través de cambios en la vida media (del orden ~0,1). ms) y espectro de la fluorescencia. [26] [85] [86] [87] [88]
El curio no tiene ningún significado biológico. [89] Hay algunos informes sobre la biosorción de Cm 3+ por bacterias y arqueas , pero no hay evidencia de la incorporación de curio en ellas. [90] [91]

El curio es uno de los elementos aislables más radiactivos. Sus dos isótopos más comunes, 242 Cm y 244 Cm, son fuertes emisores alfa (energía 6 MeV); tienen vidas medias bastante cortas, 162,8 días y 18,1 años, y proporcionan hasta 120 W/g y 3 W/g de calor, respectivamente. [13] [92] [93] Por lo tanto, el curio se puede utilizar en su forma de óxido común en generadores termoeléctricos de radioisótopos como los de las naves espaciales. Esta aplicación se ha estudiado para el isótopo 244 Cm, mientras que el 242 Cm fue abandonado debido a su precio prohibitivo, alrededor de 2.000 USD/g. 243 Cm con una vida media de ~30 años y un buen rendimiento energético de ~1,6 W/g podría ser un combustible adecuado, pero produce cantidades significativas de rayos gamma y beta dañinos procedentes de productos de desintegración radiactiva. Como emisor α, 244 Cm necesita mucho menos protección contra la radiación, pero tiene una alta tasa de fisión espontánea y, por lo tanto, mucha radiación de neutrones y gamma. En comparación con un isótopo generador termoeléctrico de la competencia, como el 238 Pu, el 244 Cm emite 500 veces más neutrones, y su mayor emisión gamma requiere un escudo que es 20 veces más grueso: 2 pulgadas (51 mm) de plomo para una fuente de 1 kW, en comparación con 0,1 pulgadas (2,5 mm) para 238 Pu. Por lo tanto, este uso del curio se considera actualmente poco práctico. [58]
Un uso más prometedor de 242 Cm es para fabricar 238 Pu, un mejor radioisótopo para generadores termoeléctricos como los marcapasos cardíacos. Las rutas alternativas al 238 Pu utilizan la reacción (n,γ) de 237 Np, o bombardeo de uranio con deuterones , aunque ambas reacciones siempre producen 236 Pu como subproducto no deseado ya que este último decae a 232 U con una fuerte emisión gamma. [94] El curio es un material de partida común para fabricar elementos transuránicos superiores y superpesados . Por lo tanto, bombardear 248 Cm con neón ( 22 Ne), magnesio ( 26 Mg) o calcio ( 48 Ca ) produce isótopos de seaborgio ( 265 Sg), hasio ( 269 Hs y 270 Hs) y hígadomorio ( 292 Lv, 293 Lv) . , y posiblemente 294 Lv). [95] El californio se descubrió cuando se irradió un objetivo de curio-242 del tamaño de un microgramo con partículas alfa de 35 MeV utilizando el ciclotrón de 60 pulgadas (150 cm) en Berkeley:
En este experimento sólo se produjeron unos 5.000 átomos de californio. [96]
Los isótopos de curio de masa impar 243 Cm, 245 Cm y 247 Cm son todos altamente fisibles y pueden liberar energía adicional en un reactor nuclear de espectro térmico . Todos los isótopos de curio son fisionables en reactores de neutrones rápidos. Este es uno de los motivos de la separación y transmutación menor de actínidos en el ciclo del combustible nuclear , lo que ayuda a reducir la radiotoxicidad a largo plazo del combustible nuclear usado o gastado .

La aplicación más práctica de 244 Cm, aunque bastante limitada en volumen total, es como fuente de partículas α en espectrómetros de rayos X de partículas alfa (APXS). Estos instrumentos fueron instalados en el Sojourner , Mars , Mars 96 , Mars Exploration Rovers y Philae comet lander , [97] así como en el Mars Science Laboratory para analizar la composición y estructura de las rocas en la superficie del planeta Marte . [98] APXS también se utilizó en las sondas lunares Surveyor 5–7 , pero con una fuente de 242 cm. [55] [99] [100]
Una elaborada configuración APXS tiene un cabezal sensor que contiene seis fuentes de curio con una tasa de desintegración total de varias decenas de milicurios (aproximadamente un gigabecquerel ). Las fuentes se coliman en una muestra y se analizan los espectros de energía de las partículas alfa y los protones dispersos de la muestra (el análisis de protones se realiza sólo en algunos espectrómetros). Estos espectros contienen información cuantitativa sobre todos los elementos principales de la muestra, excepto hidrógeno, helio y litio. [101]
Debido a su radioactividad, el curio y sus compuestos deben manipularse en laboratorios apropiados y bajo disposiciones especiales. Mientras que el propio curio emite principalmente partículas α que son absorbidas por finas capas de materiales comunes, algunos de sus productos de desintegración emiten fracciones importantes de rayos beta y gamma, que requieren una protección más elaborada. [53] Si se consume, el curio se excreta en unos pocos días y sólo el 0,05% se absorbe en la sangre. De ahí, ~45% va al hígado , 45% a los huesos y el 10% restante se excreta. En los huesos, el curio se acumula en el interior de las interfaces con la médula ósea y no se redistribuye significativamente con el tiempo; su radiación destruye la médula ósea y, por tanto, detiene la creación de glóbulos rojos . La vida media biológica del curio es de unos 20 años en el hígado y de 50 años en los huesos. [53] [55] El curio se absorbe en el cuerpo mucho más fuertemente mediante inhalación, y la dosis total permitida de 244 Cm en forma soluble es de 0,3 μ Ci . [13] La inyección intravenosa de soluciones que contienen 242 Cm y 244 Cm a ratas aumentó la incidencia de tumores óseos , y la inhalación promovió el cáncer de pulmón y de hígado . [53]
Los isótopos de curio están inevitablemente presentes en el combustible nuclear gastado (unos 20 g/tonelada). [102] Los isótopos 245 Cm – 248 Cm tienen tiempos de desintegración de miles de años y deben eliminarse para neutralizar el combustible que se va a eliminar. [103] Este procedimiento implica varios pasos, donde primero se separa el curio y luego se convierte mediante bombardeo de neutrones en reactores especiales en nucleidos de vida corta. Este procedimiento, la transmutación nuclear , aunque está bien documentado para otros elementos, todavía se está desarrollando para el curio. [25]
{{cite web}}: Mantenimiento CS1: nombres numéricos: lista de autores ( enlace ){{cite web}}: Mantenimiento CS1: copia archivada como título ( enlace ) Mantenimiento CS1: bot: estado de la URL original desconocido ( enlace )