
Un plásmido es una pequeña molécula de ADN extracromosómico dentro de una célula que está físicamente separada del ADN cromosómico y puede replicarse de forma independiente. Se encuentran más comúnmente como pequeñas moléculas circulares de ADN de doble cadena en las bacterias ; sin embargo, los plásmidos a veces están presentes en arqueas y organismos eucariotas . [1] [2] Los plásmidos a menudo portan genes útiles, como los de resistencia a los antibióticos . Mientras que los cromosomas son grandes y contienen toda la información genética esencial para vivir en condiciones normales, los plásmidos suelen ser muy pequeños y contienen genes adicionales para circunstancias especiales.
Los plásmidos artificiales se utilizan ampliamente como vectores en la clonación molecular y sirven para impulsar la replicación de secuencias de ADN recombinante dentro de los organismos huéspedes. En el laboratorio, los plásmidos pueden introducirse en una célula mediante transformación . Los plásmidos sintéticos están disponibles para su adquisición a través de Internet. [3] [4] [5]
Los plásmidos se consideran replicones , unidades de ADN capaces de replicarse de forma autónoma dentro de un huésped adecuado. Sin embargo, los plásmidos, al igual que los virus , generalmente no se clasifican como vida . [6] Los plásmidos se transmiten de una bacteria a otra (incluso de otra especie) principalmente mediante conjugación . [7] Esta transferencia de material genético de huésped a huésped es un mecanismo de transferencia horizontal de genes , y los plásmidos se consideran parte del mobiloma . A diferencia de los virus, que encierran su material genético en una capa proteica protectora llamada cápside , los plásmidos son ADN "desnudo" y no codifican los genes necesarios para encerrar el material genético para su transferencia a un nuevo huésped; sin embargo, algunas clases de plásmidos codifican el pilus "sexual" conjugativo necesario para su propia transferencia. Los plásmidos varían en tamaño desde 1 hasta más de 400 k pb , [8] y el número de plásmidos idénticos en una sola célula puede variar desde uno hasta miles.
El término plásmido fue introducido en 1952 por el biólogo molecular estadounidense Joshua Lederberg para referirse a "cualquier determinante hereditario extracromosómico". [9] El uso inicial del término incluía cualquier material genético bacteriano que exista extracromosómicamente durante al menos parte de su ciclo de replicación, pero debido a que esa descripción incluye virus bacterianos, la noción de plásmido se perfeccionó con el tiempo para referirse a elementos genéticos que se reproducen de forma autónoma. [10] Más tarde, en 1968, se decidió que el término plásmido debería adoptarse como término para el elemento genético extracromosómico, [11] y para distinguirlo de los virus, la definición se limitó a elementos genéticos que existen exclusiva o predominantemente fuera del cromosoma y puede replicarse de forma autónoma. [10]

Para que los plásmidos se repliquen de forma independiente dentro de una célula, deben poseer un tramo de ADN que pueda actuar como origen de replicación . La unidad autorreplicante, en este caso el plásmido, se denomina replicón . Un replicón bacteriano típico puede constar de varios elementos, como el gen de la proteína de iniciación de replicación (Rep) específica del plásmido, unidades repetidas llamadas iterones , cajas de ADNA y una región adyacente rica en AT. [10] Los plásmidos más pequeños utilizan las enzimas replicativas del huésped para hacer copias de sí mismos, mientras que los plásmidos más grandes pueden portar genes específicos para la replicación de esos plásmidos. Algunos tipos de plásmidos también pueden insertarse en el cromosoma del huésped, y estos plásmidos integrativos a veces se denominan episomas en procariotas . [12]
Los plásmidos casi siempre portan al menos un gen. Muchos de los genes transportados por un plásmido son beneficiosos para las células huésped, por ejemplo: permiten que la célula huésped sobreviva en un entorno que de otro modo sería letal o restrictivo para el crecimiento. Algunos de estos genes codifican rasgos de resistencia a los antibióticos o a metales pesados, mientras que otros pueden producir factores de virulencia que permiten a una bacteria colonizar un huésped y superar sus defensas o tener funciones metabólicas específicas que le permiten a la bacteria utilizar un nutriente particular, incluido el capacidad de degradar compuestos orgánicos recalcitrantes o tóxicos. [13] Los plásmidos también pueden proporcionar a las bacterias la capacidad de fijar nitrógeno . Sin embargo, algunos plásmidos no tienen ningún efecto observable sobre el fenotipo de la célula huésped o no se puede determinar su beneficio para las células huésped, y estos plásmidos se denominan plásmidos crípticos. [14]
Los plásmidos naturales varían mucho en sus propiedades físicas. Su tamaño puede variar desde miniplásmidos muy pequeños de menos de 1 kilopar de bases (kpb) hasta megaplásmidos muy grandes de varios pares de megabases (Mbp). En el extremo superior, poco se diferencia entre un megaplásmido y un minicromosoma . Los plásmidos son generalmente circulares, pero también se conocen ejemplos de plásmidos lineales. Estos plásmidos lineales requieren mecanismos especializados para replicar sus extremos. [10]
Los plásmidos pueden estar presentes en una célula individual en número variable, desde uno hasta varios cientos. El número normal de copias de plásmido que se pueden encontrar en una sola célula se llama número de copias de plásmido y está determinado por cómo se regula el inicio de la replicación y el tamaño de la molécula. Los plásmidos más grandes tienden a tener números de copias más bajos. [12] Los plásmidos con un número de copias bajo que existen sólo como una o unas pocas copias en cada bacteria corren el riesgo de perderse, tras la división celular , en una de las bacterias segregantes. Estos plásmidos de copia única tienen sistemas que intentan distribuir activamente una copia a ambas células hijas. Estos sistemas, que incluyen el sistema parABS y el sistema parMRC , a menudo se denominan sistema de partición o función de partición de un plásmido. [15]
Los plásmidos de forma lineal son desconocidos entre los fitopatógenos con una excepción, Rhodococcus fascians . [dieciséis]

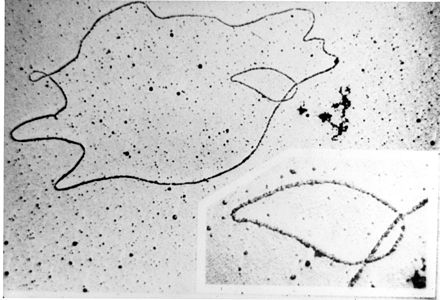

Los plásmidos se pueden clasificar de varias maneras. Los plásmidos se pueden clasificar ampliamente en plásmidos conjugativos y plásmidos no conjugativos. Los plásmidos conjugativos contienen un conjunto de genes de transferencia que promueven la conjugación sexual entre diferentes células. [12] En el complejo proceso de conjugación , los plásmidos pueden transferirse de una bacteria a otra a través de pili sexuales codificados por algunos de los genes de transferencia (ver figura). [17] Los plásmidos no conjugativos son incapaces de iniciar la conjugación, por lo que sólo pueden transferirse con la ayuda de plásmidos conjugativos. Una clase intermedia de plásmidos es movilizable y porta sólo un subconjunto de los genes necesarios para la transferencia. Pueden parasitar un plásmido conjugativo, transfiriendo a alta frecuencia sólo en su presencia. [ cita necesaria ]
Los plásmidos también se pueden clasificar en grupos de incompatibilidad. Un microbio puede albergar diferentes tipos de plásmidos, pero diferentes plásmidos sólo pueden existir en una única célula bacteriana si son compatibles. Si dos plásmidos no son compatibles, uno u otro se perderá rápidamente de la célula. Por lo tanto, se pueden asignar diferentes plásmidos a diferentes grupos de incompatibilidad dependiendo de si pueden coexistir juntos. Los plásmidos incompatibles (que pertenecen al mismo grupo de incompatibilidad) normalmente comparten los mismos mecanismos de replicación o partición y, por lo tanto, no pueden mantenerse juntos en una sola célula. [18] [19]
Otra forma de clasificar los plásmidos es por función. Hay cinco clases principales:
Los plásmidos pueden pertenecer a más de uno de estos grupos funcionales.
Aunque la mayoría de los plásmidos son moléculas de ADN de doble cadena, algunos consisten en ADN monocatenario o predominantemente ARN bicatenario . Los plásmidos de ARN son replicones de ARN lineales extracromosómicos no infecciosos, tanto encapsidados como no encapsidados, que se han encontrado en hongos y diversas plantas, desde algas hasta plantas terrestres. Sin embargo, en muchos casos puede resultar difícil o imposible distinguir claramente los plásmidos de ARN de los virus de ARN y otros ARN infecciosos. [20]
Los cromidos son elementos que existen en el límite entre un cromosoma y un plásmido y se encuentran en aproximadamente el 10% de las especies bacterianas secuenciadas en 2009. Estos elementos portan genes centrales y tienen un uso de codones similar al del cromosoma, pero utilizan un mecanismo de replicación de tipo plásmido como como el número de copia bajo RepABC. Como resultado, en el pasado se han clasificado de diversas formas como minicromosomas o megaplásmidos. [21] En Vibrio , la bacteria sincroniza la replicación del cromosoma y el cromido mediante una relación de tamaño del genoma conservada. [22]
Los plásmidos construidos artificialmente pueden usarse como vectores en ingeniería genética . Estos plásmidos sirven como herramientas importantes en los laboratorios de genética y biotecnología, donde se utilizan comúnmente para clonar y amplificar (hacer muchas copias) o expresar genes particulares. [23] Hay una amplia variedad de plásmidos disponibles comercialmente para tales usos. El gen que se va a replicar normalmente se inserta en un plásmido que normalmente contiene una serie de características para su uso. Estos incluyen un gen que confiere resistencia a antibióticos particulares ( la ampicilina se usa con mayor frecuencia para cepas bacterianas), un origen de replicación para permitir que las células bacterianas repliquen el ADN plasmídico y un sitio adecuado para la clonación (denominado sitio de clonación múltiple). ).
La inestabilidad estructural del ADN se puede definir como una serie de eventos espontáneos que culminan en un reordenamiento, pérdida o ganancia imprevista de material genético. Estos eventos frecuentemente son desencadenados por la transposición de elementos móviles o por la presencia de elementos inestables como estructuras no canónicas (no B). Las regiones accesorias pertenecientes a la columna vertebral bacteriana pueden participar en una amplia gama de fenómenos de inestabilidad estructural. Los catalizadores de inestabilidad genética bien conocidos incluyen repeticiones directas, invertidas y en tándem, que se sabe que son notorias en una gran cantidad de vectores de expresión y clonación disponibles comercialmente. [24] Las secuencias de inserción también pueden afectar gravemente la función y el rendimiento del plásmido, al provocar deleciones y reordenamientos, activación, regulación negativa o inactivación de la expresión de genes vecinos . [25] Por lo tanto, la reducción o eliminación completa de secuencias principales no codificantes extrañas reduciría significativamente la propensión a que se produzcan tales eventos y, en consecuencia, el potencial recombinógeno general del plásmido. [26] [27]
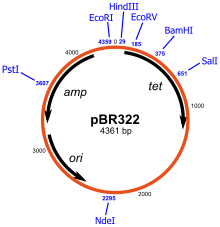
Los plásmidos son los vectores de clonación bacteriana más utilizados. [28] Estos vectores de clonación contienen un sitio que permite insertar fragmentos de ADN, por ejemplo, un sitio de clonación múltiple o polienlazador que tiene varios sitios de restricción comúnmente utilizados a los que se pueden ligar fragmentos de ADN . Una vez insertado el gen de interés, los plásmidos se introducen en las bacterias mediante un proceso llamado transformación . Estos plásmidos contienen un marcador seleccionable , generalmente un gen de resistencia a los antibióticos, que confiere a las bacterias la capacidad de sobrevivir y proliferar en un medio de crecimiento selectivo que contiene los antibióticos particulares. Las células después de la transformación se exponen a los medios selectivos y sólo las células que contienen el plásmido pueden sobrevivir. De esta forma, los antibióticos actúan como un filtro para seleccionar únicamente las bacterias que contienen el ADN plasmídico. El vector también puede contener otros genes marcadores o genes indicadores para facilitar la selección de plásmidos con inserciones clonadas. Las bacterias que contienen el plásmido pueden luego cultivarse en grandes cantidades, recolectarse y luego aislarse el plásmido de interés utilizando diversos métodos de preparación de plásmidos .
Normalmente se utiliza un vector de clonación de plásmido para clonar fragmentos de ADN de hasta 15 kpb . [29] Para clonar longitudes más largas de ADN, se utilizan fagos lambda con genes de lisogenia eliminados, cósmidos , cromosomas artificiales bacterianos o cromosomas artificiales de levadura .
Otro uso importante de los plásmidos es producir grandes cantidades de proteínas. En este caso, los investigadores cultivan bacterias que contienen un plásmido que alberga el gen de interés. Así como la bacteria produce proteínas para conferirle resistencia a los antibióticos, también se le puede inducir a producir grandes cantidades de proteínas a partir del gen insertado. Esta es una manera fácil y barata de producir en masa la proteína que el gen codifica, por ejemplo, la insulina .
Los plásmidos también se pueden utilizar para la transferencia de genes como tratamiento potencial en la terapia génica para que puedan expresar la proteína que falta en las células. Algunas formas de terapia génica requieren la inserción de genes terapéuticos en sitios cromosómicos objetivo preseleccionados dentro del genoma humano . Los vectores plasmídicos son uno de los muchos enfoques que podrían usarse para este propósito. Las nucleasas con dedos de zinc (ZFN) ofrecen una forma de provocar una rotura de doble cadena específica del sitio en el genoma del ADN y provocar una recombinación homóloga . Los plásmidos que codifican ZFN podrían ayudar a administrar un gen terapéutico a un sitio específico para evitar el daño celular , las mutaciones que causan cáncer o una respuesta inmune . [30]
Históricamente, los plásmidos se utilizaron para diseñar genéticamente células madre embrionarias de ratas para crear modelos de enfermedades genéticas de ratas. La eficacia limitada de las técnicas basadas en plásmidos impidió su uso en la creación de modelos de células humanas más precisos. Sin embargo, los avances en las técnicas de recombinación de virus adenoasociados y las nucleasas con dedos de zinc han permitido la creación de una nueva generación de modelos isogénicos de enfermedades humanas .
El término episoma fue introducido por François Jacob y Élie Wollman en 1958 para referirse al material genético extracromosómico que puede replicarse de forma autónoma o integrarse en el cromosoma. [31] [32] Sin embargo, desde que se introdujo el término, su uso ha cambiado, ya que plásmido se ha convertido en el término preferido para replicar de forma autónoma el ADN extracromosómico. En un simposio celebrado en Londres en 1968, algunos participantes sugirieron que se abandonara el término episoma , aunque otros continuaron utilizándolo con un cambio de significado. [33] [34]
Hoy en día, algunos autores utilizan episoma en el contexto de procariotas para referirse a un plásmido que es capaz de integrarse en el cromosoma. Los plásmidos integrativos pueden replicarse y mantenerse de manera estable en una célula a lo largo de múltiples generaciones, pero en algún momento existirán como una molécula de plásmido independiente. [35] En el contexto de los eucariotas, el término episoma se utiliza para referirse a una molécula de ADN circular cerrada extracromosómica no integrada que puede replicarse en el núcleo. [36] [37] Los virus son los ejemplos más comunes de esto, como los herpesvirus , los adenovirus y los poliomavirus , pero algunos son plásmidos. Otros ejemplos incluyen fragmentos cromosómicos aberrantes, como los cromosomas diminutos dobles , que pueden surgir durante amplificaciones genéticas artificiales o en procesos patológicos (p. ej., transformación de células cancerosas). Los episomas en eucariotas se comportan de manera similar a los plásmidos en procariotas en el sentido de que el ADN se mantiene y replica de manera estable con la célula huésped. También pueden aparecer episomas virales citoplasmáticos (como en las infecciones por poxvirus ). Algunos episomas, como los herpesvirus, se replican en un mecanismo de círculo rodante , similar a los bacteriófagos (virus de fagos bacterianos). Otros se replican mediante un mecanismo de replicación bidireccional ( plásmidos tipo Theta ). En cualquier caso, los episomas permanecen físicamente separados de los cromosomas de la célula huésped. Varios virus cancerosos, incluido el virus de Epstein-Barr y el herpesvirus asociado al sarcoma de Kaposi , se mantienen como episomas latentes y cromosómicamente distintos en las células cancerosas, donde los virus expresan oncogenes que promueven la proliferación de células cancerosas. En los cánceres, estos episomas se replican pasivamente junto con los cromosomas del huésped cuando la célula se divide. Cuando estos episomas virales inician la replicación lítica para generar múltiples partículas virales, generalmente activan mecanismos de defensa de la inmunidad celular innata que matan a la célula huésped.
Algunos plásmidos o huéspedes microbianos incluyen un sistema de adicción o sistema de muerte postsgregacional (PSK), como el sistema hok/sok (muerte del huésped/supresor de la muerte) del plásmido R1 en Escherichia coli . [38] Esta variante produce tanto un veneno de larga duración como un antídoto de corta duración . En la literatura se describieron varios tipos de sistemas de adicción a plásmidos (toxina/antitoxina, basados en el metabolismo, sistemas ORT) [39] y se utilizaron en aplicaciones biotécnicas (fermentación) o biomédicas (terapia con vacunas). Las células hijas que retienen una copia del plásmido sobreviven, mientras que una célula hija que no hereda el plásmido muere o sufre una tasa de crecimiento reducida debido al veneno persistente de la célula madre. Por último, se podría mejorar la productividad general.
Por el contrario, los plásmidos utilizados en biotecnología, como pUC18, pBR322 y vectores derivados, casi nunca contienen sistemas de adicción a toxina-antitoxina y, por lo tanto, deben mantenerse bajo presión antibiótica para evitar la pérdida de plásmidos.
Las levaduras albergan de forma natural varios plásmidos. Entre ellos destacan los plásmidos de 2 μm (pequeños plásmidos circulares que se utilizan a menudo para la ingeniería genética de levaduras) y los plásmidos pGKL lineales de Kluyveromyces lactis , que son responsables de los fenotipos asesinos. [40]
Otros tipos de plásmidos suelen estar relacionados con vectores de clonación de levaduras que incluyen:
Las mitocondrias de muchas plantas superiores contienen moléculas de ADN circulares o lineales extracromosómicas autorreplicantes que se han considerado plásmidos. Estos pueden tener un tamaño de entre 0,7 kb y 20 kb. Los plásmidos generalmente se han clasificado en dos categorías: circulares y lineales. [41] Los plásmidos circulares han sido aislados y encontrados en muchas plantas diferentes, siendo los de Vicia faba y Chenopodium album los más estudiados y cuyo mecanismo de replicación se conoce. Los plásmidos circulares pueden replicarse usando el modelo θ de replicación (como en Vicia faba ) y mediante replicación de círculo rodante (como en C.album ). [42] Se han identificado plásmidos lineales en algunas especies de plantas como Beta vulgaris , Brassica napus , Zea mays , etc., pero son más raros que sus homólogos circulares.
La función y el origen de estos plásmidos siguen siendo en gran medida desconocidos. Se ha sugerido que los plásmidos circulares comparten un ancestro común; algunos genes del plásmido mitocondrial tienen contrapartes en el ADN nuclear, lo que sugiere un intercambio entre compartimentos. Mientras tanto, los plásmidos lineales comparten similitudes estructurales, como los invertrones con ADN viral y los plásmidos fúngicos, al igual que los plásmidos fúngicos, también tienen un bajo contenido de GC. Estas observaciones han llevado a algunos a plantear la hipótesis de que estos plásmidos lineales tienen orígenes virales o han terminado en las mitocondrias de las plantas. mediante transferencia horizontal de genes de hongos patógenos. [41] [43]
Los plásmidos se utilizan a menudo para purificar una secuencia específica, ya que pueden purificarse fácilmente del resto del genoma. Para su uso como vectores y para la clonación molecular , a menudo es necesario aislar los plásmidos.
Existen varios métodos para aislar el ADN plasmídico de bacterias, desde el miniprep hasta el maxiprep o el Bulkprep . [23] El primero se puede utilizar para descubrir rápidamente si el plásmido es correcto en cualquiera de varios clones bacterianos. El rendimiento es una pequeña cantidad de ADN plasmídico impuro, que es suficiente para el análisis mediante digestión de restricción y para algunas técnicas de clonación.
En este último caso, se cultivan volúmenes mucho mayores de suspensión bacteriana a partir de los cuales se puede realizar una maxipreparación. En esencia, se trata de una minipreparación ampliada seguida de una purificación adicional. Esto da como resultado cantidades relativamente grandes (varios cientos de microgramos) de ADN plasmídico muy puro.
Se han creado muchos kits comerciales para realizar la extracción de plásmidos en diversas escalas, pureza y niveles de automatización.
El ADN plasmídico puede aparecer en una de cinco conformaciones que (para un tamaño determinado) corren a diferentes velocidades en un gel durante la electroforesis . Las conformaciones se enumeran a continuación en orden de movilidad electroforética (velocidad para un voltaje aplicado determinado) de más lenta a más rápida:
La tasa de migración de pequeños fragmentos lineales es directamente proporcional al voltaje aplicado a bajos voltajes. A voltajes más altos, los fragmentos más grandes migran a velocidades cada vez mayores pero diferentes. Por tanto, la resolución de un gel disminuye al aumentar el voltaje.
A un voltaje bajo específico, la tasa de migración de pequeños fragmentos lineales de ADN es función de su longitud. Los fragmentos lineales grandes (más de 20 kb aproximadamente) migran a una velocidad fija determinada independientemente de su longitud. Esto se debe a que las moléculas "respiran", y la mayor parte de la molécula sigue el extremo principal a través de la matriz del gel. Los resúmenes de restricción se utilizan con frecuencia para analizar plásmidos purificados. Estas enzimas rompen específicamente el ADN en ciertas secuencias cortas. "Los fragmentos lineales resultantes forman "bandas" después de la electroforesis en gel . Es posible purificar ciertos fragmentos cortando las bandas del gel y disolviendo el gel para liberar los fragmentos de ADN.
Debido a su conformación estrecha, el ADN superenrollado migra más rápido a través de un gel que el ADN lineal o circular abierto.
El uso de plásmidos como técnica en biología molecular está respaldado por software bioinformático . Estos programas registran la secuencia de ADN de los vectores plasmídicos, ayudan a predecir los sitios de corte de las enzimas de restricción y a planificar manipulaciones. Ejemplos de paquetes de software que manejan mapas de plásmidos son ApE, Clone Manager , GeneConstructionKit, Geneious, Genome Compiler , LabGenius, Lasergene, MacVector , pDraw32, Serial Cloner, VectorFriends, Vector NTI y WebDSV. Estas piezas de software ayudan a realizar experimentos completos in silico antes de realizar experimentos húmedos. [44]
A lo largo de los años se han creado muchos plásmidos y los investigadores los han distribuido a bases de datos de plásmidos como las organizaciones sin fines de lucro Addgene y BCCM/LMBP. Se pueden buscar y solicitar plásmidos de esas bases de datos para investigaciones. Los investigadores también suelen cargar secuencias de plásmidos en la base de datos del NCBI, desde donde se pueden recuperar secuencias de plásmidos específicos.
{{cite journal}}: Mantenimiento CS1: varios nombres: lista de autores ( enlace )