

Los carbonilos metálicos son complejos de coordinación de metales de transición con ligandos de monóxido de carbono . Los carbonilos metálicos son útiles en síntesis orgánica y como catalizadores o precursores de catalizadores en catálisis homogénea , como la hidroformilación y la química de Reppe . En el proceso Mond , se utiliza níquel tetracarbonilo para producir níquel puro . En química organometálica , los carbonilos metálicos sirven como precursores para la preparación de otros complejos organometálicos.
Los carbonilos metálicos son tóxicos por contacto con la piel, inhalación o ingestión, en parte debido a su capacidad para carbonilar la hemoglobina para dar carboxihemoglobina , lo que impide la unión del oxígeno . [1]
La nomenclatura de los carbonilos metálicos depende de la carga del complejo, el número y tipo de átomos centrales, y el número y tipo de ligandos y sus modos de unión. Se presentan como complejos neutros, como cationes carbonilo metálicos cargados positivamente o como carbonilatos metálicos cargados negativamente . El ligando de monóxido de carbono puede estar unido terminalmente a un único átomo metálico o formando un puente con dos o más átomos metálicos. Estos complejos pueden ser homolépticos y contener sólo ligandos de CO, como el tetracarbonilo de níquel (Ni(CO) 4 ), pero más comúnmente los carbonilos metálicos son heterolépticos y contienen una mezcla de ligandos. [ cita necesaria ]
Los carbonilos metálicos mononucleares contienen solo un átomo metálico como átomo central. Excepto el vanadio hexacarbonilo , sólo los metales con número atómico par, como el cromo , el hierro , el níquel y sus homólogos, forman complejos mononucleares neutros. Los carbonilos metálicos polinucleares se forman a partir de metales con números atómicos impares y contienen un enlace metal-metal . [2] Los complejos con diferentes metales pero solo un tipo de ligando se llaman isolépticos. [2]
El monóxido de carbono tiene distintos modos de unión en los carbonilos metálicos. Se diferencian en términos de su hapticidad , denotada η , y su modo de puente. En los complejos η 2 -CO, tanto el carbono como el oxígeno están unidos al metal. Lo más habitual es que sólo se enlace carbono, en cuyo caso no se menciona la hapticidad. [3]
El ligando carbonilo participa en una amplia gama de modos de enlace en grupos y dímeros de carbonilo metálico. En el modo de puente más común, denominado μ 2 o simplemente μ , el ligando de CO une un par de metales. Este modo de enlace se observa en los carbonilos metálicos comúnmente disponibles: Co 2 (CO) 8 , Fe 2 (CO) 9 , Fe 3 (CO) 12 y Co 4 (CO) 12 . [1] [4] En ciertos grupos de nuclearidad superior, el CO forma un puente entre tres o incluso cuatro metales. Estos ligandos se denominan μ 3 -CO y μ 4 -CO. Menos comunes son los modos de enlace en los que tanto C como O se unen al metal, como μ 3 η 2 . [ cita necesaria ]

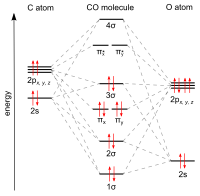
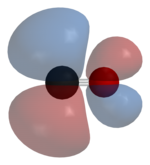
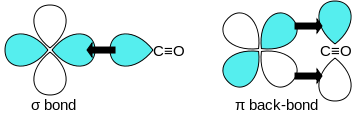
El monóxido de carbono se une a metales de transición mediante " uniones posteriores sinérgicas pi* ". El enlace MC tiene tres componentes, dando lugar a un triple enlace parcial. Un enlace sigma (σ) surge de la superposición del par de electrones con hibridación sp no enlazante (o débilmente antienlazante) en el carbono con una mezcla de orbitales d , s y p en el metal. Un par de enlaces pi (π) surge de la superposición de orbitales d llenos en el metal con un par de orbitales antienlazantes π* que se proyectan desde el átomo de carbono del CO. El último tipo de unión requiere que el metal tenga electrones d , y que el metal se encuentra en un estado de oxidación relativamente bajo (0 o +1), lo que hace que la retrodonación de densidad electrónica sea favorable. A medida que los electrones del metal llenan el orbital antienlazante π del CO, debilitan el enlace carbono-oxígeno en comparación con el monóxido de carbono libre, mientras que el enlace metal-carbono se fortalece. Debido al carácter de enlace múltiple del enlace M-CO, la distancia entre el metal y el átomo de carbono es relativamente corta, a menudo menos de 1,8 Å, aproximadamente 0,2 Å más corta que un enlace metal- alquilo . La distancia M-CO y MC-O son sensibles a otros ligandos del metal. Ilustrativos de estos efectos son los siguientes datos para las distancias Mo-C y CO en Mo(CO) 6 y Mo(CO) 3 (4-metilpiridina) 3 : 2,06 frente a 1,90 y 1,11 frente a 1,18 Å. [5]
La espectroscopia infrarroja es una sonda sensible para detectar la presencia de ligandos carbonilo puente. Para compuestos con ligandos de CO de doble puente, denominados μ 2 -CO o, a menudo, simplemente μ -CO, la frecuencia de estiramiento del enlace ν CO generalmente se desplaza entre 100 y 200 cm −1 para obtener una energía más baja en comparación con las firmas del CO terminal, que están en la región 1800 cm −1 . Las bandas para ligandos de CO que cubren la cara ( μ 3 ) aparecen a energías aún más bajas. Además de los modos de puente simétricos, se puede encontrar que el CO forma un puente asimétricamente o mediante donación desde un orbital d metálico al orbital π* del CO. [6] [7] [8] El aumento del enlace π debido a la retrodonación de múltiples centros metálicos dan como resultado un mayor debilitamiento del enlace C-O. [ cita necesaria ]
La mayoría de los complejos carbonílicos mononucleares son líquidos o sólidos volátiles incoloros o de color amarillo pálido que son inflamables y tóxicos. [9] El hexacarbonilo de vanadio , un carbonilo metálico de 17 electrones excepcionalmente estable, es un sólido negro azulado. [1] Los carbonilos dimetálicos y polimetálicos tienden a tener colores más intensos. El triiron dodecacarbonilo (Fe 3 (CO) 12 ) forma cristales de color verde intenso. Los carbonilos metálicos cristalinos suelen ser sublimables en el vacío, aunque este proceso suele ir acompañado de degradación. Los carbonilos metálicos son solubles en disolventes orgánicos polares y no polares como el benceno , el éter dietílico , la acetona , el ácido acético glacial y el tetracloruro de carbono . Algunas sales de carbonilos metálicos catiónicos y aniónicos son solubles en agua o alcoholes inferiores. [10]

Además de la cristalografía de rayos X , otras técnicas analíticas importantes para la caracterización de carbonilos metálicos son la espectroscopia infrarroja y la espectroscopia de 13 C NMR . Estas dos técnicas proporcionan información estructural en dos escalas de tiempo muy diferentes. Los modos de vibración activos por infrarrojos , como las vibraciones de estiramiento de CO, suelen ser rápidos en comparación con los procesos intramoleculares, mientras que las transiciones de RMN ocurren a frecuencias más bajas y, por lo tanto, muestrean estructuras en una escala de tiempo que, resulta, es comparable a la velocidad del ligando intramolecular. procesos de intercambio. Los datos de RMN proporcionan información sobre "estructuras promediadas en el tiempo", mientras que los IR son una "instantánea" instantánea. [11] Como ilustración de las diferentes escalas de tiempo, la investigación del dicobalto octacarbonilo (Co 2 (CO) 8 ) mediante espectroscopia infrarroja proporciona bandas de 13 ν CO , mucho más de lo esperado para un solo compuesto. Esta complejidad refleja la presencia de isómeros con y sin ligandos de CO puente. El espectro de 13 C NMR de la misma sustancia exhibe solo una señal con un desplazamiento químico de 204 ppm. Esta simplicidad indica que los isómeros se interconvierten rápidamente (en la escala de tiempo de RMN). [ cita necesaria ]
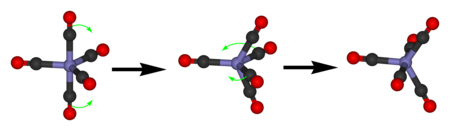
El pentacarbonilo de hierro exhibe solo una única señal de 13 C NMR debido al rápido intercambio de los ligandos de CO axial y ecuatorial por la pseudorotación de Berry . [ cita necesaria ]

Una técnica importante para caracterizar carbonilos metálicos es la espectroscopia infrarroja . [13] La vibración C – O, típicamente denotada como ν CO , ocurre a 2143 cm −1 para el gas monóxido de carbono. Las energías de la banda ν CO para los carbonilos metálicos se correlacionan con la fuerza del enlace carbono-oxígeno e inversamente con la fuerza del enlace π entre el metal y el carbono. La basicidad π del centro metálico depende de muchos factores; En la serie isoelectrónica ( titanio a hierro ) en la parte inferior de esta sección, los hexacarbonilos muestran un enlace π decreciente a medida que se aumenta (se hace más positiva) la carga del metal. Los ligandos π-básicos aumentan la densidad de los electrones π en el metal y la unión mejorada reduce el ν CO . El parámetro electrónico de Tolman utiliza el fragmento Ni(CO) 3 para ordenar ligandos según sus capacidades de donación de π. [14] [15]
El número de modos vibratorios de un complejo de carbonilo metálico puede determinarse mediante la teoría de grupos . Sólo los modos vibratorios que se transforman cuando el operador del dipolo eléctrico tendrán productos directos distintos de cero y se observarán. De este modo se puede predecir el número de transiciones IR observables (pero no sus energías). [16] [17] [18] Por ejemplo, los ligandos CO de complejos octaédricos, como Cr(CO) 6 , se transforman como 1g , por ejemplo , y t 1u , pero sólo el modo t 1u ( estiramiento antisimétrico del ligandos de carbonilo apicales) está permitido por IR. Por lo tanto, solo se observa una única banda de ν CO en los espectros IR de los hexacarbonilos metálicos octaédricos. Los espectros de complejos de menor simetría son más complejos. Por ejemplo, el espectro IR de Fe 2 (CO) 9 muestra bandas de CO en 2082, 2019 y 1829 cm −1 . En la tabla se muestra el número de modos de vibración observables por infrarrojos para algunos carbonilos metálicos. Se encuentran disponibles tabulaciones exhaustivas. [13] Estas reglas se aplican a los carbonilos metálicos en solución o en fase gaseosa. Los disolventes de baja polaridad son ideales para alta resolución. Para mediciones en muestras sólidas de carbonilos metálicos, el número de bandas puede aumentar debido en parte a la simetría del sitio. [19]
Los carbonilos metálicos se caracterizan a menudo mediante espectroscopia de RMN de 13 C. Para mejorar la sensibilidad de esta técnica, los complejos suelen enriquecerse con 13 CO. El rango de desplazamiento químico típico para ligandos unidos terminalmente es de 150 a 220 ppm. Los ligandos puente resuenan entre 230 y 280 ppm. [1] Las señales de 13 C se desplazan hacia campos más altos con un número atómico creciente del metal central.
La espectroscopia de RMN se puede utilizar para la determinación experimental de la fluxionalidad . [26]
La energía de activación de los procesos de intercambio de ligandos puede determinarse mediante la dependencia de la temperatura del ensanchamiento de la línea. [27]
La espectrometría de masas proporciona información sobre la estructura y composición de los complejos. Los espectros de los policarbonilos metálicos suelen ser fácilmente interpretables, porque el proceso de fragmentación dominante es la pérdida de ligandos carbonilo ( m / z = 28).
La ionización electrónica es la técnica más común para caracterizar los carbonilos metálicos neutros. Los carbonilos metálicos neutros se pueden convertir en especies cargadas mediante derivatización , lo que permite el uso de ionización por electropulverización (ESI), cuya instrumentación suele estar ampliamente disponible. Por ejemplo, el tratamiento de un carbonilo metálico con alcóxido genera un metalaformiato aniónico que es susceptible de análisis mediante ESI-MS:
Algunos carbonilos metálicos reaccionan con azida para dar complejos de isocianato con liberación de nitrógeno . [28] Al ajustar el voltaje o la temperatura del cono, se puede controlar el grado de fragmentación. Se puede determinar la masa molar del complejo original, así como información sobre reordenamientos estructurales que implican la pérdida de ligandos carbonilo en condiciones ESI-MS. [29]
La espectrometría de masas combinada con la espectroscopia de fotodisociación infrarroja puede proporcionar información vibratoria para complejos de carbonilo iónicos en fase gaseosa. [30]

En la investigación del espectro infrarrojo del centro galáctico de la Vía Láctea se detectaron vibraciones de monóxido de carbonilos de hierro en nubes de polvo interestelares . [32] También se observaron grupos de carbonilo de hierro en condritas Jiange H5 identificadas mediante espectroscopía infrarroja. Se encontraron cuatro frecuencias de estiramiento infrarrojo para los ligandos terminales y puente de monóxido de carbono. [33]
En la atmósfera terrestre rica en oxígeno, los carbonilos metálicos están sujetos a oxidación para formar óxidos metálicos. Se discute si en los ambientes hidrotermales reductores de la prehistoria prebiótica se formaron tales complejos y podrían haber estado disponibles como catalizadores para la síntesis de compuestos bioquímicos críticos como el ácido pirúvico . [34] Se encontraron trazas de carbonilos de hierro, níquel y tungsteno en las emanaciones gaseosas de los lodos de depuradora de las plantas de tratamiento municipales . [35]
Las enzimas hidrogenasas contienen CO unido al hierro. Se cree que el CO estabiliza los estados de oxidación bajos, lo que facilita la unión del hidrógeno . Las enzimas monóxido de carbono deshidrogenasa y acetil-CoA sintasa también participan en el bioprocesamiento de CO. [36] Los complejos que contienen monóxido de carbono se invocan para la toxicidad del CO y la señalización. [37]
La síntesis de carbonilos metálicos es un tema ampliamente estudiado en la investigación organometálica. Desde el trabajo de Mond y luego de Hieber, se han desarrollado muchos procedimientos para la preparación de carbonilos metálicos mononucleares, así como grupos de carbonilos homo y heterometálicos. [38]
El tetracarbonilo de níquel y el pentacarbonilo de hierro se pueden preparar de acuerdo con las siguientes ecuaciones mediante la reacción de un metal finamente dividido con monóxido de carbono : [39]
El tetracarbonilo de níquel se forma con monóxido de carbono ya a 80 °C y presión atmosférica, el hierro finamente dividido reacciona a temperaturas entre 150 y 200 °C y una presión de monóxido de carbono de 50 a 200 bar. [40] Otros carbonilos metálicos se preparan mediante métodos menos directos. [41]
Algunos carbonilos metálicos se preparan mediante la reducción de haluros metálicos en presencia de alta presión de monóxido de carbono. Se emplean una variedad de agentes reductores, incluidos cobre , aluminio , hidrógeno y alquilos metálicos como el trietilaluminio . Es ilustrativa la formación de hexacarbonilo de cromo a partir de cloruro de cromo (III) anhidro en benceno con aluminio como agente reductor y cloruro de aluminio como catalizador: [39]
El uso de alquilos metálicos, como trietilaluminio y dietilzinc , como agente reductor conduce al acoplamiento oxidativo del radical alquilo para formar el alcano dímero :
Las sales de tungsteno , molibdeno , manganeso y rodio se pueden reducir con hidruro de litio y aluminio . El hexacarbonilo de vanadio se prepara con sodio como agente reductor en disolventes quelantes como la diglima . [9]
En la fase acuosa se pueden reducir las sales de níquel o cobalto, por ejemplo mediante ditionito de sodio . En presencia de monóxido de carbono, las sales de cobalto se convierten cuantitativamente en el anión tetracarbonilcobalto(-1): [9]
Algunos carbonilos metálicos se preparan utilizando CO directamente como agente reductor . De esta manera, Hieber y Fuchs prepararon por primera vez dirhenio decacarbonilo a partir del óxido: [42]
Si se utilizan óxidos metálicos, se forma dióxido de carbono como producto de reacción. En la reducción de cloruros metálicos con monóxido de carbono se forma fosgeno , como en la preparación de cloruro de osmiocarbonilo a partir de las sales de cloruro. [38] El monóxido de carbono también es adecuado para la reducción de sulfuros , donde el sulfuro de carbonilo es el subproducto.
La fotólisis o termólisis de carbonilos mononucleares genera carbonilos di y polimetálicos como el nonacarbonilo de hierro (Fe 2 (CO) 9 ). [43] [44] Al calentarse más, los productos eventualmente se descomponen en metal y monóxido de carbono. [ cita necesaria ]
La descomposición térmica del triosmio dodecacarbonilo (Os 3 (CO) 12 ) proporciona grupos de carbonilo de osmio de núcleo superior, como Os 4 (CO) 13 , Os 6 (CO) 18 hasta Os 8 (CO) 23 . [9]
Los ligandos carbonilos mixtos de rutenio , osmio , rodio e iridio a menudo se generan mediante la extracción de CO de disolventes como la dimetilformamida (DMF) y el 2-metoxietanol . Típica es la síntesis de IrCl(CO)(PPh 3 ) 2 a partir de la reacción de cloruro de iridio (III) y trifenilfosfina en una solución hirviendo de DMF. [45]
La reacción de metátesis de sales como KCo(CO) 4 con [Ru(CO) 3 Cl 2 ] 2 conduce selectivamente a carbonilos de metales mixtos como RuCo 2 (CO) 11 . [46]
La síntesis de complejos carbonílicos iónicos es posible mediante oxidación o reducción de los complejos neutros. Los carbonilatos de metales aniónicos se pueden obtener, por ejemplo, mediante reducción de complejos dinucleares con sodio. Un ejemplo familiar es la sal sódica del tetracarbonilato de hierro (Na 2 Fe (CO) 4 , reactivo de Collman ), que se utiliza en síntesis orgánica. [47]
Las sales catiónicas de hexacarbonilo de manganeso , tecnecio y renio se pueden preparar a partir de haluros de carbonilo bajo presión de monóxido de carbono mediante reacción con un ácido de Lewis .
El uso de ácidos fuertes permitió preparar cationes carbonilo de oro como el [Au(CO) 2 ] + , que se utiliza como catalizador para la carbonilación de alquenos . [48] El complejo catiónico de platino-carbonilo [Pt(CO) 4 ] 2+ se puede preparar trabajando en los llamados superácidos , como el pentafluoruro de antimonio . [49] Aunque el CO se considera generalmente como un ligando para iones metálicos de baja valencia, el complejo de hierro tetravalente [Cp* 2 Fe] 2+ (complejo de 16 electrones de valencia) se une cuantitativamente al CO para dar el Fe(IV)-carbonilo diamagnético. [Cp* 2 FeCO] 2+ (complejo de electrones de valencia de 18). [50]
Los carbonilos metálicos son precursores importantes para la síntesis de otros complejos organometálicos. Las reacciones comunes son la sustitución de monóxido de carbono por otros ligandos, las reacciones de oxidación o reducción del centro metálico y reacciones en el ligando de monóxido de carbono. [1]
La sustitución de ligandos de CO puede inducirse térmica o fotoquímicamente mediante ligandos donantes. La gama de ligandos es amplia e incluye fosfinas , cianuro (CN − ), donadores de nitrógeno e incluso éteres, especialmente quelantes. Los alquenos , especialmente los dienos , son ligandos eficaces que producen derivados sintéticamente útiles. La sustitución de complejos de 18 electrones generalmente sigue un mecanismo disociativo , que involucra intermediarios de 16 electrones. [51]
La sustitución se produce mediante un mecanismo disociativo :
La energía de disociación es 105 kJ/mol (25 kcal/mol) para el tetracarbonilo de níquel y 155 kJ/mol (37 kcal/mol) para el hexacarbonilo de cromo . [1]
La sustitución en complejos de 17 electrones, que son poco comunes, se produce mediante mecanismos asociativos con intermediarios de 19 electrones.
La tasa de sustitución en complejos de 18 electrones a veces es catalizada por cantidades catalíticas de oxidantes, mediante transferencia de electrones . [52]
Los carbonilos metálicos reaccionan con agentes reductores como el sodio metálico o la amalgama de sodio para dar aniones carbonilmetalato (o carbonilato):
Para el pentacarbonilo de hierro, se obtiene el tetracarbonilferrato con pérdida de CO:
El mercurio puede insertarse en los enlaces metal-metal de algunos carbonilos metálicos polinucleares:
El ligando CO es a menudo susceptible al ataque de nucleófilos . Por ejemplo, el óxido de trimetilamina y la bis(trimetilsilil)amida de potasio convierten los ligandos de CO en CO 2 y CN − , respectivamente. En la " reacción base de Hieber ", el ion hidróxido ataca al ligando CO para dar un ácido metalocarboxílico , seguido de la liberación de dióxido de carbono y la formación de hidruros metálicos o carbonilmetalatos. Un ejemplo bien estudiado de esta adición nucleofílica es la conversión de pentacarbonilo de hierro en anión hidridohierro tetracarbonilo :
Los reactivos de hidruro también atacan a los ligandos de CO, especialmente en complejos metálicos catiónicos, para dar el derivado formilo :
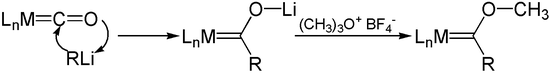
Los reactivos de organolitio se suman a los aniones carbonilo acilmetal con carbonilos metálicos. La O - alquilación de estos aniones, como con las sales de Meerwein , produce carbenos de Fischer .
A pesar de estar en estados de oxidación formal bajos , los carbonilos metálicos son relativamente poco reactivos con muchos electrófilos . Por ejemplo, resisten el ataque de agentes alquilantes, ácidos suaves y agentes oxidantes suaves . La mayoría de los carbonilos metálicos sufren halogenación . El pentacarbonilo de hierro , por ejemplo, forma haluros de carbonilo ferrosos:
Los halógenos rompen los enlaces metal-metal. Dependiendo del esquema de conteo de electrones utilizado, esto puede considerarse como una oxidación de los átomos metálicos:
La mayoría de los complejos de carbonilo metálico contienen una mezcla de ligandos. Los ejemplos incluyen el históricamente importante IrCl(CO)(P(C 6 H 5 ) 3 ) 2 y el agente antidetonante (CH 3 C 5 H 4 )Mn(CO) 3 . Los compuestos originales de muchos de estos complejos de ligandos mixtos son los carbonilos binarios, aquellas especies de fórmula [M x (CO) n ] z , muchas de las cuales están disponibles comercialmente. Las fórmulas de muchos carbonilos metálicos se pueden inferir a partir de la regla de los 18 electrones .
También son bien conocidos los grandes grupos aniónicos de níquel , paladio y platino . Muchos aniones de carbonilo metálico pueden protonarse para dar hidruros de carbonilo metálico .
No clásico describe aquellos complejos carbonílicos donde ν CO es mayor que el del monóxido de carbono libre. En los complejos de CO no clásicos, la distancia del CO es más corta que la del CO libre (113,7 pm). La estructura de [Fe(CO) 6 ] 2+ , con d C-O = 112,9 pm, ilustra este efecto. Estos complejos suelen ser catiónicos, a veces dicatiónicos. [58]

Los carbonilos metálicos se utilizan en varios procesos industriales. Quizás la primera aplicación fue la extracción y purificación de níquel mediante tetracarbonilo de níquel mediante el proceso Mond (ver también metalurgia del carbonilo ). [ cita necesaria ]
Mediante un proceso similar se prepara carbonilo hierro , un polvo metálico de gran pureza, mediante descomposición térmica del pentacarbonilo de hierro. El carbonilo hierro se utiliza, entre otras cosas, para la preparación de inductores , pigmentos , como suplemento dietético , [59] en la producción de materiales absorbentes de radar en la tecnología furtiva , [60] y en la pulverización térmica . [ cita necesaria ]
Los carbonilos metálicos se utilizan en varias reacciones de carbonilación de importancia industrial . En el proceso oxo , un alqueno , gas hidrógeno y monóxido de carbono reaccionan junto con un catalizador (como el dicobalto octacarbonilo ) para dar aldehídos . Es ilustrativa la producción de butiraldehído a partir de propileno :
El butiraldehído se convierte a escala industrial en 2-etilhexanol , un precursor de los plastificantes de PVC , mediante condensación aldólica , seguida de la hidrogenación del hidroxialdehído resultante. Los "oxoaldehídos" resultantes de la hidroformilación se utilizan para la síntesis a gran escala de alcoholes grasos, que son precursores de los detergentes . La hidroformilación es una reacción con alta economía atómica , especialmente si la reacción transcurre con alta regioselectividad . [ cita necesaria ]
Otra reacción importante catalizada por carbonilos metálicos es la hidrocarboxilación . El siguiente ejemplo es para la síntesis de ácido acrílico y ésteres de ácido acrílico:
Además, la ciclación de acetileno a ciclooctatetraeno utiliza catalizadores de carbonilo metálico: [61]
En los procesos de Monsanto y Cativa , el ácido acético se produce a partir de metanol, monóxido de carbono y agua utilizando yoduro de hidrógeno , así como catalizadores carbonílicos de rodio e iridio, respectivamente. Las reacciones de carbonilación relacionadas producen anhídrido acético . [62]
Las moléculas liberadoras de monóxido de carbono son complejos de carbonilo metálico que se están desarrollando como fármacos potenciales para liberar CO. En concentraciones bajas, el CO funciona como un agente vasodilatador y antiinflamatorio. Los CO-RM se han concebido como un enfoque estratégico farmacológico para transportar y administrar cantidades controladas de CO a tejidos y órganos. [63]
Se sabe que muchos ligandos forman complejos de ligandos homolépticos y mixtos que son análogos a los carbonilos metálicos. [ cita necesaria ]
Los nitrosilos metálicos, compuestos que NO contienen ligandos , son numerosos. Sin embargo, a diferencia de los carbonilos metálicos, los nitrosilos metálicos homolépticos son raros. El NO es un aceptor π más fuerte que el CO. Los nitrosilcarbonilos bien conocidos incluyen CoNO(CO) 3 y Fe(NO) 2 (CO) 2 , que son análogos de Ni(CO) 4 . [64]
Los complejos que contienen CS son conocidos pero poco comunes. [65] [66] La rareza de tales complejos se puede atribuir en parte al hecho de que el material fuente obvio, el monosulfuro de carbono , es inestable. Así, la síntesis de complejos de tiocarbonilo requiere rutas indirectas, como la reacción del tetracarbonilferrato disódico con tiofosgeno :
Se han caracterizado complejos de CSe y CTe. [67]
Los isocianuros también forman extensas familias de complejos relacionados con los carbonilos metálicos. Ligandos de isocianuro típicos son isocianuro de metilo e isocianuro de t -butilo (Me 3 CNC). Un caso especial es el CF 3 NC , una molécula inestable que forma complejos estables cuyo comportamiento es muy paralelo al de los carbonilos metálicos. [68]
La toxicidad de los carbonilos metálicos se debe a la toxicidad del monóxido de carbono , el metal, y debido a la volatilidad e inestabilidad de los complejos, cualquier toxicidad inherente del metal generalmente se vuelve mucho más grave debido a la facilidad de exposición. La exposición se produce por inhalación, o en el caso de carbonilos metálicos líquidos, por ingestión o debido a la buena solubilidad en grasas por resorción cutánea. La mayor parte de la experiencia clínica se obtuvo de intoxicaciones toxicológicas con tetracarbonilo de níquel y pentacarbonilo de hierro debido a su uso en la industria. El tetracarbonilo de níquel se considera uno de los venenos de inhalación más potentes. [69]
La inhalación de tetracarbonilo de níquel causa síntomas agudos no específicos similares a una intoxicación por monóxido de carbono , como náuseas , tos , dolor de cabeza , fiebre y mareos . Después de un tiempo, aparecen síntomas pulmonares graves como tos, taquicardia y cianosis , o problemas en el tracto gastrointestinal . Además de alteraciones patológicas del pulmón, como por ejemplo por metalación de los alvéolos, se observan daños en el cerebro, hígado, riñones, glándulas suprarrenales y bazo. Una intoxicación por carbonilo metálico a menudo requiere una recuperación prolongada. [70]
La exposición crónica por inhalación de bajas concentraciones de tetracarbonilo de níquel puede provocar síntomas neurológicos como insomnio, dolores de cabeza, mareos y pérdida de memoria. [70] El tetracarbonilo de níquel se considera cancerígeno, pero pueden pasar de 20 a 30 años desde el inicio de la exposición hasta la manifestación clínica del cáncer. [71]

Los primeros experimentos sobre la reacción del monóxido de carbono con metales los llevó a cabo Justus von Liebig en 1834. Pasando monóxido de carbono sobre potasio fundido preparó una sustancia que tenía la fórmula empírica KCO, a la que llamó Kohlenoxidkalium . [72] Como se demostró más tarde, el compuesto no era un carbonilo, sino la sal potásica de bencenohexol (K 6 C 6 O 6 ) y la sal potásica de acetilendiol (K 2 C 2 O 2 ). [38]

La síntesis del primer verdadero complejo carbonílico de metal heteroléptico fue realizada por Paul Schützenberger en 1868 pasando cloro y monóxido de carbono sobre negro de platino , donde se formó dicarbonildicloroplatino (Pt(CO)2Cl2) . [73]
Ludwig Mond , uno de los fundadores de Imperial Chemical Industries , investigó en la década de 1890 con Carl Langer y Friedrich Quincke varios procesos para la recuperación del cloro perdido en el proceso Solvay por metales, óxidos y sales de níquel . [38] Como parte de sus experimentos, el grupo trató el níquel con monóxido de carbono. Descubrieron que el gas resultante coloreaba la llama de un quemador con un color verdoso-amarillento; cuando se calentaba en un tubo de vidrio formaba un espejo de níquel. El gas podría condensarse hasta obtener un líquido incoloro y transparente como el agua con un punto de ebullición de 43 °C. Así, Mond y su compañero de trabajo habían descubierto el primer carbonilo metálico homoléptico puro, el tetracarbonilo de níquel (Ni (CO) 4 ). [74] La inusual alta volatilidad del compuesto metálico níquel tetracarbonilo llevó a Kelvin a afirmar que Mond había "dado alas a los metales pesados". [75]
Al año siguiente, Mond y Marcellin Berthelot descubrieron de forma independiente el pentacarbonilo de hierro , que se produce mediante un procedimiento similar al del tetracarbonilo de níquel. Mond reconoció el potencial económico de esta clase de compuestos, que utilizó comercialmente en el proceso Mond y financió más investigaciones sobre compuestos relacionados. Heinrich Hirtz y su colega M. Dalton Cowap sintetizaron carbonilos metálicos de cobalto , molibdeno , rutenio y nonacarbonilo de hierro . [76] [77] En 1906, James Dewar y HO Jones pudieron determinar la estructura del diiron nonacarbonilo, que se produce a partir del hierro pentacarbonilo por la acción de la luz solar. [78] Después de Mond, que murió en 1909, la química de los carbonilos metálicos cayó durante varios años en el olvido. BASF inició en 1924 la producción industrial de pentacarbonilo de hierro mediante un proceso desarrollado por Alwin Mittasch . El pentacarbonilo de hierro se utilizó para la producción de hierro de alta pureza, el llamado carbonilo de hierro , y pigmento de óxido de hierro . [40] No fue hasta 1927 que A. Job y A. Cassal lograron la preparación de hexacarbonilo de cromo y hexacarbonilo de tungsteno , la primera síntesis de otros carbonilos metálicos homolépticos. [ cita necesaria ]
Walter Hieber desempeñó en los años posteriores a 1928 un papel decisivo en el desarrollo de la química de los carbonilos metálicos. Investigó y descubrió sistemáticamente, entre otras cosas, la reacción de la base de Hieber , la primera ruta conocida para obtener hidruros de carbonilo metálico y vías sintéticas que conducen a carbonilos metálicos como el dirhenio decacarbonilo . [79] Hieber, que fue desde 1934 director del Instituto de Química Inorgánica de la Universidad Técnica de Munich, publicó en cuatro décadas 249 artículos sobre química de carbonilos metálicos. [38]
También en la década de 1930 , Walter Reppe , químico industrial y más tarde miembro de la junta directiva de BASF, descubrió una serie de procesos catalíticos homogéneos, como la hidrocarboxilación , en la que olefinas o alquinos reaccionan con monóxido de carbono y agua para formar productos como ácidos insaturados y sus derivados. [38] En estas reacciones, por ejemplo, el tetracarbonilo de níquel o los carbonilos de cobalto actúan como catalizadores. [80] Reppe también descubrió la ciclotrimerización y tetramerización del acetileno y sus derivados a benceno y derivados de benceno con carbonilos metálicos como catalizadores. BASF construyó en los años 60 una planta de producción de ácido acrílico mediante el proceso Reppe, que no fue sustituido hasta 1996 por métodos más modernos basados en la oxidación catalítica del propileno . [ cita necesaria ]

Para el diseño racional de nuevos complejos se ha encontrado útil el concepto de analogía isolobal. Roald Hoffmann recibió el Premio Nobel de Química por el desarrollo del concepto. Esto describe fragmentos de carbonilo metálico de M(CO) n como partes de bloques de construcción octaédricos en analogía con los fragmentos tetraédricos CH 3 –, CH 2 – o CH– en química orgánica. En el ejemplo , el dimanganeso decacarbonilo se forma en términos de la analogía isolobal de dos fragmentos d7Mn(CO)5, que son isolobales al radical metilo CH .•
3. De manera análoga a cómo los radicales metilo se combinan para formar etano , estos pueden combinarse para formar dimanganeso decacarbonilo . La presencia de fragmentos análogos isolobales no significa que se puedan sintetizar las estructuras deseadas. En su conferencia del Premio Nobel, Hoffmann enfatizó que la analogía isolobal es un modelo útil pero simple, y en algunos casos no conduce al éxito. [81]
Los beneficios económicos de las carbonilaciones catalizadas por metales , como la química de Reppe y la hidroformilación , llevaron al crecimiento del área. Se descubrieron compuestos de carbonilo metálico en los sitios activos de tres enzimas naturales. [82]
{{cite book}}: Mantenimiento CS1: varios nombres: lista de autores ( enlace ){{cite journal}}: Falta o está vacío |title=( ayuda )