Imatinib , vendido bajo las marcas Gleevec y Glivec (ambas comercializadas en todo el mundo por Novartis ), entre otras, es un medicamento de terapia dirigida oral que se utiliza para tratar el cáncer . [2] Imatinib es un inhibidor de molécula pequeña que se dirige a múltiples tirosina quinasas como CSF1R , ABL , c-KIT , FLT3 y PDGFR-β . [6] [7] Específicamente, se usa para la leucemia mielógena crónica (LMC) y la leucemia linfocítica aguda (LLA) que tienen cromosoma Filadelfia positivo (Ph + ), ciertos tipos de tumores del estroma gastrointestinal (GIST), síndrome hipereosinofílico (HES ), leucemia eosinofílica crónica (CEL), mastocitosis sistémica y síndrome mielodisplásico . [2]
Los efectos secundarios comunes incluyen vómitos, diarrea, dolor muscular, dolor de cabeza y sarpullido. Los efectos secundarios graves pueden incluir retención de líquidos , hemorragia gastrointestinal , supresión de la médula ósea , problemas hepáticos e insuficiencia cardíaca . El uso durante el embarazo puede provocar daños al bebé. Imatinib actúa deteniendo la tirosina quinasa Bcr-Abl . Esto puede retardar el crecimiento o provocar la muerte celular programada de ciertos tipos de células cancerosas. [2]
Imatinib fue aprobado para uso médico en los Estados Unidos en 2001. [2] Está en la Lista de medicamentos esenciales de la Organización Mundial de la Salud . [8] Una versión genérica estuvo disponible en el Reino Unido a partir de 2017. [9]
Imatinib se usa para tratar la leucemia mielógena crónica (LMC), los tumores del estroma gastrointestinal (GIST) y otras neoplasias malignas . En 2006, la FDA amplió el uso aprobado para incluir el dermatofibrosarcoma protuberans (DFSP), las enfermedades mielodisplásicas /mieloproliferativas (MDS/MPD) y la mastocitosis sistémica agresiva (ASM). [10]
El imatinib se considera un tratamiento muy eficaz para la leucemia mieloide crónica y se ha demostrado que mejora los resultados en personas con este tipo de leucemia. También se puede utilizar para tratar algunos tipos de ALL, pero no se considera un estándar de atención para ALL. En muchos casos, Imatinib puede inducir una respuesta citogenética completa (CCyR) y una respuesta molecular mayor (MMR) y muchos pacientes pueden tener una remisión a largo plazo. También se utiliza para mantener la remisión en pacientes con leucemia mieloide crónica en fase crónica.
Si bien el imatinib es un tratamiento muy eficaz para la leucemia mieloide crónica y algunos tipos de ALL, no es una cura para la leucemia. Más bien, se trata de una 'terapia crónica' que ayuda a controlar la enfermedad y evitar que progrese. Es posible que algunos pacientes necesiten continuar tomando Imatinib durante un período prolongado para mantener la remisión, y algunos pacientes pueden eventualmente requerir opciones de tratamiento adicionales.
La Administración de Medicamentos y Alimentos de los EE. UU. (FDA) ha aprobado el imatinib como tratamiento de primera línea para la leucemia mieloide crónica con cromosoma Filadelfia positivo, tanto en adultos como en niños. El fármaco está aprobado en múltiples contextos de leucemia mieloide crónica con cromosoma Filadelfia positivo, incluso después de un trasplante de células madre, en crisis blástica y en pacientes recién diagnosticados. [11]
Debido en parte al desarrollo de imatinib y medicamentos relacionados, la tasa de supervivencia a cinco años para las personas con leucemia mieloide crónica aumentó del 31 % en 1993 al 59 % en 2009, [ 12] al 70 % en 2016. [13] En 2023, la tasa de supervivencia a cinco años de las personas con leucemia mieloide crónica había aumentado al 90%. [14] A partir de 2011, quedó claro que los pacientes con leucemia mieloide crónica que continúan respondiendo al imatinib tienen la misma o casi la misma esperanza de vida que la población general. [15]
La FDA otorgó la aprobación por primera vez para pacientes con GIST avanzado en 2002. El 1 de febrero de 2012, se aprobó el uso de imatinib después de la extirpación quirúrgica de tumores KIT positivos para ayudar a prevenir la recurrencia. [16] El fármaco también está aprobado en GIST KIT positivos irresecables. [11]
La FDA otorgó la aprobación para el tratamiento de pacientes con dermatofibrosarcoma protuberans (DFSP) en 2006. [10] Específicamente pacientes adultos con dermatofibrosarcoma protuberans (DFSP) irresecable, recurrente y/o metastásico . Antes de la aprobación, se consideraba que el DFSP no respondía a los tratamientos de quimioterapia .
La FDA ha aprobado el uso de imatinib en adultos con leucemia linfoblástica aguda (LLA Ph+) con cromosoma Filadelfia positivo en recaída o refractaria, enfermedades mielodisplásicas / mieloproliferativas asociadas con reordenamientos del gen del receptor del factor de crecimiento derivado de plaquetas , mastocitosis sistémica agresiva sin D816V c- o desconocido. Mutación KIT, síndrome hipereosinofílico y/o leucemia eosinofílica crónica que tienen la fusión quinasa FIP1L1-PDGFRα (deleción del alelo CHIC2) o la fusión quinasa FIP1L1-PDGFRα negativa o dermatofibrosarcoma protuberans desconocida, irresecable, recurrente y/o metastásica. [11] El 25 de enero de 2013, se aprobó el uso de Gleevec en niños con LLA Ph+. [17]
Para el tratamiento de neurofibromas plexiformes progresivos asociados con neurofibromatosis tipo I , las primeras investigaciones han demostrado potencial para utilizar las propiedades bloqueantes de la tirosina quinasa c-KIT del imatinib. [18] [19] [20] [21] Según un pequeño ensayo, el imatinib es un fármaco eficaz en algunos pacientes con fibromatosis agresiva . [22]
La única contraindicación conocida del imatinib es la hipersensibilidad al imatinib. [23] Las precauciones incluyen: [24]

Los efectos secundarios más comunes incluyen náuseas, vómitos, diarrea, dolores de cabeza, dolores/calambres en las piernas, retención de líquidos, alteraciones visuales, sarpullido con picazón, menor resistencia a las infecciones, hematomas o sangrado, pérdida de apetito, [25] aumento de peso, reducción del número de células sanguíneas ( neutropenia , trombocitopenia , anemia ) y edema . [26]
En algunos individuos, se informó que el uso de imatinib estaba asociado con disfunción ventricular izquierda que a veces progresaba a insuficiencia cardíaca congestiva a pesar de la ausencia de enfermedad cardíaca previa. Los ensayos clínicos de imatinib no informaron efectos adversos cardíacos, pero informaron una incidencia notablemente alta de edema periférico, y algunos casos se clasificaron como graves. [27]
Las biopsias de pacientes, así como las de ratones tratados con grandes dosis de imatinib, mostraron signos celulares de cardiotoxicidad . Los efectos cardiotóxicos parecían estar mediados por la inhibición de la tirosina quinasa ABL1 citoplasmática . [27]
Múltiples estudios en humanos y animales sugieren que si imatinib se usa en niños prepúberes, puede retrasar el crecimiento normal (más específicamente el alargamiento óseo), aunque algunos pueden experimentar al menos una recuperación parcial del crecimiento durante la pubertad . [28]
El motivo de este efecto secundario no está claro; puede estar implicada la interferencia con una vía relacionada con la hormona del crecimiento (GH) (el crecimiento prepuberal depende de la GH, mientras que el crecimiento puberal es promovido sinérgicamente tanto por la GH como por las hormonas sexuales). [28]
El uso de imatinib puede causar aclaramiento/despigmentación u oscurecimiento/repigmentación del cabello (como es el caso con algunos otros inhibidores de la tirosina quinasa) y/o de la piel, así como hiperpigmentación de las encías . La mediana de aparición del cambio de color del cabello es 4 semanas después del inicio del tratamiento (pero puede ocurrir más de un año después del inicio), depende de la dosis y es reversible al suspender el tratamiento o reducir la dosis. [29]
Los receptores C-kit , uno de los objetivos biológicos de imatinib, se expresan en los melanocitos. [29]
La experiencia médica con la sobredosis de imatinib es limitada. [30] El tratamiento es de apoyo. [30] El imatinib se une en gran medida a las proteínas plasmáticas: [30] es poco probable que la diálisis sea útil para eliminar el imatinib.
Se desaconseja su uso en personas que toman inhibidores potentes del CYP3A4 como claritromicina , cloranfenicol , ketoconazol , ritonavir y nefazodona debido a su dependencia del CYP3A4 para el metabolismo. [24] Asimismo, es un inhibidor de CYP3A4 , CYP2D6 y CYP2C9 y, por lo tanto, el tratamiento concomitante con sustratos de cualquiera de estas enzimas puede aumentar las concentraciones plasmáticas de dichos fármacos. [24] Dado que imatinib se metaboliza principalmente a través de la enzima hepática CYP3A4, las sustancias que influyen en la actividad de esta enzima cambian la concentración plasmática del fármaco. Un ejemplo de fármaco que aumenta la actividad del imatinib y, por tanto, los efectos secundarios al bloquear el CYP3A4 es el ketoconazol . Lo mismo podría ocurrir con el itraconazol , la claritromicina , el zumo de pomelo , entre otros. Por el contrario, los inductores del CYP3A4 como la rifampicina y la hierba de San Juan reducen la actividad del fármaco, lo que corre el riesgo de que el tratamiento fracase. Imatinib también actúa como inhibidor de CYP3A4, 2C9 y 2D6, aumentando las concentraciones plasmáticas de otros fármacos como simvastatina , ciclosporina , pimozida , warfarina , metoprolol y posiblemente paracetamol . El fármaco también reduce los niveles plasmáticos de levotiroxina mediante un mecanismo desconocido. [26]
Como ocurre con otros inmunosupresores, la aplicación de vacunas vivas está contraindicada porque los microorganismos de la vacuna podrían multiplicarse e infectar al paciente. Las vacunas inactivadas y con toxoides no conllevan este riesgo, pero pueden no ser eficaces bajo el tratamiento con imatinib. [31]
Se desaconseja encarecidamente comer pomelo y beber jugo de pomelo, ya que aumenta la concentración de imatinib en la sangre. [32]
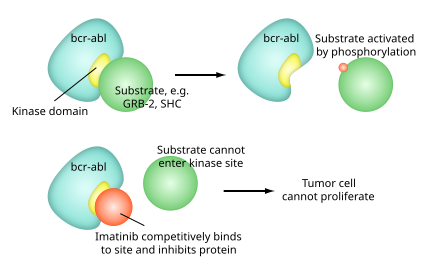
Imatinib es un derivado de 2- fenilaminopirimidina que funciona como un inhibidor específico de varias enzimas tirosina quinasa. Ocupa el sitio activo de TK , lo que provoca una disminución de la actividad.
Hay una gran cantidad de enzimas TK en el cuerpo, incluido el receptor de insulina . Imatinib es específico para el dominio TK en abl (el protooncogén de Abelson), c-kit y PDGF-R ( receptor del factor de crecimiento derivado de plaquetas ).
En la leucemia mielógena crónica , el cromosoma Filadelfia conduce a una proteína de fusión de abl con bcr ( región de grupo de punto de ruptura ), denominada bcr-abl . Como ahora es una tirosina quinasa constitutivamente activa , imatinib se usa para disminuir la actividad de bcr-abl .
Cada uno de los sitios activos de las tirosina quinasas tiene un sitio de unión para el ATP . La actividad enzimática catalizada por una tirosina quinasa es la transferencia del fosfato terminal del ATP a los residuos de tirosina en sus sustratos , un proceso conocido como fosforilación de proteína tirosina . Imatinib actúa uniéndose cerca del sitio de unión de ATP de bcr-abl , bloqueándolo en una conformación cerrada o autoinhibida y, por lo tanto, inhibiendo la actividad enzimática de la proteína de forma semicompetitiva . [34] Este hecho explica por qué muchas mutaciones de BCR-ABL pueden causar resistencia al imatinib al cambiar su equilibrio hacia la conformación abierta o activa. [35]
Imatinib es bastante selectivo para bcr-abl , aunque también inhibe otros objetivos mencionados anteriormente (c-kit y PDGF-R), así como las tirosina quinasas ABL2 (ARG) y DDR1 y NQO2, una oxidorreductasa. [36] Imatinib también inhibe la proteína abl de las células no cancerosas, pero estas células normalmente tienen tirosina quinasas redundantes adicionales, lo que les permite continuar funcionando incluso si la tirosina quinasa abl está inhibida. Algunas células tumorales , sin embargo, dependen de bcr-abl . [37] La inhibición de la tirosina quinasa bcr-abl también estimula su entrada al núcleo, donde es incapaz de realizar cualquiera de sus funciones antiapotópicas normales , lo que lleva a la muerte de las células tumorales. [38]
La vía Bcr-Abl tiene muchas vías posteriores que incluyen [39]
Imatinib se absorbe rápidamente cuando se administra por vía oral y tiene una alta biodisponibilidad : el 98% de una dosis oral llega al torrente sanguíneo. El metabolismo de imatinib ocurre en el hígado y está mediado por varias isoenzimas del sistema del citocromo P450 , incluido CYP3A4 y, en menor medida, CYP1A2 , CYP2D6 , CYP2C9 y CYP2C19 . El metabolito principal , el derivado de piperazina N -desmetilado , también está activo. La principal vía de eliminación es la bilis y las heces; sólo una pequeña porción del fármaco se excreta por la orina. La mayor parte del imatinib se elimina en forma de metabolitos; sólo el 25% se elimina sin cambios. Las vidas medias de imatinib y su metabolito principal son de 18 h y 40 h, respectivamente. Bloquea la actividad de la tirosina quinasa citoplasmática de Abelson (ABL), c-Kit y el receptor del factor de crecimiento derivado de plaquetas (PDGFR). Como inhibidor del PDGFR, el mesilato de imatinib parece tener utilidad en el tratamiento de una variedad de enfermedades dermatológicas. Se ha informado que imatinib es un tratamiento eficaz para la enfermedad de mastocitos FIP1L1-PDGFRalfa+ , el síndrome hipereosinofílico y el dermatofibrosarcoma protuberans . [40]
Imatinib fue inventado a finales de los años 1990 por científicos de Ciba-Geigy (que se fusionó con Sandoz en 1996 para convertirse en Novartis ), en un equipo liderado por el bioquímico británico Nicholas Lydon y que incluía a Elisabeth Buchdunger y Jürg Zimmermann, [41] y su uso para tratar la leucemia mieloide crónica fue impulsada por el oncólogo Brian Druker de la Universidad de Ciencias y Salud de Oregón (OHSU). [42] Otras contribuciones importantes al desarrollo de imatinib fueron realizadas por el biólogo Anthony R. Hunter del Instituto Salk de Estudios Biológicos en La Jolla, California, Carlo Gambacorti-Passerini , médico, científico y hematólogo de la Universidad de Milano Bicocca , Italia, John Goldman en el Hammersmith Hospital de Londres, y más tarde por Charles Sawyers del Memorial Sloan Kettering Cancer Center de Nueva York. [42] [43]
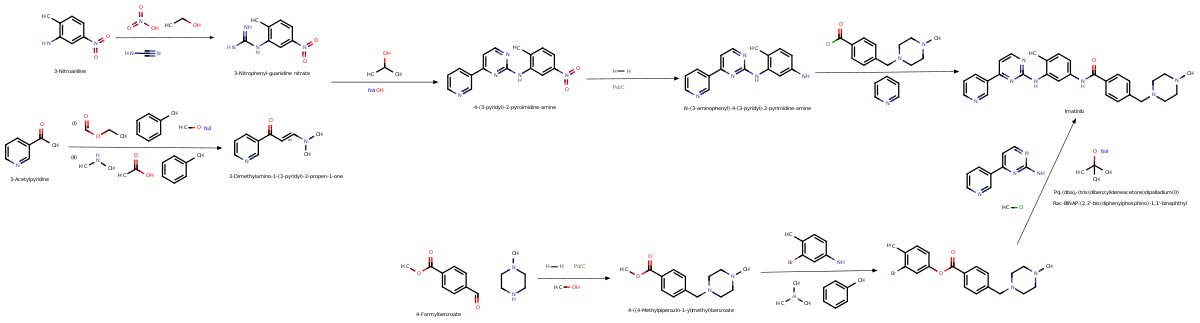
Imatinib fue desarrollado mediante un diseño racional de fármacos . Después de que se descubrieron la mutación del cromosoma Filadelfia y la proteína bcr-abl hiperactiva , los investigadores examinaron bibliotecas químicas para encontrar un fármaco que inhibiera esa proteína. Con un cribado de alto rendimiento , identificaron 2-fenilaminopirimidina. Luego, este compuesto principal se probó y modificó mediante la introducción de grupos metilo y benzamida para darle propiedades de unión mejoradas, lo que dio como resultado imatinib. [44]
Cuando Novartis probó imatinib en ratas, ratones, conejos, perros y monos en 1996, se descubrió que tenía varios efectos tóxicos; en particular, los resultados que indicaron daño hepático en perros casi detuvieron por completo el desarrollo del fármaco. Sin embargo, los resultados favorables en estudios con monos y células humanas in vitro permitieron continuar las pruebas en humanos. [45] [46] [47]
El primer ensayo clínico de Gleevec tuvo lugar en 1998, después de que Novartis sintetizara y liberara a regañadientes unos pocos gramos del fármaco para Druker, suficientes para que éste realizara un ensayo con un centenar de pacientes. [48] Mel Mann, que entró en el ensayo clínico en agosto de 1998, es la persona que vive más tiempo en ser tratada con el fármaco. [49] [50] [51] [52] [53] El medicamento recibió la aprobación de la FDA en mayo de 2001, sólo dos años y medio después de que se presentó la solicitud de nuevo medicamento. [41] [54] Ese mismo mes apareció en la portada de la revista TIME como una "bala" para usar contra el cáncer. Druker, Lydon y Sawyers recibieron el Premio de Investigación Médica Clínica Lasker-DeBakey en 2009 por "convertir un cáncer mortal en una enfermedad crónica manejable". [42]
Durante la revisión de la FDA, el nombre comercial del medicamento para el mercado estadounidense se cambió de "Glivec" a "Gleevec" a pedido de la FDA, para evitar confusión con Glyset , un medicamento para la diabetes. [55] [56] [57]
En abril de 1992 se presentó una solicitud de patente suiza sobre imatinib y varias sales, que luego se presentó en la UE, EE. UU. y otros países en marzo y abril de 1993. [58] [59] y en 1996, patente estadounidense y europea Las oficinas emitieron patentes que incluían a Jürg Zimmermann como inventor. [58] [60]
En julio de 1997, Novartis presentó una nueva solicitud de patente en Suiza sobre la forma beta cristalina del mesilato de imatinib (la sal mesilato de imatinib). La "forma beta cristalina" de la molécula es un polimorfo específico del mesilato de imatinib; una forma específica en que las moléculas individuales se empaquetan para formar un sólido. Esta es la forma real del fármaco vendido como Gleevec/Glivec; una sal (mesilato de imatinib) en lugar de una base libre, y la forma beta cristalina en lugar de la alfa u otra forma. [61] : 3 y 4 En 1998, Novartis presentó solicitudes de patente internacionales reivindicando prioridad sobre la presentación de 1997. [62] [63] En 2005 se concedió una patente en los Estados Unidos. [64]

En 2013, más de 100 especialistas en cáncer publicaron una carta en Blood diciendo que los precios de muchos medicamentos nuevos contra el cáncer, incluido el imatinib, son tan altos que la gente en los Estados Unidos no podría pagarlos, y que el nivel de precios y ganancias, era tan alto que resultaba inmoral. Entre los firmantes de la carta se encontraban Brian Druker, Carlo Gambacorti-Passerini y John Goldman, desarrolladores de imatinib. [65] [66] Escribieron que en 2001, el imatinib tenía un precio de 30.000 dólares (equivalente a 51.622 dólares en 2023) al año, que se basaba en el precio del interferón , entonces el tratamiento estándar, y que a este precio Novartis habría recuperado sus costos iniciales de desarrollo en dos años. Escribieron que después de convertirse inesperadamente en un éxito de taquilla, Novartis aumentó el precio a 92.000 dólares (equivalente a 122.098 dólares en 2023) por año en 2012, con ingresos anuales de 4.700 millones de dólares . Otros médicos se han quejado del coste. [67] [68] [69]
Druker, que dirigió los estudios clínicos, nunca recibió regalías ni beneficios por el éxito del fármaco. [70]
Para 2016, el precio mayorista promedio había aumentado a 120.000 dólares (equivalente a 152.346 dólares en 2023) al año, según un análisis preparado para The Washington Post por Stacie Dusetzina de la Universidad de Carolina del Norte en Chapel Hill . Cuando llegaron al mercado medicamentos competitivos, se vendieron a un precio más alto para reflejar la población más pequeña, [ se necesita aclaración ] y Novartis aumentó el precio de Gleevec para igualarlo. [71]
Un análisis económico de 2012 financiado por Bristol-Myers Squibb estimó que el descubrimiento y desarrollo de imatinib y medicamentos relacionados habían creado 143 mil millones de dólares en valor social a un costo para los consumidores de aproximadamente 14 mil millones de dólares. La cifra de 143 mil millones de dólares se basó en una ventaja de supervivencia estimada de 7,5 a 17,5 años conferida por el tratamiento con imatinib, e incluyó el valor (descontado al 3% anual) de los beneficios continuos para la sociedad después de la expiración de la patente de imatinib. [72]
Los precios de una pastilla de 100 mg de Gleevec a nivel internacional oscilan entre 20 y 30 dólares, [73] aunque el imatinib genérico es más barato, tan solo 2 dólares por pastilla. [74]
Novartis libró una controvertida batalla de siete años para patentar Gleevec en la India y llevó el caso hasta la Corte Suprema de la India . La solicitud de patente en el centro del caso fue presentada por Novartis en India en 1998, después de que India aceptara ingresar a la Organización Mundial del Comercio y cumplir con los estándares mundiales de propiedad intelectual bajo el acuerdo ADPIC . Como parte de este acuerdo, India realizó cambios en su ley de patentes, el mayor de los cuales fue que antes de estos cambios, las patentes sobre productos no estaban permitidas, mientras que después sí lo estaban, aunque con restricciones. Estos cambios entraron en vigor en 2005, por lo que la solicitud de patente de Novartis esperó en un "buzón" junto con otras hasta entonces, según los procedimientos que India instituyó para gestionar la transición. India también aprobó ciertas enmiendas a su ley de patentes en 2005, justo antes de que las leyes entraran en vigor. [75] [76]
La solicitud de patente [63] [77] reivindicaba la forma final de Gleevec (la forma beta cristalina del mesilato de imatinib ). [78] : 3 En 1993, durante el tiempo en que la India no permitía patentes sobre productos, Novartis había patentado el imatinib, con sales vagamente especificadas, en muchos países, pero no podía patentarlo en la India. [58] [60] Las diferencias clave entre las dos solicitudes de patente fueron que la solicitud de patente de 1998 especificaba el contraión (Gleevec es una sal específica: mesilato de imatinib), mientras que la solicitud de patente de 1993 no reivindicaba ninguna sal específica ni mencionaba el mesilato. y la solicitud de patente de 1998 especificaba la forma sólida de Gleevec –la forma en que las moléculas individuales se empaquetan juntas en un sólido cuando se fabrica el fármaco en sí (esto es independiente de los procesos mediante los cuales el fármaco en sí se formula en píldoras o cápsulas)–, mientras que la La solicitud de patente de 1993 no lo hizo. La forma sólida del mesilato de imatinib en Gleevec es beta cristalina. [79]
Según lo dispuesto en el acuerdo ADPIC, Novartis solicitó Derechos Exclusivos de Comercialización (REM) para Gleevec a la Oficina de Patentes de la India y el EMR le fue concedido en noviembre de 2003. [80] Novartis hizo uso del EMR para obtener pedidos contra algunos fabricantes de genéricos que habían ya lanzó Gleevec en India. [81] [82]
Cuando comenzó el examen de la solicitud de patente de Novartis en 2005, fue inmediatamente atacada por oposiciones iniciadas por compañías genéricas que ya vendían Gleevec en India y por grupos de defensa. La solicitud fue rechazada por la oficina de patentes y por una junta de apelación. La base clave para el rechazo fue la parte de la ley de patentes india creada mediante enmienda en 2005, que describe la patentabilidad de nuevos usos para medicamentos conocidos y modificaciones de medicamentos conocidos. Esa sección, 3d, especificaba que tales invenciones son patentables sólo si "difieren significativamente en propiedades con respecto a la eficacia". [81] [83] En un momento, Novartis acudió a los tribunales para intentar invalidar la Sección 3d; argumentó que la disposición era inconstitucionalmente vaga y que violaba los ADPIC. Novartis perdió ese caso y no apeló. [84] Novartis apeló el rechazo de la oficina de patentes ante el Tribunal Supremo de la India, que tomó el caso.
El caso de la Corte Suprema dependía de la interpretación de la Sección 3d. La Corte Suprema emitió su decisión en 2013, dictaminando que la sustancia que Novartis buscaba patentar era en realidad una modificación de un fármaco conocido (la forma cruda de imatinib, que se reveló públicamente en la solicitud de patente de 1993 y en artículos científicos), que Novartis no presentó evidencia de una diferencia en la eficacia terapéutica entre la forma final de Gleevec y la forma cruda de imatinib y que, por lo tanto, la solicitud de patente fue rechazada adecuadamente por la oficina de patentes y los tribunales inferiores. [85]
Un estudio demostró que el mesilato de imatinib fue eficaz en pacientes con mastocitosis sistémica , incluidos aquellos que tenían la mutación D816V en c-KIT. [86] Sin embargo, dado que imatinib se une a las tirosina quinasas cuando están en la configuración inactiva y el mutante D816V de c-KIT es constitutivamente activo, imatinib no inhibe la actividad quinasa del mutante D816V de c-KIT. Sin embargo, la experiencia ha demostrado que el imatinib es mucho menos eficaz en pacientes con esta mutación, y los pacientes con la mutación representan casi el 90% de los casos de mastocitosis.
Inicialmente se pensó que el imatinib tenía un papel potencial en el tratamiento de la hipertensión pulmonar . Se demostró que reduce tanto la hipertrofia del músculo liso como la hiperplasia de la vasculatura pulmonar en una variedad de procesos patológicos, incluida la hipertensión portopulmonar . [87] Sin embargo, un ensayo a largo plazo de imatinib en personas con hipertensión arterial pulmonar no tuvo éxito y los eventos adversos graves e inesperados fueron frecuentes. Estos incluyeron 6 hematomas subdurales y 17 muertes durante o dentro de los 30 días posteriores al final del estudio. [88]
En la esclerosis sistémica , se ha probado el uso potencial del fármaco para desacelerar la fibrosis pulmonar . En entornos de laboratorio, imatinib se está utilizando como agente experimental para suprimir el factor de crecimiento derivado de plaquetas (PDGF) mediante la inhibición de su receptor (PDGF-Rβ). Uno de sus efectos es retrasar la aterosclerosis en ratones sin [89] o con diabetes . [90]
Los estudios en animales con ratones han sugerido que imatinib y medicamentos relacionados pueden ser útiles en el tratamiento de la viruela , en caso de que alguna vez ocurra un brote. [91]
Los estudios in vitro identificaron que una versión modificada de imatinib puede unirse a la proteína activadora de la gamma-secretasa ( GSAP ). GSAP aumenta selectivamente la producción y acumulación de placas de beta-amiloide neurotóxicas , lo que sugiere que las moléculas que se dirigen a GSAP y son capaces de cruzar la barrera hematoencefálica son agentes terapéuticos potenciales para el tratamiento de la enfermedad de Alzheimer . [92] Otro estudio sugiere que es posible que el imatinib no necesite cruzar la barrera hematoencefálica para ser eficaz en el tratamiento del Alzheimer, ya que la investigación indica que la producción de beta-amiloide puede comenzar en el hígado. Las pruebas en ratones indican que imatinib es eficaz para reducir el beta-amiloide en el cerebro. [93] No se sabe si la reducción de beta-amiloide es una forma viable de tratar el Alzheimer, ya que se ha demostrado que una vacuna anti-beta-amiloide limpia las placas del cerebro sin tener ningún efecto sobre los síntomas de Alzheimer. [94]
Una formulación de imatinib con una ciclodextrina (Captisol) como vehículo para superar la barrera hematoencefálica ha demostrado la reversión de la tolerancia a los opioides en un estudio de 2012 en ratas. [95]
Imatinib es un fármaco experimental en el tratamiento del tumor desmoide o fibromatosis agresiva . [96]
La raíz de la palabra -tinib hace referencia a la acción del fármaco como inhibidor de la tirosina quinasa (TYK). [97]