La fascitis necrosante ( NF ), también conocida como enfermedad carnívora , es una infección bacteriana que provoca la muerte de partes del tejido blando del cuerpo . [3] Es una enfermedad grave de aparición repentina que se propaga rápidamente. [3] Los síntomas suelen incluir piel roja o morada en la zona afectada, dolor intenso, fiebre y vómitos. [3] Las zonas más comúnmente afectadas son las extremidades y el perineo . [2]
Por lo general, la infección ingresa al cuerpo a través de una herida en la piel, como un corte o una quemadura . [3] Los factores de riesgo incluyen una función inmunológica deficiente, como la diabetes o el cáncer , la obesidad , el alcoholismo , el uso intravenoso de drogas y la enfermedad arterial periférica . [2] [3] Por lo general, no se transmite entre personas. [3] La enfermedad se clasifica en cuatro tipos, según el organismo infectante. [4] Entre el 55 y el 80% de los casos involucran más de un tipo de bacteria . [4] El Staphylococcus aureus resistente a la meticilina (MRSA) está involucrado en hasta un tercio de los casos. [4] Las imágenes médicas a menudo son útiles para confirmar el diagnóstico. [4]
La fascitis necrosante se puede prevenir con un cuidado adecuado de la herida y el lavado de manos . [3] Por lo general, se trata con cirugía para extirpar el tejido infectado y antibióticos intravenosos . [2] [3] A menudo, se utiliza una combinación de antibióticos, como penicilina G , clindamicina , vancomicina IV y gentamicina . [2] Los retrasos en la cirugía se asocian con un riesgo mucho mayor de muerte. [4] A pesar de un tratamiento de alta calidad, el riesgo de muerte está entre el 25 y el 35%. [2]
La fascitis necrosante se presenta en aproximadamente 4 personas por millón por año en los EE. UU., y aproximadamente 1 por 100 000 en Europa occidental. [4] Ambos sexos se ven afectados por igual. [2] Se vuelve más común entre las personas mayores y es rara en los niños. [4] Se ha descrito al menos desde la época de Hipócrates . [2] El término "fascitis necrosante" comenzó a usarse en 1952. [4] [7]
Los síntomas pueden incluir fiebre, hinchazón y quejas de dolor excesivo. Los cambios iniciales en la piel son similares a la celulitis o absceso , lo que dificulta el diagnóstico en etapas tempranas. El endurecimiento de la piel y el tejido blando y la hinchazón más allá del área de los cambios en la piel son comunes en aquellos con cambios necrosantes tempranos. [2] El enrojecimiento y la hinchazón generalmente se mezclan con los tejidos normales circundantes. La piel suprayacente puede verse brillante y tensa. [8] Otros signos que son más sugestivos de cambios necrosantes (pero presentes en etapas posteriores en el 7 al 44% de los casos) son: formación de ampollas , sangrado en la piel que está presente antes de la necrosis cutánea [2] (la piel se vuelve roja a púrpura y negra debido a la trombosis de los vasos sanguíneos), [8] presencia de gas en los tejidos y sensibilidad reducida o ausente sobre la piel [2] (debido a la necrosis de los nervios subyacentes). [8] La progresión rápida al shock a pesar de la terapia con antibióticos es otra indicación de fascitis necrosante. Los cambios necrotizantes que afectan la ingle se conocen como gangrena de Fournier . [2]
Sin embargo, las personas inmunodeprimidas (con cáncer, que usan corticosteroides , en radioterapia , quimioterapia , VIH/SIDA o con trasplante previo de órganos o médula ósea ) pueden no mostrar síntomas típicos. Las personas inmunodeprimidas también tienen el doble de riesgo de muerte por infecciones necrosantes, por lo que se debe mantener una mayor sospecha en este grupo. [2]
Más del 70% de los casos se registran en personas con al menos una de estas situaciones clínicas: inmunosupresión, diabetes, alcoholismo/abuso de drogas/tabaquismo, neoplasias malignas y enfermedades sistémicas crónicas. Por razones que no están claras, en ocasiones se presenta en personas con un estado general aparentemente normal. [9]
La fascitis necrosante puede ocurrir en cualquier parte del cuerpo, pero es más común en las extremidades, el perineo y los genitales . Solo unos pocos de estos casos surgen del tórax y el abdomen. El traumatismo es la causa habitual de la infección, como la inyección intravenosa de medicamentos, la inyección de insulina, las picaduras de animales e insectos, la inserción de un catéter sobre la piel o una fístula que conecta la piel con los órganos internos del cuerpo. Las infecciones de la piel, como los abscesos y las úlceras, también pueden complicar la fascitis necrosante. Se ha sugerido la propagación de la infección a través de la sangre en las personas con faringitis estreptocócica. En el caso de la infección del perineo y los genitales ( gangrena de Fournier ), las causas habituales son el traumatismo, la cirugía, la infección del tracto urinario , los cálculos y el absceso de la glándula de Bartholin . [2]
El riesgo de desarrollar fascitis necrotizante a partir de una herida se puede reducir con un buen cuidado de la herida y el lavado de manos. [3]
Los tipos de infección necrosante de tejidos blandos se pueden dividir en cuatro clases según los tipos de bacterias que infectan los tejidos blandos. Este sistema de clasificación fue descrito por primera vez por Giuliano y sus colegas en 1977. [4] [2]
Infección de tipo I : este es el tipo de infección más común y representa el 70 a 80% de los casos. Es causada por una mezcla de tipos bacterianos, generalmente en áreas abdominales o inguinales. [4] Este tipo de infección generalmente es causada por varias especies de cocos grampositivos ( Staphylococcus aureus , Streptococcus pyogenes y enterococos ), bacilos gramnegativos ( Escherichia coli , Pseudomonas aeruginosa ) y anaerobios ( especies de Bacteroides y Clostridium ). [4] Las poblaciones de afectados suelen ser mayores con comorbilidades médicas como diabetes mellitus, obesidad e inmunodeficiencia. [4] Por lo general, el traumatismo no es la causa de tales infecciones. Se pueden obtener antecedentes de infección de absceso o perforación intestinal con translocación bacteriana . La infección clostridial representa el 10% de las infecciones de tipo I. Las especies de Clostridium implicadas son Clostridium perfringens , Clostridium septicum y Clostridium sordellii , que suelen causar gangrena gaseosa (también conocida como mionecrosis). Clostridium perfringens produce dos toxinas mortales: la toxina alfa y la toxina theta. La toxina alfa provoca una agregación plaquetaria excesiva que bloquea los vasos sanguíneos y priva a los órganos vitales del suministro de oxígeno. Esto crea un entorno ácido y deficiente en oxígeno para la proliferación de bacterias. Cuando la toxina alfa es absorbida por los tejidos blandos, puede inhibir la migración de glóbulos blancos de los vasos sanguíneos al tejido blando , lo que perjudica la función de los fagocitos . Las dos toxinas juntas pueden causar la destrucción de los glóbulos rojos en los vasos sanguíneos , daño a la integridad de los vasos sanguíneos y supresión de la función cardíaca. [ cita requerida ]
Paraclostridium sordellii también puede producir dos toxinas importantes: todas las cepas virulentas conocidas producen el factor de virulencia esencial toxina letal (TcsL), y varias también producen toxina hemorrágica (TcsH). TcsL y TcsH son miembros de la gran familia de citotoxinas clostridiales (LCC). [10] El factor de virulencia clave de Clostridium septicum es una toxina formadora de poros llamada toxina alfa, aunque no está relacionada con latoxina alfa de Clostridium perfringens . Las infecciones mionecróticas causadas por estas especies clostridiales ocurren comúnmente en usuarios de heroína inyectable . Aquellos con infecciones clostridiales generalmente tienen dolor intenso en el sitio de la herida, donde la herida generalmente drena sangre maloliente mezclada con suero (secreción serosanguinolenta). El shock puede progresar rápidamente después de la lesión o infección inicial, y una vez que se establece el estado de shock, la probabilidad de morir supera el 50%. Otra bacteria asociada con una progresión rápida similar de la enfermedad es la infección por estreptococos del grupo A (principalmente Streptococcus pyogenes ). Mientras tanto, otras infecciones bacterianas requieren dos o más días para volverse sintomáticas. [2]
Infección de tipo II : Esta infección representa entre el 20 y el 30% de los casos y afecta principalmente a las extremidades. [4] [11] Esta infección afecta principalmente a la bacteria Streptococcus pyogenes , sola o en combinación con infecciones estafilocócicas. Ambos tipos de bacterias pueden progresar rápidamente y manifestarse como síndrome de choque tóxico . Las especies de Streptococcus producen proteína M , que actúa como un superantígeno , estimulando una respuesta inmunitaria sistémica masiva que no es efectiva contra el antígeno bacteriano, precipitando el choque. La infección de tipo II afecta más comúnmente a adultos jóvenes y sanos con antecedentes de lesiones. [2]
Infección de tipo III : Vibrio vulnificus , una bacteria presente en el agua salada , es una causa poco frecuente de esta infección, que se produce a través de una herida en la piel. La progresión de la enfermedad es similar a la del tipo II, pero a veces con cambios cutáneos poco visibles. [2]
Infección de tipo IV : La infección de tipo IV, que representa menos del 1% de los casos, es causada por el hongo Candida albicans . Los factores de riesgo incluyen la edad y la inmunodeficiencia. [4] [12]

El diagnóstico precoz es difícil, ya que la enfermedad suele parecer una simple infección superficial de la piel . [4] Aunque varias modalidades de laboratorio y de diagnóstico por imágenes pueden hacer sospechar la existencia de fascitis necrosante, ninguna puede descartarla. [14] El estándar de oro para el diagnóstico es una exploración quirúrgica en un entorno de alta sospecha. En caso de duda, se puede realizar una pequeña incisión en el tejido afectado y, si un dedo separa fácilmente el tejido a lo largo del plano fascial , se confirma el diagnóstico y se debe realizar un desbridamiento extenso. [2]
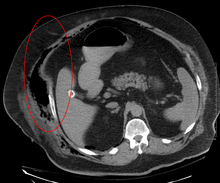
Las imágenes tienen un papel limitado en el diagnóstico de la fascitis necrosante. El tiempo de demora en la realización de las imágenes es una preocupación importante. La radiografía simple puede mostrar enfisema subcutáneo (gas en el tejido subcutáneo ), lo que sugiere fuertemente cambios necrosantes, pero no es lo suficientemente sensible para detectar todos los casos, porque las infecciones cutáneas necrosantes causadas por bacterias distintas de las infecciones clostridiales generalmente no muestran enfisema subcutáneo. Si el diagnóstico aún está en duda, las tomografías computarizadas (TC) y las imágenes por resonancia magnética (IRM) son modalidades más sensibles que la radiografía simple. Sin embargo, tanto la TC como la RM no son lo suficientemente sensibles para descartar por completo los cambios necrosantes. [2] La TC puede mostrar engrosamiento fascial, edema, gas subcutáneo y formación de abscesos. [2] En la RM, cuando se produce una acumulación de líquido con afectación de la fascia profunda, engrosamiento o realce con la inyección de contraste , se debe sospechar firmemente la fascitis necrosante. Mientras tanto, la ecografía puede mostrar la formación de abscesos superficiales, pero no es lo suficientemente sensible para diagnosticar la fascitis necrosante. [2] La tomografía computarizada puede detectar alrededor del 80% de los casos, mientras que la resonancia magnética puede detectar un poco más. [15]
Un recuento de glóbulos blancos superior a 15.000 células/mm 3 y un nivel de sodio sérico inferior a 135 mmol/L tienen una sensibilidad del 90% para detectar la infección necrosante de tejidos blandos. [ cita requerida ] También tiene una probabilidad del 99% de descartar cambios necrosantes si los valores han demostrado lo contrario . Se están desarrollando varios sistemas de puntuación para determinar la probabilidad de contraer fascitis necrosante, pero un sistema de puntuación desarrollado por Wong y colegas en 2004 es el más utilizado. Es la puntuación del indicador de riesgo de laboratorio para fascitis necrosante (LRINEC), que se puede utilizar para estratificar por riesgo a aquellas personas que tienen signos de celulitis grave o absceso para determinar la probabilidad de que exista fascitis necrosante. Utiliza seis valores de laboratorio: proteína C reactiva , recuento total de glóbulos blancos , hemoglobina , sodio , creatinina y glucosa en sangre . [2] Una puntuación de 6 o más indica que se debe considerar seriamente la fascitis necrosante. [16] Los criterios de puntuación son:
Sin embargo, el sistema de puntuación no ha sido validado. Los valores serían falsamente positivos si estuvieran presentes otras afecciones inflamatorias. Por lo tanto, los valores derivados de este sistema de puntuación deben interpretarse con precaución. [2] Alrededor del 10% de los pacientes con fascitis necrosante en el estudio original todavía tenían una puntuación LRINEC <6. [16] Un estudio de validación mostró que los pacientes con una puntuación LRINEC ≥6 tienen una mayor tasa de muerte y amputación. [18]
La fascitis necrosante se puede prevenir en parte con un buen cuidado de las heridas y el lavado de manos. [3]
El desbridamiento quirúrgico (extirpación del tejido afectado) es la base del tratamiento de la fascitis necrosante. El tratamiento médico temprano suele ser presuntivo; por lo tanto, se deben iniciar antibióticos tan pronto como se sospeche esta afección. Se toman cultivos de tejido (en lugar de hisopos de la herida) para determinar la cobertura antibiótica adecuada, y los antibióticos pueden cambiarse en función de los resultados. Además del control de la presión arterial y la hidratación, se debe iniciar el apoyo para aquellos con signos vitales inestables y baja producción de orina. [2]
El desbridamiento agresivo de la herida debe realizarse de manera temprana, generalmente tan pronto como se realiza el diagnóstico de infección necrosante de tejidos blandos (INTB). Las incisiones quirúrgicas a menudo se extienden más allá de las áreas de induración (el tejido endurecido) para eliminar los vasos sanguíneos dañados que son responsables de la induración. Sin embargo, los tejidos blandos celulíticos a veces se salvan del desbridamiento para cubrir posteriormente la herida con piel. Se puede utilizar más de una operación para eliminar tejido necrótico adicional. En algunos casos cuando una extremidad se ve afectada por una INTB, la amputación puede ser el tratamiento quirúrgico de elección. Después del desbridamiento de la herida, se deben aplicar apósitos adecuados para evitar la exposición de huesos, tendones y cartílagos para que dichas estructuras no se sequen y para promover la cicatrización de la herida. [2]
En el caso de una infección necrosante de la zona perineal (gangrena de Fournier), el desbridamiento y el cuidado de la herida en esta zona pueden resultar difíciles debido a los productos excretores que a menudo ensucian esta zona y afectan el proceso de cicatrización de la herida. Por lo tanto, los cambios regulares de apósitos con un sistema de gestión fecal pueden ayudar a mantener limpia la herida en la zona perineal. A veces, puede ser necesaria una colostomía para desviar los productos excretores y mantener limpia la herida en la zona perineal. [2]
Los antibióticos empíricos suelen iniciarse tan pronto como se realiza el diagnóstico de la NSTI y luego se cambian a una terapia antibiótica guiada por cultivo. En el caso de las NSTI, los antibióticos empíricos son de amplio espectro y cubren bacterias grampositivas (incluido el SAMR), gramnegativas y anaerobias. [19]
Si bien los estudios han comparado la moxifloxacina (una fluoroquinolona) y la amoxicilina-clavulanato (una penicilina) y han evaluado la duración adecuada del tratamiento (que varía de 7 a 21 días), no se pudieron sacar conclusiones definitivas sobre la eficacia del tratamiento, la duración ideal del tratamiento o los efectos adversos debido a la evidencia de baja calidad. [19]
La fascitis necrosante afecta a aproximadamente 0,4 de cada 100.000 personas por año en los Estados Unidos. [4] Se producen alrededor de 1.000 casos de fascitis necrosante por año en los Estados Unidos, pero las tasas han ido aumentando. Esto podría deberse a una mayor concienciación de esta afección, lo que lleva a un aumento de los informes, o a la virulencia bacteriana o al aumento de la resistencia bacteriana a los antibióticos. [2] En algunas zonas del mundo, es tan común como una de cada 100.000 personas. [4]
Se observan tasas más altas de fascitis necrosante en personas con obesidad o diabetes, y en aquellas que están inmunodeprimidas o son alcohólicas, o tienen enfermedad arterial periférica . Sin embargo, la enfermedad también puede ocurrir en adultos jóvenes y sanos sin enfermedades subyacentes. Los AINE pueden aumentar las tasas de infecciones necrosantes debido a la modificación de la respuesta inmune en el cuerpo, porque los AINE inhiben las enzimas cicloxigenasa -1 y cicloxigenasa-2 que son importantes en la producción de tromboxano y prostaglandina E2 . La prostaglandina ha sido responsable de la fiebre, la inflamación y el dolor. La inhibición de la producción de prostaglandina E2 reduce la respuesta inflamatoria y la adhesión de leucocitos, y por lo tanto reduce la respuesta inmune contra la invasión bacteriana, dando lugar a la infección de tejidos blandos. [2]
En el siglo V a. C., Hipócrates describió la infección necrosante de tejidos blandos como una enfermedad en la que los afectados tenían " erisipela por todo el cuerpo, aunque la causa era solo un accidente trivial. Los huesos, la carne y los tendones (cuerda, tendón o nervio) se caían del cuerpo y se producían muchas muertes". La primera descripción en inglés de la infección necrosante de tejidos blandos la hizo el cirujano británico Leonard Gillespie y los médicos británicos Gilbert Blaine y Thomas Trotter en el siglo XVIII. En aquella época, las infecciones necrosantes de tejidos blandos se conocían de diversas formas: "úlcera fagedenal" (ulceración que se extiende y destruye el tejido circundante), "fagedena gangrenosa", "úlcera gangrenosa", "úlcera maligna", "úlcera pútrida", "gangrena fulminante", "erisipela necrosante", "erisipela gangrenosa", "celulitis crepitante", "celulitis gangrenosa", "celulitis de Meleney", "celulitis sinérgica necrosante", "gangrena estreptocócica hemolítica", "gangrena sinérgica bacteriana progresiva" o "absceso necrosante". [20] Más tarde, el término "gangrena hospitalaria" se empezó a utilizar con más frecuencia. En 1871, el cirujano del ejército de los Estados Confederados Joseph Jones informó de 2.642 casos de gangrena hospitalaria con una tasa de mortalidad del 46%. En 1883, el Dr. Jean-Alfred Fournier describió la infección necrosante del perineo y el escroto , ahora llamada gangrena de Fournier . El término "fascitis necrosante" fue acuñado por Wilson en 1952. Su definición se ha ampliado para incluir no solo la infección de la fascia , sino también otras infecciones de tejidos blandos. [2] A pesar de que la comunidad médica lo desaprueba, el término "gangrena galopante" se utiliza con frecuencia en los medios de comunicación sensacionalistas para referirse a los brotes de fascitis necrosante. [21]