La intoxicación por paracetamol , también conocida como intoxicación por acetaminofeno , es causada por el uso excesivo del medicamento paracetamol (acetaminofén). [2] La mayoría de las personas tienen pocos síntomas o síntomas no específicos en las primeras 24 horas posteriores a la sobredosis. Estos síntomas incluyen sensación de cansancio, dolor abdominal o náuseas . Esto suele ir seguido de la ausencia de síntomas durante un par de días, después de lo cual aparece piel amarillenta , problemas de coagulación sanguínea y confusión como resultado de insuficiencia hepática . Las complicaciones adicionales pueden incluir insuficiencia renal , pancreatitis , niveles bajos de azúcar en sangre y acidosis láctica . Si no se produce la muerte, las personas tienden a recuperarse por completo en un par de semanas. [3] [4] Sin tratamiento, la muerte por toxicidad ocurre entre 4 y 18 días después. [5]
La intoxicación por paracetamol puede ocurrir accidentalmente o como un intento de suicidio . Los factores de riesgo de toxicidad incluyen el alcoholismo , la desnutrición y la toma de otros medicamentos hepatotóxicos . [1] El daño hepático no es resultado del paracetamol en sí, sino de uno de sus metabolitos , la N -acetil- p -benzoquinona imina (NAPQI). [6] La NAPQI disminuye el glutatión del hígado y daña directamente las células del hígado. [7] El diagnóstico se basa en el nivel de paracetamol en sangre en momentos específicos después de la toma del medicamento. [1] Estos valores a menudo se grafican en el nomograma de Rumack-Matthew para determinar el nivel de preocupación. [1]
El tratamiento puede incluir carbón activado si la persona busca ayuda médica poco después de la sobredosis. [1] No se recomienda intentar obligar a la persona a vomitar . [6] Si existe un potencial de toxicidad, se recomienda el antídoto acetilcisteína . [1] El medicamento generalmente se administra durante al menos 24 horas. [6] Puede ser necesaria atención psiquiátrica después de la recuperación. [1] Puede ser necesario un trasplante de hígado si el daño al hígado se vuelve grave. La necesidad de trasplante a menudo se basa en un pH sanguíneo bajo , un lactato sanguíneo alto , una coagulación sanguínea deficiente o una encefalopatía hepática significativa . Con un tratamiento temprano, la insuficiencia hepática es rara. [6] La muerte ocurre en aproximadamente el 0,1% de los casos. [1]
La intoxicación por paracetamol se describió por primera vez en la década de 1960. [6] Las tasas de intoxicación varían significativamente entre regiones del mundo. [8] En los Estados Unidos ocurren más de 100.000 casos al año. [1] En el Reino Unido es el medicamento responsable del mayor número de sobredosis. [7] Los niños pequeños son los más comúnmente afectados. [1] En los Estados Unidos y el Reino Unido, el paracetamol es la causa más común de insuficiencia hepática aguda . [9] [1]
Los signos y síntomas de la toxicidad del paracetamol se presentan en tres fases. La primera fase comienza a las pocas horas de la sobredosis y consiste en náuseas , vómitos, palidez y sudoración . [10] Sin embargo, los pacientes a menudo no presentan síntomas específicos o solo presentan síntomas leves en las primeras 24 horas de intoxicación. En raras ocasiones, después de sobredosis masivas, los pacientes pueden desarrollar síntomas de acidosis metabólica y coma al comienzo de la intoxicación. [11] [12]
La segunda fase ocurre entre 24 y 72 horas después de la sobredosis y consiste en signos de daño hepático creciente. En general, el daño ocurre en las células hepáticas a medida que metabolizan el paracetamol. La patología característica en la biopsia hepática incluye regiones de necrosis coagulativa en la zona 3 del acino hepático , alrededor de las vénulas centrales , ya que estos hepatocitos tienen concentraciones más altas de enzimas del citocromo P450 en comparación con los hepatocitos de la zona 1 que rodean la vénula portal del acino. Los hepatocitos viables restantes con frecuencia muestran lesión por abombamiento y esteatosis . [13] El individuo puede experimentar dolor abdominal en el cuadrante superior derecho . El daño hepático creciente también cambia los marcadores bioquímicos de la función hepática; el índice internacional normalizado (INR) y las transaminasas hepáticas ALT y AST aumentan a niveles anormales. [14] La insuficiencia renal aguda también puede ocurrir durante esta fase, generalmente causada por el síndrome hepatorrenal o el síndrome de disfunción orgánica múltiple . En algunos casos, la insuficiencia renal aguda puede ser la manifestación clínica primaria de la toxicidad. En estos casos, se ha sugerido que el metabolito tóxico se produce más en los riñones que en el hígado. [15]
La tercera fase sigue a los 3 a 5 días, y está marcada por complicaciones de necrosis hepática masiva que conduce a insuficiencia hepática fulminante con complicaciones de defectos de coagulación , bajo nivel de azúcar en sangre , insuficiencia renal, encefalopatía hepática , hinchazón cerebral , sepsis , insuficiencia orgánica múltiple y muerte. [10] Si se sobrevive a la tercera fase, la necrosis hepática sigue su curso y la función hepática y renal generalmente regresa a la normalidad en unas pocas semanas. [16] La gravedad de la toxicidad del paracetamol varía según la dosis y si se recibe el tratamiento adecuado.
La dosis tóxica de paracetamol es muy variable. En general, la dosis diaria máxima recomendada para adultos sanos es de 4 gramos. [17] [18] Las dosis más altas aumentan el riesgo de toxicidad. En adultos, dosis únicas superiores a 10 gramos o 200 mg/kg de peso corporal, lo que sea menor, tienen una probabilidad razonable de causar toxicidad. [19] [20] La toxicidad también puede ocurrir cuando múltiples dosis más pequeñas en 24 horas exceden estos niveles. [20] Después de una dosis de 1 gramo de paracetamol cuatro veces al día durante dos semanas, los pacientes pueden esperar un aumento de la alanina transaminasa en su hígado a aproximadamente tres veces el valor normal. [21] Es poco probable que esta dosis provoque insuficiencia hepática . [22] Los estudios han demostrado que la hepatotoxicidad significativa es poco común en pacientes que han tomado dosis mayores de lo normal durante 3 a 4 días. [23] En adultos, una dosis de 6 gramos al día durante las 48 horas anteriores podría potencialmente producir toxicidad, [20] mientras que en niños dosis agudas superiores a 200 mg/kg podrían potencialmente causar toxicidad. [24] La sobredosis aguda de paracetamol en niños rara vez causa enfermedad o muerte, y es muy poco común que los niños tengan niveles que requieran tratamiento, siendo las dosis crónicas mayores de lo normal la principal causa de toxicidad en niños. [20]
La sobredosis intencional (autoenvenenamiento con intención suicida) se asocia frecuentemente a la toxicidad del paracetamol. [25] En una revisión de 2006, el paracetamol fue el compuesto ingerido con mayor frecuencia en casos de sobredosis intencional. [26]
En raras ocasiones, la toxicidad del paracetamol puede ser consecuencia del uso normal. [27] Esto puede deberse a diferencias individuales (" idiosincrásicas ") en la expresión y actividad de ciertas enzimas en una de las vías metabólicas que manejan el paracetamol (ver metabolismo del paracetamol ).
Varios factores pueden aumentar potencialmente el riesgo de desarrollar toxicidad por paracetamol. El consumo excesivo crónico de alcohol puede inducir CYP2E1 , aumentando así la toxicidad potencial del paracetamol. En un estudio de pacientes con lesión hepática, el 64% informó ingestas de alcohol de más de 80 gramos al día, mientras que el 35% tomó 60 gramos al día o menos. [28] Algunos toxicólogos clínicos han debatido si el alcoholismo crónico debe considerarse un factor de riesgo. [29] [30] Para los consumidores crónicos de alcohol, la ingestión aguda de alcohol en el momento de una sobredosis de paracetamol puede tener un efecto protector. [29] [31] Para los consumidores no crónicos de alcohol, el consumo agudo de alcohol no tuvo ningún efecto protector.
El ayuno es un factor de riesgo, posiblemente debido al agotamiento de las reservas hepáticas de glutatión. [20] El uso concomitante del inductor de CYP2E1 isoniazida aumenta el riesgo de hepatotoxicidad, aunque no está claro si la inducción de 2E1 está relacionada con la hepatotoxicidad en este caso. [32] [33] El uso concomitante de otros fármacos que inducen enzimas CYP, como antiepilépticos como carbamazepina , fenitoína y barbitúricos , también se han descrito como factores de riesgo. [34]

Cuando se toma en dosis terapéuticas normales, se ha demostrado que el paracetamol es seguro. [14] Después de una dosis terapéutica, se convierte principalmente en metabolitos no tóxicos a través del metabolismo de fase II por conjugación con sulfato y glucurónido , y una pequeña porción se oxida a través del sistema enzimático del citocromo P450 . [35] Los citocromos P450 2E1 y 3A4 convierten aproximadamente el 5% del paracetamol en un metabolito intermediario altamente reactivo, N -acetil- p -benzoquinona imina (NAPQI). [35] [14] [36] [37] [38] En condiciones normales, NAPQI se desintoxica por conjugación con glutatión para formar conjugados de cisteína y ácido mercaptúrico. [35] [39]
En caso de sobredosis de paracetamol, las vías de sulfato y glucurónido se saturan y se desvía más paracetamol al sistema del citocromo P450 para producir NAPQI. Como resultado, los suministros hepatocelulares de glutatión se agotan, ya que la demanda de glutatión es mayor que su regeneración. [39] Por lo tanto, NAPQI permanece en su forma tóxica en el hígado y reacciona con las moléculas de la membrana celular , lo que resulta en daño generalizado y muerte de los hepatocitos , lo que conduce a una necrosis hepática aguda. [35] [40] En estudios con animales, las reservas de glutatión del hígado deben agotarse a menos del 70% de los niveles normales antes de que se produzca toxicidad hepática. [36]
_line.pdf/page1-440px-Rumack_Matthew_nomogram_with_treatment_(study)_line.pdf.jpg)
El historial de toma de paracetamol de una persona es algo preciso para el diagnóstico. [41] La forma más eficaz de diagnosticar una intoxicación es mediante la obtención de un nivel de paracetamol en sangre. Un nomograma de fármacos desarrollado en 1975, llamado nomograma de Rumack-Matthew , estima el riesgo de toxicidad basándose en la concentración sérica de paracetamol a un número determinado de horas después de la ingestión. [10] Para determinar el riesgo de hepatotoxicidad potencial, se traza el nivel de paracetamol a lo largo del nomograma. El uso de un nivel sérico de paracetamol cronometrado trazado en el nomograma parece ser el mejor marcador que indica el potencial de lesión hepática. [20] Un nivel de paracetamol obtenido en las primeras cuatro horas después de la ingestión puede subestimar la cantidad en el sistema porque el paracetamol todavía puede estar en proceso de ser absorbido desde el tracto gastrointestinal . Por lo tanto, no se recomienda un nivel sérico tomado antes de las 4 horas. [19]
La evidencia clínica o bioquímica de toxicidad hepática puede desarrollarse en uno a cuatro días, aunque, en casos graves, puede ser evidente en 12 horas. [42] Puede haber dolor en el cuadrante superior derecho del abdomen que puede ayudar en el diagnóstico. Los estudios de laboratorio pueden mostrar evidencia de necrosis hepática con AST elevada , ALT , bilirrubina y tiempos de coagulación prolongados, particularmente un tiempo de protrombina elevado . [43] Después de una sobredosis de paracetamol, cuando AST y ALT superan las 1000 UI/L, se puede diagnosticar hepatotoxicidad inducida por paracetamol. [42] En algunos casos, los niveles de AST y ALT pueden superar las 10 000 UI/L. [44]
El paracetamol puede cuantificarse en sangre, plasma u orina como herramienta diagnóstica en situaciones de intoxicación clínica o para ayudar en la investigación médico-legal de muertes sospechosas. La concentración en suero después de una dosis típica de paracetamol suele alcanzar un máximo inferior a 30 mg/L, lo que equivale a 200 μmol/L. [45] A menudo se observan niveles de 30-300 mg/L (200-2000 μmol/L) en pacientes con sobredosis. Los niveles sanguíneos post mortem han oscilado entre 50 y 400 mg/L en personas que mueren debido a una sobredosis aguda. Actualmente se utilizan técnicas colorimétricas automatizadas , cromatografía de gases y cromatografía líquida para el análisis de laboratorio del fármaco en muestras fisiológicas. [46] [47]
En algunos países se ha intentado limitar la disponibilidad de comprimidos de paracetamol. En el Reino Unido, las ventas de paracetamol sin receta están restringidas a paquetes de 32 comprimidos de 500 mg en farmacias y 16 comprimidos de 500 mg en establecimientos no farmacéuticos. Los farmacéuticos pueden proporcionar hasta 100 comprimidos a personas con enfermedades crónicas a discreción del farmacéutico. [48] [49] En Irlanda, los límites son 24 y 12 comprimidos, respectivamente. [50] Un estudio posterior sugiere que la disponibilidad reducida en grandes cantidades tuvo un efecto significativo en la reducción de las muertes por intoxicación por sobredosis de paracetamol. [51]
Un método de prevención sugerido es hacer que el paracetamol sea un medicamento de venta con receta médica o retirarlo por completo del mercado. Sin embargo, la sobredosis es un problema relativamente menor; por ejemplo, el 0,08% de la población del Reino Unido (más de 50.000 personas) presenta una sobredosis de paracetamol cada año. En cambio, el paracetamol es un medicamento seguro y eficaz que millones de personas toman sin complicaciones. [52] Además, los analgésicos alternativos, como la aspirina, son más tóxicos en caso de sobredosis, mientras que los antiinflamatorios no esteroideos se asocian a más efectos adversos tras su uso normal. [53]
Una estrategia para reducir el daño causado por las sobredosis de paracetamol es vender paracetamol precombinado en tabletas, ya sea con un emético [52] o un antídoto. Paradote era una tableta vendida en el Reino Unido que combinaba 500 mg de paracetamol con 100 mg de metionina [54] , un aminoácido que anteriormente [20] se usaba en el tratamiento de la sobredosis de paracetamol.
Hasta el momento no se han realizado estudios sobre la eficacia del paracetamol cuando se administra en combinación con su antídoto más comúnmente utilizado, la acetilcisteína. [55]
El calcitriol , el metabolito activo de la vitamina D 3 , parece ser un catalizador para la producción de glutatión. [56] Se encontró que el calcitriol aumentaba los niveles de glutatión en cultivos primarios de astrocitos de rata en promedio un 42%, aumentando las concentraciones de proteína glutatión de 29 nmol/mg a 41 nmol/mg, 24 y 48 horas después de la administración; continuó teniendo una influencia en los niveles de glutatión 96 horas después de la administración. [57] Se ha propuesto que la coadministración de calcitriol, mediante inyección, puede mejorar los resultados del tratamiento.
El profármaco éster de paracetamol que contiene ácido L-piroglutámico (PGA), un precursor biosintético del glutatión, se ha sintetizado para reducir la hepatotoxicidad del paracetamol y mejorar la biodisponibilidad . Los estudios toxicológicos de diferentes ésteres de paracetamol muestran que el carboxilato de L-5-oxo-pirrolidina-2-paracetamol reduce la toxicidad después de la administración de una sobredosis de paracetamol a ratones. Los valores de glutatión hepático en ratones inducidos por inyección intraperitoneal del éster son superponibles con los niveles de GSH registrados en el grupo de control de ratones no tratados. El grupo de ratones tratados con una dosis equivalente de paracetamol mostró una disminución significativa del glutatión del 35% (p < 0,01 frente al grupo de control no tratado). Se encontró que la LD50 oral era mayor de 2000 mg kg-1, mientras que la LD50 intraperitoneal fue de 1900 mg kg-1. Estos resultados, junto con los buenos datos de hidrólisis y biodisponibilidad, muestran que este éster es un candidato potencial como profármaco del paracetamol. [58]
En adultos, el tratamiento inicial para la sobredosis de paracetamol es la descontaminación gastrointestinal. La absorción de paracetamol en el tracto gastrointestinal se completa en dos horas en circunstancias normales, por lo que la descontaminación es más útil si se realiza dentro de este período de tiempo. El lavado gástrico , mejor conocido como lavado de estómago, puede considerarse si la cantidad ingerida es potencialmente mortal y el procedimiento puede realizarse dentro de los 60 minutos posteriores a la ingestión. [59] La administración de carbón activado es el procedimiento de descontaminación gastrointestinal más común, ya que adsorbe eficazmente el paracetamol, lo que reduce su absorción gastrointestinal. [60] [61] La administración de carbón activado también presenta un menor riesgo de aspiración que el lavado gástrico. [62]
Parece que el mayor beneficio del carbón activado se obtiene si se administra dentro de los 30 minutos a dos horas de la ingestión. [63] [62] La administración de carbón activado después de 2 horas se puede considerar en pacientes que pueden tener un vaciamiento gástrico retrasado debido a medicamentos co-ingeridos o después de la ingestión de preparaciones de paracetamol de liberación sostenida o retardada. El carbón activado también debe administrarse si los medicamentos co-ingeridos justifican la descontaminación. [42] Hubo reticencia a administrar carbón activado en sobredosis de paracetamol, debido a la preocupación de que también pueda absorber el antídoto oral acetilcisteína. [64] Los estudios han demostrado que se absorbe un 39% menos de acetilcisteína en el cuerpo cuando se administran juntos. [65] Hay recomendaciones contradictorias sobre si cambiar la dosis de acetilcisteína oral después de la administración de carbón activado, e incluso si la dosis de acetilcisteína necesita ser alterada en absoluto. [65] [66] La acetilcisteína intravenosa no tiene interacción con el carbón activado.
La inducción del vómito con jarabe de ipecacuana no tiene ningún papel en la sobredosis de paracetamol porque el vómito que induce retrasa la administración efectiva de carbón activado y acetilcisteína oral. [19] La lesión hepática es extremadamente rara después de la ingestión accidental aguda en niños menores de 6 años de edad. Los niños con exposiciones accidentales no requieren descontaminación gastrointestinal ni con lavado gástrico, carbón activado ni jarabe de ipecacuana. [20]
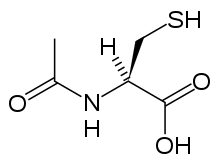
La acetilcisteína , también llamada N -acetilcisteína o NAC, actúa para reducir la toxicidad del paracetamol al reponer las reservas corporales del antioxidante glutatión . El glutatión reacciona con el metabolito tóxico NAPQI para que no dañe las células y pueda excretarse de forma segura. [67] La NAC generalmente se administraba siguiendo un nomograma de tratamiento (uno para pacientes con factores de riesgo y otro para aquellos sin ellos), pero el uso del nomograma ya no se recomienda ya que la base de evidencia para respaldar el uso de factores de riesgo era pobre e inconsistente y muchos de los factores de riesgo son imprecisos y difíciles de determinar con suficiente certeza en la práctica clínica. [68] La cisteamina y la metionina también se han utilizado para prevenir la hepatotoxicidad, [69] aunque los estudios muestran que ambas están asociadas con más efectos adversos que la acetilcisteína. [20] Además, se ha demostrado que la acetilcisteína es un antídoto más eficaz, en particular en pacientes que presentan síntomas de insuficiencia hepática más de 8 horas después de la ingestión [70] y en aquellos que la presentan. [61]
Si la persona se presenta menos de ocho horas después de la sobredosis de paracetamol, entonces la acetilcisteína reduce significativamente el riesgo de hepatotoxicidad grave y garantiza la supervivencia. [20] Si la acetilcisteína se inicia más de 8 horas después de la ingestión, hay una marcada disminución en su eficacia porque la cascada de eventos tóxicos en el hígado ya ha comenzado, y el riesgo de necrosis hepática aguda y muerte aumenta dramáticamente. Aunque la acetilcisteína es más eficaz si se administra temprano, todavía tiene efectos beneficiosos si se administra tan tarde como 48 horas después de la ingestión. [71] Si la persona se presenta más de ocho horas después de la sobredosis de paracetamol, entonces el carbón activado no es útil y la acetilcisteína se inicia inmediatamente. En presentaciones más tempranas, el carbón se puede administrar cuando llega el paciente y se inicia la acetilcisteína mientras se espera que regresen los resultados del nivel de paracetamol del laboratorio. [20]
En la práctica de los Estados Unidos, la administración intravenosa (IV) y oral se consideran igualmente efectivas y seguras si se administran dentro de las 8 horas posteriores a la ingestión. [72] [73] Sin embargo, la IV es la única vía recomendada en la práctica de Australasia y Gran Bretaña. [20] [74] La acetilcisteína oral se administra como una dosis de carga de 140 mg/kg seguida de 70 mg/kg cada cuatro horas durante 17 dosis más, y si el paciente vomita dentro de la hora posterior a la dosis, la dosis debe repetirse. [75] [76] La acetilcisteína oral puede ser mal tolerada debido a su sabor y olor desagradables y su tendencia a causar náuseas y vómitos. [72] Si se indican dosis repetidas de carbón debido a otro fármaco ingerido, entonces las dosis posteriores de carbón y acetilcisteína deben escalonarse. [42]
La acetilcisteína intravenosa se administra como una infusión continua durante 20 horas para una dosis total de 300 mg/kg. La administración recomendada implica la infusión de una dosis de carga de 150 mg/kg durante 15 a 60 minutos, seguida de una infusión de 50 mg/kg durante cuatro horas; los últimos 100 mg/kg se infunden durante las 16 horas restantes del protocolo. [20] La acetilcisteína intravenosa tiene la ventaja de acortar la estancia hospitalaria, aumentar la comodidad tanto del médico como del paciente y permitir la administración de carbón activado para reducir la absorción tanto del paracetamol como de cualquier fármaco ingerido conjuntamente sin preocupaciones por la interferencia con la acetilcisteína oral. [77] [ necesita actualización ] La dosificación intravenosa varía con el peso, específicamente en niños. Para pacientes de menos de 20 kg, la dosis de carga es de 150 mg/kg en 3 mL/kg de diluyente, administrada durante 60 minutos; La segunda dosis es de 50 mg/kg en un diluyente de 7 mL/kg durante 4 horas; y la tercera y última dosis es de 100 mg/kg en un diluyente de 14 mL/kg durante 16 horas. [76] Debido al riesgo de eventos adversos, se han sugerido alteraciones electrolíticas y cambios de fluidos asociados con dosis más altas de regímenes de limitación de dosis de acetilcisteína. Hasta la fecha, no se ha observado un mayor riesgo de lesión o insuficiencia hepática con esta estrategia de limitación de dosis. [78]
El efecto adverso más común del tratamiento con acetilcisteína es una reacción anafilactoide , que generalmente se manifiesta por erupción cutánea, sibilancias o hipotensión leve . Las reacciones adversas son más comunes en personas tratadas con acetilcisteína IV y ocurren hasta en el 20 % de los pacientes. [79] [80] Es más probable que ocurran reacciones anafilactoides con la primera infusión (la dosis de carga). [79] En raras ocasiones, pueden ocurrir reacciones graves potencialmente mortales en individuos predispuestos, como pacientes con asma o dermatitis atópica, y pueden caracterizarse por dificultad respiratoria, hinchazón facial e incluso la muerte. [79] [81] [82]
Si se produce una reacción anafilactoide, se suspende o reduce temporalmente la acetilcisteína y se administran antihistamínicos y otros tratamientos de apoyo. [79] [83] [84] Por ejemplo, un beta-agonista nebulizado como el salbutamol puede estar indicado en caso de broncoespasmo significativo (o de forma profiláctica en pacientes con antecedentes de broncoespasmo secundario a la acetilcisteína). También es importante controlar de cerca los líquidos y los electrolitos. [79]
En las personas que desarrollan insuficiencia hepática aguda o que se espera que mueran por insuficiencia hepática, el pilar del tratamiento es el trasplante de hígado . [52] Los trasplantes de hígado se realizan en centros especializados. Los criterios más utilizados para el trasplante de hígado fueron desarrollados por médicos del King's College Hospital de Londres. Se recomienda el trasplante a los pacientes si tienen un pH de sangre arterial inferior a 7,3 después de la reanimación con líquidos o si un paciente tiene encefalopatía de grado III o IV, un tiempo de protrombina superior a 100 segundos y una creatinina sérica superior a 300 mmol/L en un período de 24 horas. [85] Se han utilizado otras formas de apoyo hepático, incluidos los trasplantes de hígado parciales. Estas técnicas tienen la ventaja de apoyar al paciente mientras su propio hígado se regenera. Una vez que la función hepática regresa, se comienzan a administrar medicamentos inmunosupresores y deben tomar medicamentos inmunosupresores durante el resto de sus vidas. [86] [87]
La tasa de mortalidad por sobredosis de paracetamol aumenta dos días después de la ingestión, alcanza un máximo el día cuatro y luego disminuye gradualmente. La acidosis es el indicador individual más importante de mortalidad probable y la necesidad de trasplante. Se informó una tasa de mortalidad del 95% sin trasplante en pacientes que tenían un pH documentado menor de 7,30. Otros indicadores de mal pronóstico incluyen enfermedad renal crónica (estadio 3 o peor), encefalopatía hepática , un tiempo de protrombina notablemente elevado o un nivel elevado de ácido láctico en sangre ( acidosis láctica ). [85] [88] Un estudio ha demostrado que un nivel de factor V menor del 10% de lo normal indica un mal pronóstico (mortalidad del 91%), mientras que una relación de factor VIII a factor V menor de 30 indica un buen pronóstico (supervivencia del 100%). [89] Los pacientes con un mal pronóstico generalmente se identifican para un probable trasplante de hígado. [85] Se espera que los pacientes que no mueren se recuperen completamente y tengan una expectativa de vida y calidad de vida normales . [90]
Muchos medicamentos de venta libre y con receta contienen paracetamol. Debido a su amplia disponibilidad, junto con una toxicidad comparativamente alta (en comparación con el ibuprofeno y la aspirina ), existe un potencial mucho mayor de sobredosis. [91] La toxicidad por paracetamol es una de las causas más comunes de intoxicación en todo el mundo. [25] En los Estados Unidos, el Reino Unido, Australia y Nueva Zelanda, el paracetamol es la causa más común de sobredosis de drogas. [20] [92] [93] Además, tanto en los Estados Unidos como en el Reino Unido es la causa más común de insuficiencia hepática aguda. [94] [9]
En Inglaterra y Gales se estima que se produjeron 41.200 casos de intoxicación por paracetamol entre 1989 y 1990, con una mortalidad del 0,40%. Se calcula que cada año se producen entre 150 y 200 muertes y entre 15 y 20 trasplantes de hígado como resultado de la intoxicación en Inglaterra y Gales. [80] La sobredosis de paracetamol da lugar a más llamadas a los centros de control de intoxicaciones en los EE. UU. que la sobredosis de cualquier otra sustancia farmacológica, lo que representa más de 100.000 llamadas, así como 56.000 visitas a urgencias, 2.600 hospitalizaciones y 458 muertes por insuficiencia hepática aguda al año. [95] Un estudio de casos de insuficiencia hepática aguda entre noviembre de 2000 y octubre de 2004 realizado por los Centros para el Control y la Prevención de Enfermedades de los EE. UU. encontró que el paracetamol era la causa del 41% de todos los casos en adultos y del 25% de los casos en niños. [96]
{{cite journal}}: CS1 maint: varios nombres: lista de autores ( enlace ){{cite journal}}: CS1 maint: varios nombres: lista de autores ( enlace ){{cite journal}}: CS1 maint: varios nombres: lista de autores ( enlace )