Metaloproteína
La presencia de los iones metálicos en las metaloenzimas les permite llevar a cabo funciones tales como reacciones redox que no pueden ser fácilmente realizadas por el conjunto limitado de grupos funcionales que se encuentran en los aminoácidos.
En la oxigenación los dos átomos de cobre(I) del sitio activo se oxidan a cobre(II) y las moléculas de dioxígeno se reducen a peróxido, O22-.
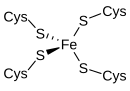
[9][10] La rubredoxina es un portador de electrones encontrado en bacterias y arqueas que metabolizan azufre.
En ambos estados de oxidación del metal hay un alto espín lo que ayuda a minimizar los cambios estructurales.
La naturaleza exacta del sitio de unión no se ha determinado todavía.
Exhibe actividad oxidasa, la cual está asociada con la posible oxidación del Fe2+ (ion ferroso) en Fe3+ (ion férrico), por lo tanto, ayuda en su transporte en el plasma, en asociación con la transferrina, que sólo pueden llevar el hierro en estado férrico.
Las metaloenzimas tienen una característica en común, que el ion metálico se une a la proteína con un sitio coordinación lábil.
Los iones metálicos catalizan reacciones que son difíciles de lograr en la química orgánica.
[13] La estructura de esta coenzima la determinó Dorothy Hodgkin, para lo cual recibió un premio Nobel.
La reacción puede ser escrita como: La estructura exacta del sitio activo ha sido difícil de determinar.
[17] El ion superóxido, O2- se genera en los sistemas biológicos por la reducción de oxígeno molecular.
Tiene un electrón desapareado, por lo que se comporta como un radical libre y es un poderoso agente oxidante.
Estas propiedades hacen que el ion superóxido sea muy tóxico y lo utilicen los fagocitos para matar a microorganismos invasores.
En caso contrario, el superóxido debe ser destruido antes de que haga daño no deseado a las células.
En humanos el metal activo es cobre, como Cu2+ o Cu+, coordinado como tetraedro por residuos de histidina.
Ni-SOD es particularmente interesante ya que involucra al níquel(III), un estado de oxidación inusual para este elemento.
Por el contrario, el fotón es absorbido por el anillo de clorina, cuya estructura electrónica está adaptada para este fin.
La calmodulina participa en los sistemas de señalización intracelular al actuar como un segundo mensajero ante los primeros estímulos.