Anexo:Isótopos de hidrógeno
El 2H (también H-2 o hidrógeno-2) es más comúnmente referido como deuterio mientras que el 3H (también H-3 o hidrógeno-3) es más aludido como tritio; también es común referirse a estos isótopos con los símbolos de D y T (en lugar de 2H y 3H) como si fueran elementos químicos puros; sin embargo la IUPAC ha declarado que si bien esta forma de referirse a estos isótopos es común, no es recomendable.
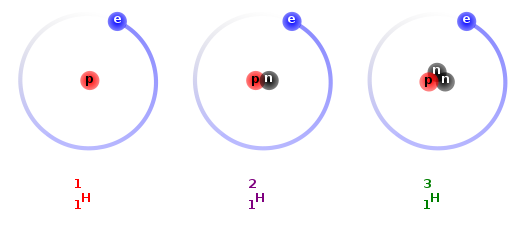
Al átomo de hidrógeno que no contiene ningún neutrón en su núcleo se le conoce como protio; sin embargo se le conoce más como simplemente hidrógeno o hidrógeno-1.
Debido a que su núcleo está compuesto por un único protón se le da el nombre descriptivo de protio; sin embargo este nombre es poco usado en la práctica, a diferencia de los nombres de los otros isótopos del hidrógeno que son más usados en las prácticas comunes.
El deuterio, hidrógeno-2, 2H o 2H es otro de los isótopos estables del hidrógeno; su núcleo atómico está compuesto por un protón y un neutrón.
El agua pesada es utilizada como moderador de neutrones y refrigerante en reactores nucleares.
Este isótopo es radioactivo; decae a helio-3 mediante desintegración beta, y tiene una vida media de 12,32 años.
El tritio es usado frecuentemente en marcaciones químicas y biológicas como marcador radioactivo.
[7] El hidrógeno-5, 5H o 5H es un isótopo altamente inestable del hidrógeno; su núcleo está compuesto por un protón y cuatro neutrones.
Los dos protones remanentes fueron detectados por el «telescopio RIKEN», un aparato compuesto por múltiples capas de sensores.