Aspectos biológicos del flúor
Tiene una amplia gama de aplicaciones biológicas en la ecología, la ciencia médica y la ingeniería bioquímica.
Los PFC (perfluorocarbonos) son capaces de contener suficiente oxígeno para permitir la respiración líquida humana.
Se han encontrado algunos compuestos organofluorados sintetizados naturalmente en microorganismos y plantas,[1] pero no en animales.
[3] Existen unas cuanrenta plantas verdes en Australia, Brasil y África que sintetizan este compuesto como defensa contra los herbívoros.
Otros organofluorados de síntesis biológica son los ω-fluoro ácidos grasoss, la fluoroacetona, y el 2-fluorocitrato, posiblemente biosintetizados en las vías bioquímicas del intermedio fluoroacetaldehido.
[2] En las bacterias, se ha aislado la enzima adenosil-fluoruro sintasa, capaz de catalizar la formación del enlace carbono-flúor.
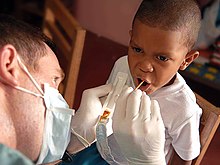
[6] Desde mediados del siglo XX, se ha podido discernir a partir de estudios poblacionales que el fluoruro reduce la caries dental.
Inicialmente, los investigadores plantearon la hipótesis de que el flúor ayuda a convertir la hidroxiapatita, presente en el esmalte dental, en fluorapatita, mineral menos soluble en ácido.
La teoría más aceptada actualmente es que el flúor previene las caries en las primeras etapas de su formación.
Si la caries no está demasiado avanzada, el flúor parece reducir la desmineralización y aumentar la remineralización.
[12] Una revisión sistemática en 2000 y 2007, mostró una reducción significativa de las caries en los niños asociada con la fluoración del agua.
Los barnices, que pueden ser aplicados más rápidamente, existen y realizan una función similar.
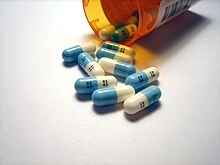
[15] El veinte por ciento de los medicamentos comercializados, contienen flúor, incluidos fármacos importantes en muchas clases farmacéuticas diferentes.
[16] Debido a la considerable estabilidad del enlace carbono-flúor, muchos fármacos están fluorados para retrasar su metabolismo y posterior eliminación.
Sin embargo, la sustitución de un flúor en una posición del anillo aromático lo protege e impide que se produzca el epóxido.
[18] Los fluoros también encuentran su uso en los mineralocorticoides comunes, una clase de fármacos que aumentan la presión arterial.
Los anestésicos fluorados modernos son más duraderos y casi insolubles en la sangre, lo que acelera la reanimación tras la anestesia.
Muchos otros antidepresivos del mismo tipo contienen flúor, como Celexa, Luvox y Lexapro.
[29] Además, los gases fluorados inertes tienen el potencial de ser una herramienta barata y eficiente para observar la ventilación pulmonar.
[36] La compañía Alliance Pharmaceuticals inició ensayos clínicos, abandonados por no presentar ventajas suficientes en comparación con otras terapias.
[39][40] Otros usos potenciales incluyen el buceo en aguas profundas y los viajes espaciales, aplicaciones que requieren una ventilación total, no parcial, con el líquido.
[49] Más tarde la Unión Europea lo prohibió, aunque Dow Agrosciences hizo un caso para cancelar la decisión en 2011.
De esta forma, el fluoruro atraviesa las membranas celulares y luego se une con el calcio e interfiere con diversas enzimas.
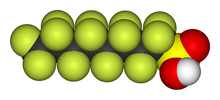
[69] Debido a la fuerza del enlace carbono-flúor, los organofluoruros no se descomponen en el medio ambiente.
Su distribución de tejido en humanos es desconocida, pero varios estudios en ratas sugieren que está presente principalmente en el hígado, el riñón y la sangre.
Muchos animales muestran diferencias sexuales en la capacidad de excretar PFOA, pero sin un patrón claro.
En dosis altas, tanto los PFOA como los PFOS causan cáncer y la muerte de recién nacidos en roedores.
[71][72][75] Las causas bioquímicas de la toxicidad tampoco son claras y pueden diferir según la molécula, la salud, e incluso el animal.
PPAR-alfa es una proteína que interactúa con PFOA y está comúnmente implicada en el cáncer de roedores.
[71][72][75] También se pueden detectar productos químicos fluorados (es decir, compuestos no perfluorados) en el medio ambiente.