El virus de Epstein-Barr ( EBV ), formalmente llamado gammaherpesvirus humano 4 , es uno de los nueve tipos de herpesvirus humanos conocidos de la familia del herpes y es uno de los virus más comunes en humanos. EBV es un virus de ADN de doble cadena . [2] El virus de Epstein-Barr (VEB) es el primer virus oncogénico identificado , que establece una infección permanente en humanos. El VEB causa mononucleosis infecciosa y también está estrechamente relacionado con muchas enfermedades malignas. Se probaron varias formulaciones de vacunas en diferentes animales o en humanos. Sin embargo, ninguno de ellos pudo prevenir la infección por EBV y hasta la fecha no se ha aprobado ninguna vacuna. [3]
El virus causa mononucleosis infecciosa ("mono" o "fiebre glandular"). También se asocia con diversas enfermedades linfoproliferativas no malignas, premalignas y malignas asociadas al virus de Epstein-Barr, como el linfoma de Burkitt , la linfohistiocitosis hemofagocítica , [4] y el linfoma de Hodgkin ; neoplasias malignas no linfoides tales como cáncer gástrico y carcinoma nasofaríngeo ; y afecciones asociadas con el virus de la inmunodeficiencia humana , como la leucoplasia vellosa y los linfomas del sistema nervioso central . [5] [6] El virus también está asociado con los trastornos infantiles del síndrome de Alicia en el país de las maravillas [7] y la ataxia cerebelosa aguda [8] y, según algunas pruebas, mayores riesgos de desarrollar ciertas enfermedades autoinmunes , [9] especialmente dermatomiositis , lupus eritematoso sistémico , artritis reumatoide y síndrome de Sjögren . [10] [11] Se cree que alrededor de 200.000 casos de cáncer al año en todo el mundo son atribuibles al EBV. [12] [13] En 2022, un gran estudio (con una población de 10 millones durante 20 años) sugirió que el EBV es la principal causa de esclerosis múltiple , y una infección reciente por EBV provoca un aumento de 32 veces en el riesgo de desarrollar esclerosis múltiple. [14] [15] [16] [17] [18]
La infección por EBV se produce por la transferencia oral de saliva [19] y secreciones genitales. La mayoría de las personas se infectan con EBV y adquieren inmunidad adaptativa . En Estados Unidos, aproximadamente la mitad de los niños de cinco años y alrededor del 90% de los adultos tienen evidencia de infección previa. [20] Los bebés se vuelven susceptibles al VEB tan pronto como desaparece la protección de los anticuerpos maternos . Muchos niños que se infectan con EBV no presentan síntomas o los síntomas son indistinguibles de otras enfermedades leves y breves de la infancia. [21] Cuando la infección ocurre durante la adolescencia o la edad adulta temprana, causa mononucleosis infecciosa del 35 al 50% de las veces. [22]
El VEB infecta las células B del sistema inmunológico y las células epiteliales . Una vez que se controla la infección lítica inicial del VEB , la latencia del VEB persiste en las células B de memoria del individuo por el resto de su vida. [19] [23] [24]
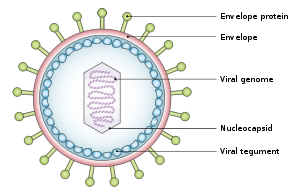
El virus tiene entre 122 y 180 nm de diámetro y está compuesto por una doble hélice de ácido desoxirribonucleico (ADN) que contiene alrededor de 172.000 pares de bases que codifican 85 genes . [19] El ADN está rodeado por una nucleocápside proteica , que está rodeada por un tegumento hecho de proteína, que a su vez está rodeado por una envoltura que contiene lípidos y proyecciones superficiales de glicoproteínas , que son esenciales para la infección de la célula huésped. [25] En julio de 2020, un equipo de investigadores informó sobre el primer modelo atómico completo de la nucleocápside del virus. Este "primer modelo atómico completo [incluye] la cápside icosaédrica, el complejo tegumentario asociado a la cápside (CATC) y el portal dodecamérico: el aparato de translocación del genoma viral". [26] [27]
El término tropismo viral se refiere a qué tipos de células infecta el EBV. El VEB puede infectar diferentes tipos de células, incluidas las células B y las células epiteliales . [28]
Los complejos virales de glicoproteínas de tres partes de gHgL gp42 median la fusión de la membrana de las células B; aunque los complejos de dos partes de gHgL median en la fusión de la membrana de las células epiteliales. Los EBV que se producen en las células B tienen un número bajo de complejos gHgLgp42, porque estos complejos de tres partes interactúan con las moléculas de antígeno leucocitario humano de clase II presentes en las células B en el retículo endoplásmico y se degradan. Por el contrario, los EBV de las células epiteliales son ricos en complejos de tres partes porque estas células normalmente no contienen moléculas HLA de clase II . Como consecuencia, el EBV elaborado a partir de células B es más infeccioso para las células epiteliales, y el EBV elaborado a partir de células epiteliales es más infeccioso para las células B. Los virus que carecen de la porción gp42 pueden unirse a las células B humanas, pero no pueden infectar. [29]

El VEB puede infectar tanto a las células B como a las células epiteliales. Los mecanismos para ingresar a estas dos células son diferentes.
Para ingresar a las células B, la glicoproteína viral gp350 se une al receptor celular CD21 (también conocido como CR2). [30] Luego, la glicoproteína viral gp42 interactúa con las moléculas celulares del MHC de clase II . Esto desencadena la fusión de la envoltura viral con la membrana celular, lo que permite que el EBV ingrese a las células B. [25] El CD35 humano, también conocido como receptor 1 del complemento (CR1), es un factor de unión adicional para gp350/220 y puede proporcionar una ruta para la entrada del VEB en las células CD21 negativas, incluidas las células B inmaduras. La infección por EBV regula negativamente la expresión de CD35. [31]
Para ingresar a las células epiteliales, la proteína viral BMRF-2 interactúa con las integrinas β1 celulares . Luego, la proteína viral gH/gL interactúa con las integrinas celulares αvβ6/αvβ8. Esto desencadena la fusión de la envoltura viral con la membrana de la célula epitelial, lo que permite que el EBV ingrese a la célula epitelial. [25] A diferencia de la entrada de células B, la entrada de células epiteliales en realidad está impedida por la glicoproteína viral gp42. [30]
Una vez que el EBV ingresa a la célula, la cápside viral se disuelve y el genoma viral se transporta al núcleo celular . [ cita necesaria ]
El ciclo lítico , o infección productiva, da como resultado la producción de viriones infecciosos . El VEB puede sufrir replicación lítica tanto en células B como en células epiteliales. En las células B, la replicación lítica normalmente sólo tiene lugar después de la reactivación de la latencia. En las células epiteliales, la replicación lítica a menudo sigue directamente a la entrada viral. [25]
Para que se produzca la replicación lítica, el genoma viral debe ser lineal. El genoma latente del EBV es circular, por lo que debe linealizarse en el proceso de reactivación lítica. Durante la replicación lítica, la ADN polimerasa viral es responsable de copiar el genoma viral. Esto contrasta con la latencia, en la que la ADN polimerasa de la célula huésped copia el genoma viral. [25]
Los productos del gen lítico se producen en tres etapas consecutivas: inmediata-temprana, temprana y tardía. [25] Los productos de genes líticos inmediatos tempranos actúan como transactivadores , mejorando la expresión de genes líticos posteriores. Los productos de genes líticos tempranos inmediatos incluyen BZLF1 (también conocido como Zta, EB1, asociado con su gen producto ZEBRA ) y BRLF1 (asociado con su gen producto Rta ). [25] Los productos de genes líticos tempranos tienen muchas más funciones, como la replicación, el metabolismo y el bloqueo del procesamiento de antígenos . Los primeros productos de genes líticos incluyen BLNF2. [25] Finalmente, los productos de genes líticos tardíos tienden a ser proteínas con funciones estructurales, como VCA , que forma la cápside viral . Otros productos de genes líticos tardíos, como BCRF1, ayudan al EBV a evadir el sistema inmunológico. [25]
EGCG , un polifenol del té verde , ha demostrado en un estudio que inhibe la infección lítica espontánea por EBV en los niveles de ADN, transcripción genética y proteínas de una manera dependiente del tiempo y la dosis ; la expresión de los genes líticos del VEB Zta, Rta y el complejo de antígeno temprano EA-D (inducido por Rta ); sin embargo, el gen EBNA-1 altamente estable que se encuentra en todas las etapas de la infección por el VEB no se ve afectado. [32] Los inhibidores específicos (de las vías) sugieren que la vía Ras/MEK/MAPK contribuye a la infección lítica por EBV a través de la vía BZLF1 y PI3-K a través de BRLF1, este último anula por completo la capacidad de un vector de adenovirus BRLF1 para inducir la forma lítica de Infección por VEB. [32] Además, se está estudiando la activación de algunos genes, pero no de otros, para determinar cómo inducir la destrucción inmune de células B latentemente infectadas mediante el uso de TPA o butirato de sodio . [32]
A diferencia de la replicación lítica, la latencia no da como resultado la producción de viriones. [25] En cambio, el ADN circular del genoma del VEB reside en el núcleo celular como un episoma y es copiado por la ADN polimerasa celular . [25] Persiste en las células B de memoria del individuo . [19] [24] Los cambios epigenéticos, como la metilación del ADN y los constituyentes de la cromatina celular , suprimen la mayoría de los genes virales en las células infectadas de forma latente. [33] Sólo se expresa una parte de los genes del EBV , que respaldan el estado latente del virus. [33] [19] [34] El EBV latente expresa sus genes en uno de tres patrones, conocidos como programas de latencia. El VEB puede persistir de forma latente dentro de las células B y las células epiteliales , pero son posibles diferentes programas de latencia en los dos tipos de células. [ cita necesaria ]
EBV puede exhibir uno de tres programas de latencia: Latencia I, Latencia II o Latencia III. Cada programa de latencia conduce a la producción de un conjunto limitado y distinto de proteínas virales y ARN virales . [35] [36]
Además, se postula un programa en el que se desactiva toda expresión de proteínas virales (Latencia 0). [37]
Dentro de las células B, los tres programas de latencia son posibles. [19] La latencia del VEB dentro de las células B generalmente progresa de Latencia III a Latencia II y luego Latencia I. Cada etapa de latencia influye de manera única en el comportamiento de las células B. [19] Al infectar una célula B ingenua en reposo , el VEB entra en Latencia III. El conjunto de proteínas y ARN producidos en Latencia III transforma la célula B en una explosión proliferativa (también conocida como activación de células B). [19] [25] Más tarde, el virus restringe su expresión genética y entra en Latencia II. El conjunto más limitado de proteínas y ARN producidos en Latencia II induce a la célula B a diferenciarse en una célula B de memoria . [19] [25] Finalmente, el VEB restringe aún más la expresión genética y entra en Latencia I. La expresión de EBNA-1 permite que el genoma del VEB se replique cuando las células B de memoria se dividen. [19] [25]
Dentro de las células epiteliales, sólo es posible la Latencia II. [38]
En la infección primaria, el VEB se replica en las células epiteliales orofaríngeas y establece infecciones de Latencia III, II e I en los linfocitos B. La infección latente de los linfocitos B por EBV es necesaria para la persistencia del virus, su posterior replicación en las células epiteliales y la liberación del virus infeccioso en la saliva. Las infecciones por EBV en latencia III y II de linfocitos B, la infección en latencia II de células epiteliales orales y la infección en latencia II de células NK o T pueden provocar neoplasias malignas, marcadas por la presencia uniforme del genoma del EBV y la expresión genética. [39]
El EBV latente en las células B se puede reactivar para pasar a la replicación lítica. Se sabe que esto sucede in vivo , pero no se sabe con precisión qué lo desencadena. In vitro , el VEB latente en las células B puede reactivarse estimulando el receptor de las células B, por lo que es probable que la reactivación in vivo tenga lugar después de que las células B infectadas de forma latente respondan a infecciones no relacionadas. [25]
Cuando el VEB infecta células B in vitro , eventualmente emergen líneas celulares linfoblastoides que son capaces de crecer indefinidamente. La transformación del crecimiento de estas líneas celulares es consecuencia de la expresión de proteínas virales. [40]
EBNA-2, EBNA-3C y LMP-1 son esenciales para la transformación, mientras que EBNA-LP y EBER no lo son. [41]
Después de la infección natural con EBV, se cree que el virus ejecuta parte o la totalidad de su repertorio de programas de expresión genética para establecer una infección persistente. Dada la ausencia inicial de inmunidad del huésped , el ciclo lítico produce una gran cantidad de viriones para infectar otros (presumiblemente) linfocitos B dentro del huésped.
Los programas latentes reprograman y subvierten los linfocitos B infectados para que proliferen y lleven células infectadas a los sitios en los que presumiblemente persiste el virus. Finalmente, cuando se desarrolla la inmunidad del huésped, el virus persiste desactivando la mayoría (o posiblemente todos) de sus genes y sólo ocasionalmente se reactiva y produce viriones descendientes. Finalmente se logra un equilibrio entre la reactivación viral ocasional y la vigilancia inmune del huésped que elimina las células que activan la expresión de genes virales. La manipulación de la epigenética del cuerpo humano por parte del EBV puede alterar el genoma de la célula para dejar fenotipos oncogénicos. [42] Como resultado, la modificación realizada por el EBV aumenta la probabilidad del huésped de desarrollar cáncer relacionado con el EBV. [43] Los cánceres relacionados con el VEB son únicos porque con frecuencia producen cambios epigenéticos, pero tienen menos probabilidades de mutar. [44]
El sitio de persistencia del VEB puede ser la médula ósea . Los pacientes EBV positivos a quienes se les ha reemplazado su propia médula ósea con médula ósea de un donante EBV negativo resultan ser EBV negativos después del trasplante . [45]
Todas las proteínas nucleares del EBV se producen mediante corte y empalme alternativo de una transcripción que comienza en los promotores Cp o Wp en el extremo izquierdo del genoma (en la nomenclatura convencional). Los genes están ordenados EBNA-LP/EBNA-2/EBNA-3A/EBNA-3B/EBNA-3C/EBNA-1 dentro del genoma.
El codón de iniciación de la región codificante EBNA-LP se crea mediante un empalme alternativo del transcrito de la proteína nuclear. En ausencia de este codón de iniciación, EBNA-2/EBNA-3A/EBNA-3B/EBNA-3C/EBNA-1 se expresará dependiendo de cuál de estos genes se empalme alternativamente en la transcripción.
El EBV se puede dividir en dos tipos principales, EBV tipo 1 y EBV tipo 2. Estos dos subtipos tienen genes EBNA-3 diferentes . Como resultado, los dos subtipos difieren en sus capacidades de transformación y capacidad de reactivación. El tipo 1 es dominante en la mayor parte del mundo, pero los dos tipos son igualmente prevalentes en África . Se puede distinguir el EBV tipo 1 del EBV tipo 2 cortando el genoma viral con una enzima de restricción y comparando los patrones de digestión resultantes mediante electroforesis en gel . [25]
Los ARN pequeños codificados por el virus de Epstein-Barr (EBER) son, con diferencia, los productos de EBV más abundantes transcritos en células infectadas por EBV. Se utilizan habitualmente como dianas para la detección de EBV en tejidos histológicos. [46]
El VEB causa mononucleosis infecciosa. [50] Los niños infectados con EBV tienen pocos síntomas o pueden parecer asintomáticos, pero cuando la infección se retrasa hasta la adolescencia o la edad adulta, puede causar fatiga , fiebre , inflamación de garganta , inflamación de los ganglios linfáticos del cuello, agrandamiento del bazo , inflamación del hígado o sarpullido. . [20] El síndrome de fatiga crónica posinfecciosa también se ha asociado con la infección por EBV. [51] [52]
El VEB también se ha implicado en varias otras enfermedades, incluido el linfoma de Burkitt , [53] linfohistiocitosis hemofagocítica , [54] linfoma de Hodgkin , [55] cáncer de estómago , [12] [56] carcinoma nasofaríngeo , [57] esclerosis múltiple , [15] [16] [58] [17] y granulomatosis linfomatoide . [59]
Específicamente, se ha demostrado que las células B infectadas con EBV residen dentro de las lesiones cerebrales de pacientes con esclerosis múltiple , [17] y un estudio de 2022 de muestras de sangre históricas de 10 millones de soldados mostró que "las personas que no estaban infectadas con el virus Epstein-Barr prácticamente nunca contraer esclerosis múltiple. Sólo después de la infección por el virus de Epstein-Barr el riesgo de esclerosis múltiple aumenta más de 30 veces", y que sólo el EBV de muchas infecciones tenía una conexión tan clara con la enfermedad. [60]
Otras enfermedades que se han relacionado con el VEB incluyen el síndrome de Gianotti-Crosti , el eritema multiforme , las úlceras genitales agudas y la leucoplasia oral vellosa . [61] La infección viral también está asociada con, y a menudo contribuye al desarrollo de, una amplia gama de enfermedades linfoproliferativas no malignas, como hipersensibilidad grave, reacciones alérgicas a las picaduras de mosquitos , [62] úlceras mucocutáneas positivas al virus de Epstein-Barr y hydroa vacciniforme , así como enfermedades linfoproliferativas malignas como el linfoma de Burkitt positivo para el virus de Epstein-Barr , [63] el linfoma de Hodgkin positivo para el virus de Epstein-Barr , [64] y el linfoma de derrame primario . [sesenta y cinco]
El virus de Epstein-Barr se ha implicado en trastornos relacionados con la agregación de alfa-sinucleína (p. ej. , enfermedad de Parkinson , demencia con cuerpos de Lewy y atrofia multisistémica ). [66]
Se ha descubierto que EBNA1 puede inducir rotura cromosómica en el cromosoma 11 , específicamente en la región 11q23 entre el gen FAM55D y FAM55B, por el cual EBNA-1 parece tener una alta afinidad debido a que su dominio de unión al ADN tiene interés en un repetición palindrómica específica en esta sección del genoma. [67] Si bien se desconocen la causa y el mecanismo exacto de esto, el subproducto produce errores y rotura de la estructura cromosómica a medida que las células derivadas de la línea del genoma contaminado sufren mitosis . Dado que los genes en esta área han sido implicados en la leucemia y albergan un gen supresor de tumores que está modificado o no está presente en la mayoría de la expresión de genes tumorales, se ha planteado la hipótesis de que la rotura en esta área es el principal culpable detrás de los cánceres en los que el VEB aumenta las posibilidades. de. La rotura también depende de la dosis, una persona con una infección latente tendrá menos rotura que una persona con una infección nueva o reactivada ya que los niveles de EBNA1 en el núcleo y el nucléolo son más altos durante el ataque activo del cuerpo debido a la constante replicación y absorción. -exceso de células en el cuerpo.
El virus Epstein-Barr lleva el nombre de MA Epstein e Yvonne Barr , quienes descubrieron el virus junto con Bert Achong . [68] [69] En 1961, Epstein, patólogo y microscopista electrónico experto , asistió a una conferencia sobre "El cáncer infantil más común en África tropical: un síndrome hasta ahora no reconocido" impartida por DP Burkitt , un cirujano que ejerce en Uganda , en la que Burkitt describió la "variante endémica" (forma pediátrica) de la enfermedad que ahora lleva su nombre . En 1963, se envió una muestra desde Uganda al Hospital de Middlesex para su cultivo. Se identificaron partículas de virus en las células cultivadas y los resultados fueron publicados en The Lancet en 1964 por Epstein, Achong y Barr. [69] [70] Se enviaron líneas celulares a Werner y Gertrude Henle en el Hospital Infantil de Filadelfia , quienes desarrollaron marcadores serológicos . [71] En 1967, un técnico de su laboratorio desarrolló mononucleosis y pudieron comparar una muestra de suero almacenada, mostrando que se desarrollaban anticuerpos contra el virus. [70] [72] [73] En 1968, descubrieron que el VEB puede inmortalizar directamente las células B después de la infección, imitando algunas formas de infecciones relacionadas con el VEB, [71] y confirmaron el vínculo entre el virus y la mononucleosis infecciosa. [74]
Como virus relativamente complejo, el EBV aún no se comprende completamente. Laboratorios de todo el mundo continúan estudiando el virus y desarrollando nuevas formas de tratar las enfermedades que causa. Una forma popular de estudiar el VEB in vitro es utilizar cromosomas artificiales bacterianos . [75] El virus de Epstein-Barr se puede mantener y manipular en el laboratorio en latencia continua (una propiedad compartida con el herpesvirus asociado al sarcoma de Kaposi , otro de los ocho herpesvirus humanos). Aunque se supone que muchos virus tienen esta propiedad durante la infección de sus huéspedes naturales, no existe un sistema fácilmente manejable para estudiar esta parte del ciclo de vida viral. Los estudios genómicos del VEB han podido explorar la reactivación lítica y la regulación del episoma viral latente. [76]
Aunque se está investigando activamente, aún no está disponible una vacuna contra el virus de Epstein-Barr . El desarrollo de una vacuna eficaz podría prevenir hasta 200.000 cánceres al año en todo el mundo. [12] La ausencia de modelos animales eficaces es un obstáculo para el desarrollo de vacunas profilácticas y terapéuticas contra el VEB. [24]
Al igual que otros herpesvirus humanos, Epstein-Barr podría permitir su propia erradicación mediante un tratamiento con el fármaco valaciclovir , pero se necesita más investigación para determinar si la erradicación es realmente posible. [42] Los agentes antivirales actúan inhibiendo la replicación del ADN viral, pero hay poca evidencia de que sean eficaces contra el virus de Epstein-Barr. Además, son costosos, corren el riesgo de causar resistencia a los agentes antivirales y (en el 1% al 10% de los casos) pueden causar efectos secundarios desagradables . [43]