


Una batería recargable , batería de almacenamiento o celda secundaria (formalmente un tipo de acumulador de energía ), es un tipo de batería eléctrica que se puede cargar, descargar en una carga y recargar muchas veces, a diferencia de una batería desechable o primaria , que Se suministra completamente cargado y se desecha después de su uso. Está compuesto por una o más celdas electroquímicas . El término "acumulador" se utiliza ya que acumula y almacena energía mediante una reacción electroquímica reversible . Las baterías recargables se producen en muchas formas y tamaños diferentes, desde pilas de botón hasta sistemas de megavatios conectados para estabilizar una red de distribución eléctrica . Se utilizan varias combinaciones diferentes de materiales de electrodos y electrolitos , incluidas plomo-ácido , zinc-aire , níquel-cadmio (NiCd), níquel-hidruro metálico (NiMH), iones de litio (Li-ion), fosfato de hierro y litio (LiFePO4). y polímero de iones de litio (polímero de iones de litio).
Las baterías recargables suelen costar inicialmente más que las baterías desechables, pero tienen un costo total de propiedad y un impacto ambiental mucho menores , ya que se pueden recargar de forma económica muchas veces antes de que sea necesario reemplazarlas. Algunos tipos de baterías recargables están disponibles en los mismos tamaños y voltajes que los tipos desechables y se pueden usar indistintamente con ellos. Se están invirtiendo miles de millones de dólares en investigación en todo el mundo para mejorar las baterías a medida que la industria se concentra en construir mejores baterías. [1] [2] [3]



Los dispositivos que utilizan baterías recargables incluyen arrancadores de automóviles , dispositivos de consumo portátiles, vehículos ligeros (como sillas de ruedas motorizadas , carritos de golf , bicicletas eléctricas y montacargas eléctricos ), vehículos de carretera (coches, furgonetas, camiones, motocicletas), trenes, aviones pequeños, herramientas. , sistemas de alimentación ininterrumpida y centrales eléctricas con almacenamiento de baterías . Las aplicaciones emergentes en vehículos híbridos con batería de combustión interna y eléctricos impulsan la tecnología para reducir costos, peso y tamaño, y aumentar la vida útil. [4]
Las baterías recargables más antiguas se autodescargan relativamente rápido [ vago ] y requieren cargarse antes del primer uso; Algunas baterías NiMH de baja autodescarga más nuevas mantienen su carga durante muchos meses y, por lo general, se venden cargadas de fábrica hasta aproximadamente el 70% de su capacidad nominal.
Las centrales eléctricas de almacenamiento de baterías utilizan baterías recargables para nivelar la carga (almacenar energía eléctrica en momentos de baja demanda para su uso durante los períodos pico) y para usos de energía renovable (como almacenar energía generada a partir de paneles fotovoltaicos durante el día para usarla durante la noche). La nivelación de carga reduce la potencia máxima que una planta debe poder generar, lo que reduce el costo de capital y la necesidad de plantas de energía en picos .
Según un informe de Research and Markets, los analistas pronostican que el mercado mundial de baterías recargables crecerá a una tasa compuesta anual del 8,32% durante el período 2018-2022. [5]
Las pequeñas baterías recargables pueden alimentar dispositivos electrónicos portátiles , herramientas eléctricas, electrodomésticos, etc. Baterías de alta resistencia alimentan vehículos eléctricos , desde scooters hasta locomotoras y barcos . Se utilizan en generación eléctrica distribuida y en sistemas eléctricos autónomos .

Durante la carga, el material activo positivo se oxida , liberando electrones , y el material negativo se reduce , absorbiendo electrones. Estos electrones constituyen el flujo de corriente en el circuito externo . El electrolito puede servir como un simple amortiguador para el flujo interno de iones entre los electrodos , como en las celdas de iones de litio y níquel-cadmio , o puede ser un participante activo en la reacción electroquímica , como en las celdas de plomo-ácido .
La energía utilizada para cargar baterías recargables generalmente proviene de un cargador de baterías que utiliza electricidad de la red eléctrica de CA , aunque algunas están equipadas para usar la toma de corriente de 12 voltios CC de un vehículo. El voltaje de la fuente debe ser mayor que el de la batería para forzar que la corriente fluya hacia ella, pero no demasiado alto o la batería podría dañarse.
Los cargadores tardan desde unos minutos hasta varias horas en cargar una batería. Los cargadores lentos y "tontos" sin capacidad de detección de voltaje o temperatura se cargarán a un ritmo bajo y, por lo general, tardarán 14 horas o más en alcanzar una carga completa. Los cargadores rápidos normalmente pueden cargar las celdas en dos a cinco horas, según el modelo, y los más rápidos tardan tan solo quince minutos. Los cargadores rápidos deben tener múltiples formas de detectar cuándo una celda alcanza la carga completa (cambio en el voltaje del terminal, temperatura, etc.) para detener la carga antes de que se produzca una sobrecarga o un sobrecalentamiento dañinos. Los cargadores más rápidos suelen incorporar ventiladores de refrigeración para evitar que las celdas se sobrecalienten. Los paquetes de baterías destinados a una carga rápida pueden incluir un sensor de temperatura que el cargador utiliza para proteger el paquete; el sensor tendrá uno o más contactos eléctricos adicionales.
Las diferentes químicas de las baterías requieren diferentes esquemas de carga. Por ejemplo, algunos tipos de baterías se pueden recargar de forma segura desde una fuente de voltaje constante. Otros tipos deben cargarse con una fuente de corriente regulada que disminuye a medida que la batería alcanza el voltaje de carga completa. Cargar una batería incorrectamente puede dañarla; En casos extremos, las baterías pueden sobrecalentarse, incendiarse o liberar explosivamente su contenido.
Las tasas de carga y descarga de la batería a menudo se analizan haciendo referencia a una tasa de corriente "C". La tasa C es la que teóricamente cargaría o descargaría completamente la batería en una hora. Por ejemplo, la carga lenta se puede realizar a C/20 (o una tasa de "20 horas"), mientras que la carga y descarga típicas pueden ocurrir a C/2 (dos horas para capacidad total). La capacidad disponible de las celdas electroquímicas varía según la tasa de descarga. Se pierde algo de energía en la resistencia interna de los componentes de la celda (placas, electrolitos, interconexiones) y la velocidad de descarga está limitada por la velocidad a la que los químicos en la celda pueden moverse. Para las pilas de plomo-ácido, la relación entre el tiempo y la tasa de descarga se describe mediante la ley de Peukert ; una celda de plomo-ácido que ya no puede sostener un voltaje terminal utilizable a una corriente alta aún puede tener capacidad utilizable, si se descarga a una velocidad mucho menor. Las hojas de datos de celdas recargables a menudo enumeran la capacidad de descarga en 8 o 20 horas u otro tiempo establecido; Las celdas para sistemas de suministro de energía ininterrumpida pueden tener una clasificación de descarga de 15 minutos.
El voltaje terminal de la batería no es constante durante la carga y descarga. Algunos tipos tienen un voltaje relativamente constante durante la descarga en gran parte de su capacidad. Las pilas alcalinas y de zinc-carbono no recargables emiten 1,5 V cuando son nuevas, pero este voltaje cae con el uso. La mayoría de las pilas NiMH AA y AAA tienen una potencia nominal de 1,2 V, pero tienen una curva de descarga más plana que las alcalinas y normalmente se pueden utilizar en equipos diseñados para utilizar pilas alcalinas .
Las notas técnicas de los fabricantes de baterías a menudo hacen referencia al voltaje por celda (VPC) de las celdas individuales que componen la batería. Por ejemplo, para cargar una batería de plomo-ácido de 12 V (que contiene 6 celdas de 2 V cada una) a 2,3 VPC se requiere un voltaje de 13,8 V en los terminales de la batería.
Someter una celda descargada a una corriente en la dirección que tiende a descargarla más hasta el punto en que los terminales positivo y negativo cambian de polaridad causa una condición llamadainversión celular . Generalmente, empujar corriente a través de una celda descargada de esta manera provoca que se produzcan reacciones químicas indeseables e irreversibles, lo que resulta en un daño permanente a la celda. La reversión celular puede ocurrir bajo varias circunstancias, siendo las dos más comunes:
En el último caso, el problema se debe a que las diferentes celdas de una batería tienen capacidades ligeramente diferentes. Cuando una celda alcanza el nivel de descarga antes que el resto, las celdas restantes forzarán la corriente a través de la celda descargada.
Muchos dispositivos que funcionan con baterías tienen un corte de bajo voltaje que evita que se produzcan descargas profundas que podrían provocar la inversión de la celda. Una batería inteligente tiene un circuito de monitoreo de voltaje integrado en su interior.
La inversión de celda puede ocurrir en una celda débilmente cargada incluso antes de que esté completamente descargada. Si la corriente de drenaje de la batería es lo suficientemente alta, la resistencia interna de la celda puede crear una caída de voltaje resistivo mayor que la fem directa de la celda . Esto da como resultado la inversión de la polaridad de la celda mientras fluye la corriente. [6] [7] Cuanto mayor sea la tasa de descarga requerida de una batería, mejor coincidirán las celdas, tanto en el tipo de celda como en el estado de carga, para reducir las posibilidades de inversión de celda.
En algunas situaciones, como cuando se corrigen baterías de NiCd que han sido sobrecargadas previamente, [8] puede ser conveniente descargar completamente la batería. Para evitar daños por el efecto de inversión de celda, es necesario acceder a cada celda por separado: cada celda se descarga individualmente conectando un clip de carga a través de los terminales de cada celda, evitando así la inversión de celda.
Si una batería de varias celdas está completamente descargada, a menudo se dañará debido al efecto de inversión de celdas mencionado anteriormente. Sin embargo, es posible descargar completamente una batería sin provocar la inversión de las celdas, ya sea descargando cada celda por separado o permitiendo que la fuga interna de cada celda disipe su carga con el tiempo.
Sin embargo, incluso si una celda se lleva a un estado completamente descargado sin revertirla, es posible que se produzcan daños con el tiempo simplemente por permanecer en el estado descargado. Un ejemplo de esto es la sulfatación que se produce en las baterías de plomo-ácido que se dejan en un estante durante largos períodos. Por este motivo, a menudo se recomienda cargar una batería que está destinada a permanecer almacenada y mantener su nivel de carga recargándola periódicamente. Dado que también pueden producirse daños si la batería se sobrecarga, el nivel óptimo de carga durante el almacenamiento suele oscilar entre el 30% y el 70%.
La profundidad de descarga (DOD) normalmente se expresa como un porcentaje de la capacidad nominal en amperios-hora; 0% DOD significa que no hay descarga. Como la capacidad utilizable de un sistema de batería depende de la velocidad de descarga y del voltaje permitido al final de la descarga, se debe calificar la profundidad de la descarga para mostrar la forma en que se debe medir. Debido a variaciones durante la fabricación y el envejecimiento, el DOD para descarga completa puede cambiar con el tiempo o la cantidad de ciclos de carga . Generalmente, un sistema de batería recargable tolerará más ciclos de carga/descarga si el DOD es menor en cada ciclo. [9] Las baterías de litio pueden descargarse entre el 80 y el 90% de su capacidad nominal. Las baterías de plomo-ácido pueden descargarse entre un 50% y un 60%. Mientras que las baterías de flujo pueden descargarse al 100%. [10]
Si las baterías se utilizan repetidamente incluso sin maltratarlas, van perdiendo capacidad a medida que aumenta el número de ciclos de carga, hasta que finalmente se considera que han llegado al final de su vida útil. Los diferentes sistemas de baterías tienen diferentes mecanismos de desgaste. Por ejemplo, en las baterías de plomo-ácido, no todo el material activo se devuelve a las placas en cada ciclo de carga/descarga; eventualmente se pierde suficiente material como para reducir la capacidad de la batería. En los tipos de iones de litio, especialmente en descargas profundas, se puede formar algo de litio metálico reactivo durante la carga, que ya no está disponible para participar en el siguiente ciclo de descarga. Las baterías selladas pueden perder humedad de su electrolito líquido, especialmente si se sobrecargan o se operan a altas temperaturas. Esto reduce la vida útil del ciclo. [11]

El tiempo de recarga es un parámetro importante para el usuario de un producto alimentado por baterías recargables. Incluso si la fuente de alimentación de carga proporciona suficiente energía para operar el dispositivo y recargar la batería, el dispositivo está conectado a una fuente de alimentación externa durante el tiempo de carga. Para los vehículos eléctricos utilizados industrialmente, la carga fuera de turno puede ser aceptable. Para los vehículos eléctricos de carretera, la carga rápida es necesaria para cargar en un tiempo razonable.
Una batería recargable no se puede recargar a un ritmo arbitrariamente alto. La resistencia interna de la batería producirá calor y un aumento excesivo de temperatura dañará o destruirá la batería. Para algunos tipos, la velocidad de carga máxima estará limitada por la velocidad a la que el material activo puede difundirse a través de un electrolito líquido. Las altas velocidades de carga pueden producir un exceso de gas en una batería o pueden provocar reacciones secundarias dañinas que reducen permanentemente la capacidad de la batería. De manera muy aproximada, y con muchas excepciones y advertencias, restaurar la capacidad total de una batería en una hora o menos se considera carga rápida. Un sistema de cargador de baterías incluirá circuitos de control y estrategias de carga más complejos para una carga rápida que un cargador diseñado para una recarga más lenta.
Los componentes activos en una celda secundaria son los químicos que forman los materiales activos positivos y negativos y el electrolito . Los electrodos positivo y negativo están hechos de diferentes materiales, el positivo presenta un potencial de reducción y el negativo tiene un potencial de oxidación . La suma de los potenciales de estas semireacciones es el potencial o voltaje de celda estándar .
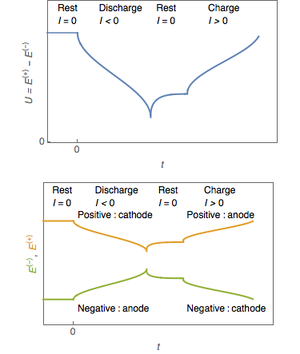
En las celdas primarias los electrodos positivo y negativo se conocen como cátodo y ánodo , respectivamente. Aunque esta convención a veces se aplica a los sistemas recargables (especialmente con celdas de iones de litio , debido a sus orígenes en celdas de litio primarias), esta práctica puede generar confusión. En las pilas recargables, el electrodo positivo es el cátodo en descarga y el ánodo en carga, y viceversa para el electrodo negativo.

La batería de plomo-ácido , inventada en 1859 por el físico francés Gaston Planté , es el tipo de batería recargable más antigua. A pesar de tener una relación energía-peso muy baja y una relación energía-volumen baja, su capacidad para suministrar altas sobrecorrientes significa que las celdas tienen una relación potencia-peso relativamente grande . Estas características, junto con el bajo costo, lo hacen atractivo para su uso en vehículos de motor para proporcionar la alta corriente requerida por los motores de arranque de los automóviles .
La batería de níquel-cadmio (NiCd) fue inventada por Waldemar Jungner de Suecia en 1899. Utiliza hidróxido de óxido de níquel y cadmio metálico como electrodos . El cadmio es un elemento tóxico y la Unión Europea lo prohibió para la mayoría de sus usos en 2004. Las baterías de níquel-cadmio han sido reemplazadas casi por completo por las baterías de níquel-hidruro metálico (NiMH).
La batería de níquel-hierro (NiFe) también fue desarrollada por Waldemar Jungner en 1899; y comercializado por Thomas Edison en 1901 en Estados Unidos para vehículos eléctricos y señalización ferroviaria . Está compuesto únicamente por elementos no tóxicos, a diferencia de muchos tipos de baterías que contienen mercurio, cadmio o plomo tóxicos.
La batería de hidruro metálico de níquel (NiMH) estuvo disponible en 1989. [12] Ahora son un tipo industrial y de consumo común. La batería tiene una aleación que absorbe hidrógeno para el electrodo negativo en lugar de cadmio .
La batería de iones de litio se introdujo en el mercado en 1991, es la opción en la mayoría de los productos electrónicos de consumo, ya que tiene la mejor densidad de energía y una pérdida de carga muy lenta cuando no está en uso. También tiene desventajas, particularmente el riesgo de una ignición inesperada debido al calor generado por la batería. [13] Estos incidentes son raros y, según los expertos, se pueden minimizar "mediante un diseño, instalación, procedimientos y capas de salvaguardias apropiados" para que el riesgo sea aceptable. [14]
Las baterías de polímero de iones de litio (LiPo) son livianas, ofrecen una densidad de energía ligeramente mayor que las de iones de litio a un costo ligeramente mayor y pueden fabricarse en cualquier forma. Están disponibles [15] pero no han desplazado al Li-ion en el mercado. [16] Un uso principal de las baterías LiPo es la alimentación de automóviles, barcos y aviones controlados a distancia. Los paquetes de LiPo están disponibles en el mercado de consumo, en varias configuraciones, hasta 44,4 V, para alimentar ciertos vehículos R/C y helicópteros o drones. [17] [18] Algunos informes de pruebas advierten del riesgo de incendio cuando las baterías no se utilizan de acuerdo con las instrucciones. [19] Revisiones independientes de la tecnología analizan el riesgo de incendio y explosión de las baterías de iones de litio en determinadas condiciones porque utilizan electrolitos líquidos. [20]
‡ se necesitan citas para estos parámetros
Se han desarrollado varios tipos de baterías de litio y azufre y numerosos grupos de investigación y organizaciones han demostrado que las baterías basadas en litio y azufre pueden lograr una densidad de energía superior a otras tecnologías de litio. [39] Mientras que las baterías de iones de litio ofrecen una densidad de energía en el rango de 150 a 260 Wh/kg, se espera que las baterías basadas en litio-azufre alcancen 450 a 500 Wh/kg y puedan eliminar el cobalto, el níquel y el manganeso de la producción. proceso. [23] [40] Además, si bien inicialmente las baterías de litio-azufre sufrieron problemas de estabilidad, investigaciones recientes han logrado avances en el desarrollo de baterías de litio-azufre que tienen ciclos tan largos (o más largos) que las baterías basadas en tecnologías convencionales de iones de litio. [41]
La batería de película delgada (TFB) es un refinamiento de la tecnología de iones de litio de Excellatron. [42] Los desarrolladores afirman un gran aumento en los ciclos de recarga a alrededor de 40.000 y tasas de carga y descarga más altas, al menos una tasa de carga de 5 C. Descarga sostenida de 60 C y tasa de descarga máxima de 1000 C y un aumento significativo en la energía específica y la densidad de energía. [43]
En algunas aplicaciones se utilizan baterías de fosfato de hierro y litio .
UltraBattery , una batería híbrida de plomo-ácido y un ultracondensador inventado por la organización científica nacional CSIRO de Australia , exhibe decenas de miles de ciclos de estado de carga parcial y ha superado a las celdas tradicionales de plomo-ácido, litio y NiMH en comparación con las pruebas en este modo. contra perfiles de potencia de gestión de variabilidad. [44] UltraBattery cuenta con instalaciones a escala de kW y MW en Australia, Japón y EE. UU. También ha sido sometido a pruebas exhaustivas en vehículos eléctricos híbridos y se ha demostrado que dura más de 100 000 millas en pruebas comerciales en carretera. en un vehículo de mensajería. Se afirma que la tecnología tiene una vida útil de 7 a 10 veces mayor que la de las baterías de plomo-ácido convencionales en uso en estado de carga parcial de alta velocidad, con beneficios ambientales y de seguridad reclamados sobre competidores como el de iones de litio. Su fabricante sugiere que ya existe una tasa de reciclaje de casi el 100% para el producto.
La batería de iones de potasio ofrece alrededor de un millón de ciclos, debido a la extraordinaria estabilidad electroquímica de los materiales de inserción/extracción de potasio, como el azul de Prusia . [45]
La batería de iones de sodio está destinada al almacenamiento estacionario y compite con las baterías de plomo-ácido. Su objetivo es lograr un bajo coste total de propiedad por kWh de almacenamiento. Esto se logra mediante una vida útil larga y estable. El número efectivo de ciclos es superior a 5000 y la batería no se daña por una descarga profunda. La densidad de energía es bastante baja, algo menor que la del plomo-ácido. [ cita necesaria ]
Una batería recargable es sólo uno de varios tipos de sistemas de almacenamiento de energía recargables. [46] Existen o están en desarrollo varias alternativas a las baterías recargables. Para usos como radios portátiles , las baterías recargables pueden ser reemplazadas por mecanismos de relojería que se dan cuerda a mano, impulsando dinamos , aunque este sistema puede usarse para cargar una batería en lugar de operar la radio directamente. Las linternas pueden funcionar directamente con una dinamo. Para el transporte, los sistemas de suministro de energía ininterrumpida y los laboratorios, los sistemas de almacenamiento de energía del volante almacenan energía en un rotor giratorio para convertirla en energía eléctrica cuando sea necesario; Estos sistemas se pueden utilizar para proporcionar grandes impulsos de energía que de otro modo serían objetables en una red eléctrica común.
También se utilizan ultracondensadores (condensadores de valor extremadamente alto); En 2007 se introdujo un destornillador eléctrico que se carga en 90 segundos y acciona aproximadamente la mitad de tornillos que un dispositivo que utiliza una batería recargable, [47] y se han producido linternas similares. De acuerdo con el concepto de ultracondensadores, las baterías betavoltaicas se pueden utilizar como método para proporcionar una carga lenta a una batería secundaria, extendiendo en gran medida la vida útil y la capacidad energética del sistema de batería que se emplea; Los miembros de la industria a menudo se refieren a este tipo de disposición como una "fuente de energía betavoltaica híbrida". [48]
Se están desarrollando ultracondensadores para el transporte, utilizando un condensador grande para almacenar energía en lugar de los bancos de baterías recargables utilizados en los vehículos híbridos . Una desventaja de los condensadores en comparación con las baterías es que el voltaje en los terminales cae rápidamente; un capacitor al que le queda el 25% de su energía inicial tendrá la mitad de su voltaje inicial. Por el contrario, los sistemas de baterías tienden a tener un voltaje terminal que no disminuye rápidamente hasta que casi se agota. Esta caída de tensión en los terminales complica el diseño de la electrónica de potencia para su uso con ultracondensadores. Sin embargo, existen beneficios potenciales en la eficiencia, la vida útil y el peso del ciclo en comparación con los sistemas recargables. China empezó a utilizar ultracondensadores en dos rutas de autobuses comerciales en 2006; una de ellas es la ruta 11 en Shanghai . [49]
Las baterías de flujo , utilizadas para aplicaciones especializadas, se recargan reemplazando el electrolito líquido. Una batería de flujo puede considerarse un tipo de pila de combustible recargable .
La investigación sobre baterías recargables incluye el desarrollo de nuevos sistemas electroquímicos, así como la mejora de la vida útil y la capacidad de los tipos actuales.
Mantenga cerca un extintor seco o un balde grande con arena seca, que es un extintor económico y eficaz.
Voltajes, recuentos de celdas y capacidades ideales para tu tipo de carrera... Tasas de descarga desde 50 C hasta 100 C... Equilibrado para una vida útil más larga y lograr el máximo de 4,2 V/celda.
Todavía no he oído hablar de un LiPo que se incendiara durante el almacenamiento. Todos los incidentes de incendio que conozco ocurrieron durante la carga o descarga de la batería. De esos casos, la mayoría de los problemas ocurrieron durante la carga. En esos casos, la falla generalmente recaía en el cargador o en la persona que lo operaba... pero no siempre.