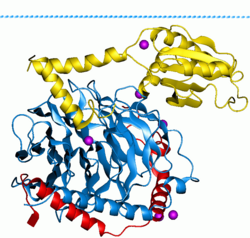
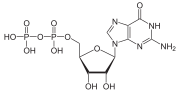

Las proteínas G , también conocidas como proteínas de unión al nucleótido de guanina , son una familia de proteínas que actúan como interruptores moleculares dentro de las células y están involucradas en la transmisión de señales desde una variedad de estímulos fuera de una célula a su interior. Su actividad está regulada por factores que controlan su capacidad para unirse e hidrolizar el trifosfato de guanosina (GTP) a difosfato de guanosina (GDP). Cuando están unidas al GTP, están "activadas" y, cuando están unidas al GDP, están "desactivadas". Las proteínas G pertenecen al grupo más grande de enzimas llamadas GTPasas .
Existen dos clases de proteínas G. Las primeras funcionan como pequeñas GTPasas monoméricas (proteínas G pequeñas), mientras que las segundas funcionan como complejos de proteína G heterotriméricos . La última clase de complejos está formada por subunidades alfa (G α ), beta (G β ) y gamma (G γ ) . [1] Además, las subunidades beta y gamma pueden formar un complejo dimérico estable denominado complejo beta-gamma . [2]
Las proteínas G heterotriméricas ubicadas dentro de la célula son activadas por receptores acoplados a proteína G (GPCR) que abarcan la membrana celular . [3] Las moléculas de señalización se unen a un dominio del GPCR ubicado fuera de la célula, y un dominio GPCR intracelular activa a su vez una proteína G particular. También se ha demostrado que algunos GPCR en estado activo están "preacoplados" con proteínas G, mientras que en otros casos se cree que ocurre un mecanismo de acoplamiento por colisión. [4] [5] [6] La proteína G desencadena una cascada de eventos de señalización adicionales que finalmente resultan en un cambio en la función celular. Los receptores acoplados a proteína G y las proteínas G que trabajan juntos transmiten señales de muchas hormonas , neurotransmisores y otros factores de señalización. [7] Las proteínas G regulan las enzimas metabólicas , los canales iónicos , las proteínas transportadoras y otras partes de la maquinaria celular, controlando la transcripción , la motilidad , la contractilidad y la secreción , que a su vez regulan diversas funciones sistémicas como el desarrollo embrionario , el aprendizaje y la memoria, y la homeostasis . [8]
Las proteínas G se descubrieron en 1980 cuando Alfred G. Gilman y Martin Rodbell investigaron la estimulación de las células por la adrenalina . Descubrieron que cuando la adrenalina se une a un receptor, el receptor no estimula las enzimas (dentro de la célula) directamente. En cambio, el receptor estimula una proteína G, que a su vez estimula una enzima. Un ejemplo es la adenilato ciclasa , que produce el segundo mensajero AMP cíclico . [9] Por este descubrimiento, ganaron el Premio Nobel de Fisiología o Medicina en 1994. [10]
Se han otorgado premios Nobel por muchos aspectos de la señalización de las proteínas G y GPCR. Estos incluyen antagonistas de receptores , neurotransmisores , recaptación de neurotransmisores , receptores acoplados a proteína G , proteínas G, segundos mensajeros , las enzimas que desencadenan la fosforilación de proteínas en respuesta al AMPc y los procesos metabólicos consecuentes como la glucogenólisis .
Algunos ejemplos destacados incluyen (en orden cronológico de concesión):
Las proteínas G son moléculas transductoras de señales importantes en las células. "El mal funcionamiento de las vías de señalización de GPCR [G Protein-Coupled Receptor] está involucrado en muchas enfermedades, como diabetes , ceguera, alergias, depresión, defectos cardiovasculares y ciertas formas de cáncer . Se estima que alrededor del 30% de los objetivos celulares de los medicamentos modernos son GPCR". [15] El genoma humano codifica aproximadamente 800 [16] receptores acoplados a proteína G , que detectan fotones de luz, hormonas, factores de crecimiento, medicamentos y otros ligandos endógenos . Aproximadamente 150 de los GPCR encontrados en el genoma humano aún tienen funciones desconocidas.
Mientras que las proteínas G son activadas por receptores acoplados a proteínas G , son inactivadas por proteínas RGS (por "Regulador de la señalización de la proteína G"). Los receptores estimulan la unión de GTP (activando la proteína G). Las proteínas RGS estimulan la hidrólisis de GTP (creando GDP, desactivando así la proteína G).
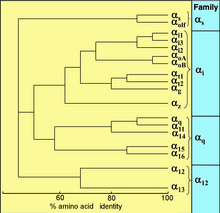
Todos los eucariotas utilizan proteínas G para la señalización y han desarrollado una gran diversidad de proteínas G. Por ejemplo, los humanos codifican 18 proteínas G α diferentes , 5 proteínas G β y 12 proteínas G γ . [17]
La proteína G puede referirse a dos familias distintas de proteínas. Las proteínas G heterotriméricas , a veces denominadas proteínas G "grandes", son activadas por receptores acoplados a proteínas G y están formadas por subunidades alfa (α), beta (β) y gamma (γ) . Las proteínas G "pequeñas" (20-25 kDa) pertenecen a la superfamilia Ras de GTPasas pequeñas . Estas proteínas son homólogas a la subunidad alfa (α) que se encuentra en los heterotrímeros, pero de hecho son monoméricas, constan de una sola unidad. Sin embargo, al igual que sus parientes más grandes, también se unen a GTP y GDP y están involucradas en la transducción de señales .
Los distintos tipos de proteínas G heterotriméricas comparten un mecanismo común. Se activan en respuesta a un cambio conformacional en el GPCR, intercambiando GDP por GTP y disociándose para activar otras proteínas en una vía de transducción de señales particular . [18] Sin embargo, los mecanismos específicos difieren entre los tipos de proteínas.

Las proteínas G activadas por receptores están unidas a la superficie interna de la membrana celular . Consisten en las subunidades G α y G βγ estrechamente asociadas . Hay cuatro familias principales de subunidades G α : Gα s (G estimuladora), Gα i (G inhibidora), Gα q/11 y Gα 12/13 . [20] [21] Se comportan de manera diferente en el reconocimiento de la molécula efectora, pero comparten un mecanismo de activación similar.
Cuando un ligando activa el receptor acoplado a proteína G , induce un cambio conformacional en el receptor que le permite funcionar como un factor de intercambio de nucleótidos de guanina (GEF) que intercambia GDP por GTP. El GTP (o GDP) está unido a la subunidad G α en la visión tradicional de la activación del GPCR heterotrimérico. Este intercambio desencadena la disociación de la subunidad G α (que está unida a GTP) del dímero G βγ y del receptor en su conjunto. Sin embargo, los modelos que sugieren reordenamiento molecular, reorganización y precomplejación de moléculas efectoras están empezando a ser aceptados. [4] [22] [23] Tanto G α -GTP como G βγ pueden activar diferentes cascadas de señalización (o vías de segundo mensajero ) y proteínas efectoras, mientras que el receptor puede activar la siguiente proteína G. [24]
La subunidad G α eventualmente hidrolizará el GTP unido a GDP por su actividad enzimática inherente , lo que le permitirá volver a asociarse con G βγ y comenzar un nuevo ciclo. Un grupo de proteínas llamadas Reguladores de la señalización de la proteína G (RGSs), actúan como proteínas activadoras de GTPasa (GAPs), son específicas para las subunidades G α . Estas proteínas aceleran la hidrólisis de GTP a GDP, terminando así la señal transducida. En algunos casos, el propio efector puede poseer actividad GAP intrínseca, que luego puede ayudar a desactivar la vía. Esto es cierto en el caso de la fosfolipasa C -beta, que posee actividad GAP dentro de su región C-terminal . Esta es una forma alternativa de regulación para la subunidad G α . Tales GAPs G α no tienen residuos catalíticos (secuencias de aminoácidos específicas) para activar la proteína G α . En cambio, funcionan reduciendo la energía de activación requerida para que se lleve a cabo la reacción. [25]
La G αs activa la vía dependiente del AMPc al estimular la producción de AMP cíclico (AMPc) a partir de ATP . Esto se logra mediante la estimulación directa de la enzima asociada a la membrana adenilato ciclasa . El AMPc puede entonces actuar como un segundo mensajero que interactúa con la proteína quinasa A (PKA) y la activa. La PKA puede fosforilar una gran cantidad de dianas posteriores.
La vía dependiente de AMPc se utiliza como vía de transducción de señales para muchas hormonas, entre ellas:
G αi inhibe la producción de AMPc a partir de ATP, por ejemplo, somatostatina, prostaglandinas.
La G αq/11 estimula la fosfolipasa C beta unida a la membrana, que luego escinde el fosfatidilinositol 4,5-bisfosfato (PIP 2 ) en dos segundos mensajeros, el trifosfato de inositol (IP 3 ) y el diacilglicerol (DAG). El IP 3 induce la liberación de calcio del retículo endoplásmico . El DAG activa la proteína quinasa C . La vía dependiente de fosfolípidos de inositol se utiliza como vía de transducción de señales para muchas hormonas, entre ellas:
Las GTPasas pequeñas, también conocidas como proteínas G pequeñas, se unen a GTP y GDP de la misma manera, y están involucradas en la transducción de señales . Estas proteínas son homólogas a la subunidad alfa (α) que se encuentra en los heterotrímeros, pero existen como monómeros. Son proteínas pequeñas (de 20 kDa a 25 kDa) que se unen al trifosfato de guanosina ( GTP ). Esta familia de proteínas es homóloga a las GTPasas Ras y también se denomina GTPasas de la superfamilia Ras .
Para asociarse con la capa interna de la membrana plasmática, muchas proteínas G y GTPasas pequeñas se lipidan [ cita requerida ] , es decir, se modifican covalentemente con extensiones lipídicas. Pueden ser miristoiladas , palmitoiladas o preniladas .
{{cite book}}: Mantenimiento de CS1: falta la ubicación del editor ( enlace )