La nutrición parenteral ( NP ) es la alimentación de una persona con productos nutricionales por vía intravenosa , [1] sin pasar por el proceso habitual de alimentación y digestión. Los productos son fabricados por entidades de formulación de compuestos farmacéuticos o compañías farmacéuticas estándar. [2] [3] La persona recibe una mezcla nutricional según una fórmula que incluye glucosa , sales , aminoácidos , lípidos y vitaminas y minerales dietéticos . [4] Se denomina nutrición parenteral total ( NPT ) o mezcla total de nutrientes ( TNA ) cuando no se obtiene una nutrición significativa por otras vías, y nutrición parenteral parcial ( PPN ) cuando la nutrición también es parcialmente entérica . Se denomina nutrición parenteral periférica ( NPP ) cuando se administra a través del acceso venoso de una extremidad en lugar de a través de una vena central como nutrición venosa central ( NVC ). [5]
La nutrición parenteral total (NPT) se proporciona cuando el tracto gastrointestinal no funciona debido a una interrupción en su continuidad (está bloqueado o tiene una fuga, una fístula ) o porque su capacidad de absorción está alterada. [6] Se ha utilizado para pacientes comatosos , aunque la alimentación enteral suele ser preferible y menos propensa a complicaciones. La nutrición parenteral se utiliza para prevenir la desnutrición en pacientes que no pueden obtener los nutrientes adecuados por vía oral o enteral . [7] La Sociedad de Medicina de Cuidados Críticos (SCCM) y la Sociedad Estadounidense de Nutrición Parenteral y Enteral recomiendan esperar hasta el séptimo día de atención hospitalaria. [8]
Las enfermedades que requerirían el uso de NPT incluyen: [8]
La NPT puede ser la única opción factible para proporcionar nutrición a pacientes que no tienen un tracto gastrointestinal funcional o que tienen trastornos que requieren reposo intestinal completo, incluida obstrucción intestinal , [9] síndrome del intestino corto , [9] gastrosquisis , [9] diarrea prolongada . independientemente de su causa, [9] enfermedad de Crohn muy grave [9] o colitis ulcerosa , [9] y ciertos trastornos gastrointestinales pediátricos, incluidas anomalías gastrointestinales congénitas y enterocolitis necrotizante . [10]
Existen diferencias físicas, fisiológicas o mentales en la población geriátrica que potencialmente podrían conducir a una ingesta deficiente de nutrientes que requeriría una terapia nutricional. [11] Los pacientes geriátricos son más propensos a tener una restauración muscular retrasada en comparación con la población más joven. Además, se observa que los pacientes mayores tienen mayor insuficiencia cardíaca y renal, resistencia a la insulina y deficiencias de vitaminas y elementos cruciales. Los pacientes que requieren terapia nutricional pero tienen contraindicaciones o no pueden tolerar la nutrición enteral son candidatos apropiados para la nutrición parenteral. En la población geriátrica, está indicado si la nutrición oral o enteral es imposible durante 3 días o cuando es probable que la nutrición oral o enteral sea insuficiente durante más de 7 a 10 días. Si bien no existen complicaciones de la nutrición parenteral específicas de la población geriátrica, las complicaciones son más prevalentes en esta población debido al aumento de comorbilidades . [12]
Los pacientes a los que se les diagnostica cáncer, ya sea de forma ambulatoria en tratamiento u hospitalizados, tienen mayor riesgo de sufrir desnutrición y caquexia . La desnutrición relacionada con el cáncer puede atribuirse a la disminución de la ingesta de alimentos, al aumento de la necesidad de energía y a la alteración del metabolismo. [13] Los pacientes deben ser evaluados desde el principio del tratamiento contra el cáncer para detectar cualquier riesgo nutricional, como por ejemplo, tomando pesas e IMC de forma rutinaria. La nutrición parenteral está indicada en pacientes con cáncer cuando no es posible acceder al tracto digestivo o si el tracto es ineficaz. En pacientes con cáncer avanzado, el uso de NP debe discutirse en el contexto de los riesgos y beneficios, como por ejemplo si la tasa de supervivencia aproximada es superior a 3 meses y si se esperaría que la NP mejorara en gran medida la calidad de vida de los pacientes. [13]
No está claro si la nutrición parenteral domiciliaria mejora la supervivencia o la calidad de vida en personas con obstrucción intestinal maligna . [14]
La NP a corto plazo se puede utilizar si el sistema digestivo de una persona se ha detenido (por ejemplo, debido a peritonitis ) y su peso es lo suficientemente bajo como para causar preocupaciones sobre la nutrición durante una estadía prolongada en el hospital. La NP a largo plazo se utiliza ocasionalmente para tratar a personas que sufren las consecuencias prolongadas de un accidente, una cirugía o un trastorno digestivo. La NP ha alargado la vida de niños que nacen con órganos inexistentes o gravemente deformados.
Aproximadamente 40 000 personas utilizan la NPT en sus hogares en los Estados Unidos y, debido a que su administración requiere de 10 a 16 horas, la vida diaria puede verse afectada. [15] Aunque el estilo de vida diario se puede cambiar, la mayoría de los pacientes están de acuerdo en que estos cambios son mejores que quedarse en el hospital. [16] Existen muchos tipos diferentes de bombas para limitar el tiempo que el paciente está "conectado". Por lo general, se utiliza una bomba de mochila, lo que permite la movilidad. El tiempo necesario para estar conectado a la vía intravenosa depende de la situación de cada paciente; algunos requieren una vez al día o cinco días a la semana. [15]
Es importante que los pacientes eviten tantos cambios como sea posible relacionados con la NPT en sus estilos de vida. Esto permite la mejor situación de salud mental posible; Ser reprimido constantemente puede generar resentimiento y depresión . También se recomienda encarecidamente la actividad física , pero los pacientes deben evitar los deportes de contacto (daños en el equipo) y la natación (infección). A muchos adolescentes les resulta difícil vivir con NPT debido a problemas relacionados con la imagen corporal y a no poder participar en actividades y eventos. [15]
La NPT evita por completo el tracto gastrointestinal y los métodos normales de absorción de nutrientes. A continuación se enumeran las posibles complicaciones, que pueden ser importantes. Además de las que se enumeran a continuación, las complicaciones comunes de la NPT incluyen hipofosfatemia, hipopotasemia, hiperglucemia, hipercapnia, disminución de los niveles de cobre y zinc, tiempo de protrombina elevado (si se asocia con lesión hepática), acidosis metabólica hiperclorémica y disminución de la motilidad gastrointestinal. [8]
La NPT requiere un acceso intravenoso crónico para que pase la solución y la complicación más común es la infección de este catéter. La infección es una causa común de muerte en estos pacientes, con una tasa de mortalidad de aproximadamente el 15% por infección, y la muerte generalmente se debe a un shock séptico . [17] Cuando se utiliza un acceso venoso central, se prefiere la vena subclavia (o axilar) debido a su facilidad de acceso y menores complicaciones infecciosas en comparación con las inserciones de las venas yugular y femoral. [6]
Las complicaciones del catéter incluyen neumotórax , punción arterial accidental y sepsis relacionada con el catéter. La tasa de complicaciones en el momento de la inserción debe ser inferior al 5%. Las infecciones relacionadas con el catéter se pueden minimizar mediante la elección adecuada del catéter y la técnica de inserción. [18]
El acceso intravenoso crónico deja un cuerpo extraño en el sistema vascular y los coágulos de sangre en esta vía intravenosa son comunes. [19] La muerte puede resultar de una embolia pulmonar en la que un coágulo que comienza en la vía intravenosa se rompe y viaja a los pulmones, bloqueando el flujo sanguíneo. [20]
Los pacientes con NPT que tienen coágulos que obstruyen su catéter pueden recibir un lavado trombolítico para disolver los coágulos y prevenir complicaciones adicionales.
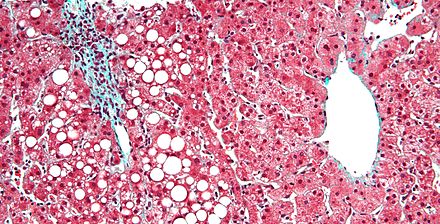
El hígado graso suele ser una complicación a largo plazo de la NPT, aunque en un ciclo suficientemente prolongado es bastante común. La patogénesis se debe al uso de ácido linoleico (un ácido graso omega-6 componente del aceite de soja) como fuente principal de calorías. [21] [22] La enfermedad hepática asociada a la NPT afecta hasta al 50% de los pacientes en un plazo de 5 a 7 años, lo que se correlaciona con una tasa de mortalidad del 2 al 50%. La aparición de esta enfermedad hepática es la principal complicación que lleva a los pacientes con NPT a requerir un trasplante intestinal . [23]
Intralipid ( Fresenius-Kabi ), la emulsión lipídica estándar de EE. UU. para la nutrición NPT, contiene una proporción de 7:1 de n-6/n-3 de ácidos grasos poliinsaturados (PUFA). Por el contrario, Omegaven tiene una proporción de 1:8 y se mostró prometedor en múltiples estudios clínicos. Por lo tanto, las grasas ricas en n-3 pueden alterar el curso de la enfermedad hepática asociada a la nutrición parenteral (PNALD). [24]
Debido a que los pacientes reciben alimentación intravenosa, el sujeto no come físicamente, lo que provoca intensas punzadas de hambre (dolores). El cerebro utiliza señales de la boca ( gusto y olfato ), el estómago y el tracto gastrointestinal (llenura) y la sangre ( niveles de nutrientes ) para determinar la sensación consciente de hambre . [25] En los casos de NPT, los requisitos de gusto, olfato y plenitud física no se satisfacen, por lo que el paciente experimenta hambre, aunque el cuerpo está completamente nutrido.
Los pacientes que ingieren alimentos a pesar de la incapacidad pueden experimentar una amplia gama de complicaciones, como el síndrome de realimentación . [26]
La nutrición parenteral total aumenta el riesgo de colecistitis aguda [27] debido a la falta de uso total del tracto gastrointestinal, lo que puede provocar estasis biliar en la vesícula biliar . Otras posibles disfunciones hepatobiliares incluyen esteatosis , [28] esteatohepatitis , colestasis y colelitiasis . [29] El seis por ciento de los pacientes con NPT durante más de tres semanas y el 100% de los pacientes con NPT durante más de 13 semanas desarrollan lodo biliar . La formación de lodo es el resultado de la estasis debida a la falta de estimulación entérica y no se debe a cambios en la composición de la bilis. El lodo de la vesícula biliar desaparece después de cuatro semanas de una dieta oral normal. Se ha demostrado que la administración de colecistoquinina exógena (CCK) o la estimulación de CCK endógena mediante un pulso periódico de grandes cantidades de aminoácidos ayuda a prevenir la formación de lodos. Estas terapias no se recomiendan de forma rutinaria. [30] Se sugiere que tales complicaciones son la principal razón de mortalidad en personas que requieren nutrición parenteral total a largo plazo, como en el síndrome del intestino corto . [31] En los recién nacidos con síndrome del intestino corto con menos del 10% de la longitud intestinal esperada, por lo que dependen de la nutrición parenteral total, la supervivencia a cinco años es aproximadamente del 20%. [32]
Los bebés que reciben NPT sin alimentos por vía oral durante períodos prolongados corren el riesgo de desarrollar atrofia intestinal. [33]
La hipersensibilidad es una complicación raramente descrita pero significativa del tratamiento de nutrición parenteral. Reportadas por primera vez en 1965, [34] se especula que la incidencia de estas reacciones es de alrededor de uno en 1,5 millones de pacientes que reciben nutrición parenteral. [35] Existe una amplia gama en cómo y cuándo se manifiestan estas reacciones. Las manifestaciones cutáneas son la presentación más común. Se cree que se produce hipersensibilidad a los componentes individuales de la NPT, siendo la emulsión lipídica intravenosa el componente más frecuentemente implicado, seguido de la solución multivitamínica y la solución de aminoácidos . [35]
Medicamentos
Es posible que los pacientes que reciben nutrición parenteral intravenosa también necesiten recibir medicamentos intravenosos utilizando el mismo sitio en Y. Es importante evaluar la compatibilidad de los medicamentos con los componentes nutricionales. Las incompatibilidades se pueden observar físicamente mediante decoloración, separación de fases o precipitación. [36]
Las complicaciones metabólicas incluyen el síndrome de realimentación caracterizado por hipopotasemia , hipofosfatemia e hipomagnesemia . La hiperglucemia es común al inicio del tratamiento, pero se puede tratar agregando insulina a la solución de NPT. Es probable que se produzca hipoglucemia al suspender bruscamente la NPT. La disfunción hepática puede limitarse a una ictericia colestásica reversible y a una infiltración grasa (demostrada por elevación de las transaminasas). La disfunción hepática grave es una complicación rara. [37] En general, los pacientes que reciben NPT tienen una tasa más alta de complicaciones infecciosas. Esto puede estar relacionado con la hiperglucemia. [38]
El embarazo puede causar complicaciones importantes al intentar dosificar adecuadamente la mezcla de nutrientes. Debido a que toda la nutrición del bebé proviene del torrente sanguíneo de la madre, el médico debe calcular adecuadamente la dosis de nutrientes para satisfacer las necesidades de ambos receptores y tenerlos en formas utilizables. La dosis incorrecta puede provocar muchos efectos adversos difíciles de adivinar, como la muerte y diversos grados de deformación u otros problemas de desarrollo . [39]
Se recomienda que la administración de nutrición parenteral comience después de un período de nutrición natural para que los médicos puedan calcular adecuadamente las necesidades nutricionales del feto . De lo contrario, sólo debería ser administrado por un equipo de médicos altamente capacitados que puedan evaluar con precisión las necesidades del feto. [39]

Las soluciones para la nutrición parenteral total se pueden personalizar según los requisitos individuales del paciente o se pueden utilizar soluciones estandarizadas. El uso de soluciones de nutrición parenteral estandarizadas es rentable y puede proporcionar un mejor control de los electrolitos séricos. [40] Lo ideal es que cada paciente sea evaluado individualmente antes de comenzar con la nutrición parenteral, y un equipo formado por médicos especializados, enfermeras, farmacéuticos clínicos y dietistas registrados evalúe los datos individuales del paciente y decida qué fórmula de NP usar y a qué velocidad de infusión.
Sólo como energía se utilizan generalmente soluciones intravenosas de azúcar con dextrosa o glucosa . Esto no se considera nutrición parenteral ya que no previene la desnutrición cuando se usa solo. Las soluciones estandarizadas también pueden diferir entre los desarrolladores. A continuación se muestran algunos ejemplos de las composiciones que pueden tener. La solución para pacientes normales se puede administrar tanto de forma central como periférica.
Las soluciones preparadas generalmente consisten en agua y electrolitos; glucosa , aminoácidos y lípidos; Las vitaminas , minerales y oligoelementos esenciales se añaden o se administran por separado. Anteriormente las emulsiones lipídicas se administraban por separado, pero cada vez es más común administrar una solución "tres en uno" de glucosa, proteínas y lípidos. [41] [42]
Se pueden agregar componentes de nutrientes individuales para ajustar con mayor precisión su contenido corporal. Ese nutriente individual puede, si es posible, infundirse individualmente o puede inyectarse en una bolsa de solución nutritiva o líquidos intravenosos ( solución expansora de volumen ) que se administra al paciente.
La administración de componentes individuales puede ser más peligrosa que la administración de soluciones premezcladas tales como las utilizadas en la nutrición parenteral total, porque estas últimas generalmente ya están equilibradas con respecto, por ejemplo, a la osmolaridad y la capacidad de infusión periférica. La administración intravenosa incorrecta de potasio concentrado puede ser letal, pero esto no representa un peligro si el potasio se mezcla en una solución de NPT y se diluye. [43]
Se pueden agregar vitaminas a un nutriente premezclado a granel inmediatamente antes de la administración, ya que las vitaminas adicionales pueden promover el deterioro del producto almacenado. [ cita necesaria ] Las vitaminas se pueden agregar en dos dosis, una soluble en grasa y la otra soluble en agua.También existen preparados monodosis con vitaminas tanto liposolubles como hidrosolubles como Cernevit . [44] [45]
Los minerales y oligoelementos para la nutrición parenteral están disponibles en mezclas preparadas, como Addaven . [46]
Sin embargo, estos componentes adicionales en la nutrición parenteral estuvieron sujetos a controles de estabilidad, ya que afectan en gran medida la estabilidad de las emulsiones lipídicas que sirven como base para estas formulaciones. Los estudios han demostrado diferencias en las estabilidades físicas y químicas de estas soluciones de nutrición parenteral total, [47] [48] [49], lo que influye en gran medida en la fabricación farmacéutica de estas mezclas.
Sólo un número limitado de emulsionantes se consideran comúnmente seguros para la administración parenteral, de los cuales el más importante es la lecitina . [ cita médica necesaria ] La lecitina se puede biodegradar y metabolizar, ya que es una parte integral de las membranas biológicas, lo que la hace prácticamente no tóxica. Otros emulsionantes solo pueden excretarse a través de los riñones, [ cita necesaria ] creando una carga tóxica. El emulsionante elegido para la mayoría de las emulsiones grasas utilizadas para la nutrición parenteral es una lecitina de huevo altamente purificada, [50] debido a su baja toxicidad y su completa integración con las membranas celulares.
No se recomienda el uso de emulsionantes derivados del huevo a personas alérgicas al huevo debido al riesgo de reacción. En situaciones en las que no existe un agente emulsionante adecuado para una persona con riesgo de desarrollar una deficiencia de ácidos grasos esenciales, los aceites de cocina pueden esparcirse sobre grandes porciones de piel disponible para complementarlos mediante absorción transdérmica. [51]
Otro tipo de emulsión grasa Omegaven se está utilizando de forma experimental en los EE. UU. principalmente en la población pediátrica. Está hecho de aceite de pescado en lugar de las fórmulas a base de aceite de soja que se utilizan más ampliamente. Las investigaciones han demostrado que el uso de Omegaven puede revertir y prevenir enfermedades hepáticas y colestasis. [52]
Desarrollado en la década de 1960 por el Dr. Stanley Dudrick , quien como residente de cirugía en la Universidad de Pensilvania, trabajando en el laboratorio de ciencias básicas del Dr. Jonathan Rhoads, fue el primero en alimentar con éxito inicialmente a cachorros Beagle y posteriormente a bebés recién nacidos con catastróficas neoplasias gastrointestinales. . [53] El Dr. Dudrick colaboró con el Dr. Willmore y el Dr. Vars para completar el trabajo necesario para que esta técnica nutricional sea segura y exitosa. [54]
En 2019, el Reino Unido experimentó una grave escasez de bolsas TPN debido a las restricciones de seguridad en el único sitio de fabricación, operado por Calea. El Servicio Nacional de Salud calificó la situación de emergencia. [55]