La estenosis aórtica ( EA o AoS ) es el estrechamiento de la salida del ventrículo izquierdo del corazón (donde comienza la aorta ), de tal manera que se producen problemas. [1] Puede ocurrir en la válvula aórtica , así como por encima y por debajo de este nivel. [1] Por lo general, empeora con el tiempo. [1] Los síntomas a menudo aparecen gradualmente y a menudo ocurre primero una disminución de la capacidad para hacer ejercicio. [1] Si se produce insuficiencia cardíaca , pérdida del conocimiento o dolor en el pecho relacionado con el corazón debido a la EA, los resultados son peores. [1] La pérdida del conocimiento generalmente ocurre al estar de pie o haciendo ejercicio. [1] Los signos de insuficiencia cardíaca incluyen dificultad para respirar, especialmente al acostarse , por la noche o al hacer ejercicio, e hinchazón de las piernas . [1] El engrosamiento de la válvula sin causar obstrucción se conoce como esclerosis aórtica . [1]
Las causas incluyen nacer con una válvula aórtica bicúspide y fiebre reumática ; Una válvula normal también puede endurecerse con el paso de las décadas debido a la calcificación . [2] [1] Una válvula aórtica bicúspide afecta aproximadamente al uno o dos por ciento de la población. [1] A partir de 2014, las enfermedades cardíacas reumáticas ocurren principalmente en el mundo en desarrollo . [1] Los factores de riesgo son similares a los de la enfermedad de las arterias coronarias e incluyen fumar , presión arterial alta , colesterol alto , diabetes y ser hombre. [1] La válvula aórtica generalmente tiene tres valvas y está ubicada entre el ventrículo izquierdo del corazón y la aorta. [1] La AS generalmente resulta en un soplo cardíaco . [1] Su gravedad se puede dividir en leve, moderada, grave y muy grave, distinguible mediante ecografía del corazón . [1]
La estenosis aórtica generalmente se sigue mediante ecografías repetidas. [1] Una vez que se ha vuelto grave, el tratamiento implica principalmente la cirugía de reemplazo valvular , siendo el reemplazo valvular aórtico transcatéter (TAVR) una opción en algunas personas que tienen un alto riesgo de cirugía. [1] Las válvulas pueden ser mecánicas o bioprotésicas , y cada una tiene riesgos y beneficios. [1] Otro procedimiento menos invasivo, la valvuloplastia aórtica con balón (BAV), puede resultar beneficioso, pero solo durante unos meses. [1] Las complicaciones como la insuficiencia cardíaca se pueden tratar de la misma manera que en aquellos con EA leve a moderada. [1] En aquellos con enfermedad grave se deben evitar varios medicamentos, incluidos los inhibidores de la ECA , la nitroglicerina y algunos betabloqueantes . [1] Se puede utilizar nitroprusiato o fenilefrina en personas con insuficiencia cardíaca descompensada dependiendo de la presión arterial. [1] [3]
La estenosis aórtica es la valvulopatía cardíaca más común en el mundo desarrollado . [4] Afecta aproximadamente al 2% de las personas mayores de 65 años. [1] Las tasas estimadas no se conocían en la mayor parte del mundo en desarrollo en 2014. [5] En aquellos que tienen síntomas, sin reparación, la probabilidad de muerte a los cinco años es aproximadamente del 50% y a los 10 años es aproximadamente del 90%. [1] La estenosis aórtica fue descrita por primera vez por el médico francés Lazare Rivière en 1663. [6]
Los síntomas relacionados con la estenosis aórtica dependen del grado de estenosis. La mayoría de las personas con estenosis aórtica de leve a moderada no presentan síntomas. Los síntomas generalmente se presentan en personas con estenosis aórtica grave, aunque también pueden ocurrir en personas con estenosis aórtica leve a moderada. Los tres síntomas principales de la estenosis aórtica son pérdida del conocimiento , dolor anginoso en el pecho y dificultad para respirar con la actividad u otros síntomas de insuficiencia cardíaca como dificultad para respirar al estar acostado , episodios de dificultad para respirar durante la noche o piernas y pies hinchados . [4] [7] También puede ir acompañado de la apariencia de palidez característica de la " porcelana de Dresde " con un ligero rubor . [8] [ se necesita aclaración ]
La angina en el contexto de insuficiencia cardíaca también aumenta el riesgo de muerte. En personas con angina, la tasa de mortalidad a 5 años es del 50% si no se reemplaza la válvula aórtica. [9]
La angina en el contexto de la EA se produce debido a la hipertrofia ventricular izquierda (HVI) que es causada por la producción constante de aumento de presión necesario para superar el gradiente de presión causado por la EA. Mientras que la capa muscular del ventrículo izquierdo se espesa, las arterias que irrigan el músculo no se alargan ni crecen significativamente, por lo que es posible que el músculo no reciba suficiente suministro de sangre para satisfacer sus necesidades de oxígeno. Esta isquemia puede ser evidente por primera vez durante el ejercicio, cuando el músculo cardíaco requiere un mayor suministro de sangre para compensar el aumento de la carga de trabajo. El individuo puede quejarse de dolor torácico anginoso con el esfuerzo. Las pruebas de esfuerzo con o sin imágenes están estrictamente contraindicadas en pacientes sintomáticos con estenosis aórtica grave. Las guías actuales recomiendan ahora la prueba de esfuerzo en pacientes asintomáticos y puede proporcionar un valor pronóstico incremental. [10]
Sin embargo, con el tiempo, el músculo cardíaco necesitará más suministro de sangre en reposo del que pueden suministrar las ramas de las arterias coronarias . En este punto puede haber signos de patrón de tensión ventricular (depresión del segmento ST e inversión de la onda T) en el ECG , lo que sugiere isquemia subendocárdica. El subendocardio es la región más susceptible a la isquemia porque es la más alejada de las arterias coronarias epicárdicas. [11]
El síncope (desmayos) debido a la estenosis de la válvula aórtica suele ser causado por el esfuerzo. [4] [12] En el caso de insuficiencia cardíaca, aumenta el riesgo de muerte. En personas con síncope, la tasa de mortalidad a tres años es del 50% si no se reemplaza la válvula aórtica. [13]
No está claro por qué la estenosis aórtica causa síncope. Una teoría es que la EA grave produce un gasto cardíaco casi fijo . [14] Cuando una persona con estenosis aórtica hace ejercicio, su resistencia vascular periférica disminuirá a medida que los vasos sanguíneos de los músculos esqueléticos se dilatan para permitir que los músculos reciban más sangre y puedan realizar más trabajo. Esta disminución de la resistencia vascular periférica normalmente se compensa con un aumento del gasto cardíaco. Dado que las personas con EA grave no pueden aumentar su gasto cardíaco, la presión arterial cae y la persona se desmayará debido a la disminución de la perfusión sanguínea al cerebro . [15]
Una segunda teoría es que durante el ejercicio las altas presiones generadas en el ventrículo izquierdo hipertrofiado provocan una respuesta vasodepresora, que provoca una vasodilatación periférica secundaria que, a su vez, provoca una disminución del flujo sanguíneo al cerebro resultando en la pérdida del conocimiento. De hecho, en la estenosis aórtica, debido a la obstrucción fija del flujo sanguíneo que sale del corazón, puede resultar imposible que el corazón aumente su gasto para compensar la vasodilatación periférica. [ cita necesaria ]
A veces puede estar operativo un tercer mecanismo. Debido a la hipertrofia del ventrículo izquierdo en la estenosis aórtica, incluida la consiguiente incapacidad de las arterias coronarias para suministrar sangre adecuadamente al miocardio (ver "Angina" a continuación), se pueden desarrollar ritmos cardíacos anormales . Estos pueden provocar un síncope. [dieciséis]
Finalmente, al menos en la estenosis aórtica calcificada [17] [18] , la calcificación dentro y alrededor de la válvula aórtica puede progresar y extenderse hasta afectar el sistema de conducción eléctrica del corazón . Si eso ocurre, el resultado puede ser un bloqueo cardíaco , una condición potencialmente letal de la cual el síncope puede ser un síntoma. [ cita necesaria ]
La insuficiencia cardíaca congestiva (ICC) conlleva un pronóstico grave en personas con EA. Las personas con ICC atribuible a EA tienen una tasa de mortalidad a 2 años del 50% si no se reemplaza la válvula aórtica. [ cita necesaria ] La insuficiencia cardíaca congestiva en el contexto de la EA se debe a una combinación de hipertrofia ventricular izquierda con fibrosis, disfunción sistólica (una disminución en la fracción de eyección ) y disfunción diastólica (presión de llenado elevada del VI). [4]
En el síndrome de Heyde , la estenosis aórtica se asocia con hemorragia gastrointestinal debido a angiodisplasia del colon . [19] Investigaciones recientes han demostrado que la estenosis causa una forma de enfermedad de von Willebrand al descomponer su factor de coagulación asociado ( antígeno asociado al factor VIII , también llamado factor von Willebrand ), [20] debido al aumento de la turbulencia alrededor de la válvula estenótica.
A pesar de lo anterior [ se necesita aclaración ] , la Asociación Estadounidense del Corazón cambió sus recomendaciones con respecto a la profilaxis antibiótica para la endocarditis . Específicamente, a partir de 2007 se recomienda que dicha profilaxis se limite únicamente a aquellos con prótesis valvulares cardíacas, aquellos con episodios previos de endocarditis y aquellos con ciertos tipos de cardiopatías congénitas. [21]
Dado que la válvula aórtica estenosada puede limitar el gasto del corazón, las personas con estenosis aórtica corren el riesgo de sufrir síncope y presión arterial peligrosamente baja si usan cualquiera de varios medicamentos para enfermedades cardiovasculares que a menudo coexisten con la estenosis aórtica. Los ejemplos incluyen nitroglicerina , nitratos , inhibidores de la ECA , terazosina (Hytrin) e hidralazina . Tenga en cuenta que todas estas sustancias provocan vasodilatación periférica . En circunstancias normales, en ausencia de estenosis aórtica, el corazón puede aumentar su gasto y así contrarrestar el efecto de los vasos sanguíneos dilatados. Sin embargo, en algunos casos de estenosis aórtica, debido a la obstrucción del flujo sanguíneo que sale del corazón causada por la válvula aórtica estenosada, no se puede aumentar el gasto cardíaco . Puede producirse presión arterial baja o síncope. [ cita necesaria ]

La estenosis aórtica es causada más comúnmente por enfermedad valvular aórtica calcificada progresiva (CAVD) relacionada con la edad (>50% de los casos), con una edad promedio de 65 a 70 años. CAVD es la acumulación de calcio en las cúspides de la válvula y esta calcificación provoca endurecimiento y estenosis de la válvula. [22] Otra causa importante de estenosis aórtica es la calcificación de una válvula aórtica bicúspide congénita o, más raramente, de una válvula aórtica unicúspide congénita. Las personas con válvulas aórticas unicúspides suelen necesitar intervención cuando son muy jóvenes, a menudo recién nacidos. Mientras que aquellos con válvula aórtica bicúspide congénita representan entre el 30% y el 40% de los que se presentan durante la edad adulta [23] y, por lo general, se presentan antes (entre 40 y 50 años o más) que aquellos con válvula aórtica tricúspide (65+). [7]
La fiebre reumática aguda posinflamatoria es la causa de menos del 10% de los casos. [24] Las causas raras de estenosis aórtica incluyen la enfermedad de Fabry , el lupus eritematoso sistémico , la enfermedad de Paget , los niveles elevados de ácido úrico en sangre y la infección . [25]

La válvula aórtica humana normalmente consta de tres cúspides o valvas y tiene una abertura de 3,0 a 4,0 centímetros cuadrados. [6] [25] Cuando el ventrículo izquierdo se contrae, fuerza la sangre a través de la válvula hacia la aorta y posteriormente al resto del cuerpo. Cuando el ventrículo izquierdo se expande nuevamente, la válvula aórtica se cierra e impide que la sangre de la aorta fluya hacia atrás ( regurgitación ) hacia el ventrículo izquierdo. En la estenosis aórtica, la abertura de la válvula aórtica se estrecha o se contrae ( estenótica ) (p. ej., debido a la calcificación). La estenosis aórtica degenerativa (la variedad más común) y bicúspide comienzan con daño a las células endoteliales debido a un aumento del estrés mecánico. [7] [25] Se cree que la inflamación está involucrada en las primeras etapas de la patogénesis de la EA y se sabe que sus factores de riesgo asociados promueven la deposición de colesterol LDL y lipoproteína (a) , una sustancia altamente dañina, en la válvula aórtica. , provocando daños importantes y estenosis con el tiempo. [7] [25] Se produce una infiltración de células inflamatorias (macrófagos, linfocitos T), seguida de la liberación de mediadores inflamatorios como la interleucina-1-beta y el factor de crecimiento transformante beta-1. Posteriormente, los fibroblastos se diferencian en células similares a los osteoblastos, lo que da como resultado un depósito anormal de matriz ósea que conduce a una calcificación y estenosis valvular progresiva. [26]
Como consecuencia de esta estenosis, el ventrículo izquierdo debe generar una presión más alta con cada contracción para hacer avanzar la sangre de manera efectiva hacia la aorta. [4] [27] Inicialmente, el VI genera este aumento de presión engrosando sus paredes musculares (hipertrofia miocárdica). El tipo de hipertrofia que se observa con mayor frecuencia en la EA se conoce como hipertrofia concéntrica, [4] en la que las paredes del VI están (aproximadamente) igualmente engrosadas.
En las últimas etapas, el ventrículo izquierdo se dilata, la pared se adelgaza y la función sistólica se deteriora (lo que da como resultado una capacidad deficiente para bombear sangre hacia adelante). Morris e Innasimuthu et al. demostró que una anatomía coronaria diferente se asocia con diferentes enfermedades valvulares. En 2010 se estaban realizando investigaciones para ver si una anatomía coronaria diferente podría provocar un flujo turbulento a nivel de las válvulas, lo que provocaría inflamación y degeneración. [28] [29] [30]
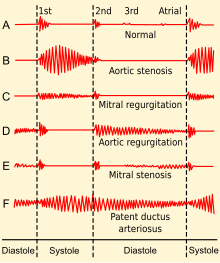

La estenosis aórtica se diagnostica con mayor frecuencia cuando es asintomática y, a veces, puede detectarse durante un examen de rutina del corazón y del sistema circulatorio. Existe buena evidencia que demuestra que ciertas características del pulso periférico pueden influir en el diagnóstico. [31] En particular, puede haber un ascenso lento y/o sostenido del pulso arterial, y el pulso puede ser de bajo volumen. Esto a veces se denomina pulso parvus et tardus . [12] [24] También puede haber un retraso notable entre el primer ruido cardíaco (en la auscultación ) y el pulso correspondiente en la arteria carótida ("retraso apical-carótida"). De manera similar, puede haber un retraso entre la aparición de cada pulso en la arteria braquial (en el brazo) y la arteria radial (en la muñeca). [ cita necesaria ]
El primer ruido cardíaco puede ir seguido de un sonido de expulsión agudo ("clic de expulsión") que se escucha mejor en el borde esternal inferior izquierdo y en el ápice y, por lo tanto, parece estar "dividido". El sonido de eyección, causado por el impacto del flujo de salida del ventrículo izquierdo contra las valvas de la válvula aórtica parcialmente fusionadas, se asocia más comúnmente con una válvula aórtica bicúspide móvil que con una válvula aórtica calcificada inmóvil. La intensidad de este sonido no varía con la respiración, lo que ayuda a distinguirlo del clic de eyección producido por una válvula pulmonar estenótica, que disminuirá ligeramente en intensidad durante la inspiración. [32]
Un soplo sistólico , crescendo-decrescendo (es decir, de 'eyección'), fácilmente audible, se escucha con mayor intensidad en el borde esternal superior derecho, en el segundo espacio intercostal derecho , [24] y se irradia a las arterias carótidas bilateralmente. [4] [12] El soplo aumenta al ponerse en cuclillas y disminuye al estar de pie y con la contracción muscular isométrica, como la maniobra de Valsalva , que ayuda a distinguirlo de la miocardiopatía hipertrófica obstructiva (MCHO). El soplo es más fuerte durante la espiración pero también se escucha fácilmente durante la inspiración. Cuanto más grave es el grado de estenosis, más tarde se produce el pico en el crescendo-decrescendo del soplo. [33]
El segundo ruido cardíaco ( A 2 ) tiende a disminuir y suavizarse a medida que la estenosis aórtica se vuelve más grave. [24] Esto es el resultado de la creciente calcificación de la válvula, lo que impide que se "cierre de golpe" y produzca un sonido fuerte y agudo. Debido al aumento de la presión del ventrículo izquierdo debido a la válvula aórtica estenótica, con el tiempo el ventrículo puede hipertrofiarse, lo que provoca disfunción diastólica. Como resultado, puede haber un cuarto ruido cardíaco debido a la rigidez del ventrículo. [12] Con aumentos continuos en la presión ventricular, se producirá dilatación del ventrículo y puede manifestarse un tercer ruido cardíaco. [34]
Finalmente, la estenosis aórtica suele coexistir con algún grado de insuficiencia aórtica ( insuficiencia aórtica ). Por lo tanto, el examen físico en la estenosis aórtica también puede revelar signos de esta última, por ejemplo, un soplo diastólico decrescendo temprano. De hecho, cuando ambas anomalías valvulares están presentes, los hallazgos esperados de cualquiera de ellas pueden modificarse o incluso pueden no estar presentes. Más bien, surgen nuevos signos que reflejan la presencia simultánea de estenosis e insuficiencia aórtica, por ejemplo, pulso bisferiens . [ cita necesaria ]
Según un metanálisis , los hallazgos más útiles para determinar la estenosis aórtica en el entorno clínico fueron la lenta tasa de aumento del pulso carotídeo ( el índice de probabilidad positivo osciló entre 2,8 y 130 en todos los estudios), la intensidad máxima media y tardía del soplo ( índice de probabilidad positivo, 8,0–101) y disminución de la intensidad del segundo ruido cardíaco (índice de probabilidad positivo, 3,1–50). [31]
Otros signos periféricos incluyen: [ cita necesaria ]
Para la estenosis valvular aórtica grave asintomática, las directrices europeas [35] recomiendan mediciones del péptido natriurético tipo B ( BNP ) para ayudar a la estratificación del riesgo y optimizar el momento de la cirugía de reemplazo de la válvula aórtica . [36] [37] En pacientes con estenosis valvular aórtica asintomática no grave, el aumento de los niveles de péptido natriurético procerebral N-terminal ajustado por edad y sexo ( NT-proBNP ) solo y combinado con un aumento de 50 % o más respecto del valor inicial tuvo Se ha encontrado asociación con mayores tasas de eventos relacionados con la estenosis de la válvula aórtica ( muerte cardiovascular , hospitalización con insuficiencia cardíaca debido a la progresión de la estenosis de la válvula aórtica o cirugía de reemplazo de la válvula aórtica ). [38] En pacientes con estenosis valvular aórtica asintomática no grave y sin enfermedad arterial coronaria manifiesta , se encontró que el aumento de troponina T (por encima de 14 pg/mL) se asoció con una mayor tasa de eventos cardíacos isquémicos a 5 años ( infarto de miocardio , intervención coronaria percutánea o cirugía de bypass de arteria coronaria ). [39]
Aunque la estenosis aórtica no produce ningún hallazgo específico en el electrocardiograma (ECG), a menudo provoca una serie de anomalías electrocardiográficas. Las manifestaciones ECG de hipertrofia ventricular izquierda (HVI) son comunes en la estenosis aórtica [7] [12] y surgen como resultado de que la estenosis ha colocado una carga crónica de alta presión en el ventrículo izquierdo (siendo la HVI la respuesta esperada a la presión crónica). cargas en el ventrículo izquierdo sin importar la causa). [40]
Como se señaló anteriormente, el proceso de calcificación que ocurre en la estenosis aórtica puede progresar hasta extenderse más allá de la válvula aórtica y dentro del sistema de conducción eléctrica del corazón . En raras ocasiones, la evidencia de este fenómeno puede incluir patrones de ECG característicos de ciertos tipos de bloqueo cardíaco , como el bloqueo de rama izquierda . [7]
El cateterismo de la cámara cardíaca proporciona un diagnóstico definitivo, que indica una estenosis grave en el área valvular de <1,0 cm 2 (normalmente alrededor de 3 cm 2 ). [41] Puede medir directamente la presión en ambos lados de la válvula aórtica. El gradiente de presión puede utilizarse como punto de decisión para el tratamiento. Es útil en personas sintomáticas antes de la cirugía. [12] El estándar para el diagnóstico de la estenosis aórtica son las pruebas no invasivas con ecocardiografía. El cateterismo cardíaco se reserva para los casos en los que existe discrepancia entre el cuadro clínico y las pruebas no invasivas, debido a los riesgos inherentes al cruce de la válvula aórtica, como el accidente cerebrovascular. [7]
El ecocardiograma (ultrasonido cardíaco) es la mejor forma no invasiva de evaluar la anatomía y función de la válvula aórtica. [42]
El área de la válvula aórtica se puede calcular de forma no invasiva utilizando velocidades de flujo ecocardiográficas. Utilizando la velocidad de la sangre a través de la válvula, el gradiente de presión a través de la válvula se puede calcular mediante la ecuación de continuidad o utilizando la ecuación de Bernoulli modificada :
Gradiente = 4(velocidad)² mmHg
Una válvula aórtica normal tiene un gradiente de sólo unos pocos mmHg. Una disminución del área valvular provoca un aumento del gradiente de presión, y estos parámetros se utilizan para clasificar y graduar la estenosis aórtica como leve, moderada o grave. El gradiente de presión puede ser anormalmente bajo en presencia de estenosis mitral , insuficiencia cardíaca , insuficiencia aórtica coexistente y también cardiopatía isquémica (enfermedad relacionada con la disminución del suministro de sangre y oxígeno que causa isquemia). [43]
El ecocardiograma también puede mostrar hipertrofia del ventrículo izquierdo, válvula aórtica engrosada e inmóvil y raíz aórtica dilatada. [12] Sin embargo, puede parecer engañosamente normal en casos agudos. [24]
Una radiografía de tórax también puede ayudar en el diagnóstico y proporcionar pistas sobre la gravedad de la enfermedad, mostrando el grado de calcificación de la válvula y, en una enfermedad crónica , un ventrículo izquierdo agrandado [12] [24] y la aurícula. [12]
El uso de la puntuación de calcio por TC está ganando difusión como herramienta diagnóstica complementaria a la ecografía en la evaluación de pacientes con estenosis aórtica. [44] [45] La puntuación del calcio de la válvula aórtica mediante tomografía computarizada multidetector (CT-AVC) se utiliza para cuantificar el grado de calcificación de la válvula aórtica. [46] Según las Directrices ESC/EACTS de 2021 para el tratamiento de las valvulopatías cardíacas, los umbrales recomendados que indican estenosis aórtica grave son > 1200 AU en mujeres y > 2000 AU en hombres. [47]
Por lo general, el tratamiento no es necesario en personas sin síntomas. [12] En casos moderados, se realiza una ecocardiografía cada 1 a 2 años para monitorear la progresión, posiblemente complementada con una prueba de esfuerzo cardíaco . [24] En casos graves, la ecocardiografía se realiza cada 3 a 6 meses. [24] Tanto en los casos moderados como en los leves, la persona debe realizar una nueva visita de inmediato o ser admitida para recibir atención hospitalaria si aparece algún síntoma nuevo relacionado. [24] Actualmente no existen opciones terapéuticas disponibles para tratar a las personas con estenosis de la válvula aórtica; sin embargo, estudios realizados en 2014 indicaron que la enfermedad se produce como resultado de procesos celulares activos, lo que sugiere que abordar estos procesos puede conducir a enfoques terapéuticos viables. [48]
Los estudios observacionales demostraron una asociación entre la reducción del colesterol con estatinas y la disminución de la progresión, pero un ensayo clínico aleatorizado publicado en 2005 no logró encontrar ningún efecto sobre la estenosis aórtica calcificada. El efecto de las estatinas sobre la progresión de la EA no está claro. Un estudio de 2007 encontró una desaceleración de la estenosis aórtica con rosuvastatina . [7] [49] En 2013 se informó que los ensayos no mostraron ningún beneficio en la desaceleración de la progresión de la EA, [7] pero sí demostraron una disminución en los eventos cardiovasculares isquémicos. [4]
En general, el tratamiento médico tiene una eficacia relativamente pobre en el tratamiento de la estenosis aórtica. [12] Sin embargo, puede ser útil para controlar afecciones comúnmente coexistentes que se correlacionan con la estenosis aórtica: [50]
La reparación de la válvula aórtica o reconstrucción de la válvula aórtica describe la reconstrucción tanto de la forma como de la función de la válvula aórtica nativa y disfuncional. Se aplica con mayor frecuencia para el tratamiento de la insuficiencia aórtica. También puede resultar necesario para el tratamiento de un aneurisma aórtico y, con menos frecuencia, de una estenosis aórtica congénita. [53]
En los adultos, la estenosis aórtica grave sintomática suele requerir reemplazo de la válvula aórtica (AVR). [4] Si bien la AVR quirúrgica sigue siendo el tratamiento más eficaz para este proceso patológico y actualmente se recomienda para los pacientes después de la aparición de los síntomas, a partir de 2016 [actualizar]los enfoques de reemplazo de la válvula aórtica incluían cirugía a corazón abierto, cirugía cardíaca mínimamente invasiva (MICS) y Reemplazo de válvula aórtica mediante catéter mínimamente invasivo (percutáneo). [54] [55] [56] Sin embargo, el reemplazo quirúrgico de la válvula aórtica está bien estudiado y, en general, tiene un pronóstico a largo plazo bueno y bien establecido. [57]
Una válvula aórtica enferma se reemplaza más comúnmente mediante un procedimiento quirúrgico con una válvula mecánica o de tejido. El procedimiento se realiza mediante un procedimiento quirúrgico a corazón abierto o, en un número cada vez menor pero creciente de casos, mediante un procedimiento de cirugía cardíaca mínimamente invasiva (MICS). [ cita necesaria ] El abordaje mínimamente invasivo mediante minitoracotomía derecha es más beneficioso en pacientes de alto riesgo, como los ancianos, los obesos, aquellos con enfermedad pulmonar obstructiva crónica, enfermedad renal crónica y aquellos que requieren cirugía reoperatoria. [58] [59]
En todo el mundo, más de 250.000 personas han recibido una intervención valvular aórtica transcatéter (TAVI). Para las personas que no son candidatas a un reemplazo valvular quirúrgico y la mayoría de los pacientes mayores de 75 años, el TAVI puede ser una alternativa adecuada. [54] [55] Las anomalías de la conducción que requieren la implantación de un marcapasos permanente (MPP) siguen siendo un hallazgo común después del TAVI debido a la estrecha proximidad del sistema de conducción auriculoventricular a la raíz aórtica. [60]
Para bebés y niños, la valvuloplastia con balón , en la que se infla un globo para estirar la válvula y permitir un mayor flujo, también puede ser eficaz. En los adultos, sin embargo, generalmente es ineficaz, ya que la válvula tiende a volver a un estado estenosado. El cirujano hará una pequeña incisión en la parte superior de la pierna de la persona y procederá a insertar el globo en la arteria. Luego, el globo se hace avanzar hasta la válvula y se infla para estirar la válvula y abrirla. [61]
La insuficiencia cardíaca aguda descompensada debido a AS puede tratarse temporalmente con un balón de contrapulsación intraaórtico mientras se espera la cirugía. [62] En personas con presión arterial alta, el nitroprusiato se puede utilizar con precaución. [1] La fenilefrina se puede utilizar en personas con presión arterial muy baja. [3]
Si no se trata, la estenosis aórtica sintomática grave conlleva un mal pronóstico, con una tasa de mortalidad a 2 años del 50-60% y una tasa de supervivencia a 3 años inferior al 30%. [63] El pronóstico después del reemplazo de la válvula aórtica para personas menores de 65 años es aproximadamente cinco años menor que el de la población general; para las personas mayores de 65 años es más o menos lo mismo. [57]
Aproximadamente el 2 % de las personas mayores de 65 años, el 3 % de las personas mayores de 75 años [4] y el 4 % de las personas mayores de 85 años tienen estenosis de la válvula aórtica. [64] La prevalencia está aumentando con el envejecimiento de la población en América del Norte y Europa. [sesenta y cinco]
Los factores de riesgo que se sabe que influyen en la progresión de la enfermedad de EA incluyen factores similares a los de la enfermedad de las arterias coronarias, como hipertensión, edad avanzada, ser hombre, hiperlipidemia , diabetes mellitus , tabaquismo, síndrome metabólico y enfermedad renal terminal . [4] [7] [25]
La estenosis aórtica fue descrita por primera vez por el médico francés Lazare Rivière en 1663. [6]
En un estudio de 2010 se descubrió que las personas que tomaban bifosfonatos tenían menos progresión de la estenosis aórtica y algunas retrocedían. [66] [67] Este hallazgo dio lugar a múltiples ensayos, en curso a partir de 2012 [actualizar]. Las investigaciones posteriores no pudieron confirmar el resultado positivo inicial. [68]
{{cite journal}}: Mantenimiento CS1: nombres numéricos: lista de autores ( enlace )