
En mecánica cuántica , el número cuántico azimutal ℓ es un número cuántico para un orbital atómico que determina su momento angular orbital y describe aspectos de la forma angular del orbital. El número cuántico azimutal es el segundo de un conjunto de números cuánticos que describen el estado cuántico único de un electrón (los otros son el número cuántico principal n , el número cuántico magnético m ℓ y el número cuántico de espín m s ).
Para un valor dado del número cuántico principal n ( capa electrónica ), los valores posibles de ℓ son los números enteros de 0 a n − 1. Por ejemplo, la capa n = 1 tiene solo orbitales con , y la capa n = 2 tiene solo orbitales con , y .
Para un valor dado del número cuántico azimutal ℓ , los valores posibles del número cuántico magnético m ℓ son los números enteros desde m ℓ =-ℓ hasta m ℓ =+ℓ , incluido el 0. Además, el número cuántico de espín m s puede tomar dos valores distintos. El conjunto de orbitales asociados con un valor particular de ℓ a veces se denomina colectivamente subcapa .
Aunque originalmente se utilizaban solo para átomos aislados, los orbitales de tipo atómico desempeñan un papel fundamental en la configuración de los electrones en compuestos como gases, líquidos y sólidos. El número cuántico ℓ desempeña un papel importante en este sentido a través de la conexión con la dependencia angular de los armónicos esféricos para los diferentes orbitales alrededor de cada átomo.
El término "número cuántico azimutal" fue introducido por Arnold Sommerfeld en 1915 [1] : II:132 como parte de una descripción ad hoc de la estructura energética de los espectros atómicos. Solo más tarde, con el modelo cuántico del átomo, se entendió que este número, ℓ , surge de la cuantización del momento angular orbital. Algunos libros de texto [2] : 199 y la norma ISO 80000-10:2019 [3] llaman a ℓ el número cuántico del momento angular orbital .
Los niveles de energía de un átomo en un campo magnético externo dependen del valor m ℓ, por lo que a veces se lo denomina número cuántico magnético. [4] : 240
La letra minúscula ℓ se utiliza para indicar el momento angular orbital de una sola partícula. Para un sistema con múltiples partículas, se utiliza la letra mayúscula L. [3]
Hay cuatro números cuánticos ( n , ℓ , m , ℓ y m , s ) relacionados con los estados de energía de los electrones de un átomo aislado. Estos cuatro números especifican el estado cuántico único y completo de cualquier electrón individual en el átomo y se combinan para componer la función de onda del electrón u orbital .
Al resolver para obtener la función de onda, la ecuación de Schrödinger se resuelve en tres ecuaciones que conducen a los tres primeros números cuánticos, lo que significa que las tres ecuaciones están relacionadas entre sí. El número cuántico azimutal surge al resolver la parte polar de la ecuación de onda, basándose en el sistema de coordenadas esféricas , que generalmente funciona mejor con modelos que tienen suficientes aspectos de simetría esférica .
El momento angular de un electrón, L , está relacionado con su número cuántico ℓ mediante la siguiente ecuación: donde ħ es la constante de Planck reducida , L es el operador de momento angular orbital y es la función de onda del electrón. El número cuántico ℓ es siempre un entero no negativo: 0, 1, 2, 3, etc. (Cabe destacar que L no tiene un significado real excepto en su uso como operador de momento angular; por lo tanto, es una práctica estándar utilizar el número cuántico ℓ cuando se hace referencia al momento angular).
Los orbitales atómicos tienen formas distintivas (ver gráfico superior), en las que las letras s , p , d , f , etc. (empleando una convención originada en la espectroscopia ) denotan la forma del orbital atómico . Las funciones de onda de estos orbitales toman la forma de armónicos esféricos , y por eso se describen mediante polinomios de Legendre . Los diversos orbitales relacionados con los diferentes valores (enteros) de ℓ a veces se denominan subcapas (se hace referencia a ellos con letras latinas minúsculas elegidas por razones históricas), como se muestra en la tabla "Subcapas cuánticas para el número cuántico azimutal".
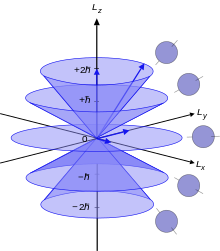
Cada uno de los diferentes estados de momento angular puede tomar 2(2 ℓ + 1) electrones. Esto se debe a que el tercer número cuántico m ℓ (que puede considerarse libremente como la proyección cuantizada del vector de momento angular en el eje z) va de − ℓ a ℓ en unidades enteras, y por lo tanto hay 2 ℓ + 1 estados posibles. Cada orbital distinto n , ℓ , m ℓ puede ser ocupado por dos electrones con espines opuestos (dados por el número cuántico m s = ± 1 ⁄ 2 ), lo que da 2(2 ℓ + 1) electrones en total. Los orbitales con ℓ más altos que los dados en la tabla son perfectamente permisibles, pero estos valores cubren todos los átomos descubiertos hasta ahora.
Para un valor dado del número cuántico principal n , los valores posibles de ℓ varían de 0 a n − 1 ; por lo tanto, la capa n = 1 solo posee una subcapa s y solo puede tomar 2 electrones, la capa n = 2 posee una subcapa s y una p y puede tomar 8 electrones en total, la capa n = 3 posee subcapas s , p y d y tiene un máximo de 18 electrones, y así sucesivamente.
Un modelo simplista de un electrón da como resultado niveles de energía que dependen únicamente del número principal. En átomos más complejos, estos niveles de energía se dividen para todos los n > 1 , colocando los estados de ℓ más altos por encima de los estados de ℓ más bajos . Por ejemplo, la energía de 2p es mayor que la de 2s, 3d ocurre más alta que 3p, que a su vez está por encima de 3s, etc. Este efecto finalmente forma la estructura de bloques de la tabla periódica. Ningún átomo conocido posee un electrón que tenga ℓ mayor que tres ( f ) en su estado fundamental .
El número cuántico de momento angular, ℓ, y el armónico esférico correspondiente determinan el número de nodos planos que pasan por el núcleo. Un nodo plano se puede describir en una onda electromagnética como el punto medio entre la cresta y el valle, que tiene magnitudes cero. En un orbital s, ningún nodo pasa por el núcleo, por lo tanto, el número cuántico azimutal correspondiente ℓ toma el valor de 0. En un orbital p , un nodo atraviesa el núcleo y, por lo tanto, ℓ tiene el valor de 1. tiene el valor .
Dependiendo del valor de n , existe un número cuántico de momento angular ℓ y la siguiente serie. Las longitudes de onda que se indican corresponden a un átomo de hidrógeno :
Dado un momento angular total cuantificado que es la suma de dos momentos angulares cuantificados individuales y , el número cuántico asociado con su magnitud puede variar de a en pasos enteros, donde y son números cuánticos correspondientes a las magnitudes de los momentos angulares individuales.

Debido a la interacción espín-órbita en un átomo, el momento angular orbital ya no conmuta con el hamiltoniano , ni tampoco lo hace el espín . Por lo tanto, estos cambian con el tiempo. Sin embargo, el momento angular total J sí conmuta con el hamiltoniano de un electrón y, por lo tanto, es constante. J se define como L siendo el momento angular orbital y S el espín. El momento angular total satisface las mismas relaciones de conmutación que el momento angular orbital , es decir, de lo que se deduce que donde J i representa J x , J y y J z .
Los números cuánticos que describen el sistema, que son constantes en el tiempo, son ahora j y m j , definidos a través de la acción de J sobre la función de onda.
De modo que j está relacionado con la norma del momento angular total y m j con su proyección a lo largo de un eje especificado. El número j tiene una importancia particular para la química cuántica relativista , ya que a menudo aparece en subíndice en para estados más profundos cerca del núcleo para los que el acoplamiento espín-órbita es importante.
Al igual que con cualquier momento angular en mecánica cuántica , la proyección de J a lo largo de otros ejes no se puede codefinir con J z , porque no conmutan. Los vectores propios de j , s , m j y paridad, que también son vectores propios del hamiltoniano, son combinaciones lineales de los vectores propios de ℓ , s , m ℓ y m s .

Los números cuánticos de momento angular se refieren estrictamente a átomos aislados. Sin embargo, tienen usos más amplios para átomos en sólidos, líquidos o gases. El número cuántico ℓ m corresponde a armónicos esféricos específicos y se usa comúnmente para describir características observadas en métodos espectroscópicos como la espectroscopia de fotoelectrones de rayos X [6] y la espectroscopia de pérdida de energía de electrones [7] (La notación es ligeramente diferente, con la notación de rayos X donde K, L, M se usan para excitaciones fuera de estados electrónicos con ).
Los números cuánticos del momento angular también se utilizan cuando se describen los estados de los electrones en métodos como la teoría funcional de la densidad de Kohn-Sham [8] o con orbitales gaussianos . [9] Por ejemplo, en el silicio , las propiedades electrónicas utilizadas en los dispositivos semiconductores se deben a los estados tipo p con centrado en cada átomo, mientras que muchas propiedades de los metales de transición dependen de los estados tipo d con . [10]
El número cuántico azimutal se tomó del modelo atómico de Bohr y fue postulado por Arnold Sommerfeld . [11] El modelo de Bohr se derivó del análisis espectroscópico de átomos en combinación con el modelo atómico de Rutherford . Se encontró que el nivel cuántico más bajo tenía un momento angular de cero. Las órbitas con momento angular cero se consideraron cargas oscilantes en una dimensión y, por lo tanto, se describieron como órbitas de "péndulo", pero no se encontraron en la naturaleza. [12] En tres dimensiones, las órbitas se vuelven esféricas sin ningún nodo que cruce el núcleo, similar (en el estado de energía más bajo) a una cuerda para saltar que oscila en un gran círculo.