Kuru es un trastorno neurodegenerativo poco común, incurable y fatal que anteriormente era común entre el pueblo Fore de Papúa Nueva Guinea . El kuru es una forma de encefalopatía espongiforme transmisible (EET) causada por la transmisión de proteínas ( priones ) plegadas anormalmente, lo que provoca síntomas como temblores y pérdida de coordinación por neurodegeneración .
El término kuru deriva de la palabra anterior kuria o guria ("sacudir"), [2] debido a los temblores corporales que son un síntoma clásico de la enfermedad. El propio Kúru significa "temblor". [3] También se la conoce como la "enfermedad de la risa" debido a los estallidos de risa patológicos que son un síntoma de la enfermedad. Actualmente se acepta ampliamente que el kuru se transmitió entre los miembros de la tribu Fore de Papua Nueva Guinea a través del canibalismo funerario . Tradicionalmente se cocinaba y comía a los familiares fallecidos, lo que se pensaba que ayudaba a liberar el espíritu de los muertos. [4] Las mujeres y los niños generalmente consumían el cerebro, el órgano en el que se concentraban más los priones infecciosos, lo que permitía la transmisión del kuru. Por tanto, la enfermedad era más prevalente entre mujeres y niños.
La epidemia probablemente comenzó cuando un aldeano desarrolló la enfermedad de Creutzfeldt-Jakob esporádica y murió. Cuando los aldeanos comieron el cerebro, contrajeron la enfermedad y luego la transmitieron a otros aldeanos que comieron sus cerebros infectados. [5]
Si bien el pueblo Fore dejó de consumir carne humana a principios de la década de 1960, cuando se especuló por primera vez que se transmitía mediante endocanibalismo , la enfermedad persistió debido al largo período de incubación del kuru , de entre 10 y más de 50 años. [6] La epidemia finalmente disminuyó drásticamente después de medio siglo, de 200 muertes por año en 1957 a ninguna muerte desde al menos 2010 en adelante, y las fuentes no están de acuerdo sobre si la última víctima conocida de kuru murió en 2005 o 2009. [7] [8 ] [9] [10]
Kuru, una encefalopatía espongiforme transmisible, es una enfermedad del sistema nervioso que causa efectos fisiológicos y neurológicos que finalmente conducen a la muerte. Se caracteriza por una ataxia cerebelosa progresiva , o pérdida de coordinación y control sobre los movimientos musculares. [11] [12]
La fase preclínica o asintomática , también llamada período de incubación, dura en promedio entre 10 y 13 años, pero puede durar tan solo cinco y se estima que dura hasta 50 años o más después de la exposición inicial. [13]
La etapa clínica, que comienza con la aparición de los primeros síntomas, dura una media de 12 meses. La progresión clínica del kuru se divide en tres etapas específicas: la etapa ambulante, la sedentaria y la terminal. Si bien existe cierta variación en estas etapas de un individuo a otro, están altamente conservadas entre la población afectada. [11] Antes de la aparición de los síntomas clínicos, un individuo también puede presentar síntomas prodrómicos que incluyen dolor de cabeza y dolor en las articulaciones de las piernas. [14]
En la etapa ambulante, el individuo infectado puede presentar una postura y un andar inestables, disminución del control muscular, dificultad para pronunciar palabras ( disartria ) y temblores ( titubación ). Esta etapa se denomina ambulante porque el individuo todavía puede caminar a pesar de los síntomas. [14]
En la fase sedentaria, el individuo infectado es incapaz de caminar sin apoyo y experimenta ataxia y temblores intensos. Además, el individuo muestra signos de inestabilidad emocional y depresión, pero exhibe risas incontroladas y esporádicas. A pesar de los demás síntomas neurológicos, los reflejos tendinosos todavía están intactos en esta etapa de la enfermedad. [14]
En la etapa terminal, los síntomas existentes del individuo infectado, como la ataxia, progresan hasta el punto en que ya no es posible sentarse sin apoyo. También surgen nuevos síntomas: el individuo desarrolla disfagia , que puede conducir a una desnutrición grave, y también puede volverse incontinente, perder la capacidad o la voluntad de hablar y dejar de responder a su entorno a pesar de mantener la conciencia. [14] Hacia el final de la etapa terminal, los pacientes a menudo desarrollan heridas ulceradas en decúbito crónicas que pueden infectarse fácilmente. Una persona infectada generalmente muere entre tres meses y dos años después de los primeros síntomas de la etapa terminal, a menudo debido a neumonía por aspiración [15] u otras infecciones secundarias . [dieciséis]
Kuru se localiza en gran medida en el pueblo Fore y en las personas con las que se casaron. [17] El pueblo Fore cocinaba y consumía ritualmente partes del cuerpo de los miembros de su familia después de su muerte para incorporar "el cuerpo de la persona muerta en los cuerpos de parientes vivos, ayudando así a liberar el espíritu de los muertos". [18] Debido a que el cerebro es el órgano enriquecido con el prión infeccioso, las mujeres y los niños que consumían cerebro tenían una probabilidad mucho mayor de infectarse que los hombres, que consumían preferentemente músculos. [19]
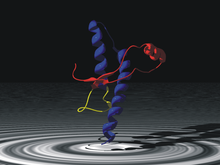

El agente infeccioso es una forma mal plegada de una proteína codificada por el huésped llamada prión (PrP). Las proteínas priónicas están codificadas por el gen de la proteína priónica ( PRNP ). [21] Las dos formas de prión se denominan PrP c , que es una proteína normalmente plegada, y PrP sc , una forma mal plegada que da lugar a la enfermedad. Las dos formas no difieren en su secuencia de aminoácidos; sin embargo, la isoforma patógena PrP sc difiere de la forma normal de PrP c en su estructura secundaria y terciaria. La isoforma PrP sc está más enriquecida en láminas beta , mientras que la forma normal de PrP c está enriquecida en hélices alfa . [19] Las diferencias en conformación permiten que PrP sc se agregue y sea extremadamente resistente a la degradación de proteínas por enzimas o por otros medios químicos y físicos. La forma normal, por el contrario, es susceptible de proteólisis completa y soluble en detergentes no desnaturalizantes. [14]
Se ha sugerido que la PrP sc preexistente o adquirida puede promover la conversión de PrP c en PrP sc , que luego convierte otras PrP c . Esto inicia una reacción en cadena que permite su rápida propagación, lo que resulta en la patogénesis de las enfermedades priónicas. [14]
En 1961, el investigador médico australiano Michael Alpers realizó extensos estudios de campo entre los Fore acompañado por la antropóloga Shirley Lindenbaum . [9] Su investigación histórica sugirió que la epidemia pudo haberse originado alrededor de 1900 a partir de un solo individuo que vivía en el borde del territorio de Fore y que se cree que desarrolló espontáneamente alguna forma de enfermedad de Creutzfeldt-Jakob. [22] La investigación de Alpers y Lindenbaum demostró de manera concluyente que el kuru se propagó fácil y rápidamente entre el pueblo Fore debido a sus prácticas funerarias endocanibalísticas, en las que los familiares consumían los cuerpos de los muertos para devolver la "fuerza vital" de la persona a la aldea, un elemento social Fore. subunidad. [23] Los cadáveres de miembros de la familia a menudo eran enterrados durante días y luego exhumados una vez que los cadáveres eran colonizados por larvas de insectos, momento en el que el cadáver era desmembrado y servido con las larvas como guarnición. [24]
La distribución demográfica evidente en las tasas de infección (el kuru era de ocho a nueve veces más prevalente en mujeres y niños que en hombres en su punto máximo) se debe a que los hombres Fore consideraban consumir carne humana para debilitarlos en tiempos de conflicto o batalla, mientras que las mujeres y Los niños tenían más probabilidades de comerse los cuerpos de los fallecidos, incluido el cerebro, donde se concentraban especialmente las partículas de priones. Además, existe una gran posibilidad de que se transmitiera más fácilmente a mujeres y niños porque asumieron la tarea de limpiar a sus familiares después de la muerte y podrían haber tenido llagas abiertas y cortes en las manos. [19]
Aunque la ingestión de partículas priónicas puede provocar la enfermedad, [25] se producía un alto grado de transmisión si las partículas priónicas podían alcanzar el tejido subcutáneo. Con la eliminación del canibalismo gracias a la aplicación de la ley colonial australiana y los esfuerzos de los misioneros cristianos locales , la investigación de Alpers mostró que el kuru ya estaba disminuyendo entre los Fore a mediados de la década de 1960. Sin embargo, el período medio de incubación de la enfermedad es de 14 años, y se notificaron siete casos con latencias de 40 años o más en aquellos que eran genéticamente más resistentes, y continuaron apareciendo durante varias décadas más. Las fuentes no están de acuerdo sobre si la última persona con kuru murió en 2005 o 2009. [9] [10] [7] [8]
Kuru se diagnostica revisando el historial de signos y síntomas cerebelosos del paciente, realizando exámenes neurológicos y excluyendo otras enfermedades neurológicas durante los exámenes. [15] Los síntomas evaluados suelen ser problemas de coordinación y movimientos musculares involuntarios, pero estos marcadores pueden confundirse con otras enfermedades que afectan el sistema nervioso y muscular; A menudo se requieren exploraciones físicas para diferenciar Kuru de otros trastornos. [26] [27] No existe ninguna prueba de laboratorio para determinar la presencia de Kuru, excepto la evaluación post mortem de los tejidos del sistema nervioso central (SNC), por lo que el diagnóstico se logra eliminando otros posibles trastornos.
El electroencefalograma (EEG) se utiliza para distinguir el kuru de la enfermedad de Creutzfeldt-Jakob, una encefalopatía similar (cualquier enfermedad que afecte la estructura del cerebro). [27] Los EEG buscan actividad eléctrica en el cerebro del paciente y miden la frecuencia de cada onda para determinar si hay un problema con la actividad del cerebro. [28] Los complejos periódicos (PC), patrones recurrentes con complejos pico-onda que ocurren a intervalos, se registran con frecuencia en algunas enfermedades, pero no se presentan en las lecturas de kuru. [29] Se pueden utilizar exámenes y pruebas, como EEG, resonancias magnéticas, análisis de sangre y exploraciones, para determinar si la persona infectada tiene la enfermedad de Kuru u otra encefalopatía. Sin embargo, realizar pruebas durante períodos de tiempo puede resultar difícil.

En 2009, investigadores del Consejo de Investigación Médica descubrieron una variante natural de una proteína priónica en una población de Papua Nueva Guinea que confiere una fuerte resistencia al kuru. En el estudio, que comenzó en 1996, [30] los investigadores evaluaron a más de 3.000 personas de las poblaciones afectadas y circundantes de las tierras altas del este e identificaron una variación en la proteína priónica G127. [31] El polimorfismo G127 es el resultado de una mutación sin sentido y está muy restringido geográficamente a regiones donde la epidemia de kuru fue más extendida. Los investigadores creen que la variante PrnP ocurrió muy recientemente, estimando que el ancestro común más reciente vivió hace 10 generaciones. [31]
Los hallazgos del estudio podrían ayudar a los investigadores a comprender mejor y desarrollar tratamientos para otras enfermedades priónicas relacionadas, como la enfermedad de Creutzfeldt-Jakob [30] y otras enfermedades neurodegeneradas como la enfermedad de Alzheimer . [32]
Kuru fue descrito por primera vez en informes oficiales por oficiales australianos que patrullaban las Tierras Altas Orientales de Papua Nueva Guinea a principios de la década de 1950. [33] Algunos relatos no oficiales sitúan al kuru en la región ya en 1910. [7] En 1951, Arthur Carey fue el primero en utilizar el término kuru en un informe para describir una nueva enfermedad que afligía a las tribus Fore de Papúa Nueva Guinea (PNG). ). En su informe, Carey señaló que el kuru afectaba principalmente a las mujeres Fore y eventualmente las mataba. Kuru fue observado en los pueblos Fore, Yate y Usurufa en 1952-1953 por los antropólogos Ronald Berndt y Catherine Berndt . [7] En 1953, el kuru fue observado por el oficial de patrulla John McArthur, quien proporcionó una descripción de la enfermedad en su informe. McArthur creía que el kuru era simplemente un episodio psicosomático resultante de las prácticas de brujería de los pueblos tribales de la región. [33] Después de que la enfermedad se convirtió en una epidemia más grande, los pueblos tribales pidieron a Charles Pfarr, un funcionario médico luterano, que fuera al área para informar la enfermedad a las autoridades australianas. [7]
Inicialmente, el pueblo Fore creía que las causas del kuru eran hechicería o brujería. [34] También pensaron que la magia que causaba el kuru era contagiosa. También se le llamaba negi-nagi, que significaba persona tonta mientras las víctimas reían a intervalos espontáneos. [35] Esta enfermedad, creía la gente Fore, era causada por fantasmas, debido a los temblores y el comportamiento extraño que acompaña al kuru. Para intentar curar esto, alimentaban a las víctimas con corteza de casuarina . [36]
Cuando la enfermedad kuru se convirtió en una epidemia, Daniel Carleton Gajdusek , MD, virólogo, y Vincent Zigas , otro médico, comenzaron a investigar la enfermedad. En 1957, Zigas y Gajdusek publicaron un informe en el Medical Journal of Australia que sugería que el kuru tenía un origen genético y que "aún no se ha determinado ninguna variable étnico-ambiental que esté operando en la patogénesis del kuru". [37]
Se sospechó que el canibalismo era una posible causa desde el principio, pero no fue presentado formalmente como hipótesis hasta 1967 por Glasse y más formalmente en 1968 por Mathews, Glasse y Lindenbaum. [35]
Incluso antes de que la antropofagia se vinculara con el kuru, la administración australiana de Papua Nueva Guinea prohibió el canibalismo, y la práctica casi fue eliminada en 1960. Si bien el número de casos de kuru estaba disminuyendo, los investigadores médicos finalmente pudieron investigar adecuadamente el kuru, lo que finalmente llevó a la comprensión moderna de los priones como su causa. [38]
En un esfuerzo por comprender la patología de la enfermedad del kuru, Gajdusek estableció las primeras pruebas experimentales de kuru en chimpancés en los Institutos Nacionales de Salud (NIH). [7] Michael Alpers, un médico australiano, colaboró con Gajdusek proporcionándole muestras de tejido cerebral que había tomado de una niña Fore de 11 años que había muerto de kuru. [39] En su trabajo, Gajdusek también fue el primero en compilar una bibliografía sobre la enfermedad de kuru. [40] Joe Gibbs se unió a Gajdusek para monitorear y registrar el comportamiento de los simios en el NIH y realizar sus autopsias. Al cabo de dos años, uno de los chimpancés, Daisy, había desarrollado kuru, demostrando que un factor de enfermedad desconocido se transmitía a través de biomaterial infectado y que era capaz de cruzar la barrera de especie hacia otros primates. Después de que Elisabeth Beck confirmara que este experimento había provocado la primera transmisión experimental de kuru, el hallazgo se consideró un avance muy importante en la medicina humana, lo que llevó a la concesión del Premio Nobel de Fisiología o Medicina a Gajdusek en 1976. [7]
Posteriormente, EJ Field pasó gran parte de finales de los años 1960 y principios de los 1970 en Nueva Guinea investigando la enfermedad, [41] conectándola con la tembladera y la esclerosis múltiple . [42] Observó las interacciones de la enfermedad con las células gliales , incluida la observación crítica de que el proceso infeccioso puede depender de la reordenación estructural de las moléculas del huésped. [43] Esta fue una observación temprana de lo que más tarde se convertiría en la hipótesis del prión. [44]