
El metabolismo del calcio es el movimiento y la regulación de los iones de calcio (Ca 2+ ) dentro (a través del intestino ) y fuera (a través del intestino y los riñones ) del cuerpo, y entre los compartimentos corporales: el plasma sanguíneo , los líquidos extracelulares e intracelulares y el hueso . El hueso actúa como un centro de almacenamiento de calcio para depósitos y extracciones según las necesidades de la sangre a través de la remodelación ósea continua . [1] : 276–277
Un aspecto importante del metabolismo del calcio es la homeostasis del calcio plasmático , la regulación de los iones de calcio en el plasma sanguíneo dentro de límites estrechos . [2] El nivel de calcio en el plasma está regulado por las hormonas hormona paratiroidea (PTH) y calcitonina . La PTH es liberada por las células principales de las glándulas paratiroides cuando el nivel de calcio plasmático cae por debajo del rango normal para aumentarlo; la calcitonina es liberada por las células parafoliculares de la glándula tiroides cuando el nivel de calcio plasmático está por encima del rango normal para reducirlo.
El calcio es el mineral más abundante en el cuerpo humano . [3] El cuerpo adulto medio contiene en total aproximadamente 1 kg, el 99% en el esqueleto en forma de sales de fosfato de calcio . [3] El líquido extracelular (ECF) contiene aproximadamente 22 mmol, de los cuales unos 9 mmol están en el plasma . [4] Aproximadamente 10 mmol de calcio se intercambian entre el hueso y el ECF durante un período de veinticuatro horas. [5]
La concentración de iones de calcio en el interior de las células (en el líquido intracelular ) es más de 7.000 veces menor que en el plasma sanguíneo (es decir, <0,0002 mmol/L, en comparación con 1,4 mmol/L en el plasma).
La concentración plasmática total de calcio está en el rango de 2,2–2,6 mmol/L (9–10,5 mg/dL), y el calcio ionizado normal es de 1,3–1,5 mmol/L (4,5–5,6 mg/dL). [4] La cantidad de calcio total en la sangre varía con el nivel de albúmina plasmática , la proteína más abundante en el plasma y, por lo tanto, el principal transportador de calcio unido a proteínas en la sangre. Sin embargo, el efecto biológico del calcio está determinado por la cantidad de calcio ionizado , en lugar del calcio total. Por lo tanto, es el nivel de calcio ionizado plasmático el que está estrechamente regulado para permanecer dentro de límites muy estrechos por los sistemas de retroalimentación negativa homeostática .
Entre el 35 y el 50% del calcio plasmático está unido a proteínas y entre el 5 y el 10% está en forma de complejos con ácidos orgánicos y fosfatos. El resto (50-60%) está ionizado. El calcio ionizado se puede determinar directamente por colorimetría o se puede leer a partir de nomogramas , aunque la utilidad de estos últimos es limitada cuando el pH y el contenido proteico del plasma se desvían ampliamente de lo normal. [4]
El calcio tiene varias funciones principales en el organismo.
Se une fácilmente a las proteínas, en particular a aquellas con aminoácidos cuyas cadenas laterales terminan en grupos carboxilo (-COOH) (por ejemplo, residuos de glutamato). Cuando se produce dicha unión, las cargas eléctricas de la cadena proteica cambian, lo que hace que cambie la estructura terciaria de la proteína (es decir, la forma tridimensional). Buenos ejemplos de esto son varios de los factores de coagulación del plasma sanguíneo, que no funcionan en ausencia de iones de calcio, pero se vuelven completamente funcionales con la adición de la concentración correcta de sales de calcio.
Los canales de iones de sodio dependientes de voltaje en las membranas celulares de los nervios y músculos son particularmente sensibles a la concentración de iones de calcio en el plasma. [6] Disminuciones relativamente pequeñas en los niveles de calcio ionizado plasmático ( hipocalcemia ) hacen que estos canales filtren sodio hacia las células nerviosas o axones, volviéndolos hiperexcitables ( efecto batmotrópico positivo ), causando así espasmos musculares espontáneos ( tetania ) y parestesia (la sensación de "hormigueo") en las extremidades y alrededor de la boca. [7] Cuando el calcio ionizado plasmático aumenta por encima de lo normal ( hipercalcemia ), más calcio se une a estos canales de sodio teniendo un efecto batmotrópico negativo sobre ellos, causando letargo, debilidad muscular, anorexia, estreñimiento y emociones lábiles. [7 ]
Debido a que la concentración intracelular de iones de calcio es extremadamente baja (ver arriba), la entrada de cantidades minúsculas de iones de calcio desde el retículo endoplasmático o desde los fluidos extracelulares, causa cambios rápidos, muy marcados y fácilmente reversibles en la concentración relativa de estos iones en el citosol . Esto puede, por lo tanto, servir como una señal intracelular muy eficaz (o " segundo mensajero ") en una variedad de circunstancias, incluyendo la contracción muscular , la liberación de hormonas (por ejemplo, insulina de las células beta en los islotes pancreáticos ) o neurotransmisores (por ejemplo, acetilcolina de las terminales presinápticas de los nervios) y otras funciones.
El calcio actúa estructuralmente como material de soporte en los huesos en forma de hidroxiapatita de calcio (Ca 10 (PO 4 ) 6 (OH) 2 ).
En el músculo esquelético y cardíaco , los iones de calcio, liberados del retículo sarcoplásmico (el retículo endoplasmático de los músculos estriados ), se unen a la proteína troponina C presente en los filamentos delgados que contienen actina de las miofibrillas . La estructura 3D de la troponina cambia como resultado, haciendo que la tropomiosina a la que está unida se aleje de los sitios de unión de la miosina en las moléculas de actina que forman la columna vertebral de los filamentos delgados. La miosina puede entonces unirse a los sitios de unión de miosina expuestos en el filamento delgado, para experimentar una serie repetida de cambios conformacionales llamados ciclo de puente cruzado , para el cual el ATP proporciona la energía. Durante el ciclo, cada proteína miosina "rema" a lo largo del filamento delgado de actina, uniéndose repetidamente a los sitios de unión de miosina a lo largo del filamento de actina, haciendo clic y soltándose. En efecto, el filamento grueso se mueve o se desliza a lo largo del filamento delgado, lo que da lugar a la contracción muscular . Este proceso se conoce como el modelo de contracción muscular de filamento deslizante . [8] [9] [10] [11] [12]
No todo el calcio de la dieta se absorbe fácilmente en el intestino. El calcio que se absorbe más fácilmente se encuentra en los productos lácteos (72%), las verduras (7%), los cereales (5%), las legumbres (4%), la fruta (3%) y las proteínas (3%). El calcio contenido en la materia vegetal suele estar en forma de complejos con fitatos , [13] oxalatos , [14] citratos y otros ácidos orgánicos, como los ácidos grasos de cadena larga (p. ej., el ácido palmítico ), con los que el calcio se une para formar jabones de calcio insolubles. [15]
El flujo de calcio hacia y desde el hueso puede ser positivo, negativo o neutro. Cuando es neutro, se renuevan alrededor de 5 a 10 mmol al día. El hueso sirve como un importante punto de almacenamiento de calcio, ya que contiene el 99% del calcio corporal total. La liberación de calcio del hueso está regulada por la hormona paratiroidea junto con el calcitriol fabricado en el riñón bajo la influencia de la PTH. La calcitonina (una hormona secretada por la glándula tiroides cuando los niveles de calcio ionizado plasmático son altos o están aumentando; no debe confundirse con el "calcitriol", que se fabrica en el riñón) estimula la incorporación de calcio al hueso.
La dieta normal de un adulto contiene alrededor de 25 mmol de calcio al día, de los cuales sólo unos 5 mmol se absorben en el organismo al día (véase más adelante). [16]
El calcio se absorbe a través de la membrana del borde en cepillo de las células epiteliales intestinales . Se propuso que el canal TRPV6 fuera el principal actor en la captación intestinal de Ca 2+ . [17] Sin embargo, los ratones Trpv6 KO no mostraron una reducción significativa de los niveles de calcio sérico y mostraron solo una absorción intestinal de Ca 2+ ligeramente reducida [17] o incluso sin cambios , [18] [19] lo que indica que deben existir otras vías de absorción. Recientemente, TRPM7 se relacionó con la captación intestinal de calcio. Los autores pudieron demostrar que la eliminación intestinal de TRPM7 da como resultado niveles de calcio fuertemente reducidos en suero y huesos, [20] y niveles intensamente aumentados de calcitriol y PTH , lo que indica que TRPM7 es esencial para la captación intestinal masiva de calcio . Después de la captación celular, el calcio se une inmediatamente a la calbindina , una proteína de unión al calcio dependiente de la vitamina D. La calbindina transfiere el calcio directamente al retículo endoplasmático de la célula epitelial , a través del cual el calcio se transfiere a la membrana basal en el lado opuesto de la célula, sin entrar en su citosol o líquido intracelular. Desde allí, las bombas de calcio ( PMCA1 ) transportan activamente el calcio al cuerpo. [21] El transporte activo de calcio ocurre principalmente en la porción duodenal del intestino cuando la ingesta de calcio es baja; y a través del transporte paracelular pasivo en las partes del yeyuno e íleon cuando la ingesta de calcio es alta, independientemente del nivel de vitamina D. [22]

La absorción activa de calcio en el intestino está regulada por la concentración de calcitriol (o 1,25 dihidroxicolecalciferol, o 1,25 dihidroxivitamina D 3 ) en la sangre. El calcitriol es un derivado del colesterol. Bajo la influencia de la luz ultravioleta sobre la piel, el colesterol se convierte en previtamina D 3 que se isomeriza espontáneamente a vitamina D 3 (o colecalciferol). Luego se convierte de colecalciferol a calcifediol en el hígado. [23] Bajo la influencia de la hormona paratiroidea , los riñones convierten el calcifediol en la hormona activa calcitriol, que actúa sobre las células epiteliales ( enterocitos ) que recubren el intestino delgado para aumentar la tasa de absorción de calcio del contenido intestinal. En resumen, el ciclo es el siguiente:
Los niveles bajos de PTH en la sangre (que se producen en condiciones fisiológicas cuando los niveles de calcio ionizado plasmático son altos) inhiben la conversión de colecalciferol en calcitriol, que a su vez inhibe la absorción de calcio en el intestino. Lo contrario ocurre cuando los niveles de calcio ionizado plasmático son bajos: la hormona paratiroidea se secreta en la sangre y los riñones convierten más calcifediol en calcitriol activo, lo que aumenta la absorción de calcio en el intestino. [24]
Dado que se excretan aproximadamente 15 mmol de calcio en el intestino a través de la bilis por día [4], la cantidad total de calcio que llega al duodeno y al yeyuno cada día es de aproximadamente 40 mmol (25 mmol de la dieta más 15 mmol de la bilis), de los cuales, en promedio, 20 mmol se absorben (regresan) a la sangre. El resultado neto es que se absorben aproximadamente 5 mmol más de calcio del intestino del que se excreta en él a través de la bilis. Si no hay una formación ósea activa (como en la infancia) o una mayor necesidad de calcio durante el embarazo y la lactancia, los 5 mmol de calcio que se absorben del intestino compensan las pérdidas urinarias que solo se regulan parcialmente [16] .
Los riñones filtran 250 mmol de iones de calcio al día en la proorina (o filtrado glomerular ) y reabsorben 245 mmol, lo que produce una pérdida neta media en la orina de unos 5 mmol/d. La cantidad de iones de calcio excretados en la orina al día está parcialmente bajo la influencia del nivel plasmático de hormona paratiroidea (PTH): los niveles altos de PTH disminuyen la tasa de excreción de iones de calcio, y los niveles bajos la aumentan. [nota 1] Sin embargo, la hormona paratiroidea tiene un mayor efecto sobre la cantidad de iones de fosfato (HPO 4 2− ) excretados en la orina. [25] Los fosfatos forman sales insolubles en combinación con iones de calcio. Por tanto, las concentraciones altas de HPO 4 2− en el plasma reducen el nivel de calcio ionizado en los líquidos extracelulares. Por lo tanto, la excreción de más iones de fosfato que de calcio en la orina aumenta el nivel de calcio ionizado en el plasma, aunque la concentración total de calcio pueda disminuir.
El riñón influye en la concentración plasmática de calcio ionizado de otra manera. Procesa la vitamina D3 en calcitriol , la forma activa que es más eficaz para promover la absorción intestinal de calcio. Esta conversión de vitamina D3 en calcitriol también se ve favorecida por los altos niveles plasmáticos de hormona paratiroidea. [24] [26]
La mayor parte de la excreción del exceso de calcio se realiza a través de la bilis y las heces, porque los niveles de calcitriol plasmático (que en última instancia dependen de los niveles de calcio plasmático) regulan la cantidad de calcio biliar que se reabsorbe del contenido intestinal.
La excreción urinaria de calcio es normalmente de unos 5 mmol (200 mg)/día, una cantidad inferior a la excretada por las heces (15 mmol/día).
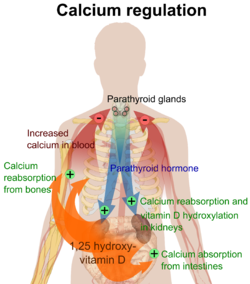
La concentración plasmática de calcio ionizado se regula dentro de límites estrechos (1,3–1,5 mmol/L). Esto se logra mediante las células parafoliculares de la glándula tiroides y las glándulas paratiroides , que detectan (es decir, miden) constantemente la concentración de iones de calcio en la sangre que fluye a través de ellas.
Cuando la concentración de calcio aumenta, las células parafoliculares de la glándula tiroides aumentan su secreción de calcitonina , una hormona polipeptídica, en la sangre. Al mismo tiempo, las glándulas paratiroides reducen la secreción de la hormona paratiroidea (PTH), también una hormona polipeptídica, en la sangre. Los altos niveles resultantes de calcitonina en la sangre estimulan a los osteoblastos en el hueso para eliminar el calcio del plasma sanguíneo y depositarlo en forma de hueso.
Los niveles reducidos de PTH inhiben la eliminación de calcio del esqueleto. Los niveles bajos de PTH tienen otros efectos: hay una mayor pérdida de calcio en la orina, pero lo más importante es que se inhibe la pérdida de iones de fosfato a través de la orina. Por lo tanto, los iones de fosfato se retendrán en el plasma, donde forman sales insolubles con los iones de calcio, eliminándolos así del depósito de calcio ionizado en la sangre. Los niveles bajos de PTH también inhiben la formación de calcitriol (que no debe confundirse con calcitonina ) a partir del colecalciferol (vitamina D 3 ) por los riñones.
La reducción de la concentración de calcitriol en sangre actúa (comparativamente lentamente) sobre las células epiteliales ( enterocitos ) del duodeno, inhibiendo su capacidad para absorber calcio del contenido intestinal. [2] [5] [28] [29] Los bajos niveles de calcitriol también actúan sobre el hueso provocando que los osteoclastos liberen menos iones de calcio al plasma sanguíneo. [25]

Cuando el nivel de calcio ionizado plasmático es bajo o cae, ocurre lo contrario. Se inhibe la secreción de calcitonina y se estimula la secreción de PTH, lo que da como resultado la eliminación de calcio del hueso para corregir rápidamente el nivel de calcio plasmático. Los altos niveles plasmáticos de PTH inhiben la pérdida de calcio a través de la orina, al tiempo que estimulan la excreción de iones de fosfato por esa vía. También estimulan los riñones para que fabriquen calcitriol (una hormona esteroide), que mejora la capacidad de las células que recubren el intestino para absorber calcio del contenido intestinal en la sangre, al estimular la producción de calbindina en estas células. La producción de calcitriol estimulada por PTH también hace que el calcio se libere del hueso a la sangre, mediante la liberación de RANKL (una citocina u hormona local ) de los osteoblastos , lo que aumenta la actividad de resorción ósea de los osteoclastos. Sin embargo, estos son procesos relativamente lentos [2] [5] [25] [28] [29]
Por lo tanto, la regulación rápida a corto plazo del nivel de calcio ionizado plasmático implica principalmente movimientos rápidos de calcio dentro o fuera del esqueleto. La regulación a largo plazo se logra regulando la cantidad de calcio absorbido desde el intestino o perdido a través de las heces. [2] [5] [28] [29]
Tanto la hipocalcemia (bajo nivel de calcio en sangre) como la hipercalcemia (alto nivel de calcio en sangre) son trastornos médicos graves. La osteoporosis , la osteomalacia y el raquitismo son trastornos óseos relacionados con trastornos del metabolismo del calcio y efectos de la vitamina D. La osteodistrofia renal es una consecuencia de la insuficiencia renal crónica relacionada con el metabolismo del calcio .
Una dieta adecuadamente rica en calcio puede reducir la pérdida de calcio de los huesos a medida que avanza la edad (posmenopáusica ) . [30] Una ingesta baja de calcio en la dieta puede ser un factor de riesgo en el desarrollo de osteoporosis en etapas posteriores de la vida; y una dieta con cantidades adecuadas y sostenidas de calcio puede reducir el riesgo de osteoporosis.
El papel que el calcio podría desempeñar en la reducción de las tasas de cáncer colorrectal ha sido objeto de numerosos estudios. Sin embargo, dada su modesta eficacia, actualmente no existe ninguna recomendación médica para utilizar calcio para la reducción del cáncer.
{{cite book}}: CS1 maint: varios nombres: lista de autores ( enlace )