La enzima lactoilglutatión liasa (EC 4.4.1.5, también conocida como glioxalasa I ) cataliza la isomerización de aductos de hemitioacetal, que se forman en una reacción espontánea entre un grupo glutatiónilo y aldehídos como el metilglioxal . [1] [2]
La glioxalasa I deriva su nombre de su catálisis del primer paso en el sistema de la glioxalasa , un sistema crítico de desintoxicación de dos pasos para el metilglioxal . El metilglioxal se produce naturalmente como un subproducto de la bioquímica normal, pero es altamente tóxico, debido a sus reacciones químicas con proteínas , ácidos nucleicos y otros componentes celulares. El segundo paso de desintoxicación, en el que el ( R ) -S -lactoilglutatión se divide en glutatión y D-lactato, lo lleva a cabo la glioxalasa II , una hidrolasa . Inusualmente, estas reacciones llevadas a cabo por el sistema de la glioxalasa no oxidan el glutatión, que generalmente actúa como una coenzima redox . Aunque la aldosa reductasa también puede desintoxicar el metilglioxal, el sistema de la glioxalasa es más eficiente y parece ser la más importante de estas vías. La glioxalasa I es un objetivo atractivo para el desarrollo de fármacos destinados a tratar infecciones causadas por algunos protozoos parásitos y el cáncer . Se han identificado varios inhibidores de la glioxalasa I, como el S-(N-hidroxi-N-metilcarbamoil)glutatión.
La glioxalasa I se clasifica como una liasa carbono-azufre aunque, estrictamente hablando, la enzima no forma ni rompe un enlace carbono-azufre. En cambio, la enzima desplaza dos átomos de hidrógeno de un átomo de carbono del metilglioxal al átomo de carbono adyacente. En efecto, la reacción es una reacción redox intramolecular ; un carbono se oxida mientras que el otro se reduce. El mecanismo procede restando y luego agregando protones , formando un intermediario enediolato, en lugar de transferir hidruros . Inusualmente para una metaloproteína , esta enzima muestra actividad con varios metales diferentes. La glioxalasa I también es inusual en el sentido de que es estereoespecífica en la segunda mitad de su mecanismo, pero no en la primera mitad. Estructuralmente, la enzima es un dímero de dominio intercambiado en muchas especies, aunque las dos subunidades se han fusionado en un monómero en la levadura , a través de la duplicación genética .
El nombre sistemático de esta clase de enzima es ( R ) -S -lactoilglutatión metilglioxal-liasa (isomerizante; formadora de glutatión); otros nombres incluyen:
En algunos casos, la porción glutatión puede ser suministrada por tripanotiona , el análogo del glutatión en protozoos parásitos como los tripanosomas . El gen humano para esta enzima se llama GLO1 .
La lactoilglutatión liasa en humanos está codificada por el gen GLO1 . [7] [8] [9]
Se han resuelto varias estructuras de la glioxalasa I. Se han publicado cuatro estructuras de la forma humana, con códigos de acceso PDB 1BH5, 1FRO, 1QIN y 1QIP. Se han publicado cinco estructuras de la forma Escherichia coli , con códigos de acceso 1FA5, 1FA6, 1FA7, 1FA8 y 1F9Z. Finalmente, se ha resuelto una estructura de la versión específica de tripanotiona de Leishmania major , 2C21. En todos estos casos, la estructura cuaternaria de la unidad biológica es un dímero de dominios intercambiados, en el que el sitio activo y la estructura secundaria de lámina beta de 8 hebras se forman a partir de ambas subunidades. Sin embargo, en levaduras como Saccharomyces cerevisiae , las dos subunidades se han fusionado en un solo monómero de tamaño doble, a través de la duplicación génica . Cada mitad del dímero estructural es un sándwich de 3-4 hélices alfa en ambos lados de una lámina beta antiparalela de 8 hebras; la interfaz del dímero está compuesta en gran parte por el encuentro cara a cara de las dos láminas beta. [1]
Las estructuras terciarias y cuaternarias de la glioxalasa I son similares a las de varios otros tipos de proteínas. Por ejemplo, la glioxalasa I se parece a varias proteínas que permiten a las bacterias resistir antibióticos como la fosfomicina , la bleomicina y la mitomicina . Del mismo modo, las enzimas no relacionadas metilmalonil-CoA epimerasa , 3-desmetilubiquinona-9 3-O-metiltransferasa y numerosas dioxigenasas como la bifenil-2,3-diol 1,2-dioxigenasa , la catecol 2,3-dioxigenasa , la 3,4-dihidroxifenilacetato 2,3-dioxigenasa y la 4-hidroxifenilpiruvato dioxigenasa se parecen todas a la glioxalasa I en estructura. [1] Finalmente, muchas proteínas de función desconocida o incierta también se parecen a la glioxalasa I, como la At5g48480 de la planta Arabidopsis thaliana .
El sitio activo tiene cuatro regiones principales.
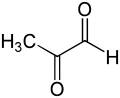
La principal función fisiológica de la glioxalasa I es la desintoxicación del metilglioxal , un 2-oxoaldehído reactivo que es citostático a bajas concentraciones [10] y citotóxico a concentraciones milimolares. [11] El metilglioxal es un subproducto de la bioquímica normal que es un carcinógeno, un mutágeno [12] y puede dañar químicamente varios componentes de la célula, como las proteínas y los ácidos nucleicos. [11] [13] El metilglioxal se forma espontáneamente a partir de fosfato de dihidroxiacetona, enzimáticamente por la triosafosfato isomerasa y la metilglioxal sintasa, como también en el catabolismo de la treonina . [14]
Para minimizar la cantidad de metilglioxal tóxico y otros 2-oxoaldehídos reactivos, se ha desarrollado el sistema de la glioxalasa . El metilglioxal reacciona espontáneamente con glutatión reducido (o su equivalente, tripanotiona ), [15] formando un hemitioacetal. El sistema de la glioxalasa convierte dichos compuestos en D - lactato y restaura el glutatión. [14] En esta conversión, los dos carbonos carbonílicos del 2-oxoaldehído se oxidan y reducen, respectivamente, el aldehído se oxida a un ácido carboxílico y el grupo acetal se reduce a un alcohol. El sistema de la glioxalasa evolucionó muy temprano en la historia de la vida y se encuentra casi universalmente en todas las formas de vida.
El sistema de la glioxalasa consta de dos enzimas, la glioxalasa I y la glioxalasa II . La primera enzima, descrita aquí, reorganiza el hemitioacetal formado naturalmente por el ataque del glutatión al metilglioxal en el producto. La glioxalasa II hidroliza el producto para volver a formar el glutatión y producir D- lactato . Por lo tanto, el glutatión actúa de manera inusual como una coenzima y se requiere solo en cantidades catalíticas (es decir, muy pequeñas); normalmente, el glutatión actúa en cambio como un par redox en reacciones de oxidación-reducción.
También se ha sugerido que el sistema de glioxalasa desempeña un papel en la regulación del crecimiento celular [16] y en el ensamblaje de microtúbulos . [17]
La glioxalasa I requiere iones metálicos ligados para la catálisis. [18] La enzima humana [19] y sus contrapartes en levadura ( Saccharomyces cerevisiae ) [20] y Pseudomonas putida [21] utilizan zinc divalente , Zn 2+ . Por el contrario, las versiones procariotas a menudo utilizan un ion níquel . La glioxalasa I encontrada en parásitos tripanosómicos eucariotas como Leishmania major y Trypanosoma cruzi también puede utilizar níquel para la actividad, [15] posiblemente reflejando una adquisición de su gen GLO1 por transferencia horizontal de genes . [22]
Una propiedad de la glioxalasa I es su falta de especificidad para el ion metálico catalítico. La mayoría de las enzimas se unen a un tipo particular de metal, y su actividad catalítica depende de haberse unido a ese metal. Por ejemplo, las oxidorreductasas a menudo utilizan un ion metálico específico como hierro , manganeso o cobre y no funcionarán si se reemplaza su ion metálico preferido, debido a las diferencias en el potencial redox ; por lo tanto, la superóxido dismutasa ferrosa no puede funcionar si su hierro catalítico se reemplaza por manganeso, y viceversa. Por el contrario, aunque la glioxalasa I humana prefiere utilizar zinc divalente, es capaz de funcionar con muchos otros metales divalentes, incluidos magnesio , manganeso , cobalto , níquel e incluso calcio . [23] sin embargo, la enzima es inactiva con el catión ferroso. [24] De manera similar, aunque la glioxalasa I procariota prefiere níquel, es capaz de funcionar con cobalto, manganeso y cadmio ; Sin embargo, la enzima es inerte con el zinc unido, debido a un cambio en la geometría de coordinación de octaédrica a bipiramidal trigonal . [15] Estudios estructurales y computacionales han revelado que el metal se une a los dos oxígenos carbonílicos de la fracción metilglioxal en dos de sus sitios de coordinación, estabilizando el intermedio de anión endiolato.
Otra propiedad inusual de la glioxalasa I es su estereoespecificidad inconsistente. El primer paso de su mecanismo de reacción (la abstracción del protón de C 1 y la posterior protonación de O 2 ) no es estereoespecífico, y funciona igualmente bien independientemente de la quiralidad inicial en C 1 en el sustrato hemitioacetal. El intermedio enediolato resultante es aquiral, pero el segundo paso del mecanismo de reacción (la abstracción de un protón de O 1 y la posterior protonación de C 2 ) es definitivamente estereoespecífico, produciendo solo la forma ( S ) de D-lactoilglutatión. Se cree que esto es el resultado de los dos glutamatos unidos de forma opuesta en el ion metálico; cualquiera de ellos es capaz de llevar a cabo el primer paso, pero solo uno es capaz de llevar a cabo el segundo paso. La razón de esta asimetría aún no está completamente determinada.
La molécula de metilglioxal consta de dos grupos carbonilo flanqueados por un átomo de hidrógeno y un grupo metilo . En la siguiente explicación, estos dos carbonos carbonílicos se denominarán C1 y C2, respectivamente. Tanto en el sustrato de hemitioacetal como en el producto (R)-S-lactoilglutatión, la fracción de glutatión está unida al grupo carbonilo C1.
El mecanismo básico de la glioxalasa I es el siguiente: el sustrato hemitioacetal se forma cuando una molécula de glutatión (probablemente en su forma reactiva de tiolato ) ataca al carbonilo C1 del metilglioxal o de un compuesto relacionado, lo que hace que ese carbono sea tetravalente. Esta reacción se produce de forma espontánea en la célula, sin la intervención de la enzima. A continuación, la enzima une este hemitioacetal y desplaza un hidrógeno de C1 a C2. El carbonilo C2 se reduce a una forma de alcohol tetravalente mediante la adición de dos protones, mientras que el carbonilo C1 se restaura perdiendo un hidrógeno mientras conserva su enlace con la fracción de glutatión.
Un estudio computacional, combinado con los datos experimentales disponibles, sugiere el siguiente mecanismo de resolución atómica para la glioxalasa I. [25] En el sitio activo, el metal catalítico adopta una geometría de coordinación octaédrica y, en ausencia de sustrato, une dos aguas, dos glutamatos opuestos , una histidina y otra cadena lateral, generalmente otra histidina o glutamatos . Cuando el sustrato entra en el sitio activo, las dos aguas se desprenden y los dos oxígenos carbonílicos del sustrato se unen directamente al ion metálico. Los dos glutamatos opuestos suman y restan protones de C1 y C2 y sus respectivos oxígenos, O1 y O2. La primera mitad de la reacción transfiere un protón de C1 a O2, mientras que la segunda mitad transfiere un protón de O1 a C2. La primera reacción puede ser llevada a cabo por cualquiera de los glutamatos opuestos, dependiendo de la quiralidad inicial de C1 en el sustrato hemitioacetal; Sin embargo, la segunda mitad es estereoespecífica y es realizada sólo por uno de los glutamatos opuestos.
Cabe destacar que el primer mecanismo confirmado teóricamente para el sustrato R de la glioxalasa se publicó recientemente. [26]
El mecanismo catalítico de la glioxalasa se ha estudiado mediante la teoría funcional de la densidad, simulaciones de dinámica molecular y métodos híbridos QM/MM. La razón de la especial especificidad de la enzima (acepta ambos enantiómeros de su sustrato quiral pero los convierte en el mismo enantiómero del producto) es la mayor basicidad y flexibilidad de uno de los glutamatos del sitio activo (Glu172). [27] [28] [29]
Originalmente se creía que la glioxalasa I operaba mediante la transferencia de un hidruro , que es un protón rodeado por dos electrones (H – ). [30] En esto, se pensó que se parecía al mecanismo clásico de reacción de Cannizzaro , en el que el ataque de un hidroxilato a un aldehído lo convierte en un anión alcohol tetravalente; este anión dona sus hidrógenos a un segundo aldehído, formando un ácido carboxílico y un alcohol. (En efecto, dos aldehídos idénticos se reducen y oxidan entre sí, dejando el estado de oxidación neto igual).
En la glioxalasa I, este mecanismo de transferencia de hidruro funcionaría de la siguiente manera: el ataque del glutatión dejaría un O cargado y el hidrógeno del aldehído unido a C 1 . Si el oxígeno del carbonilo de C 2 puede conseguir un hidrógeno de una cadena lateral ácida de la enzima, formando un alcohol, entonces el hidrógeno de C 1 podría deslizarse simultáneamente con sus electrones sobre C 2 (la transferencia de hidruro). Al mismo tiempo, el electrón adicional en el oxígeno de C 1 podría reformar el doble enlace del carbonilo, dando así el producto final.
En la década de 1970 se propuso un mecanismo alternativo (y en última instancia correcto) que utiliza la transferencia de protones (H + ). [31] En este mecanismo, una cadena lateral básica de la enzima abstrae el protón aldehído de C 1 ; al mismo tiempo, el protón a se agrega al oxígeno de C 2 , formando así un enodiol . El eno significa que se ha formado un doble enlace entre C 2 y C 1 , a partir de los electrones que quedan atrás por la abstracción del protón aldehído; el diol se refiere al hecho de que se han formado dos alcoholes a partir de los dos grupos carbonilo iniciales. En este mecanismo, el intermedio forma el producto agregando otro protón a C 2 .
Se esperaba que los protones del disolvente contribuyeran a la formación del producto a partir del intermediario enodiol del mecanismo de transferencia de protones y cuando tales contribuciones no se observaron en agua tritiada , 3 H 1 O, se favoreció el mecanismo de transferencia de hidruro. Sin embargo, no se pudo descartar una hipótesis alternativa (que el sitio activo de la enzima estaba enterrado profundamente lejos del agua) y finalmente resultó ser correcta. Las primeras indicaciones llegaron cuando las temperaturas cada vez mayores mostraron una incorporación cada vez mayor de tritio, lo que es consistente con la transferencia de protones e inesperado por la transferencia de hidruro. La evidencia concluyente puede obtenerse con estudios del efecto del isótopo hidrógeno-deuterio en sustratos fluorados en el grupo metilo y deuterados en el aldehído. El fluoruro es un buen grupo saliente; el mecanismo de transferencia de hidruro predice una menor eliminación de iones fluoruro con la muestra deuterada, mientras que el mecanismo de transferencia de protones predice más . Los experimentos en tres tipos de glioxalasa I (formas de levadura, rata y ratón) apoyaron el mecanismo de transferencia de protones en todos los casos. [32] Este mecanismo se observó finalmente en las estructuras cristalinas de la glioxalasa I.
La expresión de Glo1 se correlaciona con diferencias en el comportamiento similar a la ansiedad en ratones [33] [34] así como el comportamiento en la prueba de suspensión de la cola , que es sensible a los fármacos antidepresivos ; [35] sin embargo, la dirección de estos efectos no siempre ha sido consistente, lo que ha generado escepticismo. [36] Las diferencias en la expresión de Glo1 en ratones parecen estar causadas por una variante del número de copias que es común entre las cepas endogámicas de ratones. [37] Se ha propuesto que los efectos conductuales de Glo1 se deben a la actividad de su sustrato principal, el metilglioxal, en los receptores GABA A. [38] Se ha demostrado que un inhibidor de molécula pequeña de la glioxalasa I tiene propiedades ansiolíticas, lo que identifica otra posible indicación para los inhibidores de la glioxalasa I. [38]
La glioxalasa I es un objetivo para el desarrollo de fármacos contra bacterias, protozoos (especialmente Trypanosoma cruzi y Leishmania ) y cáncer humano. [39] Se han desarrollado numerosos inhibidores, la mayoría de los cuales comparten la fracción glutatión . Entre la familia de inhibidores que se unen más fuertemente a la enzima humana se encuentran los derivados de S -( N -aril- N -hidroxicarbamoil)glutatión, más notablemente el derivado p -bromofenilo, que tiene una constante de disociación de 14 nM. [40] Se cree que el análogo más cercano del estado de transición es S -( N -hidroxi- N - p -yodofenilcarbamoil)glutatión; la estructura cristalina de este compuesto unido a la enzima humana se ha resuelto a una resolución de 2 Å (código de acceso PDB 1QIN). [41]
Los experimentos sugieren que el metilglioxal es preferentemente tóxico para las células proliferantes, como las del cáncer. [42]
Investigaciones recientes demuestran que la expresión de GLO1 está regulada positivamente en varios tumores malignos humanos, incluido el melanoma metastásico. [43] [44]