La purina es un compuesto orgánico aromático heterocíclico que consta de dos anillos ( pirimidina e imidazol ) fusionados. Es soluble en agua . La purina también da nombre a una clase más amplia de moléculas , las purinas , que incluyen las purinas sustituidas y sus tautómeros . Son los heterociclos que contienen nitrógeno más abundantes en la naturaleza. [1]
Las purinas se encuentran en altas concentraciones en la carne y los productos cárnicos, especialmente en los órganos internos como el hígado y los riñones . En general, las dietas basadas en plantas son bajas en purinas. [2] Las plantas y algas con alto contenido de purinas incluyen algunas legumbres ( lentejas , soja y guisantes de ojo negro ) y la espirulina . Ejemplos de fuentes ricas en purinas incluyen: mollejas , anchoas , sardinas , hígado, riñones de res , sesos , extractos de carne (p. ej., Oxo , Bovril ), arenque , caballa , vieiras , carnes de caza , levadura ( cerveza , extracto de levadura , levadura nutricional ) y salsa . [3]
Una cantidad moderada de purina también se encuentra en las carnes rojas, carne de res , cerdo , aves , pescados y mariscos , espárragos , coliflor , espinacas , champiñones , guisantes , lentejas , guisantes secos, frijoles , avena , salvado de trigo , germen de trigo y copos de nieve . . [4]
Las purinas y las pirimidinas constituyen los dos grupos de bases nitrogenadas , incluidos los dos grupos de bases nucleotídicas . Las bases purínicas son guanina (G) y adenina (A), que forman los correspondientes nucleósidos- desoxirribonucleósidos ( desoxiguanosina y desoxiadenosina ) con una fracción desoxirribosa y ribonucleósidos ( guanosina , adenosina ) con una fracción ribosa. Estos nucleósidos con ácido fosfórico forman los nucleótidos correspondientes (desoxiguanilato, desoxiadenilato y guanilato, adenilato), que son los componentes básicos del ADN y el ARN , respectivamente. Las bases purínicas también desempeñan un papel esencial en muchos procesos metabólicos y de señalización dentro de los compuestos monofosfato de guanosina (GMP) y monofosfato de adenosina (AMP).
Para realizar estos procesos celulares esenciales, la célula necesita tanto purinas como pirimidinas , y en cantidades similares. Tanto la purina como la pirimidina son autoinhibidoras y activadoras . Cuando se forman purinas, inhiben las enzimas necesarias para la formación de más purinas. Esta autoinhibición se produce porque también activan las enzimas necesarias para la formación de pirimidina. La pirimidina simultáneamente se autoinhibe y activa la purina de manera similar. Debido a esto, hay casi la misma cantidad de ambas sustancias en la célula en todo momento. [5]
La purina es a la vez un ácido muy débil ( pK a 8,93) y una base aún más débil ( pK a 2,39). [6] Si se disuelve en agua pura, el pH está a medio camino entre estos dos valores de pKa.
La purina es aromática y tiene cuatro tautómeros , cada uno con un enlace de hidrógeno a uno diferente de los cuatro átomos de nitrógeno. Estos se identifican como 1-H, 3-H, 7-H y 9-H (ver imagen del anillo numerado). La forma cristalina común favorece el tautómero 7-H, mientras que en los disolventes polares predominan los tautómeros 9-H y 7-H. [7] Los sustituyentes de los anillos y las interacciones con otras moléculas pueden cambiar el equilibrio de estos tautómeros. [8]
Hay muchas purinas naturales. Incluyen las nucleobases adenina ( 2 ) y guanina ( 3 ). En el ADN , estas bases forman enlaces de hidrógeno con sus pirimidinas complementarias , timina y citosina , respectivamente. Esto se llama emparejamiento de bases complementarias. En el ARN , el complemento de la adenina es uracilo en lugar de timina.
Otras purinas destacables son la hipoxantina , la xantina , la teofilina , la teobromina , la cafeína , el ácido úrico y la isoguanina .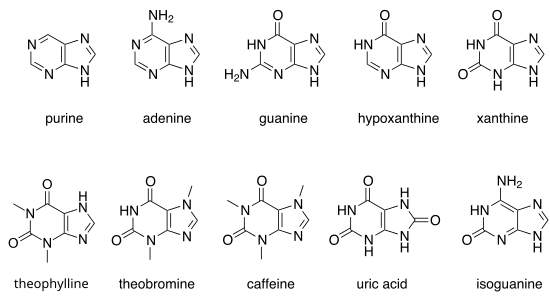 [ contradictorio ]
[ contradictorio ]

Además de las funciones cruciales de las purinas (adenina y guanina) en el ADN y el ARN, las purinas también son componentes importantes en otras biomoléculas importantes, como el ATP , el GTP , el AMP cíclico , el NADH y la coenzima A. La purina ( 1 ) en sí no se ha encontrado en la naturaleza, pero puede producirse mediante síntesis orgánica .
También pueden funcionar directamente como neurotransmisores , actuando sobre receptores purinérgicos . La adenosina activa los receptores de adenosina .
La palabra purina ( orina pura ) [9] fue acuñada por el químico alemán Emil Fischer en 1884. [10] [11] La sintetizó por primera vez en 1898. [11] El material de partida para la secuencia de reacción fue el ácido úrico. ( 8 ), que Carl Wilhelm Scheele había aislado de cálculos renales en 1776. [12] Se hizo reaccionar ácido úrico (8) con PCl 5 para dar 2,6,8-tricloropurina ( 10 ), que se convirtió con HI y PH 4 I para dar 2,6-diyodopurina ( 11 ). El producto se redujo a purina ( 1 ) usando polvo de zinc .
Muchos organismos tienen vías metabólicas para sintetizar y descomponer purinas.
Las purinas se sintetizan biológicamente como nucleósidos (bases unidas a la ribosa ).
La acumulación de nucleótidos de purina modificados afecta a diversos procesos celulares, especialmente aquellos que involucran ADN y ARN . Para ser viables, los organismos poseen varias desoxipurina fosfohidrolasas, que hidrolizan estos derivados de purina eliminándolos de los grupos activos de NTP y dNTP . La desaminación de bases purínicas puede provocar la acumulación de nucleótidos como ITP , dITP, XTP y dXTP. [13]
Los defectos en las enzimas que controlan la producción y descomposición de las purinas pueden alterar gravemente las secuencias de ADN de una célula, lo que puede explicar por qué las personas que portan ciertas variantes genéticas de las enzimas metabólicas de las purinas tienen un mayor riesgo de padecer algunos tipos de cáncer .
Los organismos de los tres dominios de la vida, eucariotas , bacterias y arqueas , son capaces de llevar a cabo la biosíntesis de novo de purinas . Esta capacidad refleja la esencialidad de las purinas para la vida. La vía bioquímica de síntesis es muy similar en especies eucariotas y bacterianas, pero es más variable entre especies de arqueas. [14] Se determinó que un conjunto casi completo o completo de genes necesarios para la biosíntesis de purinas estaba presente en 58 de las 65 especies de arqueas estudiadas. [14] Sin embargo, también se identificaron siete especies de arqueas con genes codificadores de purinas total o casi totalmente ausentes. Aparentemente, las especies de arqueas incapaces de sintetizar purinas son capaces de adquirir purinas exógenas para su crecimiento [14] y, por lo tanto, son análogas a los mutantes de purinas de eucariotas, por ejemplo, los mutantes de purinas del hongo ascomiceto Neurospora crassa , [15] que también requieren purinas exógenas para su crecimiento. crecimiento.
Un mayor nivel de consumo de carne y mariscos se asocia con un mayor riesgo de gota , mientras que un mayor nivel de consumo de productos lácteos se asocia con un menor riesgo. La ingesta moderada de verduras o proteínas ricas en purinas no se asocia con un mayor riesgo de gota. [16] Se han encontrado resultados similares con el riesgo de hiperuricemia .
Además de la síntesis in vivo de purinas en el metabolismo de las purinas , las purinas también se pueden sintetizar artificialmente.
La purina ( 1 ) se obtiene con buen rendimiento cuando se calienta formamida en un recipiente abierto a 170 °C durante 28 horas. [17]
Esta notable reacción y otras similares han sido discutidas en el contexto del origen de la vida . [18]
Patentado el 20 de agosto de 1968, el método actualmente reconocido de producción de adenina a escala industrial es una forma modificada del método de la formamida. Este método calienta formamida en condiciones de 120 grados Celsius dentro de un matraz sellado durante 5 horas para formar adenina. La cantidad de la reacción aumenta considerablemente mediante el uso de oxicloruro de fósforo (cloruro de fosforilo) o pentacloruro de fósforo como catalizador ácido y condiciones de luz solar o ultravioleta. Después de que hayan pasado las 5 horas y la solución de formamida-oxicloruro de fósforo-adenina se enfríe, se pone agua en el matraz que contiene la formamida y la adenina ahora formada. A continuación se vierte la solución de agua, formamida y adenina a través de una columna de filtración de carbón activado. Las moléculas de agua y formamida, al ser moléculas pequeñas, pasarán a través del carbón hasta el matraz de desechos; Sin embargo, las grandes moléculas de adenina se unirán o “adsorberán” al carbón debido a las fuerzas de van der waals que interactúan entre la adenina y el carbono del carbón. Debido a que el carbón tiene una gran superficie, es capaz de capturar la mayoría de las moléculas que pasan a través de él de cierto tamaño (mayor que el agua y la formamida). Para extraer la adenina de la adenina adsorbida en carbón, se vierte amoníaco gaseoso disuelto en agua (aqua amonia) sobre la estructura de carbón activado y adenina para liberar la adenina en la solución de amoníaco y agua. Luego, la solución que contiene agua, amoníaco y adenina se deja secar al aire, y la adenina pierde solubilidad debido a la pérdida de gas amoníaco que previamente hacía que la solución fuera básica y capaz de disolver la adenina, lo que hace que cristalice en un polvo blanco puro. que se puede almacenar. [19]
Oro y Kamat (1961) y sus colaboradores de Orgel (1966, 1967) han demostrado que cuatro moléculas de HCN se tetramerizan para formar diaminomaleodinitrilo ( 12 ), que puede convertirse en casi todas las purinas naturales. [20] [21] [22] [23] [24] Por ejemplo, cinco moléculas de HCN se condensan en una reacción exotérmica para producir adenina , especialmente en presencia de amoníaco.
La síntesis de purinas de Traube (1900) es una reacción clásica (llamada así en honor a Wilhelm Traube ) entre una pirimidina sustituida con amina y ácido fórmico . [25]
Para comprender cómo surgió la vida , es necesario conocer las vías químicas que permiten la formación de los componentes clave de la vida en condiciones prebióticas plausibles . Nam et al. (2018) [26] demostraron la condensación directa de nucleobases de purina y pirimidina con ribosa para dar ribonucleósidos en microgotas acuosas, un paso clave que conduce a la formación de ARN. Además, Becker et al. presentaron un proceso prebiótico plausible para sintetizar ribonucleósidos de purina. (2016). [27]