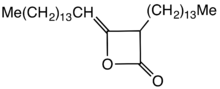
Los dímeros de alquilcetena (AKD) son una familia de compuestos orgánicos basados en el sistema de anillo de 4 miembros de oxetan-2-ona , que también es el elemento estructural central de la propiolactona y la dicetena . Unido al anillo de oxetano de los dímeros de alquilcetena técnicamente relevantes hay un grupo alquilo C12 - C16 en la posición 3 y un grupo alquilideno C13 - C17 en la posición 4.
La principal aplicación de los dímeros de cetena alquilados es en el encolado de papel y cartón , así como en la hidrofobación de fibras de celulosa . Los productos así modificados se distinguen por mayores resistencias mecánicas y menor penetración de agua, tintas o colorantes de imprenta . [1]
Los AKD presentan grupos alquilo hidrofóbicos que se extienden desde un anillo de beta-propiolactona . Un ejemplo específico se deriva de la dimerización de la cetena del ácido esteárico . Esta cetena se genera por pirólisis del cloruro de estearoilo. [2] Los AKD reaccionan con los grupos hidroxilo de la celulosa a través de una reacción de esterificación . La esterificación es competitiva con la hidrólisis del AKD. Antes del desarrollo de los AKD, la hidrofobicidad se impartía incorporando colofonia al papel. [3]
Relacionado con los AKD, está el anhídrido alquenilsuccínico (ASA). Al igual que los AKD, el ASA reacciona con los grupos hidroxi de la celulosa para formar un éster, anclando el grupo hidrofóbico a la superficie. El ASA se prepara mediante la reacción eno de hidrocarburos insaturados con anhídrido maleico . [4]
En 1901, Edgar Wedekind publicó la síntesis de dímeros de alquilcetena mediante la reacción de cloruros de ácido carboxílico con aminas terciarias : [5] [6]
RCH 2 COCl + R 3 N → RCH=C=O + R 3 NHCl El peso molecular determinado por los primeros investigadores indicó (CH 3 ) 2 CH=C=O ) n donde n > 1 para la deshidrohalogenación de cloruro de isobutirilo con trietilamina . [7] [8]

Los productos de reacción primarios de cloruros de ácido con átomos de hidrógeno en posición α y aminas terciarias fueron identificados por Hermann Staudinger [9] [10] y Norman Thomas Mortimer Wilsmore [11] como cetenos altamente reactivos (etenonas) que forman 2-oxetanonas con un grupo alquilideno cuando se dimerizan en fotocicloadiciones [2+2] .
La idea de Staudinger se complicó por la dependencia de la dimerización de los sustituyentes. La cetena simple (H 2 C=C=O) se dimeriza a dicetena (4-metilen-oxetan-2-ona), mientras que las cetenas sustituidas, como la dimetilcetena (Me 2 C=C=O, formada a partir de cloruro de isobutirilo con trietilamina) se dimerizan en una adición de cabeza a cola a 2,2,4,4-tetrametilciclobutanodiona . [7] [12]
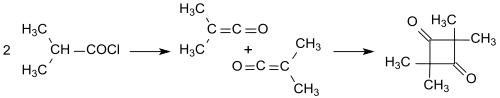
La 2,2,4,4,4-tetrametilciclobutanodiona se puede isomerizar fácilmente a dímero de dimetilcetena (4-isopropilideno-3,3-dimetil-oxetan-2-ona). [13]
La síntesis y caracterización del dímero de hexadecilo ceteno, una sustancia clave para los dímeros de ceteno alquilados, se describió por primera vez en una patente [14] en 1945 y en una publicación [15] en 1947.
La síntesis industrial de cetenímeros alquilados (en aquella época todavía llamados cetoetenonas) fue patentada en 1945 a partir de cloruros de ácidos carboxílicos de cadena larga en disolventes inertes (como éter dietílico o benceno ) con trietilamina como amina terciaria en condiciones anhidras. Después de la filtración del clorhidrato de trietilamina insoluble y la evaporación del disolvente, se obtienen dímeros de cadena alquílica de cadena larga con rendimientos de más del 90%. [14]
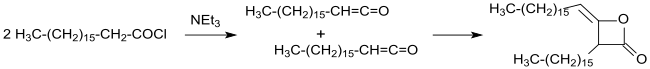
El uso de otros disolventes, como ésteres de ácido carboxílico o cetonas para una separación más fácil de los clorhidratos de trialquilamina u otras aminas, como la N,N,N',N' -tetrametil-hexano-1,6-diamina [16], no proporciona ninguna ventaja significativa.
También se describen procesos sin el uso de disolventes, en los que el clorhidrato de amina resultante se filtra o se extrae con ácidos acuosos diluidos. [17]
Un proceso continuo en el que el cloruro de ácido carboxílico de cadena larga y la amina terciaria (por ejemplo, dimetilisopropilamina, dimetilciclohexilamina o trietilamina) se suministran por separado sin disolventes a un reactor tubular, amasadora o, preferiblemente, a una extrusora de doble husillo o a una extrusora de rodillos planetarios y se hacen reaccionar a temperaturas entre 90 y 110 °C, proporciona contenidos de lactona de más del 90 % en tiempos de reacción cortos. El procesamiento se lleva a cabo mediante separación de fases o extracción ácida. [18]
Los problemas con el encolado en masa ácido (mediado por sulfato de aluminio) del papel con resinas de colofonia digeridas en álcali, introducidos desde principios del siglo XIX, llevaron, además del uso de floculantes alcalinos (como tiza o carbonato de calcio como reserva alcalina), a la búsqueda de materiales alternativos para el encolado en un entorno neutro o alcalino. Además de los anhídridos alquenilsuccínicos significativamente más reactivos (que también se hidrolizan rápidamente en presencia de agua), los dímeros de cetena alquilados han comenzado a ser los encoladores de superficie y masa preferidos en la industria del papel desde la década de 1960 en adelante, comenzando en la década de 1950. [19]

Los AKD aplicados industrialmente se derivan de ácidos grasos con longitudes de cadena entre C14 ( ácido mirístico ) a C22 ( ácido behénico ); se utilizan preferiblemente palmitilo (C16) diceteno y estearil (C18) ceteno y mezclas de los mismos, así como mezclas de ácidos grasos de la hidrólisis de grasas animales y vegetales. Debido a la longitud de cadena de los ácidos grasos originales, los AKD son sólidos cerosos con puntos de fusión entre 42 y aproximadamente 70 °C. Las mezclas de dímeros de ceteno alquilados y agua son dispersiones a temperaturas inferiores a 40 °C o emulsiones a temperaturas superiores a 45 °C. Los AKD líquidos no se utilizan ampliamente, se basan en ácidos grasos insaturados como el ácido oleico o ácidos grasos ramificados, como el ácido isoesteárico.
Las dispersiones acuosas de alquildiceteno generalmente contienen 10-20% en peso de AKD, así como coloides protectores activos (particularmente policationes como almidón catiónico, copolímeros de N -vinilpirrolidona y N -vinilimidazol cuaternizado , polietileniminas aciladas o poliacrilamidas catiónicas de alto peso molecular con una masa molar promedio de hasta 7 millones de g/mol) y otros estabilizadores (generalmente tensioactivos aniónicos, por ejemplo ligninsulfonatos o productos de condensación de sal sódica de ácido naftalenosulfónico y formaldehído ). [20] Estas dispersiones de AKD estabilizadas son activas y estables a temperatura ambiente hasta tres meses y también toleran la adición de diferentes cargas para papel o cartón (por ejemplo , caolín , tiza, talco, dióxido de titanio , sulfato de calcio , óxido de aluminio, etc.) del 5 al 25%. Las cantidades de dímeros de alquilceteno utilizadas para el encolado de papel y productos de papel están preferiblemente en el rango de 0,15 a 0,8 % en peso, a veces de 0,05 a 0,2 % en peso, [18] en base a la masa de papel seca.
Para el encolado de papel con AKD, se propuso un proceso de tres pasos que, a pesar de las polémicas discusiones de los años 1990, parece describir mejor los procesos que se llevan a cabo y explica los resultados obtenidos. [21] Los criterios decisivos para la calidad de la hidrofobicidad de los papeles son

La estructura molecular (es decir, la masa molar y el grado de reticulación), la densidad de carga molar de los grupos catiónicos, la dosis exacta del polímero catiónico como estabilizador de dispersión y ayuda a la retención, así como el mantenimiento de otros parámetros del proceso como la temperatura, el pH y los tiempos de residencia son cruciales.
Después de eliminar el exceso de agua, también para evitar la hidrólisis del AKD al beta-cetoácido y la posterior descarboxilación a cetona,

A continuación, las partículas de AKD estabilizadas se agrietan sobre la masa de papel base, se derrite la cera de AKD sólida (a unos 90 °C), se extiende la cera de AKD líquida por difusión superficial sobre las fibras de celulosa y se forman capas hidrófobas cerradas. El espesor de las capas hidrófobas depende de la concentración de AKD en la dispersión. [22]
3. La hidrofobación de fibras de celulosa con dímeros de ceteno alquilados se produce de forma más eficaz en medios neutros o preferiblemente débilmente alcalinos (pH 7,5-9,0). La temperatura de reacción es generalmente de 90-110 °C, y aproximadamente el 40 % del AKD utilizado reacciona con la celulosa. [21] Después de la reacción , se miden ángulos de contacto de >100°, lo que indica el carácter hidrófobo de las superficies del modelo modificado con AKD. La esterificación de los grupos hidroxilo de las fibras de celulosa también se demostró mediante reacciones de comparación con AKD marcado con 14 C. [21]
El encolado con AKD es adecuado para la hidrofobización permanente de papel de periódico, papel de imprenta y de escritura y cartón utilizado como recipiente para líquidos (incluidos alimentos como la leche), así como para la mejora de la estabilidad de la forma y la manejabilidad.