El 1-vinilimidazol es un monómero básico soluble en agua que forma homopolímeros cuaternizables mediante polimerización por radicales libres con una variedad de monómeros vinílicos y acrílicos . Los productos son copolímeros funcionales que se utilizan como productos químicos en yacimientos petrolíferos y como auxiliares cosméticos. El 1-vinilimidazol actúa como diluyente reactivo en lacas UV, tintas y adhesivos.
La síntesis y las propiedades del 1-vinilimidazol se describieron en un artículo completo de Walter Reppe en 1957. [2] Primero se hace reaccionar el imidazol con una solución de hidróxido de potasio para formar imidazolato de potasio y el agua formada se elimina por destilación. Se añaden óxido de cinc e hidróxido de potasio al catalizador básico imidazolato de potasio y el imidazol libre se etinila en 1,4-dioxano a 130 °C con etina en un autoclave. El rendimiento es del 62 %.
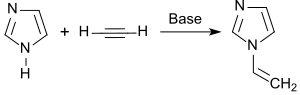
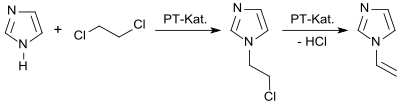
En un proceso de laboratorio, el imidazol reacciona en un sistema de dos fases en presencia de un catalizador de transferencia de fase con 1,2-dicloroetano para dar 1-(2-cloroetil)imidazol y este último se convierte al liberar cloruro de hidrógeno en 1-vinilimidazol con un rendimiento del 92%. [3]
Otro procedimiento a escala de laboratorio informa la vinilación de imidazol con bromoeteno y fluoruro de cesio soportado en kieselguhr en acetonitrilo con un rendimiento del 65%. [4]
El 1-vinilimidazol es un líquido incoloro a marrón, fotosensible, higroscópico y ligeramente alcalino que reacciona con un olor desagradable, similar al de las aminas y el pescado. El compuesto es muy soluble en agua y alcoholes. La polimerización por radicales libres del 1-vinilimidazol se produce muy lentamente a un pH de 9, pero a un pH de 1 es tan rápida como la del 1-vinilimidazol cuaternizado. [5]
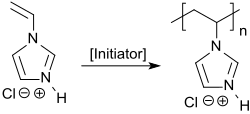
El 1-vinilimidazol se utiliza por su alta reactividad para la polimerización por radicales libres (UV) como diluyente reactivo en lacas UV, tintas y adhesivos para recubrimientos y lacas. También se utiliza para la funcionalización de superficies de polímeros mediante injerto inducido por UV para mejorar la humectabilidad y la adhesividad.
El 1-vinilimidazol se puede cuaternizar con yoduros de n-alquilo a yoduros de 3-n-alquil-1-vinilimidazolio o con sulfato de dimetilo a metosulfato de 3-metil-1-vinilimidazolio. [6] Los compuestos de amonio cuaternario resultantes se pueden polimerizar por radicales libres en solución acuosa con el iniciador azo soluble en agua ácido 4,4'-azobisvalérico.
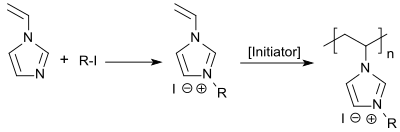
Los copolímeros de sales cuaternarias de N-vinilimidazolio y monómeros polares (en particular N-vinilpirrolidona ) son polielectrolitos catiónicos y son adecuados, entre otras cosas, como floculantes para el tratamiento de agua, como auxiliares de flotación para el procesamiento de carbón y minerales , como aditivos para fluidos de perforación y cementaciones en la extracción de petróleo, como cortadores de emulsiones para la deshidratación de emulsiones de petróleo crudo en refinerías y como inhibidores de corrosión para aleaciones de hierro. [7]
Los copolímeros de sales cuaternarias de N-vinilimidazolio y ácidos carboxílicos insaturados polimerizables (como el ácido metacrílico o los ácidos sulfónicos , como el ácido 2-acrilamido-2-metilpropanosulfónico ) reducen la carga electrostática , por ejemplo del cabello, y por lo tanto se utilizan en champús para mejorar la peinabilidad en húmedo. [8]
El 1-vinilimidazol se polimeriza radicalmente en una solución acuosa o alcohólica para formar homopolímeros con masas molares promedio de 2.000 a 50.000, [9] que, sin embargo, a menudo todavía contienen contenidos de monómero residual relativamente altos (> 600 ppm ). [10] Mediante la adición de reguladores de cadena que contienen azufre , como el mercaptoetanol , el contenido residual no deseado del N-vinilimidazol se puede reducir a menos de 50 ppm, aunque la masa molar del polímero obtenido también disminuye. [9]
Los hidrogeles de poli-1-vinilimidazol se unen de manera muy eficiente a una gran cantidad de iones de metales pesados (excepto Pb 2+ ), que pueden eluirse de forma selectiva y cuantitativa del hidrogel. [11]
El 1-vinilimidazol se puede copolimerizar por radicales libres con una variedad de monómeros vinílicos y acrílicos. Los copolímeros solubles en agua con vinilpirrolidona se utilizan como inhibidores de transferencia de color en preparaciones de detergentes, [12]
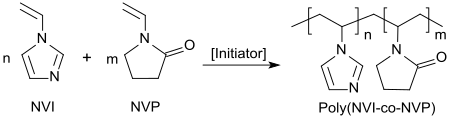
con acetato de vinilo como recubrimiento de placas de impresión litográfica , [13] con ésteres de ácido acrílico o ésteres de ácido metacrílico o metacrilato de 2-hidroxietilo como promotores de adhesión en pinturas [14] o con acrilonitrilo como precursores de fibras de carbono . [15]