Un trastorno genético es un problema de salud causado por una o más anomalías en el genoma . Puede ser causado por una mutación en un solo gen (monogénico) o en múltiples genes (poligénico) o por una anomalía cromosómica . Aunque los trastornos poligénicos son los más comunes, el término se utiliza principalmente cuando se habla de trastornos con una sola causa genética, ya sea en un gen o en un cromosoma . [1] [2] La mutación responsable puede ocurrir espontáneamente antes del desarrollo embrionario (una mutación de novo ), o puede heredarse de dos padres que son portadores de un gen defectuoso ( herencia autosómica recesiva ) o de un padre con el trastorno ( herencia autosómica dominante ). Cuando el trastorno genético se hereda de uno o ambos padres, también se clasifica como una enfermedad hereditaria . Algunos trastornos son causados por una mutación en el cromosoma X y tienen herencia ligada al cromosoma X. Muy pocos trastornos se heredan en el cromosoma Y o en el ADN mitocondrial (debido a su tamaño). [3]
Existen más de 6.000 trastornos genéticos conocidos [4] y constantemente se describen nuevos trastornos genéticos en la literatura médica [5] . Más de 600 trastornos genéticos son tratables [6] . Alrededor de 1 de cada 50 personas se ven afectadas por un trastorno monogénico conocido, mientras que alrededor de 1 de cada 263 se ven afectadas por un trastorno cromosómico [7] . Alrededor del 65% de las personas tienen algún tipo de problema de salud como resultado de mutaciones genéticas congénitas [7] . Debido al número significativamente grande de trastornos genéticos, aproximadamente 1 de cada 21 personas se ven afectadas por un trastorno genético clasificado como " raro " (generalmente definido como que afecta a menos de 1 de cada 2000 personas). La mayoría de los trastornos genéticos son raros en sí mismos [5] [8]
Los trastornos genéticos están presentes antes del nacimiento y algunos de ellos producen defectos congénitos , pero estos también pueden ser hereditarios y no relacionados con el desarrollo . Lo opuesto a una enfermedad hereditaria es una enfermedad adquirida . La mayoría de los cánceres , aunque implican mutaciones genéticas en una pequeña proporción de células del cuerpo, son enfermedades adquiridas. Sin embargo, algunos síndromes de cáncer , como las mutaciones BRCA , son trastornos genéticos hereditarios. [9]
Un trastorno monogénico (o trastorno monogénico ) es el resultado de un único gen mutado . Los trastornos monogénicos pueden transmitirse a las generaciones posteriores de varias formas. Sin embargo, la impronta genómica y la disomía uniparental pueden afectar los patrones de herencia. Las divisiones entre los tipos recesivos y dominantes no son "rígidas", aunque las divisiones entre los tipos autosómicos y ligados al cromosoma X sí lo son (ya que los últimos tipos se distinguen puramente en función de la ubicación cromosómica del gen). Por ejemplo, la forma común de enanismo , la acondroplasia , generalmente se considera un trastorno dominante, pero los niños con dos genes de acondroplasia tienen un trastorno esquelético grave y generalmente letal, del que los acondroplásicos podrían considerarse portadores. La anemia de células falciformes también se considera una afección recesiva, pero los portadores heterocigotos tienen una mayor resistencia a la malaria en la primera infancia, lo que podría describirse como una afección dominante relacionada. [18] Cuando una pareja en la que uno o ambos miembros están afectados o son portadores de una alteración genética única desea tener un hijo, puede hacerlo mediante la fertilización in vitro , que permite realizar un diagnóstico genético preimplantacional para comprobar si el embrión tiene la alteración genética. [19]
La mayoría de los trastornos metabólicos congénitos, conocidos como errores innatos del metabolismo, son resultado de defectos de un solo gen. Muchos de estos defectos de un solo gen pueden reducir la aptitud física de las personas afectadas y, por lo tanto, están presentes en la población en frecuencias más bajas en comparación con lo que se esperaría según cálculos probabilísticos simples. [20]
Solo será necesaria una copia mutada del gen para que una persona se vea afectada por un trastorno autosómico dominante. Cada persona afectada suele tener un progenitor afectado. [21] : 57 La probabilidad de que un niño herede el gen mutado es del 50%. Las afecciones autosómicas dominantes a veces tienen una penetrancia reducida , lo que significa que aunque solo se necesita una copia mutada, no todos los individuos que heredan esa mutación desarrollan la enfermedad. Ejemplos de este tipo de trastorno son la enfermedad de Huntington , [21] : 58 la neurofibromatosis tipo 1 , la neurofibromatosis tipo 2 , el síndrome de Marfan , el cáncer colorrectal hereditario sin poliposis , las exostosis múltiples hereditarias (un trastorno autosómico dominante de alta penetración), la esclerosis tuberosa , la enfermedad de Von Willebrand y la porfiria intermitente aguda . Los defectos de nacimiento también se denominan anomalías congénitas. [22]
Dos copias del gen deben estar mutadas para que una persona se vea afectada por un trastorno autosómico recesivo. Una persona afectada generalmente tiene padres no afectados que portan cada uno una sola copia del gen mutado y se denominan portadores genéticos . Cada padre con un gen defectuoso normalmente no presenta síntomas. [23] Dos personas no afectadas que portan cada una una copia del gen mutado tienen un riesgo del 25% con cada embarazo de tener un hijo afectado por el trastorno. Ejemplos de este tipo de trastorno son el albinismo , la deficiencia de acil-CoA deshidrogenasa de cadena media , la fibrosis quística , la anemia de células falciformes , la enfermedad de Tay-Sachs , la enfermedad de Niemann-Pick , la atrofia muscular espinal y el síndrome de Roberts . Ciertos otros fenotipos, como la cera húmeda frente a la cera seca , también se determinan de forma autosómica recesiva. [24] [25] Algunos trastornos autosómicos recesivos son comunes porque, en el pasado, llevar uno de los genes defectuosos conducía a una ligera protección contra una enfermedad infecciosa o toxina como la tuberculosis o la malaria . [26] Dichos trastornos incluyen la fibrosis quística, [27] la anemia de células falciformes, [28] la fenilcetonuria [29] y la talasemia . [30]

Los trastornos dominantes ligados al cromosoma X son causados por mutaciones en genes del cromosoma X. Solo unos pocos trastornos tienen este patrón de herencia, siendo un excelente ejemplo el raquitismo hipofosfatémico ligado al cromosoma X. Tanto hombres como mujeres se ven afectados por estos trastornos, siendo los hombres típicamente más gravemente afectados que las mujeres. Algunas afecciones dominantes ligadas al cromosoma X, como el síndrome de Rett , la incontinencia pigmentaria tipo 2 y el síndrome de Aicardi , suelen ser fatales en los varones, ya sea en el útero o poco después del nacimiento, y por lo tanto se observan predominantemente en mujeres. Las excepciones a este hallazgo son casos extremadamente raros en los que los niños con síndrome de Klinefelter (44 +xxy) también heredan una afección dominante ligada al cromosoma X y presentan síntomas más similares a los de una mujer en términos de gravedad de la enfermedad. La probabilidad de transmitir un trastorno dominante ligado al cromosoma X difiere entre hombres y mujeres. Los hijos de un hombre con un trastorno dominante ligado al cromosoma X no se verán afectados (ya que reciben el cromosoma Y de su padre), pero sus hijas heredarán la afección. Una mujer con un trastorno dominante ligado al cromosoma X tiene un 50% de posibilidades de tener un feto afectado en cada embarazo, aunque en casos como la incontinencia pigmentaria generalmente sólo son viables las crías femeninas.
Las enfermedades recesivas ligadas al cromosoma X también son causadas por mutaciones en los genes del cromosoma X. Los hombres se ven afectados con mucha más frecuencia que las mujeres, porque solo tienen el cromosoma X necesario para que se presente la enfermedad. La probabilidad de transmitir el trastorno difiere entre hombres y mujeres. Los hijos de un hombre con un trastorno recesivo ligado al cromosoma X no se verán afectados (ya que reciben el cromosoma Y de su padre), pero sus hijas serán portadoras de una copia del gen mutado. Una mujer portadora de un trastorno recesivo ligado al cromosoma X (X R X r ) tiene un 50% de probabilidades de tener hijos afectados y un 50% de probabilidades de tener hijas portadoras de una copia del gen mutado. Las enfermedades recesivas ligadas al cromosoma X incluyen las enfermedades graves hemofilia A , distrofia muscular de Duchenne y síndrome de Lesch-Nyhan , así como enfermedades comunes y menos graves como la calvicie de patrón masculino y el daltonismo rojo-verde . Las enfermedades recesivas ligadas al cromosoma X a veces pueden manifestarse en mujeres debido a una inactivación sesgada del cromosoma X o a una monosomía del cromosoma X ( síndrome de Turner ). [ cita requerida ]
Los trastornos ligados al cromosoma Y son causados por mutaciones en el cromosoma Y. Estas afecciones solo pueden transmitirse del sexo heterogamético (por ejemplo, los hombres) a los hijos del mismo sexo. En términos más simples, esto significa que los trastornos ligados al cromosoma Y en los seres humanos solo pueden transmitirse de los hombres a sus hijos; las mujeres nunca pueden verse afectadas porque no poseen alosomas del cromosoma Y. [ cita requerida ]
Los trastornos ligados al cromosoma Y son extremadamente raros, pero los ejemplos más conocidos suelen causar infertilidad. La reproducción en tales condiciones solo es posible evitando la infertilidad mediante una intervención médica.
Este tipo de herencia, también conocida como herencia materna, es la más rara y se aplica a los 13 genes codificados por el ADN mitocondrial . Debido a que solo los óvulos aportan mitocondrias al embrión en desarrollo, solo las madres (que están afectadas) pueden transmitir afecciones del ADN mitocondrial a sus hijos. Un ejemplo de este tipo de trastorno es la neuropatía óptica hereditaria de Leber . [31]
Es importante destacar que la gran mayoría de las enfermedades mitocondriales (en particular cuando los síntomas se desarrollan en etapas tempranas de la vida) en realidad son causadas por un defecto genético nuclear , ya que las mitocondrias se desarrollan principalmente a partir de ADN no mitocondrial. Estas enfermedades suelen seguir un patrón de herencia autosómico recesivo. [32]
Los trastornos genéticos también pueden ser complejos, multifactoriales o poligénicos, lo que significa que probablemente estén asociados con los efectos de múltiples genes en combinación con estilos de vida y factores ambientales. Los trastornos multifactoriales incluyen enfermedades cardíacas y diabetes . Aunque los trastornos complejos a menudo se agrupan en familias, no tienen un patrón claro de herencia. Esto dificulta determinar el riesgo de una persona de heredar o transmitir estos trastornos. Los trastornos complejos también son difíciles de estudiar y tratar porque los factores específicos que causan la mayoría de estos trastornos aún no se han identificado. Los estudios que apuntan a identificar la causa de los trastornos complejos pueden utilizar varios enfoques metodológicos para determinar las asociaciones genotipo - fenotipo . Un método, el enfoque genotipo primero , comienza identificando variantes genéticas dentro de los pacientes y luego determinando las manifestaciones clínicas asociadas. Esto se opone al enfoque fenotipo primero más tradicional, y puede identificar factores causales que previamente han sido oscurecidos por la heterogeneidad clínica , la penetrancia y la expresividad. [ cita requerida ]
En un árbol genealógico, las enfermedades poligénicas tienden a "transmitirse entre familias", pero la herencia no se ajusta a patrones simples como en el caso de las enfermedades mendelianas . Esto no significa que los genes no puedan ser localizados y estudiados en el futuro. También existe un fuerte componente ambiental en muchas de ellas (por ejemplo, la presión arterial ).
Otros casos similares incluyen:
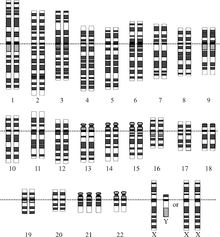
Un trastorno cromosómico es una porción faltante, adicional o irregular del ADN cromosómico. [33] Puede deberse a un número atípico de cromosomas o a una anomalía estructural en uno o más cromosomas. Un ejemplo de estos trastornos es la trisomía 21 (la forma más común del síndrome de Down ), en la que hay una copia adicional del cromosoma 21 en todas las células. [34]
Debido a la amplia gama de trastornos genéticos que se conocen, el diagnóstico es muy variado y depende del trastorno en cuestión. La mayoría de los trastornos genéticos se diagnostican antes del nacimiento , al nacer o durante la primera infancia; sin embargo, algunos, como la enfermedad de Huntington , pueden pasar desapercibidos hasta que el paciente comienza a presentar síntomas en la edad adulta. [35]
Los aspectos básicos de un trastorno genético se basan en la herencia del material genético. Con una historia familiar detallada , es posible anticipar posibles trastornos en los niños que dirigen a los profesionales médicos a pruebas específicas según el trastorno y permiten a los padres la oportunidad de prepararse para posibles cambios en el estilo de vida, anticipar la posibilidad de muerte fetal o contemplar la interrupción del embarazo . [36] El diagnóstico prenatal puede detectar la presencia de anomalías características en el desarrollo fetal a través de la ecografía , o detectar la presencia de sustancias características a través de procedimientos invasivos que implican la inserción de sondas o agujas en el útero, como en la amniocentesis . [37]
No todos los trastornos genéticos resultan directamente en la muerte; sin embargo, no se conocen curas para los trastornos genéticos. Muchos trastornos genéticos afectan etapas del desarrollo, como el síndrome de Down , mientras que otros resultan en síntomas puramente físicos como la distrofia muscular . Otros trastornos, como la enfermedad de Huntington , no muestran signos hasta la edad adulta. Durante el tiempo activo de un trastorno genético, los pacientes dependen principalmente de mantener o ralentizar la degradación de la calidad de vida y mantener la autonomía del paciente . Esto incluye fisioterapia y manejo del dolor .

El tratamiento de los trastornos genéticos es una batalla continua, con más de 1.800 ensayos clínicos de terapia genética que se han completado, están en curso o han sido aprobados en todo el mundo. [38] A pesar de esto, la mayoría de las opciones de tratamiento giran en torno al tratamiento de los síntomas de los trastornos en un intento de mejorar la calidad de vida del paciente .
La terapia génica es una forma de tratamiento en la que se introduce un gen sano en un paciente. Esto debería aliviar el defecto causado por un gen defectuoso o ralentizar la progresión de la enfermedad. Un obstáculo importante ha sido la administración de genes a la célula, el tejido y el órgano adecuados afectados por el trastorno. Los investigadores han estudiado cómo pueden introducir un gen en los billones de células que potencialmente contienen la copia defectuosa. Encontrar una respuesta a esto ha sido un obstáculo entre la comprensión del trastorno genético y su corrección. [39]
Alrededor de 1 de cada 50 personas se ve afectada por un trastorno conocido de un solo gen, mientras que alrededor de 1 de cada 263 se ve afectada por un trastorno cromosómico . [7] Alrededor del 65% de las personas tienen algún tipo de problema de salud como resultado de mutaciones genéticas congénitas. [7] Debido al número significativamente grande de trastornos genéticos, aproximadamente 1 de cada 21 personas se ve afectada por un trastorno genético clasificado como " raro " (generalmente definido como que afecta a menos de 1 de cada 2000 personas). La mayoría de los trastornos genéticos son raros en sí mismos. [5] [8] Hay más de 6000 trastornos genéticos conocidos, [4] y constantemente se describen nuevos trastornos genéticos en la literatura médica. [5]
La condición genética más antigua conocida en un homínido se encontró en la especie fósil Paranthropus robustus , con más de un tercio de los individuos mostrando amelogénesis imperfecta . [40]
(calculado a partir de "1 de cada 17" trastornos raros y "80%" de los trastornos raros que son genéticos)