ZMapp es un fármaco biofarmacéutico experimental que comprende tres anticuerpos monoclonales quiméricos en desarrollo como tratamiento para la enfermedad del virus del Ébola . [1] Dos de los tres componentes se desarrollaron originalmente en el Laboratorio Nacional de Microbiología (NML) de la Agencia de Salud Pública de Canadá , y el tercero en el Instituto de Investigación Médica de Enfermedades Infecciosas del Ejército de EE. UU .; el cóctel fue optimizado por Gary Kobinger , un científico investigador del NML [2] y se sometió a un mayor desarrollo bajo licencia de Mapp Biopharmaceutical . ZMapp se utilizó por primera vez en humanos durante la epidemia del virus del Ébola en África occidental , habiéndose probado previamente solo en animales y aún no se había sometido a un ensayo controlado aleatorio . [3] Los Institutos Nacionales de Salud (NIH) realizaron un ensayo clínico a partir de enero de 2015 con sujetos de Sierra Leona, Guinea y Liberia con el objetivo de inscribir a 200 personas, pero la epidemia disminuyó y el ensayo se cerró antes de tiempo, dejándolo demasiado poco potente estadísticamente para dar un resultado significativo sobre si ZMapp funcionó. [4]
En 2016, un estudio clínico que comparó ZMapp con el estándar actual de atención para el ébola no fue concluyente. [5]
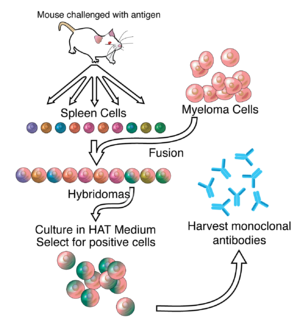
El fármaco está compuesto por tres anticuerpos monoclonales (mAbs), inicialmente cosechados de ratones expuestos a proteínas del virus del Ébola, que han sido quimerizados con regiones constantes humanas . [6] Los componentes son el anticuerpo monoclonal quimérico c13C6 de un cóctel de anticuerpos previamente existente llamado "MB-003" y dos mAbs quiméricos de un cóctel de anticuerpos diferente llamado ZMab, c2G4 y c4G7. [7] ZMapp se fabrica en la planta de tabaco Nicotiana benthamiana en el proceso de bioproducción conocido como " pharming " por Kentucky BioProcessing, una subsidiaria de Reynolds American . [1] [8] [9]
Al igual que la terapia de inmunoglobulina intravenosa , ZMapp contiene una mezcla de anticuerpos neutralizantes que confieren inmunidad pasiva a un individuo, mejorando la respuesta inmune normal, y está diseñado para ser administrado después de la exposición al virus del Ébola. [10] Dichos anticuerpos se han utilizado en el tratamiento y la prevención de diversas enfermedades infecciosas y están destinados a atacar al virus interfiriendo con su superficie y neutralizándolo para evitar daños mayores. [10] [11]

Dos de los tres componentes del fármaco se desarrollaron originalmente en el Laboratorio Nacional de Microbiología (NML) de la Agencia de Salud Pública de Canadá, y un tercero en el Instituto de Investigación Médica de Enfermedades Infecciosas del Ejército de los EE. UU. [2] El cóctel fue optimizado por Gary Kobinger, entonces jefe de la rama del NML, y está siendo desarrollado por Leaf Biopharmaceutical (LeafBio, Inc.), una división con sede en San Diego de Mapp Biopharmaceutical. [12] LeafBio creó ZMapp en colaboración con su matriz y Defyrus Inc., cada una de las cuales había licenciado su propio cóctel de anticuerpos, llamados MB-003 y ZMab. [13] [ cita requerida ]
El MB-003 es un cóctel de tres mAb humanizados o quiméricos de humano-ratón: c13C6, h13F6 y c6D8. [7] Un estudio publicado en septiembre de 2012 descubrió que los macacos rhesus infectados con el virus del Ébola (EBOV) sobrevivieron cuando recibieron MB-003 (mezcla de 3 anticuerpos monoclonales quiméricos) una hora después de la infección. Cuando se los trató 24 o 48 horas después de la infección, cuatro de los seis animales sobrevivieron y tuvieron poca o ninguna viremia y pocos síntomas clínicos, si los hubo. [14]
MB-003 fue creado por científicos del Instituto de Investigación Médica de Enfermedades Infecciosas del Ejército de EE. UU., Gene Olinger y Jamie Pettitt en colaboración con Mapp Biopharmaceutical con años de financiación de agencias del gobierno de EE. UU., incluido el Instituto Nacional de Alergias y Enfermedades Infecciosas , la Autoridad de Investigación y Desarrollo Biomédico Avanzado y la Agencia de Reducción de Amenazas de Defensa . [1] [2] [15]
El ZMAb es una mezcla de tres mAb de ratón: m1H3, m2G4 y m4G7. [7] Un estudio publicado en noviembre de 2013 descubrió que los monos macacos infectados con EBOV sobrevivieron después de recibir una terapia con una combinación de tres anticuerpos monoclonales específicos de la glucoproteína de superficie del EBOV (EBOV-GP) (ZMAb) dentro de las 24 horas posteriores a la infección. Los autores concluyeron que el tratamiento posterior a la exposición resultó en una respuesta inmunitaria sólida, con buena protección durante hasta 10 semanas y cierta protección a las 13 semanas. [16] El ZMab fue creado por el NML y licenciado a Defyrus, una empresa de biodefensa con sede en Toronto , con financiación adicional de la Agencia de Salud Pública de Canadá . [2]
Un artículo de 2014 describió cómo Mapp y sus colaboradores, incluidos investigadores de la Agencia de Salud Pública de Canadá , Kentucky BioProcessing y el Instituto Nacional de Alergias y Enfermedades Infecciosas , primero quimerizaron los tres anticuerpos que comprendían ZMAb, luego probaron combinaciones de MB-003 y los anticuerpos quiméricos ZMAb en cobayas y luego en primates para determinar la mejor combinación, que resultó ser c13C6 de MB-003 y dos mAb quiméricos de ZMAb, c2G4 y c4G7. Esto es ZMapp. [7]
En un experimento publicado también en el artículo de 2014, 21 primates macacos rhesus fueron infectados con la variante congoleña Kikwit del virus del Ébola. A tres primates del grupo de control se les administró un anticuerpo no funcional, y los 18 del grupo de tratamiento se dividieron en tres grupos de seis. Todos los primates del grupo de tratamiento recibieron tres dosis de ZMapp, espaciadas con 3 días de diferencia. El primer grupo de tratamiento recibió su primera dosis el tercer día después de ser infectado; el segundo grupo el cuarto día después de ser infectado, y el tercer grupo, el quinto día después de ser infectado. Los tres primates del grupo de control murieron; los 18 primates del grupo de tratamiento sobrevivieron. [7] Mapp luego pasó a demostrar que ZMapp inhibe la replicación de una cepa guineana del virus del Ébola en cultivos celulares. [17]
Mapp sigue involucrado en la producción del fármaco a través de sus contratos con Kentucky BioProcessing, una subsidiaria de Reynolds American . [1] Para producir el fármaco, los genes que codifican los mAb quiméricos se insertaron en vectores virales , y las plantas de tabaco se infectan con el vector viral que codifica los anticuerpos, utilizando cultivos de Agrobacterium . [18] [19] [20] Posteriormente, los anticuerpos se extraen y purifican de las plantas. Una vez que los genes que codifican los mAb quiméricos están en la mano, se cree que todo el ciclo de producción de tabaco demora unos meses. [3] El desarrollo de estos métodos de producción fue financiado por la Agencia de Proyectos de Investigación Avanzada de Defensa de los EE. UU. como parte de sus esfuerzos de biodefensa después de los ataques terroristas del 11 de septiembre. [21] [22]
ZMapp se utilizó por primera vez durante el brote del virus del Ébola en África Occidental de 2014, sin haberse sometido previamente a ningún ensayo clínico en humanos para determinar su eficacia o riesgos potenciales. [3] En octubre de 2014, la Administración de Alimentos y Medicamentos de los Estados Unidos había aprobado el uso de varios medicamentos experimentales, incluido ZMapp, para su uso en pacientes infectados con el virus del Ébola. La Organización Mundial de la Salud también consideró ético el uso de dichos medicamentos durante la epidemia . [23] En 2014, se utilizó un suministro limitado de ZMapp para tratar a 7 personas infectadas con el virus del Ébola; de estos, 2 murieron. [24] [25] El resultado no se considera estadísticamente significativo . Mapp anunció en agosto de 2014 que se habían agotado los suministros de ZMapp. [26]
La falta de medicamentos y la falta de disponibilidad de un tratamiento experimental en las regiones más afectadas por el brote del virus del Ébola en África occidental provocaron cierta controversia. [3] El hecho de que el medicamento se administrara primero a estadounidenses y a un europeo y no a africanos, según Los Angeles Times , "provocó indignación, alimentando las percepciones africanas de la insensibilidad y la arrogancia occidentales, con un profundo sentido de desconfianza y traición que aún persiste sobre la explotación y los abusos de la era colonial". [27] Salim S. Abdool Karim , director de un centro de investigación sobre el SIDA en Sudáfrica, situó el tema en el contexto de la historia de explotación y abusos. En respuesta a una pregunta sobre cómo habría reaccionado la gente si ZMapp y otros medicamentos se hubieran utilizado primero en africanos, dijo que "habría sido el titular de primera plana: 'Africanos utilizados como conejillos de indias para la medicina de una compañía farmacéutica estadounidense ' ". [3]
A principios de agosto, la Organización Mundial de la Salud pidió que se convocara un panel de autoridades médicas "para considerar si los medicamentos experimentales deberían distribuirse más ampliamente". En una declaración, Peter Piot (codescubridor del virus del Ébola); Jeremy Farrar, director del Wellcome Trust ; y David Heymann, del Chatham House Center on Global Health Security, pidieron la liberación de medicamentos experimentales para las naciones africanas afectadas . [27]
En una conferencia de prensa celebrada el 6 de agosto de 2014, se le preguntó a Barack Obama , presidente de los Estados Unidos , si se debería acelerar la aprobación del cóctel o si se debería poner a disposición de pacientes enfermos fuera de los Estados Unidos. Obama respondió: "Creo que tenemos que dejar que la ciencia nos guíe. No creo que se disponga de toda la información sobre si este fármaco es útil". [28]
El 27 de febrero de 2015, los Institutos Nacionales de Salud anunciaron el inicio de un ensayo controlado aleatorio de ZMapp que se llevaría a cabo en Liberia y los Estados Unidos. [29] Desde marzo de 2015 hasta noviembre de 2015, 72 personas infectadas con el virus del Ébola se inscribieron en el ensayo; los investigadores dejaron de inscribir nuevos sujetos en enero de 2016, al no haber logrado alcanzar su objetivo de inscripción de 200 debido a la disminución del brote de Ébola . Como resultado, aunque se calculó un riesgo de muerte un 40% menor para aquellos que recibieron ZMapp, la diferencia no fue estadísticamente significativa y, en última instancia, no se pudo determinar si el uso de ZMapp era superior al estándar de atención optimizado solo. Sin embargo, se encontró que ZMapp era seguro y bien tolerado. [4] [30] [31]
La Organización Mundial de la Salud evaluó el cóctel ZMapp para su uso en casos de emergencia según el protocolo ético MEURI . El panel estuvo de acuerdo en que "los beneficios del ZMapp superan sus riesgos", aunque señaló que presentaba desafíos logísticos, en particular el de requerir una cadena de frío para su distribución y almacenamiento. [32] También se consideraron para su uso cuatro terapias alternativas ( remdesivir , el producto de Regeneron atoltivimab/maftivimab/odesivimab , favipiravir y ansuvimab ), pero se encontraban en etapas iniciales de desarrollo. [32] En agosto de 2019, las autoridades sanitarias nacionales de la República Democrática del Congo, la Organización Mundial de la Salud y los Institutos Nacionales de Salud anunciaron que dejarían de usar ZMapp, junto con todos los demás tratamientos contra el ébola, excepto atoltivimab/maftivimab/odesivimab y ansuvimab, en sus ensayos clínicos en curso, citando las mayores tasas de mortalidad de los pacientes no tratados con atoltivimab/maftivimab/odesivimab y ansuvimab. [33] [34]
En octubre de 2020, la Administración de Alimentos y Medicamentos de Estados Unidos (FDA) aprobó atoltivimab/maftivimab/odesivimab con indicación para el tratamiento de la infección causada por el ébolavirus de Zaire . [35]