Las vías de señalización Wnt son un grupo de vías de transducción de señales que comienzan con proteínas que pasan señales a una célula a través de receptores de la superficie celular . El nombre Wnt es un acrónimo creado a partir de los nombres Wingless e Int-1. [1] Las vías de señalización Wnt utilizan comunicación entre células cercanas ( paracrina ) o comunicación entre células iguales ( autocrina ). Están altamente conservados evolutivamente en los animales, lo que significa que son similares en todas las especies animales, desde las moscas de la fruta hasta los humanos. [2] [3]
Se han caracterizado tres vías de señalización Wnt: la vía Wnt canónica , la vía de polaridad celular plana no canónica y la vía Wnt/calcio no canónica . Las tres vías se activan mediante la unión de un ligando de la proteína Wnt a un receptor de la familia Frizzled , que pasa la señal biológica a la proteína Disheveled dentro de la célula. La vía canónica Wnt conduce a la regulación de la transcripción genética y se cree que está regulada negativamente en parte por el gen SPATS1 . [4] La vía de polaridad celular plana no canónica regula el citoesqueleto que es responsable de la forma de la célula. La vía no canónica Wnt/calcio regula el calcio dentro de la célula.
La señalización Wnt se identificó primero por su papel en la carcinogénesis y luego por su función en el desarrollo embrionario . Los procesos embrionarios que controla incluyen el patrón de los ejes corporales , la especificación del destino celular , la proliferación celular y la migración celular . Estos procesos son necesarios para la formación adecuada de tejidos importantes, incluidos los huesos, el corazón y los músculos. Su papel en el desarrollo embrionario se descubrió cuando mutaciones genéticas en las proteínas de la vía Wnt produjeron embriones anormales de mosca de la fruta . Investigaciones posteriores descubrieron que los genes responsables de estas anomalías también influyeron en el desarrollo del cáncer de mama en ratones. La señalización Wnt también controla la regeneración de tejidos en la médula ósea, la piel y el intestino de adultos. [5]
La importancia clínica de esta vía quedó demostrada por mutaciones que conducen a diversas enfermedades, incluido el cáncer de mama y de próstata , el glioblastoma , la diabetes tipo II y otras. [6] [7] En los últimos años, los investigadores informaron por primera vez sobre el uso exitoso de inhibidores de la vía Wnt en modelos de enfermedad en ratones. [8]
El descubrimiento de la señalización Wnt estuvo influenciado por la investigación sobre retrovirus oncogénicos (que causan cáncer) . En 1982, Roel Nusse y Harold Varmus infectaron ratones con el virus del tumor mamario de ratón para mutar genes de ratón y ver qué genes mutados podrían causar tumores de mama. Identificaron un nuevo protooncogén de ratón al que denominaron int1 (integración 1). [3] [9]
Int1 está altamente conservado en múltiples especies, incluidos los humanos y Drosophila . Su presencia en D. melanogaster llevó a los investigadores a descubrir en 1987 que el gen int1 en Drosophila era en realidad el gen ya conocido y caracterizado de Drosophila conocido como Wingless (Wg). [3] Dado que investigaciones anteriores de Christiane Nüsslein-Volhard y Eric Wieschaus (que les valieron el Premio Nobel de Fisiología o Medicina en 1995) ya habían establecido la función de Wg como un gen de polaridad de segmento implicado en la formación del eje corporal durante el desarrollo embrionario. desarrollo , los investigadores determinaron que el mamífero int1 descubierto en ratones también está involucrado en el desarrollo embrionario. [10]
La investigación continua condujo al descubrimiento de más genes relacionados con int1; sin embargo, debido a que esos genes no se identificaron de la misma manera que int1, la nomenclatura del gen int era inadecuada. Así, la familia int/Wingless se convirtió en la familia Wnt y int1 se convirtió en Wnt1. El nombre Wnt es un acrónimo de int y Wg y significa "sitio de integración relacionado con Wingless". [3]
Wnt comprende una familia diversa de glicoproteínas de señalización modificadas con lípidos secretadas que tienen entre 350 y 400 aminoácidos de longitud. [11] La modificación lipídica de todos los Wnts es la palmitoleoilación de un único residuo de cisteína totalmente conservado. [12] La palmitoleoilación es necesaria porque es necesaria para que Wnt se una a su proteína transportadora Wntless (WLS) para que pueda transportarse a la membrana plasmática para su secreción [13] y permite que la proteína Wnt se una a su receptor Frizzled [14] [15] Las proteínas Wnt también se someten a glicosilación , que une un carbohidrato para garantizar una secreción adecuada. [16] En la señalización Wnt, estas proteínas actúan como ligandos para activar las diferentes vías Wnt a través de rutas paracrinas y autocrinas. [2] [7]
Estas proteínas están altamente conservadas entre especies. [3] Se pueden encontrar en ratones, humanos, Xenopus , pez cebra , Drosophila y muchos otros. [17]
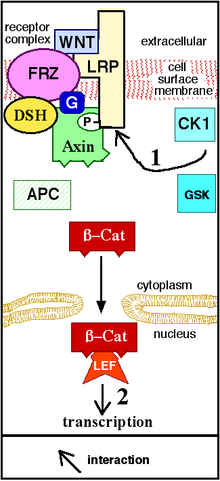

La señalización Wnt comienza cuando una proteína Wnt se une al dominio extracelular N-terminal rico en cisteína de un receptor de la familia Frizzled (Fz). [19] Estos receptores atraviesan la membrana plasmática siete veces y constituyen una familia distinta de receptores acoplados a proteína G (GPCR). [20] Sin embargo, para facilitar la señalización Wnt, es posible que se requieran correceptores junto con la interacción entre la proteína Wnt y el receptor Fz. Los ejemplos incluyen la proteína relacionada con el receptor de lipoproteína ( LRP ) -5/6, el receptor tirosina quinasa (RTK) y ROR2 . [7] Tras la activación del receptor, se envía una señal a la fosfoproteína Disheveled (Dsh), que se encuentra en el citoplasma . Esta señal se transmite mediante una interacción directa entre Fz y Dsh. Las proteínas Dsh están presentes en todos los organismos y todas comparten los siguientes dominios proteicos altamente conservados: un dominio DIX amino-terminal, un dominio PDZ central y un dominio DEP carboxi-terminal . Estos diferentes dominios son importantes porque después de Dsh, la señal Wnt puede ramificarse en múltiples vías y cada vía interactúa con una combinación diferente de los tres dominios. [21]
Las tres vías de señalización Wnt mejor caracterizadas son la vía Wnt canónica, la vía de polaridad celular plana no canónica y la vía Wnt/calcio no canónica. Como sugieren sus nombres, estas vías pertenecen a una de dos categorías: canónicas o no canónicas. La diferencia entre las categorías es que una vía canónica involucra la proteína beta-catenina (β-catenina), mientras que una vía no canónica opera independientemente de ella. [19]

La vía Wnt canónica (o vía Wnt/β-catenina) es la vía Wnt que provoca una acumulación de β-catenina en el citoplasma y su eventual translocación al núcleo para actuar como un coactivador transcripcional de factores de transcripción que pertenecen al TCF/ Familia LEF . Sin Wnt, la β-catenina no se acumularía en el citoplasma ya que normalmente un complejo de destrucción la degradaría. Este complejo de destrucción incluye las siguientes proteínas: Axina , adenomatosis poliposis coli (APC), proteína fosfatasa 2A (PP2A), glucógeno sintasa quinasa 3 (GSK3) y caseína quinasa 1 α (CK1α). [22] [23] Degrada la β-catenina al dirigirla a la ubiquitinación , que posteriormente la envía al proteasoma para ser digerida. [19] [24] Sin embargo, tan pronto como Wnt se une a Fz y LRP5 / 6 , la función del complejo de destrucción se altera. Esto se debe a que Wnt provoca la translocación del regulador Wnt negativo, Axin, y el complejo de destrucción a la membrana plasmática. Posteriormente, la fosforilación por otras proteínas en el complejo de destrucción une Axin a la cola citoplasmática de LRP5/6. La axina se desfosforila y su estabilidad y niveles disminuyen. Luego, Dsh se activa mediante fosforilación y sus dominios DIX y PDZ inhiben la actividad GSK3 del complejo de destrucción. Esto permite que la β-catenina se acumule y se localice en el núcleo y posteriormente induzca una respuesta celular mediante transducción de genes junto con los factores de transcripción TCF/LEF (factor de células T/factor potenciador linfoide) [25] . [24] La β-catenina recluta otros coactivadores transcripcionales, como BCL9 , Pygopus [26] y Parafibromin/Hyrax. [27] La complejidad del complejo transcripcional ensamblado por β-catenina está comenzando a emerger gracias a nuevos estudios proteómicos de alto rendimiento . [28] Sin embargo, todavía falta una teoría unificada de cómo la β-catenina impulsa la expresión del gen objetivo, y los actores específicos de tejido podrían ayudar a la β-catenina a definir sus genes objetivo. [29] La extensividad de la β-cateninaLas proteínas que interactúan complican nuestra comprensión: la β-catenina puede ser fosforilada directamente en Ser552 por Akt, lo que provoca su disociación de los contactos célula-célula y su acumulación en el citosol; posteriormente, 14-3-3ζ interactúa con la β-catenina (pSer552) y mejora su capacidad nuclear. translocación. [30] De hecho, se ha informado que BCL9 y Pygopus poseen varias funciones independientes de β-catenina (por lo tanto, probablemente, independientes de la señalización Wnt). [31] [32] [33]
La vía de polaridad celular plana (PCP) no canónica no implica la β-catenina. No utiliza LRP-5/6 como correceptor y se cree que utiliza NRH1, Ryk , PTK7 o ROR2 . La vía PCP se activa mediante la unión de Wnt a Fz y su correceptor. Luego, el receptor recluta Dsh , que utiliza sus dominios PDZ y DIX para formar un complejo con el activador de la morfogénesis 1 asociado a Dishevelled ( DAAM1 ). Luego, Daam1 activa la pequeña proteína G Rho a través de un factor de intercambio de guanina . Rho activa la quinasa asociada a Rho (ROCK), que es uno de los principales reguladores del citoesqueleto . Dsh también forma un complejo con rac1 y media la unión de profilina a actina . Rac1 activa JNK y también puede conducir a la polimerización de actina . La unión de profilina a la actina puede provocar la reestructuración del citoesqueleto y la gastrulación . [7] [34]

La vía no canónica Wnt/calcio tampoco implica β-catenina. Su función es ayudar a regular la liberación de calcio desde el retículo endoplásmico (RE) para controlar los niveles de calcio intracelular. Al igual que otras vías Wnt, tras la unión del ligando, el receptor Fz activado interactúa directamente con Dsh y activa dominios específicos de la proteína Dsh. Los dominios implicados en la señalización de Wnt/calcio son los dominios PDZ y DEP. [7] Sin embargo, a diferencia de otras vías Wnt, el receptor Fz interactúa directamente con una proteína G trimérica. Esta coestimulación de Dsh y la proteína G puede conducir a la activación de PLC o de PDE específica de cGMP . Si se activa PLC, el componente de la membrana plasmática PIP2 se escinde en DAG e IP3 . Cuando IP3 se une a su receptor en el RE, se libera calcio. Las concentraciones elevadas de calcio y DAG pueden activar Cdc42 a través de PKC . Cdc42 es un importante regulador del patrón ventral. El aumento de calcio también activa la calcineurina y CaMKII . CaMKII induce la activación del factor de transcripción NFAT , que regula la adhesión celular, la migración y la separación de tejidos. [7] La calcineurina activa la quinasa TAK1 y NLK , que puede interferir con la señalización de TCF/β-catenina en la vía canónica Wnt. [35] Sin embargo, si se activa la PDE, se inhibe la liberación de calcio del RE. La PDE media esto mediante la inhibición de la PKG, que posteriormente provoca la inhibición de la liberación de calcio. [7]
La distinción binaria entre vías de señalización Wnt canónicas y no canónicas ha sido objeto de escrutinio y se ha propuesto una vía Wnt integrada y convergente. [36] Se encontró alguna evidencia de esto para un ligando Wnt (Wnt5A). [37] En líneas celulares de mamíferos se describió evidencia de una vía de señalización Wnt convergente que muestra activación integrada de la señalización Wnt/Ca2+ y Wnt/β-catenina, para múltiples ligandos Wnt. [38]
La señalización Wnt también regula otras vías de señalización que no se han dilucidado tan ampliamente. Una de esas vías incluye la interacción entre Wnt y GSK3. Durante el crecimiento celular, Wnt puede inhibir GSK3 para activar mTOR en ausencia de β-catenina. Sin embargo, Wnt también puede servir como regulador negativo de mTOR mediante la activación del supresor de tumores TSC2 , que se regula positivamente mediante la interacción de Dsh y GSK3. [39] Durante la miogénesis , Wnt utiliza PA y CREB para activar los genes MyoD y Myf5 . [40] Wnt también actúa en conjunto con Ryk y Src para permitir la regulación de la repulsión neuronal durante la guía axonal . Wnt regula la gastrulación cuando CK1 actúa como inhibidor de Rap1-ATPasa para modular el citoesqueleto durante la gastrulación. Se logra una mayor regulación de la gastrulación cuando Wnt usa ROR2 junto con la vía CDC42 y JNK para regular la expresión de PAPC . Dsh también puede interactuar con aPKC, Pa3, Par6 y LGl para controlar la polaridad celular y el desarrollo del citoesqueleto de microtúbulos . Si bien estas vías se superponen con componentes asociados con la señalización de PCP y Wnt/Calcio, se consideran vías distintas porque producen respuestas diferentes. [7]
Para garantizar un funcionamiento adecuado, la señalización Wnt se regula constantemente en varios puntos a lo largo de sus vías de señalización. [41] Por ejemplo, las proteínas Wnt están palmitoiladas . La proteína puercoespín media este proceso, lo que significa que ayuda a regular cuándo se secreta el ligando Wnt determinando cuándo está completamente formado. La secreción se controla aún más con proteínas como GPR177 (wntless) y complejos de uniformidad interrumpida como el complejo retrómero . [7] [24]
Tras la secreción , se puede evitar que el ligando llegue a su receptor mediante la unión de proteínas como los estabilizadores Dally y el glipicano 3 (GPC3), que inhiben la difusión. En las células cancerosas, tanto las cadenas de heparán sulfato [42] [43] como la proteína central [44] [45] de GPC3 participan en la regulación de la unión de Wnt y la activación de la proliferación celular. [46] [47] Wnt reconoce una estructura de sulfato de heparán en GPC3, que contiene IdoA2S y GlcNS6S, y la 3-O-sulfatación en GlcNS6S3S mejora la unión de Wnt al glipicano de sulfato de heparán. [48] Se ha identificado que un dominio rico en cisteína en el lóbulo N de GPC3 forma un surco hidrofóbico de unión a Wnt que incluye fenilalanina-41 que interactúa con Wnt. [45] [49] El bloqueo del dominio de unión de Wnt utilizando un nanocuerpo llamado HN3 puede inhibir la activación de Wnt. [45]
En el receptor Fz, la unión de proteínas distintas de Wnt puede antagonizar la señalización. Los antagonistas específicos incluyen Dickkopf (Dkk), factor inhibidor Wnt 1 (WIF-1), [50] [51] proteínas secretadas relacionadas con Frizzled (SFRP), Cerberus , Frzb , Wise , SOST y Naked cuticle . Estos constituyen inhibidores de la señalización Wnt. Sin embargo, otras moléculas también actúan como activadores. Norrin y R-Spondin2 activan la señalización de Wnt en ausencia del ligando Wnt.
Las interacciones entre las vías de señalización Wnt también regulan la señalización Wnt. Como se mencionó anteriormente, la vía Wnt/calcio puede inhibir TCF/β-catenina, previniendo la señalización de la vía Wnt canónica. [7] [24] La prostaglandina E2 (PGE2) es un activador esencial de la vía de señalización canónica Wnt. La interacción de PGE2 con sus receptores E2/E4 estabiliza la β-catenina mediante la fosforilación mediada por AMPc/PKA. La síntesis de PGE2 es necesaria para los procesos mediados por la señalización Wnt, como la regeneración de tejidos y el control de la población de células madre en el pez cebra y el ratón. [5] Curiosamente, las regiones no estructuradas de varias proteínas de gran tamaño intrínsecamente desordenadas desempeñan funciones cruciales en la regulación de la señalización Wnt. [52]
La señalización Wnt juega un papel fundamental en el desarrollo embrionario. Opera tanto en vertebrados como en invertebrados , incluidos humanos, ranas, pez cebra, C. elegans , Drosophila y otros. Se encontró por primera vez en la polaridad del segmento de Drosophila, donde ayuda a establecer las polaridades anterior y posterior. Está implicado en otros procesos de desarrollo . Como sugiere su función en Drosophila , desempeña un papel clave en la formación de los ejes corporales , particularmente en la formación de los ejes anteroposterior y dorsoventral . Participa en la inducción de la diferenciación celular para impulsar la formación de órganos importantes como los pulmones y los ovarios . Wnt asegura además el desarrollo de estos tejidos mediante la regulación adecuada de la proliferación y migración celular . Las funciones de señalización de Wnt se pueden dividir en patrones de ejes, especificación del destino celular, proliferación celular y migración celular. [53]
En las primeras etapas del desarrollo embrionario, la formación de los ejes corporales primarios es un paso crucial para establecer el plan corporal general del organismo. Los ejes incluyen el eje anteroposterior, el eje dorsoventral y el eje derecha-izquierda. La señalización Wnt está implicada en la formación de los ejes anteroposterior y dorsoventral (DV). La actividad de señalización de Wnt en el desarrollo anteroposterior se puede observar en mamíferos, peces y ranas. En los mamíferos, la raya primitiva y otros tejidos circundantes producen los compuestos morfogénicos Wnts, BMP , FGF , Nodal y ácido retinoico para establecer la región posterior durante la gástrula tardía . Estas proteínas forman gradientes de concentración. Las áreas de mayor concentración establecen la región posterior mientras que las áreas de menor concentración indican la región anterior. En peces y ranas, la β-catenina producida por la señalización Wnt canónica provoca la formación de centros organizadores que, junto con las BMP, provocan la formación posterior. La participación de Wnt en la formación del eje DV se puede observar en la actividad de formación del organizador de Spemann , que establece la región dorsal. La señalización canónica de Wnt de la producción de β-catenina induce la formación de este organizador mediante la activación de los genes gemelo y siamois. [36] [53] De manera similar, en la gastrulación aviar, las células de la hoz de Koller expresan diferentes genes marcadores mesodérmicos que permiten el movimiento diferencial de las células durante la formación de la línea primitiva. La señalización Wnt activada por los FGF es responsable de este movimiento. [54] [55]
La señalización Wnt también participa en la formación de ejes de partes del cuerpo y sistemas de órganos específicos más adelante en el desarrollo. En los vertebrados, los gradientes de señalización morfogenética de Sonic hedgehog (Shh) y Wnt establecen el eje dorsoventral del sistema nervioso central durante el patrón axial del tubo neural . La señalización alta de Wnt establece la región dorsal, mientras que la señalización alta de Shh indica la región ventral. [56] Wnt participa en la formación de DV del sistema nervioso central a través de su participación en la guía del axón . Las proteínas Wnt guían los axones de la médula espinal en dirección anteroposterior. [57] Wnt también participa en la formación del eje DV de la extremidad. Específicamente, Wnt7a ayuda a producir el patrón dorsal de la extremidad en desarrollo. [36] [53]
En el modelo de desarrollo de ondas de diferenciación embrionaria , Wnt desempeña un papel fundamental como parte de un complejo de señalización en células competentes listas para diferenciarse. Wnt reacciona a la actividad del citoesqueleto, estabilizando el cambio inicial creado por una onda pasajera de contracción o expansión y simultáneamente envía señales al núcleo mediante el uso de sus diferentes vías de señalización sobre en qué onda ha participado la célula individual. De este modo, la actividad Wnt se amplifica. Señalización mecánica que se produce durante el desarrollo. [58] [59]
La especificación del destino celular o la diferenciación celular es un proceso en el que las células indiferenciadas pueden convertirse en un tipo de célula más especializada. La señalización Wnt induce la diferenciación de células madre pluripotentes en células progenitoras del mesodermo y del endodermo . [60] Estas células progenitoras se diferencian aún más en tipos de células como los linajes endotelial, cardíaco y de músculo liso vascular. [61] La señalización Wnt induce la formación de sangre a partir de células madre. Específicamente, Wnt3 conduce a células comprometidas en el mesodermo con potencial hematopoyético . [62] Wnt1 antagoniza la diferenciación neural y es un factor importante en la autorrenovación de las células madre neurales. Esto permite la regeneración de las células del sistema nervioso, lo que es una prueba más de su papel en la promoción de la proliferación de células madre neurales. [60] La señalización Wnt participa en la determinación de las células germinales , la especificación del tejido intestinal , el desarrollo de los folículos pilosos , el desarrollo del tejido pulmonar, la diferenciación de las células de la cresta neural del tronco, el desarrollo de las nefronas , el desarrollo de los ovarios y la determinación del sexo . [53] La señalización de Wnt también antagoniza la formación del corazón, y se demostró que la inhibición de Wnt es un inductor crítico del tejido cardíaco durante el desarrollo, [63] [64] [65] y los inhibidores de Wnt de molécula pequeña se utilizan habitualmente para producir cardiomiocitos a partir de células madre pluripotentes. . [66] [67]
Para tener la diferenciación masiva de células necesaria para formar los tejidos celulares específicos de diferentes organismos, debe tener lugar la proliferación y el crecimiento de células madre embrionarias . Este proceso está mediado por la señalización Wnt canónica, que aumenta la β-catenina nuclear y citoplasmática. El aumento de β-catenina puede iniciar la activación transcripcional de proteínas como la ciclina D1 y c-myc , que controlan la transición de la fase G1 a S en el ciclo celular . La entrada en la fase S provoca la replicación del ADN y, en última instancia, la mitosis , que son responsables de la proliferación celular. [68] Este aumento de la proliferación está directamente relacionado con la diferenciación celular porque a medida que las células madre proliferan, también se diferencian. Esto permite el crecimiento general y el desarrollo de sistemas de tejidos específicos durante el desarrollo embrionario. Esto es evidente en sistemas como el circulatorio, donde Wnt3a conduce a la proliferación y expansión de las células madre hematopoyéticas necesarias para la formación de glóbulos rojos. [69]
La bioquímica de las células madre cancerosas es sutilmente diferente de la de otras células tumorales. Estas células llamadas adictas a Wnt secuestran y dependen de la estimulación constante de la vía Wnt para promover su crecimiento, supervivencia y migración descontrolados. En el cáncer , la señalización Wnt puede volverse independiente de los estímulos regulares, a través de mutaciones en oncogenes posteriores y genes supresores de tumores que se activan permanentemente aunque el receptor normal no haya recibido una señal. La β-catenina se une a factores de transcripción como la proteína TCF4 y, en combinación, las moléculas activan los genes necesarios. LF3 inhibe fuertemente esta unión in vitro, en líneas celulares y reduce el crecimiento tumoral en modelos de ratón. Impidió la replicación y redujo su capacidad de migrar, todo ello sin afectar a las células sanas. No quedaron células madre cancerosas después del tratamiento. El descubrimiento fue producto del " diseño racional de fármacos ", que involucra tecnologías AlphaScreens y ELISA. [70]
La migración celular durante el desarrollo embrionario permite el establecimiento de los ejes del cuerpo, la formación de tejidos, la inducción de extremidades y varios otros procesos. La señalización Wnt ayuda a mediar en este proceso, particularmente durante la extensión convergente. Se requiere la señalización tanto de la vía Wnt PCP como de la vía Wnt canónica para una extensión convergente adecuada durante la gastrulación. La extensión convergente está regulada además por la vía Wnt/calcio, que bloquea la extensión convergente cuando se activa. La señalización Wnt también induce la migración celular en etapas posteriores del desarrollo mediante el control del comportamiento migratorio de neuroblastos , células de la cresta neural , miocitos y células traqueales. [71]
La señalización Wnt está involucrada en otro proceso de migración clave conocido como transición epitelial-mesenquimatosa (EMT). Este proceso permite que las células epiteliales se transformen en células mesenquimales de modo que ya no se mantengan en su lugar en la laminina . Implica la regulación negativa de la cadherina para que las células puedan desprenderse de la laminina y migrar. La señalización Wnt es un inductor de EMT, particularmente en el desarrollo mamario. [72]

La insulina es una hormona peptídica implicada en la homeostasis de la glucosa en ciertos organismos. Específicamente, conduce a una regulación positiva de los transportadores de glucosa en la membrana celular para aumentar la absorción de glucosa del torrente sanguíneo . Este proceso está mediado parcialmente por la activación de la señalización de Wnt/β-catenina, que puede aumentar la sensibilidad a la insulina de una célula. En particular, Wnt10b es una proteína Wnt que aumenta esta sensibilidad en las células del músculo esquelético. [73]
Desde su descubrimiento inicial, la señalización Wnt ha tenido una asociación con el cáncer . Cuando se descubrió Wnt1, se identificó por primera vez como un protooncogén en un modelo de ratón para el cáncer de mama. El hecho de que Wnt1 sea un homólogo de Wg muestra que participa en el desarrollo embrionario, que a menudo exige una rápida división y migración celular. La mala regulación de estos procesos puede conducir al desarrollo de tumores a través de una proliferación celular excesiva. [3]
La actividad de la vía canónica Wnt está implicada en el desarrollo de tumores de mama benignos y malignos . También se ha documentado bien el papel de la vía Wnt en la quimiorresistencia tumoral, así como su papel en el mantenimiento de una subpoblación distinta de células iniciadoras de cáncer. [74] Su presencia se revela por niveles elevados de β-catenina en el núcleo y/o citoplasma, que pueden detectarse con tinción inmunohistoquímica y transferencia Western . El aumento de la expresión de β-catenina se correlaciona con un mal pronóstico en pacientes con cáncer de mama. Esta acumulación puede deberse a factores como mutaciones en la β-catenina, deficiencias en el complejo de destrucción de la β-catenina, más frecuentemente por mutaciones en regiones estructuralmente desordenadas de APC , sobreexpresión de ligandos Wnt, pérdida de inhibidores y/o disminución de la actividad reguladora. vías (como la vía Wnt/calcio). [52] [75] [76] Los tumores de mama pueden metastatizar debido a la participación de Wnt en la EMT. La investigación que analizó la metástasis del cáncer de mama de tipo basal en los pulmones demostró que la represión de la señalización de Wnt/β-catenina puede prevenir la EMT, que puede inhibir la metástasis. [77]
La señalización Wnt se ha implicado en el desarrollo de otros cánceres, así como en la fibromatosis desmoide . [78] Los cambios en la expresión de CTNNB1 , que es el gen que codifica la β-catenina, se pueden medir en cánceres de mama, colorrectal , melanoma , próstata , pulmón y otros cánceres. Se observó una mayor expresión de proteínas ligando Wnt como Wnt1, Wnt2 y Wnt7A en el desarrollo de glioblastoma , cáncer de esófago y cáncer de ovario , respectivamente. Otras proteínas que causan múltiples tipos de cáncer en ausencia de un funcionamiento adecuado incluyen ROR1, ROR2, SFRP4 , Wnt5A, WIF1 y las de la familia TCF/LEF. [79] La señalización Wnt está además implicada en la patogénesis de la metástasis ósea del cáncer de mama y de próstata, con estudios que sugieren estados discretos de encendido y apagado. Wnt está regulado negativamente durante la etapa de latencia por DKK1 autocrino para evitar la vigilancia inmune, [80] así como durante las etapas de diseminación por Dact1 intracelular. [81] Mientras tanto, Wnt se activa durante la fase de crecimiento inicial por la E-selectina . [82]
El vínculo entre PGE2 y Wnt sugiere que un aumento de PGE2 relacionado con la inflamación crónica puede conducir a la activación de la vía Wnt en diferentes tejidos, lo que resulta en carcinogénesis . [5]
La diabetes mellitus tipo 2 es una enfermedad común que provoca una reducción de la secreción de insulina y un aumento de la resistencia a la insulina en la periferia. Provoca un aumento de los niveles de glucosa en sangre o hiperglucemia , que puede ser mortal si no se trata. Dado que la señalización Wnt está implicada en la sensibilidad a la insulina, podría estar implicado un mal funcionamiento de su vía. La sobreexpresión de Wnt5b, por ejemplo, puede aumentar la susceptibilidad debido a su papel en la adipogénesis , ya que la obesidad y la diabetes tipo II tienen una alta comorbilidad . [83] La señalización Wnt es un fuerte activador de la biogénesis mitocondrial . Esto conduce a una mayor producción de especies reactivas de oxígeno (ROS) que se sabe que causan daño celular y al ADN. [84] Este daño inducido por ROS es significativo porque puede causar resistencia aguda a la insulina hepática o resistencia a la insulina inducida por lesiones. [85] Las mutaciones en los factores de transcripción asociados a la señalización Wnt, como TCF7L2 , están relacionadas con una mayor susceptibilidad. [86]
{{cite book}}: |website=ignorado ( ayuda )