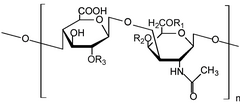
El sulfato de condroitina es un glicosaminoglicano sulfatado (GAG) [1] compuesto por una cadena de azúcares alternados ( N-acetilgalactosamina y ácido glucurónico ). Generalmente se encuentra unido a proteínas como parte de un proteoglicano . [1] Una cadena de condroitina puede tener más de 100 azúcares individuales, cada uno de los cuales puede estar sulfatado en posiciones y cantidades variables. El sulfato de condroitina es un componente estructural importante del cartílago , [2] y proporciona gran parte de su resistencia a la compresión . [3] Junto con la glucosamina , el sulfato de condroitina se ha convertido en un suplemento dietético ampliamente utilizado para el tratamiento de la osteoartritis , aunque grandes ensayos clínicos no lograron demostrar ningún beneficio sintomático de la condroitina.
La condroitina se utiliza en suplementos dietéticos como medicina alternativa para tratar la osteoartritis . [4] También está aprobada y regulada como fármaco sintomático de acción lenta para esta enfermedad (SYSADOA) en Europa y algunos otros países. Se vende comúnmente junto con la glucosamina . [5] Una revisión Cochrane de ensayos clínicos de 2015 encontró que la mayoría eran de baja calidad, pero que había alguna evidencia de mejoría a corto plazo del dolor y pocos efectos secundarios; no parece mejorar ni mantener la salud de las articulaciones afectadas . [5]
La condroitina, junto con la glucosamina de uso común, no debe utilizarse para tratar a personas con osteoartritis sintomática de la rodilla, ya que la evidencia muestra que estos tratamientos no brindan alivio para esa afección. [6]
La condroitina ha demostrado ser prometedora en el tratamiento de la enfermedad de las arterias coronarias . En un estudio doble ciego controlado con placebo de 6 años de duración en el que participaron 60 sujetos de prueba publicado en 1973, el grupo tratado con sulfato de condroitina mostró una reducción del 350% en los ataques cardíacos fatales en comparación con el grupo de control. Al analizar los datos de eventos cardiovasculares no fatales, el grupo de control experimentó ataques cardíacos no fatales a una tasa del 16%, mientras que los del grupo tratado con sulfato de condroitina tuvieron una tasa del 0%. [7]
El sulfato de condroitina se utiliza como suplemento dietético para el tratamiento de la diabetes. [8] Presenta propiedades antiinflamatorias, lo que lo convierte en una alternativa potencial al cortisol para el tratamiento de la enteritis. [9] [10]
Los estudios clínicos no han identificado efectos secundarios significativos ni sobredosis de sulfato de condroitina, lo que sugiere su seguridad a largo plazo. [11] En 2003, el comité del Grupo de Trabajo de la Liga Europea contra el Reumatismo (EULAR) clasificó el nivel de toxicidad del sulfato de condroitina en 6 en una escala de 0 a 100. [12]
El sulfato de condroitina no es metabolizado por el citocromo P450 . [13]
El efecto del sulfato de condroitina en personas con osteoartritis es probablemente el resultado de una serie de reacciones que incluyen su actividad antiinflamatoria, la estimulación de la síntesis de proteoglicanos y ácido hialurónico , y la disminución de la actividad catabólica de los condrocitos, inhibiendo la síntesis de enzimas proteolíticas , óxido nítrico y otras sustancias que contribuyen a dañar la matriz del cartílago y causar la muerte de los condrocitos articulares. Una revisión reciente resume los datos de informes relevantes que describen la base bioquímica del efecto del sulfato de condroitina sobre los tejidos articulares de la osteoartritis. [14]
Estudios farmacocinéticos realizados en humanos y animales de experimentación después de la administración oral de sulfato de condroitina revelaron que puede absorberse por vía oral. El sulfato de condroitina muestra una cinética de primer orden hasta dosis únicas de 3000 mg. [15] [16] [17] [18] Dosis múltiples de 800 mg en personas con osteoartritis no alteran la cinética del sulfato de condroitina. La biodisponibilidad del sulfato de condroitina varía del 15% al 24% de la dosis administrada por vía oral. Más particularmente, en el tejido articular, Ronca et al. [19] informaron que el sulfato de condroitina no se absorbe rápidamente en el tracto gastrointestinal y se encuentra un alto contenido de sulfato de condroitina marcado en el líquido sinovial y el cartílago.
Las cadenas de sulfato de condroitina son polisacáridos no ramificados de longitud variable que contienen dos monosacáridos alternados: ácido D -glucurónico (GlcA) y N -acetil- D -galactosamina (GalNAc). Algunos de estos residuos de GlcA pueden epimerizarse en ácido L-idurónico ( IdoA), momento en el que el glicosaminoglicano resultante se denomina dermatán sulfato , anteriormente denominado condroitín sulfato B.
El sulfato de condroitina se obtiene a partir de productos naturales, con una alta variabilidad en términos de longitud de cadena y patrón de sulfatación. La variabilidad en la composición del sulfato de condroitina se extiende a su origen, lo que permite diferenciar entre el sulfato de condroitina de fuentes terrestres y marinas. Una forma de ver esta diferencia es en términos de la proporción de unidades de disacáridos: el sulfato de condroitina de animales terrestres está compuesto casi exclusivamente de unidades no sulfatadas (O) y monosulfatadas (A y C), mientras que en las especies marinas la proporción de unidades disulfatadas (D, E y B) es mayor. Además, las cadenas de sulfato de condroitina marina tienden a ser más largas, con un peso molecular de hasta 70 kDa en el sulfato de condroitina de tiburón, mientras que en los animales terrestres el peso molecular suele ser inferior a 45 kDa. [20] [21]
Las cadenas de sulfato de condroitina están unidas a grupos hidroxilo en los residuos de serina de ciertas proteínas. No se sabe exactamente cómo se seleccionan las proteínas para la unión de los glicosaminoglicanos. Las serinas glicosiladas suelen ir seguidas de una glicina y tienen residuos ácidos vecinos, pero este motivo no siempre predice la glicosilación.
La unión de la cadena GAG comienza con cuatro monosacáridos en un patrón fijo: Xyl – Gal – Gal – GlcA. Cada azúcar se une mediante una enzima específica, lo que permite múltiples niveles de control sobre la síntesis de GAG. La xilosa comienza a unirse a las proteínas en el retículo endoplasmático , mientras que el resto de los azúcares se unen en el aparato de Golgi . [22]
El sulfato de condroitina es altamente soluble en agua . [23]
El sulfato de condroitina se aisló originalmente mucho antes de que se caracterizara su estructura, lo que con el tiempo provocó cambios en la terminología. [24] Los primeros investigadores identificaron diferentes fracciones de la sustancia con letras.
"Sulfato de condroitina B" es un nombre antiguo para el sulfato de dermatán , y ya no se clasifica como una forma de sulfato de condroitina. [25]
La condroitina , sin el "sulfato", se ha utilizado para describir una fracción con poca o ninguna sulfatación. [26] Sin embargo, esta distinción no es utilizada por todos.
Aunque el nombre "sulfato de condroitina" sugiere una sal con un contraión sulfato , este no es el caso, ya que el sulfato está unido covalentemente al azúcar. En cambio, dado que la molécula tiene múltiples cargas negativas a pH fisiológico, hay un catión presente en las sales de sulfato de condroitina. Las preparaciones comerciales de sulfato de condroitina suelen ser la sal de sodio. Barnhill et al. han sugerido que todas estas preparaciones de sulfato de condroitina se denominen "condroitina sódica" independientemente de su estado de sulfatación. [27]
En 2008, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) identificó el "sulfato de condroitina sobresulfatado" como un contaminante en la heparina originaria de China . [28] [29] [30]
En 2004, se presentó una petición a la FDA para que se etiquetara un suplemento dietético de sulfato de condroitina como reductor del riesgo de osteoartritis, deterioro del cartílago y dolor, sensibilidad e hinchazón de las articulaciones relacionados con la osteoartritis. La FDA rechazó la solicitud, afirmando que los experimentos realizados por la empresa no demostraban suficientemente la eficacia de la afirmación. Entre otros comentarios, la FDA señaló el diseño experimental deficiente de algunos ensayos. [31]
En 2007, Reichenbach et al. utilizaron métodos explícitos para realizar e informar una revisión sistemática de 20 ensayos y concluyeron que "los ensayos a gran escala y metodológicamente sólidos indican que el beneficio sintomático de la condroitina es mínimo o inexistente. Por lo tanto, se debe desaconsejar el uso de condroitina en la práctica clínica habitual". Por el contrario, y también en 2007, Bruyere et al. concluyeron que "existen pruebas convincentes de que el sulfato de glucosamina y el sulfato de condroitina pueden interferir con la progresión de la artrosis".
En 2015, el ensayo más grande realizado con el producto fue el Glucosamine and Chondroitin Arthritis Intervention Trial (GAIT), un ensayo clínico aleatorizado, multicéntrico y doble ciego patrocinado por los Institutos Nacionales de Salud de EE. UU. en 1583 personas con osteoartritis de rodilla, que se publicó en el New England Journal of Medicine en 2006. [5] [32] Los sujetos fueron asignados aleatoriamente a uno de cinco tratamientos administrados por vía oral: dos cápsulas de 250 mg de clorhidrato de glucosamina tres veces al día, dos cápsulas de 200 mg de sulfato de condroitina tres veces al día, dos cápsulas de 250 mg de clorhidrato de glucosamina más 200 mg de sulfato de condroitina tres veces al día, 200 mg de celecoxib al día o placebo. El tratamiento se administró durante 24 semanas. No mostró diferencias con respecto al placebo. [5]
Sawitzke A, et al. 2010 evaluaron la eficacia y seguridad de la glucosamina y el sulfato de condroitina, solos o en combinación, así como celecoxib y placebo en la osteoartritis dolorosa de rodilla durante 2 años como continuación del ensayo GAIT. Este fue un estudio doble ciego, controlado con placebo de 24 meses, en el que participaron 662 personas con osteoartritis de rodilla que cumplían los criterios radiográficos (cambios de grado 2 o 3 de Kellgren/Lawrence y ancho inicial del espacio articular de al menos 2 mm). Este subconjunto continuó recibiendo su tratamiento aleatorizado (glucosamina 500 mg tres veces al día, sulfato de condroitina 400 mg tres veces al día, la combinación de glucosamina y sulfato de condroitina, celecoxib 200 mg al día o placebo) durante 24 meses. El resultado primario fue una reducción del 20% del dolor durante 24 meses, medido mediante el índice de osteoartritis de la Universidad Western Ontario y McMaster (WOMAC). Los resultados secundarios incluyeron una respuesta de la Sociedad Internacional de Investigación de Reumatología/Osteoartritis y un cambio desde el inicio en el dolor y la función de WOMAC. [5] [33] Durante 2 años, ninguno de los tratamientos (ni siquiera el control positivo celecoxib) logró una diferencia clínicamente importante en el dolor o la función de WOMAC en comparación con placebo. Las reacciones adversas fueron similares entre los grupos de tratamiento y los eventos adversos graves fueron poco frecuentes para todos los tratamientos. [33]
Un estudio de 2021 mostró una reducción notable (alrededor del 40 %) del riesgo de infarto agudo de miocardio en los usuarios actuales de sulfato de condroitina en los subgrupos cardiovasculares de alto riesgo. [34]
La mayor parte de la condroitina parece estar hecha de extractos de tejidos cartilaginosos de vaca y cerdo ( tráquea de vaca y oreja y nariz de cerdo), pero también se utilizan otras fuentes como el cartílago de tiburón , pescado y aves. Dado que la condroitina no es una sustancia uniforme y está presente de forma natural en una amplia variedad de formas, la composición precisa de cada suplemento variará. [27] De hecho, aunque muchas empresas de suplementos alimenticios producen sus productos de conformidad con las Buenas Prácticas de Fabricación (BPF) de procesamiento de alimentos para humanos , la mayoría de ellas no producen sus productos de conformidad con las regulaciones BPF para productos farmacéuticos, lo que da como resultado productos que no cumplen con los requisitos farmacéuticos. [35]
Si bien es un medicamento de venta con receta o sin receta en 22 países, la condroitina está regulada en los EE. UU. como un suplemento dietético [36] por la Administración de Alimentos y Medicamentos . En Europa, las formulaciones de sulfato de condroitina están aprobadas como medicamentos con eficacia y seguridad evidenciadas demostradas por ensayos clínicos en personas con osteoartritis. [37] Adebowale et al. informaron en 2000 que de 32 suplementos de condroitina que analizaron, solo 5 estaban etiquetados correctamente y más de la mitad contenían menos del 40% de la cantidad etiquetada. [38] Con la introducción de las regulaciones GMP para suplementos dietéticos en 2008, las preparaciones de sulfato de condroitina están sujetas en los EE. UU. a estándares de etiquetado obligatorios, así como a requisitos de prueba de identidad, pureza, concentración y composición. [ cita requerida ] Los estándares de prueba de la Farmacopea de los Estados Unidos (USP) para la identificación y cuantificación de la condroitina están bien establecidos. [ cita requerida ]
No existen regulaciones de la FDA sobre el sulfato de condroitina como aditivo alimentario, ya que está reconocido por la FDA como un componente de los alimentos y es "generalmente reconocido como seguro". [31] Sin embargo, una aplicación propuesta del suplemento dietético de sulfato de condroitina como un medio para prevenir la degeneración de las articulaciones fue examinada minuciosamente por la FDA, que declaró:
"En el caso de los alimentos convencionales, esta evaluación implica considerar si el ingrediente que constituye la fuente de la sustancia está generalmente reconocido como seguro (GRAS), aprobado como aditivo alimentario o autorizado por una sanción previa emitida por la FDA (véase 21 CFR 101.70(f)). Sin embargo, los ingredientes dietéticos de los suplementos dietéticos no están sujetos a las disposiciones sobre aditivos alimentarios de la ley (véase la sección 201(s)(6) de la Ley (21 USC § 321(s)(6)). En cambio, están sujetos a las disposiciones sobre adulteración de la sección 402 de la Ley (21 USC 342) y, si corresponde, a las nuevas disposiciones sobre ingredientes dietéticos de la sección 413 de la Ley (21 USC 350b), que se refieren a los ingredientes dietéticos que no se comercializaron en los Estados Unidos antes del 15 de octubre de 1994".
— Carta sobre la relación entre el consumo de glucosamina y/o sulfato de condroitina y un menor riesgo de: osteoartritis; dolor articular relacionado con la osteoartritis, sensibilidad articular e hinchazón articular; degeneración articular; y deterioro del cartílago
En la misma carta, la FDA determinó que los estudios realizados sobre el sulfato de condroitina en forma de suplemento dietético no eran suficientes para fundamentar las afirmaciones de que es eficaz para prevenir el deterioro de las articulaciones, y denegó la solicitud de que se le permitiera etiquetar el suplemento como tal. También denegó la solicitud de comercializarlo como seguro, dado que no se habían realizado ensayos clínicos en humanos, alegando que los estudios en animales no son suficientes para la aprobación de un suplemento dietético. [31]
La condroitina y la glucosamina también se utilizan en medicina veterinaria para la osteoartritis. [39] [40] [41]
{{cite journal}}: CS1 maint: nombres numéricos: lista de autores ( enlace ){{cite journal}}: CS1 maint: nombres numéricos: lista de autores ( enlace )