El metabolismo del hierro humano es el conjunto de reacciones químicas que mantienen la homeostasis del hierro humano a nivel sistémico y celular. El hierro es necesario para el cuerpo y potencialmente tóxico. Controlar los niveles de hierro en el cuerpo es una parte de vital importancia en muchos aspectos de la salud y las enfermedades humanas. Los hematólogos se han interesado especialmente en el metabolismo sistémico del hierro , porque el hierro es esencial para los glóbulos rojos , donde se encuentra la mayor parte del hierro del cuerpo humano. Comprender el metabolismo del hierro también es importante para comprender las enfermedades por sobrecarga de hierro , como la hemocromatosis hereditaria , y la deficiencia de hierro , como la anemia por deficiencia de hierro .

El hierro es un bioelemento esencial para la mayoría de formas de vida, desde bacterias hasta mamíferos . Su importancia radica en su capacidad para mediar en la transferencia de electrones. En el estado ferroso (Fe 2+ ), el hierro actúa como donador de electrones , mientras que en el estado férrico (Fe 3+ ) actúa como aceptor . Así, el hierro juega un papel vital en la catálisis de reacciones enzimáticas que implican transferencia de electrones (reducción y oxidación, redox ). Las proteínas pueden contener hierro como parte de diferentes cofactores , como grupos hierro-azufre (Fe-S) y grupos hemo , ambos ensamblados en las mitocondrias .
Las células humanas necesitan hierro para obtener energía en forma de ATP a partir de un proceso de varios pasos conocido como respiración celular, más específicamente de la fosforilación oxidativa en las crestas mitocondriales . El hierro está presente en el grupo hierro-azufre y en los grupos hemo de las proteínas de la cadena de transporte de electrones que generan un gradiente de protones que permite a la ATP sintasa sintetizar ATP ( quimiosmosis ).
Los grupos hemo forman parte de la hemoglobina , una proteína que se encuentra en los glóbulos rojos y que sirve para transportar oxígeno desde los pulmones a otros tejidos. Los grupos hemo también están presentes en la mioglobina para almacenar y difundir oxígeno en las células musculares.
El cuerpo humano necesita hierro para el transporte de oxígeno. El oxígeno (O 2 ) es necesario para el funcionamiento y la supervivencia de casi todos los tipos de células. El oxígeno se transporta desde los pulmones al resto del cuerpo unido al grupo hemo de la hemoglobina en los glóbulos rojos. En las células de los músculos, el hierro une el oxígeno a la mioglobina , que regula su liberación.
El hierro también es potencialmente tóxico. Su capacidad para donar y aceptar electrones significa que puede catalizar la conversión del peróxido de hidrógeno en radicales libres . Los radicales libres pueden causar daño a una amplia variedad de estructuras celulares y, en última instancia, matar la célula. [1]
El hierro unido a proteínas o cofactores como el hemo es seguro. Además, prácticamente no hay iones de hierro verdaderamente libres en la célula, ya que forman fácilmente complejos con moléculas orgánicas. Sin embargo, parte del hierro intracelular está unido a complejos de baja afinidad y se denomina hierro lábil o hierro "libre". El hierro en tales complejos puede causar daños como se describe anteriormente. [2]
Para prevenir ese tipo de daño, todas las formas de vida que usan hierro unen los átomos de hierro a las proteínas . Esta unión permite que las células se beneficien del hierro y al mismo tiempo limita su capacidad de causar daño. [1] [3] Las concentraciones típicas de hierro lábil intracelular en las bacterias son de 10 a 20 micromolar, [4] aunque pueden ser 10 veces mayores en un ambiente anaeróbico, [5] donde los radicales libres y las especies reactivas de oxígeno son más escasos. En las células de mamíferos, las concentraciones de hierro lábil intracelular suelen ser inferiores a 1 micromolar, menos del 5 por ciento del hierro celular total. [2]

En respuesta a una infección bacteriana sistémica, el sistema inmunológico inicia un proceso conocido como "retención de hierro". Para que las bacterias sobrevivan, deben obtener hierro de su entorno. Las bacterias que causan enfermedades hacen esto de muchas maneras, incluida la liberación de moléculas que se unen al hierro llamadas sideróforos y luego las reabsorben para recuperar el hierro, o eliminan el hierro de la hemoglobina y la transferrina . Cuanto más tienen que trabajar las bacterias para obtener hierro, mayor es el precio metabólico que deben pagar. Eso significa que las bacterias privadas de hierro se reproducen más lentamente. Por tanto, el control de los niveles de hierro parece ser una defensa importante contra muchas infecciones bacterianas. Ciertas especies de bacterias han desarrollado estrategias para eludir esa defensa, las bacterias que causan la tuberculosis pueden residir dentro de los macrófagos , que presentan un ambiente rico en hierro y Borrelia burgdorferi usa manganeso en lugar de hierro. Las personas con mayores cantidades de hierro, como, por ejemplo, en la hemocromatosis, son más susceptibles a algunas infecciones bacterianas. [6]
Aunque este mecanismo es una respuesta elegante a una infección bacteriana a corto plazo, puede causar problemas cuando dura tanto que el cuerpo se ve privado del hierro necesario para la producción de glóbulos rojos. Las citocinas inflamatorias estimulan al hígado para que produzca la proteína hepcidina , reguladora del metabolismo del hierro , que reduce el hierro disponible. Si los niveles de hepcidina aumentan debido a fuentes de inflamación no bacterianas, como infecciones virales, cáncer, enfermedades autoinmunes u otras enfermedades crónicas, entonces puede producirse anemia por enfermedad crónica . En este caso, la retención de hierro en realidad perjudica la salud al impedir la fabricación de suficientes glóbulos rojos que contienen hemoglobina. [3]

La mayoría de las personas bien alimentadas en los países industrializados tienen de 4 a 5 gramos de hierro en el cuerpo (~38 mg de hierro/kg de peso corporal para las mujeres y ~50 mg de hierro/kg de cuerpo para los hombres). [7] De esto, aproximadamente2,5 g están contenidos en la hemoglobina necesaria para transportar oxígeno a través de la sangre (alrededor de 0,5 mg de hierro por ml de sangre), [8] y la mayor parte del resto (aproximadamente 2 gramos en hombres adultos y algo menos en mujeres en edad fértil). ) está contenido en complejos de ferritina que están presentes en todas las células, pero con mayor frecuencia en la médula ósea, el hígado y el bazo . Las reservas hepáticas de ferritina son la principal fuente fisiológica de reserva de hierro en el cuerpo. Las reservas de hierro en los países industrializados tienden a ser menores en niños y mujeres en edad fértil que en hombres y ancianos. Las mujeres que deben utilizar sus reservas para compensar la pérdida de hierro durante la menstruación , el embarazo o la lactancia tienen reservas corporales distintas de hemoglobina más bajas, que pueden consistir en500 mg , o incluso menos.
Del contenido total de hierro del cuerpo, aproximadamente400 mg se dedican a proteínas celulares que utilizan el hierro para procesos celulares importantes como almacenar oxígeno (mioglobina) o realizar reacciones redox que producen energía ( citocromos ). Una cantidad relativamente pequeña (3 a 4 mg) circula por el plasma , unida a la transferrina. [9] Debido a su toxicidad, el hierro soluble libre se mantiene en bajas concentraciones en el cuerpo.
La deficiencia de hierro afecta primero el almacenamiento de hierro en el cuerpo, y se cree que el agotamiento de estas reservas es relativamente asintomático, aunque se han asociado algunos síntomas vagos y no específicos . Dado que el hierro se necesita principalmente para la hemoglobina, la anemia ferropénica es la principal manifestación clínica de la deficiencia de hierro. Las personas con deficiencia de hierro sufrirán o morirán a causa de daños en los órganos mucho antes de que sus células se queden sin el hierro necesario para procesos intracelulares como el transporte de electrones.
Los macrófagos del sistema reticuloendotelial almacenan hierro como parte del proceso de descomposición y procesamiento de la hemoglobina de los glóbulos rojos fagocitados. El hierro también se almacena como un pigmento llamado hemosiderina , que es un depósito mal definido de proteína y hierro, creado por macrófagos donde hay exceso de hierro, ya sea local o sistémicamente, por ejemplo, entre personas con sobrecarga de hierro debido a la destrucción frecuente de las células sanguíneas y las transfusiones necesarias que su condición requiere. Si se corrige la sobrecarga sistémica de hierro, con el tiempo los macrófagos reabsorben lentamente la hemosiderina.
La homeostasis del hierro humano está regulada en dos niveles diferentes. Los niveles sistémicos de hierro se equilibran mediante la absorción controlada del hierro de la dieta por los enterocitos , las células que recubren el interior de los intestinos , y la pérdida incontrolada de hierro por descamación epitelial, sudor, lesiones y pérdida de sangre. Además, el hierro sistémico se recicla continuamente. Los niveles de hierro celular están controlados de manera diferente por diferentes tipos de células debido a la expresión de proteínas particulares reguladoras y de transporte de hierro.

La absorción del hierro de la dieta es un proceso variable y dinámico. La cantidad de hierro absorbido en comparación con la cantidad ingerida suele ser baja, pero puede oscilar entre el 5% y el 35%, según las circunstancias y el tipo de hierro. La eficiencia con la que se absorbe el hierro varía según la fuente. Generalmente, las formas de hierro mejor absorbidas provienen de productos animales. La absorción del hierro dietético en forma de sal de hierro (como en la mayoría de los suplementos) varía algo según las necesidades de hierro del cuerpo y suele oscilar entre el 10% y el 20% de la ingesta de hierro. La absorción de hierro de productos animales y algunos productos vegetales se realiza en forma de hierro hemo y es más eficiente, permitiendo una absorción del 15% al 35% de la ingesta. El hierro hemo en los animales proviene de la sangre y de las proteínas que contienen hemo en la carne y las mitocondrias, mientras que en las plantas, el hierro hemo está presente en las mitocondrias de todas las células que utilizan oxígeno para la respiración.
Como la mayoría de los nutrientes minerales, la mayor parte del hierro absorbido de los alimentos o suplementos digeridos es absorbido en el duodeno por los enterocitos del revestimiento duodenal. Estas células tienen moléculas especiales que les permiten transportar hierro al cuerpo. Para ser absorbido, el hierro de la dieta puede absorberse como parte de una proteína como la proteína hemo o el hierro debe estar en su forma ferrosa Fe 2+ . Una enzima férrica reductasa en el borde en cepillo de los enterocitos , el citocromo B duodenal ( Dcytb ), reduce el Fe 3+ férrico a Fe 2+ . [10] Una proteína llamada transportador de metales divalentes 1 ( DMT1 ), que puede transportar varios metales divalentes a través de la membrana plasmática y luego transporta hierro a través de la membrana celular del enterocito hacia el interior de la célula. Si el hierro está unido al hemo, la proteína transportadora del hemo 1 (HCP1) lo transporta a través de la membrana apical . [11] Luego, la hemooxigenasa microsomal cataboliza el hemo en biliverdina , liberando Fe 2+ . [12]
Estas células del revestimiento intestinal pueden entonces almacenar el hierro como ferritina , lo que se logra mediante la unión del Fe 2+ a la apoferritina (en cuyo caso el hierro abandonará el cuerpo cuando la célula muere y se elimina en las heces ), o la célula puede liberarlo. ingresa al cuerpo a través del único exportador de hierro conocido en los mamíferos, la ferroportina . La hefestina , una ferroxidasa que puede oxidar Fe 2+ a Fe 3+ y se encuentra principalmente en el intestino delgado, ayuda a la ferroportina a transferir hierro a través del extremo basolateral de las células del intestino. Tras su liberación al torrente sanguíneo, el Fe 3+ se une a la transferrina y circula por los tejidos. Por el contrario, la ferroportina es reprimida postraduccionalmente por la hepcidina , una hormona peptídica de 25 aminoácidos. El cuerpo regula los niveles de hierro regulando cada uno de estos pasos. Por ejemplo, los enterocitos sintetizan más Dcytb, DMT1 y ferroportina en respuesta a la anemia por deficiencia de hierro. [13] La absorción de hierro de la dieta aumenta en presencia de vitamina C y disminuye con el exceso de calcio, zinc o manganeso. [14]
La tasa de absorción de hierro del cuerpo humano parece responder a una variedad de factores interdependientes, incluyendo las reservas totales de hierro, el grado en que la médula ósea produce nuevos glóbulos rojos, la concentración de hemoglobina en la sangre y el contenido de oxígeno de la sangre. sangre. El cuerpo también absorbe menos hierro durante tiempos de inflamación , para privar a las bacterias de hierro. Descubrimientos recientes demuestran que la regulación de la ferroportina por hepcidina es responsable del síndrome de anemia de la enfermedad crónica.
La mayor parte del hierro del cuerpo es acumulado y reciclado por el sistema reticuloendotelial, que descompone los glóbulos rojos envejecidos. A diferencia de la absorción y el reciclaje de hierro, no existe un mecanismo regulador fisiológico para la excreción de hierro. Las personas pierden una cantidad pequeña pero constante por pérdida de sangre gastrointestinal, sudoración y desprendimiento de células de la piel y el revestimiento mucoso del tracto gastrointestinal . La cantidad total de pérdidas para las personas sanas en el mundo desarrollado asciende a un promedio estimado de1 mg al día para hombres y 1,5 a 2 mg al día para mujeres con períodos menstruales regulares. [15] Las personas con infecciones parasitarias gastrointestinales, que se encuentran más comúnmente en los países en desarrollo, a menudo pierden más. [1] Aquellos que no pueden regular la absorción lo suficientemente bien sufren trastornos de sobrecarga de hierro. En estas enfermedades, la toxicidad del hierro comienza a superar la capacidad del cuerpo para unirlo y almacenarlo. [dieciséis]
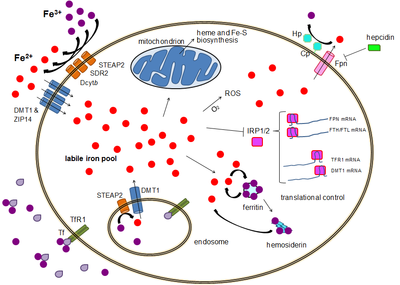
La mayoría de los tipos de células absorben hierro principalmente a través de endocitosis mediada por receptores a través del receptor de transferrina 1 (TFR1), el receptor de transferrina 2 (TFR2) y GAPDH . TFR1 tiene una afinidad 30 veces mayor por el hierro unido a transferrina que TFR2 y, por lo tanto, es el actor principal en este proceso. [17] [18] La enzima glicolítica multifuncional de orden superior gliceraldehído-3-fosfato deshidrogenasa (GAPDH) también actúa como receptor de transferrina. [19] [20] Estos receptores de transferrina reconocen el hierro férrico unido a transferrina, lo que desencadena un cambio conformacional que causa endocitosis. Luego, el hierro ingresa al citoplasma desde el endosoma a través del importador DMT1 después de ser reducido a su estado ferroso por una reductasa de la familia STEAP. [21]
Alternativamente, el hierro puede ingresar a la célula directamente a través de importadores de cationes divalentes de la membrana plasmática como DMT1 y ZIP14 (proteína 14 similar a Zrt-Irt). [22] Nuevamente, el hierro ingresa al citoplasma en estado ferroso después de ser reducido en el espacio extracelular por una reductasa como STEAP2, STEAP3 (en glóbulos rojos), Dcytb (en enterocitos) y SDR2. [21]
El hierro también puede ingresar a las células a través de CD44 en complejos unidos al ácido hialurónico durante la transición epitelial-mesenquimatosa (EMT). En este proceso, las células epiteliales se transforman en células mesenquimales con desprendimiento de la membrana basal , a la que normalmente están ancladas, allanando el camino para que las células mesenquimales móviles recién diferenciadas comiencen a migrar lejos de la capa epitelial. [23] [24]
Si bien la EMT desempeña un papel crucial en procesos fisiológicos como la implantación , donde permite que el embrión invada el endometrio para facilitar la unión placentaria , su desregulación también puede alimentar la propagación maligna de tumores , permitiéndoles invadir los tejidos circundantes y establecer colonias distantes ( metástasis ). [24]
Las células malignas a menudo presentan una mayor demanda de hierro, lo que impulsa su transición hacia un estado mesenquimatoso más invasivo. Este hierro es necesario para la expresión de genes mesenquimales, como los que codifican el factor de crecimiento transformante beta (TGF-β), crucial para la EMT. En particular, la capacidad única del hierro para catalizar la desmetilación de proteínas y ADN juega un papel vital en este proceso de expresión genética. [23]
Las vías convencionales de absorción de hierro, como las que utilizan el receptor de transferrina 1 (TfR1), a menudo resultan insuficientes para satisfacer estas elevadas demandas de hierro en las células cancerosas. Como resultado, diversas citoquinas y factores de crecimiento desencadenan la regulación positiva de CD44, una molécula de superficie capaz de internalizar el hierro unido al complejo de hialuronano. Esta vía alternativa, que depende de la endocitosis mediada por CD44, se convierte en el mecanismo de absorción de hierro dominante en comparación con la ruta tradicional dependiente de TfR1. [23] [24]
En el citoplasma, el hierro ferroso se encuentra en un estado soluble y quelante que constituye la reserva de hierro lábil (~0,001 mM). [25] En este grupo, se cree que el hierro está unido a compuestos de baja masa como péptidos, carboxilatos y fosfatos, aunque algunos pueden estar en forma libre e hidratada ( iones de agua ). [25] Alternativamente, los iones de hierro podrían unirse a proteínas especializadas conocidas como metalochaperonas . [26] Específicamente, las proteínas de unión a poli-r(C) PCBP1 y PCBP2 parecen mediar en la transferencia de hierro libre a ferritina (para almacenamiento) y enzimas de hierro no hemo (para uso en catálisis). [22] [27] La reserva de hierro lábil es potencialmente tóxica debido a la capacidad del hierro para generar especies reactivas de oxígeno. El hierro de este grupo puede ser absorbido por las mitocondrias a través de la mitoferrina para sintetizar grupos Fe-S y grupos hemo. [21]
El hierro se puede almacenar en ferritina como hierro férrico debido a la actividad ferroxidasa de la cadena pesada de ferritina. [28] La ferritina disfuncional puede acumularse en forma de hemosiderina , lo que puede ser problemático en casos de sobrecarga de hierro. [29] La reserva de hierro de almacenamiento de ferritina es mucho más grande que la reserva de hierro lábil, y su concentración oscila entre 0,7 mM y 3,6 mM. [25]
La exportación de hierro ocurre en una variedad de tipos de células, incluidas neuronas , glóbulos rojos, macrófagos y enterocitos. Los dos últimos son especialmente importantes ya que de ellos dependen los niveles sistémicos de hierro. Sólo se conoce un exportador de hierro: el ferroportin . [30] Transporta hierro ferroso fuera de la célula, generalmente con la ayuda de ceruloplasmina y/o hefestina (principalmente en los enterocitos), que oxidan el hierro a su estado férrico para que pueda unirse a la ferritina en el medio extracelular. [21] La hepcidina provoca la internalización de la ferroportina, lo que disminuye la exportación de hierro. Además, la hepcidina parece regular negativamente tanto TFR1 como DMT1 mediante un mecanismo desconocido. [31] Otro actor que ayuda a la ferroportina a efectuar la exportación de hierro celular es el GAPDH. [32] Una isoforma específica de GAPDH modificada postraduccionalmente se recluta en la superficie de las células cargadas de hierro, donde recluta apotransferrina en estrecha proximidad con la ferroportina para quelar rápidamente el hierro extruido. [33]

La expresión de hepcidina, que sólo ocurre en ciertos tipos de células como los hepatocitos , está estrechamente controlada a nivel transcripcional y representa el vínculo entre la homeostasis del hierro celular y sistémica debido al papel de la hepcidina como "guardián" de la liberación de hierro de los enterocitos al resto. del cuerpo. [21] Los eritroblastos producen eritroferrona , una hormona que inhibe la hepcidina y, por lo tanto, aumenta la disponibilidad del hierro necesario para la síntesis de hemoglobina. [35]
Aunque existe cierto control a nivel transcripcional, la regulación de los niveles de hierro celular está controlada en última instancia a nivel traduccional por las proteínas de unión a elementos sensibles al hierro IRP1 y especialmente IRP2. [36] Cuando los niveles de hierro son bajos, estas proteínas pueden unirse a elementos sensibles al hierro (IRE). Los IRE son estructuras de bucle madre en las regiones no traducidas (UTR) del ARNm. [21]
Tanto la ferritina como la ferroportina contienen un IRE en sus 5'UTR, de modo que, en caso de deficiencia de hierro, su traducción es reprimida por IRP2, impidiendo la síntesis innecesaria de proteínas de almacenamiento y la exportación perjudicial de hierro. Por el contrario, TFR1 y algunas variantes de DMT1 contienen 3'UTR IRE, que se unen a IRP2 en caso de deficiencia de hierro, estabilizando el ARNm, lo que garantiza la síntesis de los importadores de hierro. [21]

La deficiencia de hierro funcional o real puede deberse a diversas causas. Estas causas se pueden agrupar en varias categorías:
El cuerpo es capaz de reducir sustancialmente la cantidad de hierro que absorbe a través de la mucosa. No parece poder detener por completo el proceso de transporte del hierro. Además, en situaciones en las que el exceso de hierro daña el revestimiento intestinal (por ejemplo, cuando los niños comen una gran cantidad de tabletas de hierro producidas para el consumo de adultos), puede ingresar aún más hierro al torrente sanguíneo y causar un síndrome potencialmente mortal de sobrecarga de hierro. Grandes cantidades de hierro libre en la circulación causarán daño a células críticas en el hígado, el corazón y otros órganos metabólicamente activos.
La toxicidad del hierro se produce cuando la cantidad de hierro circulante excede la cantidad de transferrina disponible para unirlo, pero el cuerpo puede regular vigorosamente su absorción de hierro. Por lo tanto, la toxicidad del hierro por ingestión suele ser el resultado de circunstancias extraordinarias, como el consumo excesivo de tabletas de hierro [1] [42] , más que de variaciones en la dieta . El tipo de toxicidad aguda por la ingestión de hierro provoca, entre otros problemas, graves daños a las mucosas del tracto gastrointestinal.
El exceso de hierro se ha relacionado con mayores tasas de enfermedad y mortalidad. Por ejemplo, los pacientes con cáncer de mama con baja expresión de ferroportina (que conduce a concentraciones más altas de hierro intracelular) sobreviven durante un período de tiempo más corto en promedio, mientras que la alta expresión de ferroportina predice una supervivencia del 90% a 10 años en pacientes con cáncer de mama. [43] De manera similar, las variaciones genéticas en los genes transportadores de hierro que se sabe que aumentan los niveles séricos de hierro también reducen la esperanza de vida y el número promedio de años pasados con buena salud. [44] Se ha sugerido que las mutaciones que aumentan la absorción de hierro, como las responsables de la hemocromatosis (ver más abajo), fueron seleccionadas durante el Neolítico porque proporcionaban una ventaja selectiva contra la anemia por deficiencia de hierro. [45] El aumento de los niveles sistémicos de hierro se vuelve patológico en la vejez, lo que respalda la idea de que la pleiotropía antagonista o "hiperfunción" impulsa el envejecimiento humano. [44]
La toxicidad crónica del hierro suele ser el resultado de síndromes de sobrecarga de hierro más crónicos asociados con enfermedades genéticas, transfusiones repetidas u otras causas. En tales casos, las reservas de hierro de un adulto pueden alcanzar los 50 gramos (10 veces el hierro corporal total normal) o más. Las enfermedades más comunes por sobrecarga de hierro son la hemocromatosis hereditaria (HH), causada por mutaciones en el gen HFE , y la enfermedad más grave, la hemocromatosis juvenil (JH), causada por mutaciones en la hemojuvelina ( HJV ) [46] o la hepcidina ( HAMP ). . Los mecanismos exactos de la mayoría de las diversas formas de hemocromatosis en adultos, que constituyen la mayoría de los trastornos genéticos por sobrecarga de hierro, siguen sin resolverse. Entonces, si bien los investigadores han podido identificar mutaciones genéticas que causan varias variantes de hemocromatosis en adultos, ahora deben centrar su atención en la función normal de estos genes mutados.