
Los sistemas de secreción bacteriana son complejos proteicos presentes en las membranas celulares de las bacterias para la secreción de sustancias. En concreto, son los dispositivos celulares que utilizan las bacterias patógenas para secretar sus factores de virulencia (principalmente de proteínas) para invadir las células huésped. Se pueden clasificar en diferentes tipos en función de su estructura, composición y actividad específicas. Generalmente, las proteínas se pueden secretar mediante dos procesos diferentes. Un proceso es un mecanismo de un solo paso en el que las proteínas del citoplasma de las bacterias se transportan y entregan directamente a través de la membrana celular a la célula huésped. Otro implica una actividad de dos pasos en la que las proteínas primero se transportan fuera de la membrana celular interna, luego se depositan en el periplasma y finalmente a través de la membrana celular externa hacia la célula huésped. [2]
Estas principales diferencias se pueden distinguir entre las bacterias diderm gramnegativas y las bacterias monoderm grampositivas . Pero la clasificación no es en absoluto clara y completa. Hay al menos ocho tipos específicos de bacterias Gram negativas, cuatro de bacterias Gram positivas, mientras que dos son comunes a ambas. [3] Además, existe una diferencia apreciable entre las bacterias diderm con lipopolisacárido en la membrana externa (diderm-LPS) y aquellas con ácido micólico (diderm-micolato). [4]
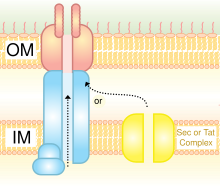
La vía de exportación es responsable de cruzar la membrana celular interna en los didermos y la única membrana celular en los monodermos. [4]
La secreción general (Sec) implica la secreción de proteínas desplegadas que primero permanecen dentro de las células. En las bacterias Gram negativas, la proteína secretada se envía a la membrana interna o al periplasma. Pero en las bacterias Gram positivas, la proteína puede permanecer en la célula o ser transportada principalmente fuera de la bacteria mediante otros sistemas de secreción. Entre las bacterias Gram negativas, Escherichia coli , Vibrio cholerae , Klebsiella pneumoniae y Yersinia enterocolitica utilizan el sistema Sec. Staphylococcus aureus y Listeria monocytogenes son bacterias Gram positivas que utilizan el sistema Sec. [5]
El sistema Sec utiliza dos vías diferentes para la secreción: la vía SecA y la de partículas de reconocimiento de señales (SRP). SecA es una proteína motora ATPasa y tiene muchas proteínas relacionadas, incluidas SecD, SecE, SecF, SegG, SecM y SecY. La SRP es una ribonucleoproteína (complejo proteína-ARN) que reconoce y dirige proteínas específicas al retículo endoplasmático en eucariotas y a la membrana celular en procariotas. Las dos vías requieren diferentes chaperonas moleculares y, en última instancia, utilizan un canal de transporte de proteínas SecYEG para transportar las proteínas a través de la membrana celular interna. [6] En la vía SecA, SecB actúa como chaperona, ayudando al transporte de proteínas al periplasma después de la síntesis completa de las cadenas peptídicas. Mientras que en la vía SRP, YidC es la chaperona y transporta proteínas a la membrana celular mientras aún están en proceso de síntesis de péptidos. [7] En Escherichia coli , las proteínas de la membrana interna están dirigidas principalmente por la vía SRP y las proteínas de la membrana externa o periplásmicas están dirigidas por la vía SecA. [8] Sin embargo, un estudio reciente de perfiles selectivos de ribosomas sugiere que la vía SecA se dirige a las proteínas de la membrana interna con grandes bucles periplásmicos. [9]
Las proteínas se sintetizan en los ribosomas mediante un proceso de adición secuencial de aminoácidos, llamado traducción. En la vía SecA, un factor desencadenante chaperona (TF) se une primero a la secuencia señal N-terminal expuesta de la cadena peptídica. A medida que continúa el alargamiento de la cadena peptídica, TF es reemplazado por SecB. SecB mantiene específicamente el péptido en un estado desplegado y ayuda en la unión de SecA. Luego, el complejo puede unirse a SecYEG, mediante el cual SecA se activa al unirse con ATP. Impulsada por la energía ATP, SecA empuja la proteína a través del canal secYEG. El complejo SecD/F también ayuda a extraer la proteína del otro lado de la membrana celular. [10]
En los últimos años, también se ha sugerido que la vía SecA tiene un mecanismo cotraduccional, lo que significa que SecA atacaría directamente al polipéptido durante su síntesis. [11]
En esta vía, SRP compite con TF y se une a la secuencia señal N-terminal. Las proteínas de la membrana interna detiene el proceso de elongación de la cadena. Luego, la SRP se une a un receptor de membrana, FtsY. Luego, el complejo cadena peptídica-SRP-FtsY se transporta a SecY, donde se reanuda el alargamiento del péptido. [7]
El sistema de translocación gemela de arginina (Tat) es similar al Sec en el proceso de secreción de proteínas, sin embargo, envía proteínas solo en su estado plegado (terciario). Es utilizado por todo tipo de bacterias, así como por arqueas, cloroplastos y mitocondrias de plantas. [12] En las bacterias, el sistema Tat exporta proteínas del citoplasma a través de la membrana celular interna; mientras que en los cloroplastos está presente en la membrana tilacoide, donde ayuda a la importación de proteínas desde el estroma. [13] Las proteínas Tat son muy variables en diferentes bacterias y se clasifican en tres tipos principales, a saber, TatA, TatB y TatC. Por ejemplo, mientras que en Bacillus subtilis sólo hay dos proteínas Tat funcionales , [14] puede haber más de cien en Streptomyces coelicolor . [15] Los péptidos señal que pueden reconocer las proteínas Tat se caracterizan por un motivo de consenso Ser/Thr-Arg-Arg-X-Phe-Leu-Lys (donde X puede ser cualquier aminoácido polar). Son las dos argininas sucesivas de las que proviene el nombre de translocación de arginina gemela. La sustitución de cualquiera de las argininas conduce a una desaceleración o falla de la secreción. [dieciséis]
La vía Wss/Esx ( sistema ESAT-6 ) a veces se denomina sistema de secreción tipo VII (T7SS) a pesar de ser una vía de exportación. [4] Está presente en bacterias Gram positivas (como WSS) y micobacterias (como Esx en todos los diderm-micolatos) como M. tuberculosis , M. bovis , Streptomyces coelicolor y S. aureus . También se le llama sistema T7b en Bacillus subtilis y S. aureus . Se compone de dos componentes básicos: una ATPasa hexamérica unida a membrana que es miembro de la familia de proteínas FtsK /SpoIIIE, [17] y cualquiera de las proteínas relacionadas con EsxA/EsxB, como EsaA, EsaD, EsxB, EsxD, como así como el sistema Ess (EssA, EssB y EsxC que se encuentran en S. aureus ). [18] EsxA y EsxB pertenecen a una superfamilia de proteínas WXG100 que forman horquillas helicoidales diméricas.
En S. aureus , T7SS secreta una toxina grande llamada EsaD, que es miembro de las enzimas nucleasas . EsaD se vuelve inofensivo (desintoxicado) durante su biosíntesis con la ayuda de su antitoxina homóloga EsaG. Luego, el complejo EsaD-EsaG se une a EsaE. La porción EsaE se une a EssC, que es una enzima ATPasa del complejo T7SS. Durante la secreción, EsaG queda en el citoplasma y sólo EsaD y EsaE se secretan juntos. Pero en algunas cepas de S. aureus , EsaD no se produce, sino que se forman dos copias de proteínas similares a EsaG. Esto podría explicar la aparición de T7SS en especies no patógenas como B. subtilis y S. coelicolor . [19]
Los sistemas de secreción se encargan de atravesar la membrana celular externa o ambas membranas en los didermos. La nomenclatura actual se aplica únicamente al diderm-LPS, ya que no se sabe nada sobre qué utilizan las bacterias diderm-micolato para cruzar su membrana externa. [4]

El sistema de secreción tipo I (T1SS o TOSS) se encuentra en las bacterias Gram-negativas. Depende de la actividad de las chaperonas que utilizan las proteínas Hly y Tol. El sistema se activa como una secuencia señal que HlyA se une a HlyB en la membrana celular. Esta secuencia de señales es un transportador ABC. El complejo HlyAB activa HlyD, que se desenrosca y se mueve hacia la membrana celular externa. La señal terminal es reconocida por TolC en la membrana interna. El HlyA se secreta fuera de la membrana externa a través de un canal proteico en forma de túnel.
T1SS transporta varias moléculas, incluidos iones, carbohidratos, fármacos y proteínas. Las moléculas secretadas varían en tamaño desde el pequeño péptido colicina V de Escherichia coli , que mide 10 kDa, hasta la proteína de adhesión celular de Pseudomonas fluorescens LapA, que mide 520 kDa. [20] Entre las moléculas más conocidas se encuentran las toxinas RTX y las enzimas lipasa.

El sistema de secreción tipo II (T2SS) depende del sistema Sec o Tat para la secreción inicial dentro de la célula bacteriana. Desde el periplasma, las proteínas se secretan a partir de las secretinas de la membrana externa. Las secretinas son un complejo multimérico (12 a 14 subunidades) de proteínas formadoras de poros. La secretina está respaldada por otras 10 a 15 proteínas de la membrana interna y externa para constituir el aparato de secreción completo. [21]

El sistema de secreción tipo III (T3SS o TTSS) es estructuralmente similar y está relacionado con el cuerpo basal de los flagelos bacterianos . Visto en algunas de las bacterias Gram negativas más virulentas, como Salmonella , Shigella , Yersinia , Vibrio , se utiliza para inyectar proteínas tóxicas en células eucariotas. La estructura de T3SS a menudo se describe como un inyectosoma o un aparato similar a una aguja/jeringa. Descubierto en Yersinia pestis , se descubrió que el T3SS puede inyectar toxinas directamente desde el citoplasma bacteriano al citoplasma de las células de su huésped. [22]
El sistema de secreción tipo IV (T4SS o TFSS) está relacionado con el sistema de conjugación bacteriana , mediante el cual diferentes bacterias pueden intercambiar su ADN. Las bacterias participantes pueden ser de la misma o diferente especie bacteriana Gram negativa. Puede transportar proteínas individuales, así como complejos proteína-proteína y ADN-proteína. La secreción se transfiere directamente desde la célula receptora a través de las membranas celulares. Agrobacterium tumefaciens , a partir del cual se descubrió originalmente, utiliza este sistema para enviar la porción de ADN T del plásmido Ti a las células vegetales, en las que se produce como resultado una agalla de la corona (tumor). Helicobacter pylori lo utiliza para administrar CagA a las células epiteliales gástricas, para inducir cáncer gástrico. [23] Bordetella pertussis , la bacteria causante de la tos ferina, secreta su toxina pertussis en parte a través de T4SS. Legionella pneumophila que causa legionelosis (enfermedad del legionario) tiene un T4SS llamado icm/dot (multiplicación intracelular / defecto en genes de tráfico de organelos ) que transporta muchas proteínas bacterianas a su huésped eucariota. [24] Más recientemente, se ha demostrado que el fitopatógeno Xanthomonas citri utiliza su T4SS para secretar efectores que son letales para otras especies bacterianas, lo que coloca a este sistema como un importante determinante de la competencia bacteriana entre especies. [25] [26] El sistema de secreción tipo IVA prototípico es el complejo VirB de Agrobacterium tumefaciens . [27]


Los sistemas de secreción tipo V (T5SS) se diferencian de otros sistemas de secreción en que se secretan a sí mismos y solo involucran la membrana celular externa. Para que la proteína secretada atraviese la membrana celular interna, T5SS depende del sistema Sec. Tienen un dominio de barril β, que se inserta en la membrana celular externa y forma un canal que puede transportar proteínas secretadas junto con él. Para esta actividad también se les denomina sistemas autotransportadores. [28] Cuando las proteínas secretadas quedan expuestas al exterior, los autotransportadores se cortan (escinden), liberando la proteína del dominio del barril β. Un ejemplo de autotransportador son las Adhesinas Autotransportadoras Triméricas . [29]
Los sistemas de secreción tipo VI (T6SS) fueron descubiertos por el equipo de John Mekalanos en la Escuela de Medicina de Harvard en 2006 a partir de Vibrio cholerae y Pseudomonas aeruginosa . [30] [31] Fueron reconocidos cuando las mutaciones en los genes Vibrio Cholerae Hcp y VrgG causaron una disminución de la virulencia y la patogenicidad. [32] [33] Además de su papel clásico como factor de patogenicidad, los T6SS también participan en la defensa contra depredadores eucarióticos simples y en las interacciones entre bacterias. [34] [35] El gen para T6SS forma un grupo de genes que consta de más de 15 genes. Los genes Hcp y VgrG son los genes más universales. La similitud estructural de T6SS con la punta de la cola del fago T4 sugiere que el proceso de infección es similar al del fago. [36]
El T7SS de las bacterias diderm-LPS es la vía acompañante-usher (CUP). [4]
El T8SS de las bacterias diderm-LPS es la vía de nucleación-precipitación extracelular (ENP). [4]

Los sistemas de secreción de tipo IX (T9SS) se encuentran regularmente en el linaje de bacterias Fibrobacteres-Chlorobi-Bacteroidetes , donde las especies miembros incluyen una membrana externa. El sistema participa de forma variable en un tipo de motilidad de deslizamiento, en la dirección adecuada de ciertos factores de virulencia a la superficie celular y en la degradación de complejos de biopolímeros. [38] T9SS también se conoce como secreción de Por (acumulación de porfirina en la superficie celular), [4] en honor al patógeno oral Porphyromonas gingivalis . Se han descrito al menos dieciséis componentes estructurales del sistema, incluida PorU, una transpeptidasa clasificadora de proteínas que elimina la señal de clasificación C-terminal de las proteínas de carga y media su unión al lipopolisacárido .