La criptococosis es una infección fúngica potencialmente mortal que afecta principalmente a los pulmones , presentándose como una neumonía , y al cerebro , donde aparece como una meningitis . [4] [9] Cuando los pulmones están infectados, se observan tos , dificultad para respirar , dolor en el pecho y fiebre . [5] Cuando el cerebro está infectado, los síntomas incluyen dolor de cabeza , fiebre, dolor de cuello , náuseas y vómitos , sensibilidad a la luz y confusión o cambios en el comportamiento. [5] También puede afectar otras partes del cuerpo, incluida la piel , donde puede aparecer como varios nódulos llenos de líquido con tejido muerto . [6]
Es causada por los hongos Cryptococcus neoformans o menos comúnmente Cryptococcus gattii , y se adquiere al respirar las esporas del aire. [4] Estos hongos se encuentran en todo el mundo en el suelo, la madera en descomposición, los excrementos de las palomas y en los huecos de algunas especies de árboles. [9] [12] Mientras que C. neoformans generalmente infecta a personas con VIH/SIDA y a quienes toman medicamentos inmunosupresores y no suele afectar a personas sanas y en forma, C. gattii (que se encuentra en algunas partes de Canadá y los EE. UU.) sí lo hace. [9] [12] Una vez inhaladas, las células de levadura secas colonizan los pulmones, donde son eliminadas por las células inmunes , permanecen latentes o causan infección y se propagan. [13]
El diagnóstico se realiza mediante el aislamiento de Cryptococcus a partir de una muestra de tejido afectado o mediante la observación directa del hongo mediante tinción de fluidos corporales. [9] Se puede cultivar a partir de líquido cefalorraquídeo , esputo y biopsia de piel . [9] El tratamiento es con fluconazol o anfotericina B. [ 9] [10]
Datos de 2009 estimaron que de los casi un millón de casos de meningitis criptocócica que ocurrieron anualmente en todo el mundo, 700.000 ocurrieron en África subsahariana y 600.000 murieron por año. [14] La criptococosis era rara antes de la década de 1970, cuando se vio un aumento en los grupos de riesgo, como las personas con trasplante de órganos o con medicamentos inmunosupresores . [9] El número de casos aumentó a mediados de la década de 1980 y más del 80% se produjo en personas con VIH/SIDA . [9] Se sabe que los criadores de palomas (o las personas que pasan un tiempo significativo con palomas) tienen una alta incidencia de infecciones criptocócicas, incluido el criptococo cutáneo primario debido a la asociación de los hongos con los excrementos de paloma. [15] [ se necesita una mejor fuente ]
El criptococo se clasifica generalmente según el modo de adquisición y el sitio de infección. [16] Por lo general, comienza en los pulmones antes de propagarse a otras partes del cuerpo, en particular el cerebro y el sistema nervioso. [1] La afectación de la piel es menos común. [1]
Cuando los pulmones están infectados, se observan tos, falta de aliento, dolor en el pecho y fiebre, con un aspecto similar al de una neumonía. [5] También puede haber sensación de cansancio . [4] Cuando el cerebro está infectado, los síntomas incluyen dolor de cabeza, fiebre, dolor de cuello, náuseas y vómitos, sensibilidad a la luz, confusión o cambios en el comportamiento. [5] También puede afectar otras partes del cuerpo, incluida la piel, los ojos, los huesos y la próstata. [9] En la piel, puede aparecer como varios nódulos llenos de líquido con tejido muerto . [6] Dependiendo del sitio de la infección, otras características pueden incluir pérdida de visión , visión borrosa , incapacidad para mover un ojo y pérdida de memoria. [9]
La aparición de los síntomas suele ser repentina cuando los pulmones están infectados y gradual durante varias semanas cuando el sistema nervioso central está afectado. [9]
Los signos y síntomas de la infección criptocócica pueden aparecer de forma tardía en las personas con VIH o SIDA. Una prueba positiva del antígeno criptocócico puede preceder a los síntomas en unas 3 semanas en las personas con VIH/SIDA. En otras personas puede reactivarse la enfermedad criptocócica latente años después. En las personas con VIH, aproximadamente el 50% de las personas tienen fiebre, pero la fiebre es poco frecuente en personas previamente sanas e inmunocompetentes con criptococosis. [17]
La criptococosis es una infección oportunista común en el SIDA y es particularmente común entre las personas que viven con SIDA en África . Otras afecciones que plantean un mayor riesgo incluyen ciertas neoplasias malignas (como el linfoma ), la cirrosis hepática , los trasplantes de órganos y la terapia con corticosteroides a largo plazo . [18]
La distribución es mundial en el suelo. [19] La prevalencia de la criptococosis ha aumentado en los últimos 50 años por muchas razones, incluido el aumento de la incidencia del SIDA y el uso ampliado de medicamentos inmunosupresores. [20]
En los seres humanos, C. neoformans infecta principalmente la piel, los pulmones y el sistema nervioso central (causando meningitis ). [20] Con menor frecuencia, puede afectar otros órganos como el ojo o la próstata. [20]
La criptococosis cutánea primaria (CCP) es un diagnóstico clínico distinto de la criptococosis cutánea secundaria que se transmite a partir de una infección sistemática. Los varones tienen más probabilidades de desarrollar la infección y un estudio de 2020 mostró que el sesgo sexual puede deberse a una hormona de crecimiento, producida por C. neoformans , llamada ácido giberélico (AG), que se regula positivamente por la testosterona. [21] Las extremidades superiores representan la mayoría de las infecciones. Los aislamientos encontrados en la CCP incluyen Cryptococcus neoformans (el más común), Cryptococcus gattii y Cryptococcus laurentii . El pronóstico para la CCP es generalmente bueno fuera de la infección diseminada. [22]
La descripción morfológica de las lesiones muestra pápulas umbilicadas, nódulos y placas violáceas que pueden imitar otras enfermedades cutáneas como el molusco contagioso y el sarcoma de Kaposi . Estas lesiones pueden estar presentes meses antes de que aparezcan otros signos de infección sistémica en pacientes con SIDA. [23]
El criptococo (tanto C. neoformans como C. gattii ) desempeña un papel común en la micosis invasiva pulmonar observada en adultos con VIH y otras afecciones inmunocomprometidas. [18] También afecta a adultos sanos con una frecuencia y gravedad mucho menores, ya que los huéspedes sanos pueden no presentar síntomas o presentar síntomas leves. [24] Los huéspedes inmunocompetentes pueden no buscar o requerir tratamiento, pero puede ser importante una observación cuidadosa. [25] La neumonía criptocócica tiene el potencial de diseminarse al sistema nervioso central (SNC), especialmente en individuos inmunocomprometidos. [26]
La criptococosis pulmonar tiene una distribución mundial y suele ser infradiagnosticada debido a las limitaciones en las capacidades diagnósticas. Dado que los nódulos pulmonares son su característica radiológica más común, puede imitar clínica y radiológicamente el cáncer de pulmón, la tuberculosis y otras micosis pulmonares. La sensibilidad de los cultivos y el antígeno criptocócico (CrAg) con dispositivo de flujo lateral en suero rara vez son positivos en ausencia de enfermedad diseminada. [18] Además, la criptococosis pulmonar empeora el pronóstico de la meningitis criptocócica. [18]
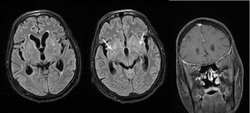
Se cree que la meningitis criptocócica (infección de las meninges , el tejido que recubre el cerebro) es resultado de la diseminación del hongo a partir de una infección pulmonar observada o no detectada. A menudo, también hay una diseminación silenciosa por todo el cerebro cuando hay meningitis. Las personas con defectos en su inmunidad celular , por ejemplo, las personas con SIDA , son especialmente susceptibles a la criptococosis diseminada. La criptococosis suele ser mortal, incluso si se trata. Se estima que la tasa de letalidad a tres meses es del 9% en las regiones de altos ingresos, del 55% en las regiones de ingresos bajos y medios y del 70% en el África subsahariana. En 2009, hubo aproximadamente 958.000 casos anuales a nivel mundial y 625.000 muertes dentro de los tres meses posteriores a la infección. [27]
Aunque la infección por C. neoformans ocurre más comúnmente como una infección oportunista en personas inmunodeprimidas (como aquellas que viven con SIDA), C. gattii a menudo también infecta a personas inmunocompetentes. [28]
Las especies de Cryptococcus (tanto C. neoformans como C. gattii ) son responsables del 68% de los casos de meningitis en personas con VIH. [17] Cryptococcus se considera una enfermedad "emergente" en adultos sanos. [29] Aunque la tasa de infección es claramente mayor en individuos inmunodeprimidos, algunos estudios sugieren una mayor tasa de mortalidad en pacientes con meningitis criptocócica no relacionada con el VIH, secundaria al papel de la reacción y la lesión mediadas por células T. [30] Las células T CD4+ han demostrado tener un papel en la defensa contra Cryptococcus , pero también pueden contribuir al deterioro clínico debido a su respuesta inflamatoria. [31]
El inicio de los síntomas suele ser subagudo, empeora progresivamente a lo largo de varias semanas y los retrasos en el diagnóstico se asocian con una mayor mortalidad. [20] [17]
La detección de antígenos criptocócicos en el líquido cefalorraquídeo (LCR) o en la sangre mediante un ensayo de flujo lateral tiene una sensibilidad y una especificidad superiores al 99 % para la criptococosis. [17] Un cultivo de hongos en el LCR puede indicar si hay una falla microbiológica (falla de las infecciones fúngicas para tratar la infección). El cultivo de hongos en el LCR tiene una sensibilidad del 90 % y una especificidad del 100 % para el diagnóstico de meningitis criptocócica. El análisis de células del LCR se caracteriza por un aumento de linfocitos, una reducción de proteínas y una reducción de glucosa. [17] Para cualquier persona que tenga criptococosis en un sitio fuera del sistema nervioso central (p. ej., criptococosis pulmonar), está indicada una punción lumbar para evaluar el líquido cefalorraquídeo (LCR) en busca de evidencia de meningitis criptocócica, incluso si no tiene signos o síntomas de enfermedad del SNC. La detección del antígeno criptocócico (material capsular) mediante cultivo de LCR, esputo y orina proporciona un diagnóstico definitivo. [32] Los hemocultivos pueden ser positivos en infecciones graves. La tinta china del LCR es un método microscópico tradicional de diagnóstico, [33] aunque la sensibilidad es baja en la infección temprana y puede pasar por alto entre el 15 y el 20 % de los pacientes con meningitis criptocócica con cultivo positivo. [34] Los métodos de diagnóstico rápido para detectar el antígeno criptocócico incluyen la prueba de aglutinación de látex, el ensayo inmunocromatográfico de flujo lateral (LFA) o el inmunoensayo enzimático (EIA). La reacción en cadena de la polimerasa (PCR) se ha utilizado en muestras de tejido, y la PCR tiene una sensibilidad del 82 % y una especificidad del 98 % para la infección criptocócica. [17]
La criptococosis es una infección muy subaguda con una fase subclínica prolongada que dura semanas o meses en personas con VIH/SIDA antes de la aparición de meningitis sintomática. En África subsahariana, las tasas de prevalencia de antígeno criptocócico detectable en sangre periférica suelen ser del 4 al 12 % en personas con recuentos de CD4 inferiores a 100 células/μL. [35] [36] La detección del antígeno criptocócico y el tratamiento preventivo con fluconazol suponen un ahorro de costes para el sistema sanitario, ya que evitan la meningitis criptocócica. [37] La Organización Mundial de la Salud recomienda la detección del antígeno criptocócico en personas infectadas por el VIH que ingresan a la atención médica con CD4 <100 células/μL. [38] Este criptococo subclínico no detectado (si no se trata de forma preventiva con terapia antifúngica) a menudo desarrollará meningitis criptocócica, a pesar de recibir terapia contra el VIH. [36] [39] La criptococosis es responsable del 20 al 25% de la mortalidad tras iniciar la terapia contra el VIH en África. Se desconoce cuál es el tratamiento preventivo eficaz, y las recomendaciones actuales sobre dosis y duración se basan en la opinión de expertos. El cribado en los Estados Unidos es controvertido, y las directrices oficiales no lo recomiendan, a pesar de su relación coste-eficacia y de una prevalencia del antígeno criptocócico en los Estados Unidos del 3% en células CD4 <100/μL. [40] [41]
La profilaxis antimicótica, como el fluconazol y el itraconazol, reduce el riesgo de contraer criptococosis en aquellas personas con un recuento bajo de células CD4 y un alto riesgo de desarrollar dicha enfermedad en un entorno en el que no se encuentran disponibles pruebas de detección de antígenos criptocócicos. [42]
Las opciones de tratamiento en personas sin infección por VIH no han sido bien estudiadas. Se recomienda la administración intravenosa de anfotericina B combinada con flucitosina por vía oral para el tratamiento inicial (terapia de inducción). [43]
Las personas que viven con SIDA a menudo tienen una mayor carga de enfermedad y una mayor mortalidad (30–70% a las 10 semanas), la terapia recomendada es con anfotericina B y flucitosina. Agregar flucitosina a la anfotericina B se asocia con una eliminación más temprana de los hongos y una mayor supervivencia, sin embargo, no está fácilmente disponible en muchas regiones de bajos ingresos. [17] Cuando la flucitosina no está disponible, se debe utilizar fluconazol con anfotericina. [38] La terapia de inducción basada en anfotericina tiene una actividad microbiológica mucho mayor que la monoterapia con fluconazol con un 30% mejor de supervivencia a las 10 semanas. [32] [44] Según una revisión sistemática, el tratamiento de inducción más rentable en entornos con recursos limitados parece ser una semana de anfotericina B combinada con fluconazol en dosis alta. [44] Después del tratamiento de inducción inicial mencionado anteriormente, la terapia de consolidación típica es con fluconazol oral durante al menos 8 semanas, utilizado con profilaxis secundaria con fluconazol a partir de entonces. [38]
La decisión sobre cuándo iniciar el tratamiento del VIH parece ser muy diferente a la de otras infecciones oportunistas. Un gran ensayo multicéntrico respalda que diferir la TAR durante 4 a 6 semanas fue, en general, preferible, con una supervivencia al año un 15 % mejor que el inicio más temprano de la TAR entre 1 y 2 semanas después del diagnóstico. [45] Una revisión Cochrane de 2018 también respalda el inicio tardío del tratamiento hasta que la criptococosis comience a mejorar con el tratamiento antimicótico. [46]
En aproximadamente el 50% de los pacientes con meningitis criptocócica asociada al VIH, se observa un aumento de la presión intracraneal y suele estar asociada a una alta carga fúngica. Las punciones lumbares periódicas (a menudo diarias) para reducir la presión intracraneal mediante el drenaje del LCR se asocian a una menor mortalidad en los pacientes con meningitis criptocócica (con o sin VIH). [17] [47] [11] Pero en aquellos con sospecha de hidrocefalia no comunicante (que puede presentarse como síntomas neurológicos focales o deterioro mental), se requiere una tomografía computarizada o una resonancia magnética del cerebro antes de la punción lumbar para descartar la hidrocefalia, debido al riesgo de hernia cerebral con la punción lumbar. La hidrocefalia no comunicante es poco frecuente en los pacientes con meningitis criptocócica asociada al VIH. [17]
El síndrome inflamatorio de reconstitución inmunitaria es posible en pacientes con infección criptocócica, especialmente en aquellos con VIH concurrente que comienzan una terapia antirretroviral . Con la terapia antirretroviral para el VIH, los recuentos de células T CD4+ se recuperan y el sistema inmunitario restaurado genera una respuesta hiperinflamatoria exagerada contra la infección criptocócica en el cuerpo. [17]
El SIRI tiene una incidencia del 5% en pacientes con VIH y criptococosis que comienzan la terapia antirretroviral. Por lo general, se presenta dentro de las 4 semanas posteriores al inicio de la terapia antirretroviral. [17] El riesgo de SIRI es mayor en aquellos con una carga fúngica alta, un recuento menor de células T CD4+ y niveles más bajos de marcadores inflamatorios. [17]
La criptococosis suele asociarse a personas inmunodeprimidas, como las que padecen SIDA , utilizan corticosteroides , tienen diabetes y reciben trasplantes de órganos . [48] Cryptococcus comprende dos especies clínicamente relevantes, Cryptococcus neoformans y Cryptococcus gattii . [49] Anteriormente se pensaba que C. gattii solo se encontraba en climas tropicales y en personas inmunocompetentes, pero hallazgos recientes de C. gattii en regiones como Canadá y las regiones occidentales de América del Norte han desafiado esta presunción inicial de los patrones geográficos. [50]
Datos de 2009 estimaron que de los casi un millón de casos de meningitis criptocócica que ocurrieron anualmente en todo el mundo, 700.000 ocurrieron en África subsahariana y 600.000 murieron por año. [14] En 2014, entre las personas que tenían un recuento bajo de células CD4+ , la tasa de incidencia anual se estimó en 278.000 casos. De ellos, 223.100 resultaron en meningitis criptocócica. [51] Alrededor del 73% de los casos de meningitis criptocócica ocurrieron en África subsahariana. Más de 180.000 muertes se atribuyen a la meningitis criptocócica, 135.000 de las cuales ocurren en África subsahariana. La letalidad de la meningitis criptocócica varía ampliamente según el país en el que se produce la infección. En los países de bajos ingresos, la letalidad de la meningitis criptocócica es del 70%. Esto difiere de los países de ingresos medios, donde la tasa de letalidad es del 40%. En los países ricos, la tasa de letalidad es del 20%. [51] El 19% de todas las muertes relacionadas con el SIDA se deben a la enfermedad criptocócica. [52] La enfermedad criptocócica es la segunda causa principal de muerte en las personas con VIH/SIDA, superada sólo por la tuberculosis, que es responsable del 40% de las muertes. [53] En el África subsahariana, aproximadamente un tercio de los pacientes con VIH desarrollarán criptococosis. [54]
En los Estados Unidos, la incidencia de criptococosis se estima en alrededor de 0,4-1,3 casos por 100.000 habitantes y de 2-7 casos por 100.000 en personas afectadas de SIDA, con una tasa de letalidad de alrededor del 12%. Desde 1990, la incidencia de criptococosis asociada al SIDA se redujo en un 90% debido a la proliferación de la terapia antirretroviral . [55] [56] La prevalencia estimada de casos de criptococosis entre pacientes con VIH en los EE. UU. es del 2,8%. [57] En pacientes inmunocompetentes, el criptococo se presenta típicamente como Cryptococcus gattii . [56] A pesar de su rareza, el criptococo se ha visto más comúnmente, con más del 20% de los casos en personas inmunocompetentes. [58] Más del 50% de las infecciones por criptococosis en América del Norte son causadas por C. gattii. Aunque originalmente se pensaba que C. gattii estaba restringido a regiones tropicales y subtropicales, se ha vuelto más frecuente en todo el mundo. [59] C. gattii se ha encontrado en más de 90 personas en los Estados Unidos, la mayoría de estos casos se originaron en Washington u Oregón. [60]
El África subsahariana es el principal foco mundial de VIH/SIDA. El VIH/SIDA representa alrededor del 0,5% de la población mundial. [61] Sorprendentemente, el África subsahariana alberga el 71% de los casos de VIH/SIDA. [62] La meningitis criptocócica es una de las principales causas de mortalidad entre las personas con VIH/SIDA en el África subsahariana. [63] Se han notificado aproximadamente 160.000 casos de meningitis criptocócica en África occidental, lo que da lugar a 130.000 muertes en el África subsahariana. [64] Se informa de que Uganda tiene la mayor incidencia de meningitis criptocócica. [54] Como reflejo de ello, Etiopía tiene la menor incidencia. [54] En la actualidad, las opciones de tratamiento implican un régimen de 7 o 14 días de anfotericina-B, junto con comprimidos antimicóticos orales o fluconazol oral. Es importante señalar que la anfotericina B no se considera un tratamiento, ya que no mostró una reducción significativa en la tasa de mortalidad. [65]
La criptococosis también se observa en gatos y, ocasionalmente, en perros. Es la enfermedad fúngica profunda más común en los gatos, que suele provocar una infección crónica de la nariz y los senos nasales, y úlceras cutáneas. Los gatos pueden desarrollar un bulto en el puente de la nariz debido a la inflamación del tejido local. Puede estar asociada con la infección por FeLV en gatos. La criptococosis es más común en perros y gatos, pero el ganado vacuno, las ovejas, las cabras, los caballos, los animales salvajes y las aves también pueden infectarse. El suelo, el estiércol de aves y los excrementos de paloma se encuentran entre las fuentes de infección. [66] [67]
{{cite journal}}: CS1 maint: DOI inactivo a partir de noviembre de 2024 ( enlace )