
La espectroscopia infrarroja ( espectroscopia IR o espectroscopia vibracional ) es la medida de la interacción de la radiación infrarroja con la materia por absorción , emisión o reflexión . Se utiliza para estudiar e identificar sustancias químicas o grupos funcionales en forma sólida, líquida o gaseosa. Puede utilizarse para caracterizar nuevos materiales o identificar y verificar muestras conocidas y desconocidas. El método o técnica de espectroscopia infrarroja se realiza con un instrumento llamado espectrómetro de infrarrojos (o espectrofotómetro) que produce un espectro infrarrojo . Un espectro IR se puede visualizar en un gráfico de absorbancia (o transmitancia ) de luz infrarroja en el eje vertical versus frecuencia , número de onda o longitud de onda en el eje horizontal. Las unidades típicas de número de onda utilizadas en los espectros IR son centímetros recíprocos , con el símbolo cm −1 . Las unidades de longitud de onda IR se dan comúnmente en micrómetros (anteriormente llamados "micrones"), de símbolo μm, que están relacionados con el número de onda de forma recíproca . Un instrumento de laboratorio común que utiliza esta técnica es un espectrómetro de infrarrojos por transformada de Fourier (FTIR) . La IR bidimensional también es posible como se analiza a continuación.
La porción infrarroja del espectro electromagnético suele dividirse en tres regiones; el infrarrojo cercano , medio y lejano , llamado así por su relación con el espectro visible. El IR cercano de mayor energía, aproximadamente 14.000 a 4.000 cm −1 (longitud de onda de 0,7 a 2,5 μm) puede excitar modos armónicos o combinados de vibraciones moleculares . El infrarrojo medio, de aproximadamente 4000 a 400 cm −1 (2,5 a 25 μm), se utiliza generalmente para estudiar las vibraciones fundamentales y la estructura rotacional-vibracional asociada . El infrarrojo lejano, de aproximadamente 400 a 10 cm −1 (25 a 1000 μm), tiene baja energía y puede usarse para espectroscopia rotacional y vibraciones de baja frecuencia. La región de 2 a 130 cm −1 , que limita con la región de microondas , se considera la región de terahercios y puede detectar vibraciones intermoleculares. [1] Los nombres y clasificaciones de estas subregiones son convenciones y sólo se basan vagamente en las propiedades moleculares o electromagnéticas relativas.

_(8225044148).jpg/440px-Portable_Screening_Devices_(1435)_(8225044148).jpg)
La espectroscopia infrarroja es una técnica sencilla y fiable ampliamente utilizada tanto en química orgánica como inorgánica, en investigación e industria. En la investigación de catálisis es una herramienta muy útil para caracterizar el catalizador, [2] [3] [4] así como para detectar intermedios [5] y productos durante la reacción catalítica. Se utiliza en aplicaciones de control de calidad, medición dinámica y monitoreo, como la medición desatendida a largo plazo de concentraciones de CO 2 en invernaderos y cámaras de crecimiento mediante analizadores de gas infrarrojos. [ cita necesaria ]
También se utiliza en análisis forenses en casos penales y civiles, por ejemplo para identificar la degradación de polímeros . Puede utilizarse para determinar el contenido de alcohol en sangre de un conductor sospechoso de estar ebrio.
La espectroscopia IR se ha utilizado con éxito en el análisis y la identificación de pigmentos en pinturas [6] y otros objetos de arte [7], como manuscritos iluminados . [8]
La espectroscopia infrarroja también es útil para medir el grado de polimerización en la fabricación de polímeros . Los cambios en el carácter o cantidad de un vínculo particular se evalúan midiendo con una frecuencia específica a lo largo del tiempo. Los instrumentos de investigación modernos pueden tomar mediciones infrarrojas en el rango de interés con una frecuencia de hasta 32 veces por segundo. Esto se puede hacer mientras se realizan mediciones simultáneas utilizando otras técnicas. Esto hace que las observaciones de reacciones y procesos químicos sean más rápidas y precisas. [ cita necesaria ]
La espectroscopia infrarroja también se ha utilizado con éxito en el campo de la microelectrónica de semiconductores: [9] por ejemplo, la espectroscopia infrarroja se puede aplicar a semiconductores como silicio , arseniuro de galio , nitruro de galio , seleniuro de zinc , silicio amorfo, nitruro de silicio , etc.
Otra aplicación importante de la espectroscopia infrarroja es en la industria alimentaria para medir la concentración de varios compuestos en diferentes productos alimenticios. [10] [11]
Los instrumentos ahora son pequeños y pueden transportarse, incluso para su uso en pruebas de campo. [ cita necesaria ]
La espectroscopia infrarroja también se utiliza en dispositivos de detección de fugas de gas como DP-IR y EyeCGA. [12] Estos dispositivos detectan fugas de gas hidrocarburo en el transporte de gas natural y petróleo crudo.
En febrero de 2014, la NASA anunció una base de datos muy mejorada, [13] basada en espectroscopia IR, para rastrear hidrocarburos aromáticos policíclicos (PAH) en el universo . Según los científicos, más del 20% del carbono del universo puede estar asociado a HAP, posibles materiales de partida para la formación de la vida . Los HAP parecen haberse formado poco después del Big Bang , están muy extendidos por todo el universo y están asociados con nuevas estrellas y exoplanetas . [14]
La espectroscopia infrarroja es un método de análisis importante en el proceso de reciclaje de plásticos de desecho domésticos y un método de separación conveniente para clasificar plásticos de diferentes polímeros ( PET , HDPE , ...). [15]
Otros desarrollos incluyen un espectrómetro IR en miniatura que está vinculado a una base de datos basada en la nube y adecuado para el uso diario personal, [16] y chips espectroscópicos NIR [17] que pueden integrarse en teléfonos inteligentes y diversos dispositivos.
La espectroscopia infrarroja, combinada con el aprendizaje automático y la inteligencia artificial, también tiene potencial para detectar bacterias de forma rápida, precisa y no invasiva. [18] La compleja composición química de las bacterias, incluidos los ácidos nucleicos, las proteínas, los carbohidratos y los ácidos grasos, da como resultado conjuntos de datos de alta dimensión donde las características esenciales están efectivamente ocultas bajo el espectro total. Por lo tanto, la extracción de las características esenciales requiere métodos estadísticos avanzados, como el aprendizaje automático y las redes neuronales profundas. Se ha demostrado el potencial de esta técnica para la clasificación de bacterias para la diferenciación a nivel taxonómico de género, [19] especie [20] y serotipo [21] , y también se ha demostrado prometedora para las pruebas de susceptibilidad a los antimicrobianos, [22] [23]. [24], lo cual es importante para muchos entornos clínicos donde las pruebas de susceptibilidad más rápidas disminuirían el tratamiento ciego innecesario con antibióticos de amplio espectro. La principal limitación de esta técnica para aplicaciones clínicas es la alta sensibilidad al equipo técnico y las técnicas de preparación de muestras, lo que dificulta la construcción de bases de datos a gran escala. Sin embargo, Bruker ha realizado intentos en esta dirección con el IR Biotyper para microbiología alimentaria. [25]

La espectroscopia infrarroja aprovecha el hecho de que las moléculas absorben frecuencias características de su estructura . Estas absorciones se producen a frecuencias de resonancia , es decir, la frecuencia de la radiación absorbida coincide con la frecuencia de vibración. Las energías se ven afectadas por la forma de las superficies de energía potencial molecular , las masas de los átomos y el acoplamiento vibrónico asociado . [ cita necesaria ]

En particular, en las aproximaciones de Born-Oppenheimer y armónicas (es decir, cuando el hamiltoniano molecular correspondiente al estado fundamental electrónico puede aproximarse mediante un oscilador armónico en las proximidades de la geometría molecular de equilibrio ), las frecuencias resonantes están asociadas con los modos normales de vibración correspondiente a la superficie de energía potencial del estado fundamental electrónico molecular . Por tanto, depende tanto de la naturaleza de los enlaces como de la masa de los átomos que intervienen. El uso de la ecuación de Schrödinger conduce a la regla de selección para el sistema que sufre cambios vibratorios:
La compresión y extensión de un enlace puede compararse con el comportamiento de un resorte ; las moléculas reales difícilmente son de naturaleza perfectamente elástica . Si, por ejemplo, se estira un enlace entre átomos, llega un punto en el que el enlace se rompe, es decir, la molécula se disocia en átomos. Por lo tanto, las moléculas de la vida real no tienen exactamente un movimiento armónico perfecto, sino que tienden a desviarse de él o existe anarmonicidad en el movimiento vibratorio molecular de la vida real. Una expresión puramente empírica que ajusta la curva de energía de una molécula diatómica que sufre extensión y compresión anarmónicas a una buena aproximación derivada de PM Morse, y se llama función Morse . El uso de la ecuación de Schrödinger conduce a la regla de selección para el sistema que sufre cambios vibratorios:
[26]
Para que un modo vibratorio en una muestra sea "IR activo", debe estar asociado con cambios en el momento dipolar molecular. No es necesario un dipolo permanente, ya que la regla requiere sólo un cambio en el momento dipolar. [27]
Una molécula puede vibrar de muchas maneras y cada una de ellas se denomina modo vibratorio . Para moléculas con N número de átomos, las moléculas geométricamente lineales tienen 3 N – 5 grados de modos vibratorios, mientras que las moléculas no lineales tienen 3 N – 6 grados de modos vibratorios (también llamados grados de libertad vibratorios). Como ejemplos, el dióxido de carbono lineal (CO 2 ) tiene 3 × 3 – 5 = 4, mientras que el agua no lineal (H 2 O) tiene solo 3 × 3 – 6 = 3. [ cita necesaria ]

Las moléculas diatómicas simples tienen un solo enlace y una sola banda vibratoria. Si la molécula es simétrica, por ejemplo N 2 , la banda no se observa en el espectro IR, sino sólo en el espectro Raman . Las moléculas diatómicas asimétricas, por ejemplo el monóxido de carbono ( CO ), absorben en el espectro IR. Las moléculas más complejas tienen muchos enlaces y sus espectros vibratorios son correspondientemente más complejos, es decir, las moléculas grandes tienen muchos picos en sus espectros IR. [ cita necesaria ]
Los átomos de un grupo CH 2 X 2 , que se encuentra comúnmente en compuestos orgánicos y donde X puede representar cualquier otro átomo, pueden vibrar de nueve maneras diferentes. Seis de estas vibraciones involucran sólo la porción CH 2 : dos modos de estiramiento (ν): simétrico (ν s ) y antisimétrico (ν as ); y cuatro modos de flexión : tijeras (δ), balanceo (ρ), meneo (ω) y torsión (τ), como se muestra a continuación. Las estructuras que no tienen los dos grupos X adicionales adjuntos tienen menos modos porque algunos modos están definidos por relaciones específicas con esos otros grupos adjuntos. Por ejemplo, en el agua, los modos de balanceo, meneo y torsión no existen porque estos tipos de movimientos de los átomos de H representan una simple rotación de toda la molécula en lugar de vibraciones dentro de ella. En el caso de moléculas más complejas, también pueden estar presentes modos de vibración fuera del plano (γ). [28]
Estas cifras no representan el " retroceso " de los átomos de C , que, aunque necesariamente están presentes para equilibrar los movimientos generales de la molécula, son mucho más pequeños que los movimientos de los átomos de H , más ligeros .
Las bandas IR más simples e importantes o fundamentales surgen de las excitaciones de los modos normales, las distorsiones más simples de la molécula, desde el estado fundamental con número cuántico vibratorio v = 0 hasta el primer estado excitado con número cuántico vibratorio v = 1. En algunos En algunos casos se observan bandas de armónicos . Una banda de armónicos surge de la absorción de un fotón que conduce a una transición directa del estado fundamental al segundo estado vibratorio excitado ( v = 2). Dicha banda aparece aproximadamente con el doble de energía que la banda fundamental para el mismo modo normal. Algunas excitaciones, las denominadas modos combinados , implican la excitación simultánea de más de un modo normal. El fenómeno de la resonancia de Fermi puede surgir cuando dos modos son similares en energía; La resonancia de Fermi da como resultado un cambio inesperado en la energía y la intensidad de las bandas, etc. [ cita necesaria ]
El espectro infrarrojo de una muestra se registra haciendo pasar un haz de luz infrarroja a través de la muestra. Cuando la frecuencia del IR es la misma que la frecuencia vibratoria de un enlace o conjunto de enlaces, se produce absorción. El examen de la luz transmitida revela cuánta energía se absorbió en cada frecuencia (o longitud de onda). Esta medición se puede lograr escaneando el rango de longitud de onda usando un monocromador . Alternativamente, se mide todo el rango de longitud de onda usando un instrumento de transformada de Fourier y luego se genera un espectro de transmitancia o absorbancia usando un procedimiento dedicado. [ cita necesaria ]
Esta técnica se utiliza comúnmente para analizar muestras con enlaces covalentes . Los espectros simples se obtienen a partir de muestras con pocos enlaces activos IR y altos niveles de pureza. Las estructuras moleculares más complejas conducen a más bandas de absorción y espectros más complejos. [ cita necesaria ]

Las muestras gaseosas requieren una celda de muestra con un largo recorrido para compensar la dilución. La longitud del camino de la celda de muestra depende de la concentración del compuesto de interés. Un simple tubo de vidrio con una longitud de 5 a 10 cm equipado con ventanas transparentes a los infrarrojos en ambos extremos del tubo puede usarse para concentraciones de hasta varios cientos de ppm. Las concentraciones de gas de muestra muy por debajo de ppm se pueden medir con una celda de White en la que la luz infrarroja se guía con espejos para viajar a través del gas. Las células de White están disponibles con una longitud de paso óptico que va desde 0,5 m hasta cien metros. [ cita necesaria ]
Las muestras líquidas se pueden intercalar entre dos placas de una sal (comúnmente cloruro de sodio o sal común, aunque también se utilizan otras sales como bromuro de potasio o fluoruro de calcio ). [29] Las placas son transparentes a la luz infrarroja y no introducen líneas en los espectros. Con la creciente tecnología en el filtrado por computadora y la manipulación de los resultados, las muestras en solución ahora se pueden medir con precisión (el agua produce una amplia absorbancia en todo el rango de interés y, por lo tanto, hace que los espectros sean ilegibles sin este tratamiento por computadora). [ cita necesaria ]
Las muestras sólidas se pueden preparar de diversas formas. Un método común es triturar la muestra con un agente emulsionante oleoso (generalmente aceite mineral Nujol ). Se aplica una fina película de caldo sobre placas de sal y se mide. El segundo método consiste en moler finamente una cantidad de la muestra con una sal especialmente purificada (normalmente bromuro de potasio ) (para eliminar los efectos de dispersión de los cristales grandes). Luego, esta mezcla de polvo se prensa en una prensa mecánica para formar una pastilla translúcida a través de la cual puede pasar el haz del espectrómetro. [29] Una tercera técnica es la técnica de la "película fundida", que se utiliza principalmente para materiales poliméricos. Primero se disuelve la muestra en un disolvente adecuado no higroscópico . Una gota de esta solución se deposita sobre la superficie de una celda de KBr o NaCl . A continuación se evapora la solución hasta sequedad y se analiza directamente la película formada sobre la célula. Es importante tener cuidado para garantizar que la película no sea demasiado gruesa, de lo contrario la luz no podría atravesarla. Esta técnica es adecuada para el análisis cualitativo. El método final consiste en utilizar microtomía para cortar una película delgada (20 a 100 μm) de una muestra sólida. Esta es una de las formas más importantes de analizar productos plásticos defectuosos, porque se preserva la integridad del sólido. [ cita necesaria ]
En espectroscopia fotoacústica la necesidad de tratamiento de la muestra es mínima. La muestra, líquida o sólida, se coloca en el recipiente para muestras que se inserta en la celda fotoacústica que luego se sella para la medición. La muestra puede ser una pieza sólida, polvo o básicamente cualquier forma para la medición. Por ejemplo, se puede insertar un trozo de roca en el recipiente de muestra y medir el espectro a partir de él. [ cita necesaria ]
Una forma útil de analizar muestras sólidas sin necesidad de cortar muestras utiliza ATR o espectroscopía de reflectancia total atenuada . Con este método, las muestras se presionan contra la cara de un solo cristal. La radiación infrarroja atraviesa el cristal y sólo interactúa con la muestra en la interfaz entre los dos materiales. [ cita necesaria ]
Es típico registrar el espectro tanto de la muestra como de una "referencia". Este paso controla una serie de variables, por ejemplo, el detector de infrarrojos , que pueden afectar el espectro. La medición de referencia permite eliminar la influencia del instrumento. [ cita necesaria ]
La "referencia" adecuada depende de la medición y su objetivo. La medición de referencia más sencilla es simplemente retirar la muestra (reemplazándola por aire). Sin embargo, a veces es más útil una referencia diferente. Por ejemplo, si la muestra es un soluto diluido disuelto en agua en un vaso de precipitados, entonces una buena medida de referencia podría ser medir agua pura en el mismo vaso de precipitados. Entonces la medición de referencia cancelaría no sólo todas las propiedades instrumentales (como qué fuente de luz se utiliza), sino también las propiedades de absorción y reflexión de la luz del agua y del vaso de precipitados, y el resultado final solo mostraría las propiedades del soluto (al menos aproximadamente). [ cita necesaria ]
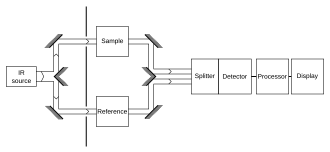
Una forma común de comparar con una referencia es secuencialmente: primero mida la referencia, luego reemplace la referencia por la muestra y mida la muestra. Esta técnica no es perfectamente fiable; Si la lámpara infrarroja es un poco más brillante durante la medición de referencia y luego un poco más tenue durante la medición de la muestra, la medición se distorsionará. Métodos más elaborados, como una configuración de "dos haces" (ver figura), pueden corregir este tipo de efectos para dar resultados muy precisos. El método de suma estándar se puede utilizar para cancelar estadísticamente estos errores.
Sin embargo, entre las diferentes técnicas basadas en absorción que se utilizan para la detección de especies gaseosas, la espectroscopia de cavidad anular (CRDS) se puede utilizar como método sin calibración. El hecho de que CRDS se base en las mediciones de la vida útil de los fotones (y no en la intensidad del láser) lo hace innecesario para cualquier calibración y comparación con una referencia [30].
Algunos instrumentos también identifican automáticamente la sustancia que se está midiendo a partir de un almacén de miles de espectros de referencia almacenados.
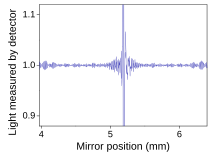
La espectroscopía infrarroja por transformada de Fourier (FTIR) es una técnica de medición que permite registrar espectros infrarrojos. La luz infrarroja se guía a través de un interferómetro y luego a través de la muestra (o viceversa). Un espejo móvil dentro del aparato altera la distribución de la luz infrarroja que pasa a través del interferómetro. La señal registrada directamente, llamada "interferograma", representa la salida de luz en función de la posición del espejo. Una técnica de procesamiento de datos llamada transformada de Fourier convierte estos datos sin procesar en el resultado deseado (el espectro de la muestra): salida de luz en función de la longitud de onda infrarroja (o equivalentemente, número de onda ). Como se describió anteriormente, el espectro de la muestra siempre se compara con una referencia. [ cita necesaria ]
Un método alternativo para adquirir espectros es el método "dispersivo" o " monocromador de barrido ". En este enfoque, la muestra se irradia secuencialmente con varias longitudes de onda únicas. El método dispersivo es más común en espectroscopia UV-Vis , pero es menos práctico en infrarrojo que el método FTIR. Una razón por la que se prefiere FTIR se llama " ventaja de Fellgett " o "ventaja múltiplex": la información en todas las frecuencias se recopila simultáneamente, lo que mejora tanto la velocidad como la relación señal-ruido . Otra se llama "Ventaja de rendimiento de Jacquinot": una medición dispersiva requiere detectar niveles de luz mucho más bajos que una medición FTIR. [31] Hay otras ventajas, así como algunas desventajas, [31] pero prácticamente todos los espectrómetros infrarrojos modernos son instrumentos FTIR.
Existen varias formas de microscopía infrarroja . Estos incluyen versiones IR de microscopía de subdifracción [32] , como IR NSOM , [33] microespectroscopia fototérmica , Nano-FTIR y espectroscopía infrarroja basada en microscopio de fuerza atómica (AFM-IR).
La espectroscopia infrarroja no es el único método para estudiar los espectros de vibración molecular. La espectroscopia Raman implica un proceso de dispersión inelástica en el que la molécula solo absorbe una parte de la energía de un fotón incidente y la parte restante se dispersa y detecta. La diferencia de energía corresponde a la energía vibratoria absorbida. [ cita necesaria ]
Las reglas de selección para la espectroscopia infrarroja y Raman son diferentes al menos para algunas simetrías moleculares , de modo que los dos métodos son complementarios en el sentido de que observan vibraciones de diferentes simetrías. [ cita necesaria ]
Otro método es la espectroscopia de pérdida de energía electrónica (EELS), en la que la energía absorbida la proporciona un electrón inelásticamente disperso en lugar de un fotón. Este método es útil para estudiar las vibraciones de moléculas adsorbidas en una superficie sólida.
Recientemente, EELS de alta resolución (HREELS) ha surgido como una técnica para realizar espectroscopia vibratoria en un microscopio electrónico de transmisión (TEM). [34] En combinación con la alta resolución espacial del TEM, se han realizado experimentos sin precedentes, como mediciones de temperatura a nanoescala, [35] [36] mapeo de moléculas marcadas isotópicamente, [37] mapeo de modos de fonones en posición- y espacio-momento, [38] [39] mapeo de modos de superficie vibratoria y volumen en nanocubos, [40] e investigaciones de modos de polaritones en cristales de van der Waals. [41] El análisis de modos vibratorios que son inactivos en IR pero que aparecen en dispersión inelástica de neutrones también es posible con alta resolución espacial utilizando EELS. [42] Aunque la resolución espacial de los HREEL es muy alta, las bandas son extremadamente amplias en comparación con otras técnicas. [34]
Mediante el uso de simulaciones por computadora y análisis en modo normal es posible calcular frecuencias teóricas de moléculas. [43]
La espectroscopia IR se utiliza a menudo para identificar estructuras porque los grupos funcionales dan lugar a bandas características tanto en términos de intensidad como de posición (frecuencia). Las posiciones de estas bandas se resumen en tablas de correlación como se muestra a continuación.

A menudo se interpreta que un espectrógrafo tiene dos regiones. [44]
En la región funcional hay de uno a unos pocos valles por grupo funcional. [44]
En la zona de las huellas dactilares hay muchos canales que forman un patrón intrincado que puede utilizarse como una huella dactilar para determinar el compuesto. [44]
Para muchos tipos de muestras, se conocen las asignaciones, es decir, qué deformaciones de enlace están asociadas con qué frecuencia. En tales casos, se puede obtener más información sobre la fuerza de un vínculo, basándose en la pauta empírica llamada regla de Badger . Publicada originalmente por Richard McLean Badger en 1934, [45] esta regla establece que la fuerza de un enlace (en términos de constante de fuerza) se correlaciona con la longitud del enlace. Es decir, el aumento de la fuerza de la unión conduce al correspondiente acortamiento de la unión y viceversa.
Los diferentes isótopos de una especie particular pueden exhibir diferentes detalles finos en la espectroscopia infrarroja. Por ejemplo, se determina experimentalmente que la frecuencia de estiramiento O – O (en centímetros recíprocos) de la oxihemocianina es 832 y 788 cm −1 para ν ( 16 O – 16 O) y ν ( 18 O – 18 O), respectivamente.
Al considerar el enlace O-O como un resorte, la frecuencia de absorbancia se puede calcular como un número de onda [= frecuencia/(velocidad de la luz)]
donde k es la constante del resorte del enlace, c es la velocidad de la luz y μ es la masa reducida del sistema A-B:
( es la masa del átomo ).
Las masas reducidas para 16 O – 16 O y 18 O – 18 O se pueden aproximar a 8 y 9 respectivamente. De este modo
Se ha descubierto que el efecto de los isótopos, tanto en la dinámica de vibración como en la de desintegración, es más fuerte de lo que se pensaba anteriormente. En algunos sistemas, como el silicio y el germanio, la desintegración del modo de estiramiento antisimétrico del oxígeno intersticial implica el modo de estiramiento simétrico con una fuerte dependencia isotópica. Por ejemplo, se demostró que para una muestra de silicio natural, la vida útil de la vibración antisimétrica es de 11,4 ps. Cuando el isótopo de uno de los átomos de silicio aumenta a 29 Si, la vida útil aumenta a 19 ps. De manera similar, cuando el átomo de silicio se cambia a 30 Si, la vida útil pasa a ser 27 ps. [46]
El análisis de espectroscopia de correlación infrarroja bidimensional combina múltiples muestras de espectros infrarrojos para revelar propiedades más complejas. Al ampliar la información espectral de una muestra perturbada, se simplifica el análisis espectral y se mejora la resolución. Los espectros 2D sincrónico y 2D asíncrono representan una descripción gráfica de los cambios espectrales debidos a una perturbación (como un cambio de concentración o un cambio de temperatura), así como la relación entre los cambios espectrales en dos números de onda diferentes. [ cita necesaria ]

La espectroscopia infrarroja bidimensional no lineal [47] [48] es la versión infrarroja de la espectroscopia de correlación . La espectroscopia infrarroja bidimensional no lineal es una técnica que está disponible con el desarrollo de pulsos de láser infrarrojo de femtosegundos . En este experimento, primero se aplica una serie de pulsos de bomba a la muestra. A esto le sigue un tiempo de espera durante el cual se permite que el sistema se relaje. El tiempo de espera típico dura de cero a varios picosegundos y la duración se puede controlar con una resolución de decenas de femtosegundos. Luego se aplica un pulso de sonda, lo que da como resultado la emisión de una señal de la muestra. El espectro infrarrojo bidimensional no lineal es un gráfico de correlación bidimensional de la frecuencia ω 1 que fue excitada por los pulsos iniciales de la bomba y la frecuencia ω 3 excitada por el pulso de la sonda después del tiempo de espera. Esto permite observar el acoplamiento entre diferentes modos vibratorios; debido a su resolución temporal extremadamente fina, se puede utilizar para monitorear la dinámica molecular en una escala de tiempo de picosegundos. Todavía es una técnica en gran medida inexplorada y se está volviendo cada vez más popular para la investigación fundamental.
Al igual que con la espectroscopia de resonancia magnética nuclear bidimensional ( 2DNMR ), esta técnica expande el espectro en dos dimensiones y permite la observación de picos cruzados que contienen información sobre el acoplamiento entre diferentes modos. A diferencia de 2DNMR, la espectroscopia infrarroja bidimensional no lineal también implica la excitación de armónicos. Estas excitaciones dan como resultado picos de absorción del estado excitado ubicados debajo de los picos diagonales y transversales. En 2DNMR, se utilizan con frecuencia dos técnicas distintas, COZY y NOESY . Los picos cruzados en el primero están relacionados con el acoplamiento escalar, mientras que en el segundo están relacionados con la transferencia de espín entre diferentes núcleos. En espectroscopía infrarroja bidimensional no lineal, se han elaborado análogos a estas técnicas 2DNMR. La espectroscopia infrarroja bidimensional no lineal con tiempo de espera cero corresponde a COSY, y la espectroscopia infrarroja bidimensional no lineal con tiempo de espera finito que permite la transferencia de población vibratoria corresponde a NOESY. La variante COZY de espectroscopía infrarroja bidimensional no lineal se ha utilizado para determinar el contenido de estructura secundaria de proteínas. [49]